扩展功能
文章信息
- 孙敏英, 周红月, 接晶, 谢飞, 翟瑞萍, 陈潭秀, 袁红艳, 台桂香
- SUN Minying, ZHOU Hongyue, JIE Jing, XIE Fei, ZHAI Ruiping, CHEN Tanxiu, YUAN Hongyan, TAI Guixiang
- 胸腺肽α1诱导MUC1特异性Th2型免疫应答
- Specific Th2 immune response of MUC1 induced by thmosin α1
- 吉林大学学报(医学版), 2018, 44(02): 299-304
- Journal of Jilin University (Medicine Edition), 2018, 44(02): 299-304
- 10.13481/j.1671-587x.20180217
-
文章历史
- 收稿日期: 2017-04-25
2. 吉林大学基础医学院免疫学教研室, 吉林 长春 130021
2. Department of Immunology, School of Basic Medical Sciences, Jilin University, Changchun 130021, China
胸腺肽α1(thmosin α1,Tα1)由28个氨基酸多肽组成,具有高度保守酸多肽结构。Tα1主要分布于胸腺组织,也存在于淋巴组织(如脾、淋巴结)和非淋巴组织(如肺、肾和脑)[1],其分泌和释放并不受其他激素或者释放因子所调节[2]。尽管Tα1确切的免疫机制还不清楚,但是实验[3]证实:Tα1具有强大的免疫调节作用,是一种细胞免疫增强剂和生物反应调节因子,在机体免疫应答过程中十分重要。大量的实验数据[4-7]证实:Tα1不仅自身具有延缓肿瘤复发、改善免疫功能的作用,在与其他抗肿瘤药物联合使用时还可提高癌症治疗效果。MUC1是Mucins黏蛋白家族成员,存在于正常腺管上皮细胞及其来源的肿瘤细胞表面, 由多肽核芯(核芯肽)和侧枝糖链构成,其核芯肽胞外段为20个氨基酸(SAPD TRPAP GSTAPPA HGVT)的串联重复序列(variable numbers tandem repeats, VNTRs)。正常组织的MUC1与肿瘤组织不同,前者分布于腺管上皮细胞分泌极,与免疫细胞相对隔离,糖基化丰富;而后者广泛分布并异常丰富地表达于癌细胞表面,糖基化不完全,因此暴露出正常情况下隐蔽的表位,成为免疫细胞攻击的靶点[8-9],是制备肿瘤疫苗的理想分子。目前研制的以MUC1为靶点的疫苗包括糖疫苗、蛋白或多肽疫苗和DNA疫苗[10-12], 其中蛋白疫苗具有一定的临床应用前景。本课题组前期研究[13-14]以MUC1为靶点,研制黏蛋白与麦芽糖结合蛋白融合蛋白(mucin1-maltose binding protein fusion protein, MUC1-MBP)的抗肿瘤疫苗,表明MUC1-MBP联合卡介苗(bacillus calmette-guérin, BCG)佐剂在小鼠体内可以诱导细胞毒性T淋巴细胞(cytotoxic Tlymphocyte, CTL)细胞毒的杀伤活性和Th1反应,可以抑制肺癌转移及实体瘤的生长,具有明显的肿瘤治疗作用[13-16]。但由于BCG是减毒活疫苗,而且其活菌数较难控制,导致疫苗稳定性差,且高剂量BCG的不良反应较大,因此探索良好的肿瘤疫苗佐剂一直是本课题组的重要研究课题。由于Tα1具有免疫调节作用,本研究探讨Tα1是否能作为MUC1-MBP的佐剂用于抗肿瘤治疗,旨在为开发新的佐剂提供依据。
1 材料与方法 1.1 实验动物、主要试剂和仪器67只雌性C57BL/6小鼠,体质量为18~20 g,6~8周龄,动物合格证号:SCXK(京)2014-0004,购自北京阜康生物科技股份有限公司。小鼠黑色素瘤细胞B16-MUC1由本室建立并保存,重组MUC1-MBP和MUC1-GST融合蛋白由本室重组构建及纯化[6]。BCG购自石家庄开创生化公司,Tα1购自成都地奥九泓制药厂,伊思柯夫改良培养液(Iscove’ s modified Dubecco’ s medium, IMDM)和G418购自美国Gibco公司,FBS和小鼠淋巴细胞分层液购自天津市灏洋生物制品有限公司,ConA购自美国Sigma公司,小鼠抗人MUC1购自美国Abcam公司,FITC-山羊抗小鼠IgG和山羊抗鼠IgG-HRP购自北京中杉金桥生物技术有限公司,鼠抗MBP多克隆抗体购自基因公司,大鼠抗鼠IgG1-HRP和山羊抗鼠IgG2a-HRP购自美国Southern Biotech公司,小鼠细胞因子干扰素γ(IFN-γ)、白细胞介素2(IL-2)、白细胞介素4(IL-4)和白细胞介素10(IL-10) ELISA检测试剂盒购自美国eBioscience公司。低温冰箱和CO2孵箱购自日本SANYO公司,酶标仪购自美国BIOTEK公司,紫外分光光度计购自日本岛津公司。
1.2 小鼠分组与免疫方案① T细胞免疫活性检测组。将21只C57BL/6小鼠随机分成3组,每组7只,分别为生理盐水组(注射生理盐水)、MUC1-MBP+ BCG组(注射MUC1-MBP+BCG)和MUC1-MBP+ Tα1组(注射MUC1-MBP+Tα1),其中MUC1-MBP+ BCG组为阳性对照组。免疫方案:小鼠颈背部皮下多点注射,MUC1-MBP 50 μg/只,BCG作为佐剂1 mg/只, Tα1为30 μg/只,隔周1次,共注射3次。②MUC1特异性抗体检测组:将25只C57BL/6小鼠随机分成5组,每组5只,分别为生理盐水组(注射生理盐水)、MUC1-MBP 50 μg组、MUC1-MBP 50 μg+ Tα1 15 μg组、MUC1-MBP 50 μg+ Tα1 30 μg组和MUC1-MBP 50 μg+ Tα1 60 μg组,各组分别用生理盐水调至400 μL。免疫方案:小鼠颈背部皮下多点注射及两侧腹股沟皮下注射,第1次免疫后2周,同等剂量加强免疫2次。③肿瘤模型组。将21只C57BL/6小鼠随机分成3组,每组7只,分别为生理盐水组(注射生理盐水)、MUC1-MBP+ BCG组(注射MUC1-MBP+BCG)和MUC1-MBP+ Tα1组(注射MUC1-MBP+Tα1),其中MUC1-MBP+BCG组为阳性对照组。免疫方案:小鼠颈背部皮下多点注射,MUC1-MBP 50 μg/只,BCG作为佐剂1 mg/只, Tα1为30 μg/只,隔周1次,共注射3次。
1.3 脾指数测定第3次免疫后第4~7天,先称每只小鼠体质量,杀鼠,无菌取脾脏,称脾脏质量,计算脾指数。脾指数=小鼠脾质量/体质量。
1.4 检测各组小鼠的刺激指数(stimulus index,SI)和特异性SI在第3次免疫后第4~7天杀鼠,无菌取脾脏、研磨、细胞计数, 制备脾细胞悬液,采用小鼠淋巴细胞分层液分离小鼠脾脏单个核细胞,采用IMDM调整细胞浓度至1×107mL-1每孔100 μL加入96孔板中。非特异性淋巴细胞增殖反应:实验分为阴性对照组和ConA刺激组(终浓度5mg·L-1),每组设3复孔,37℃的CO2培养箱中培养48 h后,加入WST-1检测试剂每孔10 μL,继续反应1 h,通过酶标仪检测450 nm处吸光度(A)值。MUC1特异淋巴细胞增殖反应:实验分为阴性对照组、IL-2单独刺激组(终浓度100 U·mL-1)和MUC1多肽刺激组(MUC1多肽20 mg·L-1+IL-2 100 U·mL-1)。37℃、CO2培养箱3 d,半量换液,继续培养5 d后,吸取每孔细胞培养上清100 μL用于细胞因子的检测,加入WST-1检测试剂每孔10 μL,继续反应1 h,通过酶标仪检测450 nm波长处测量吸光度(A)值,计算SI。SI=实验孔A值/对照孔A值。
1.5 ELISA法检测各组小鼠脾细胞培养上清中细胞因子IFN-γ、IL-2、IL-4和IL-10水平收集ConA刺激2 d和MUC1刺激5 d的淋巴细胞培养上清,按照IFN-γ、IL-2、IL-4和IL-10试剂盒说明书进行操作。包被抗体(抗IFN-γ、IL-2、IL-4和IL-10的抗体)包被96孔酶标板,每个样本设双复孔,4℃过夜。采用PBS-0.05%Tween-20洗板5次,加入封闭液封闭1 h后,洗涤2次,加入标准品(IFN-γ:2 000.000、1 000.000、500.000、250.000、125.000、62.500、32.500和15.625 ng·L-1;IL-2标准品配制:1 200、600、300、150和75 ng·L-1;IL-4标准品配制:500.0、250.0、125.0、62.5、32.5、15.6、7.8和3.9 ng·L-1;IL-10标准品配制:200.0、100.0、50.0、25.0和12.5 ng·L-1)和样品,每孔100 μL,4℃过夜。洗涤5次,加入检测抗体室温孵育1 h,洗涤5次,加入酶标抗体Avindin-HRP, 室温孵育30 min。洗7次,加入TMB,室温15 min。加入硫酸终止后,采用酶标仪于450 nm波长测定A值。计算IFN-γ、IL-2、IL-4和IL-10水平。
1.6 ELISA法检测MUC1总抗体效价及亚类第3次免疫后第4天,眶上静脉采血,分离血清,通过间接ELISA试剂盒检测MUC1特异性抗体IgG、IgG1和IgG2a。首先将包被抗原MUC1-GST包被96孔板,每个样本设双复孔,4℃过夜。采用PBS-0.05%Tween-20洗板3次,加入封闭液封闭1.5 h后,洗涤2次,加一抗(待测血清)不同用药组每只小鼠血清倍比稀释(1:500、1:1000、1:2000、1:4000、1:8000、1:16000、1:32000、1:64000),每孔100 μL,均设双复孔,37℃孵育1.5 h。洗涤6次,加酶标二抗HRP(辣根过氧化物酶)(山羊抗小鼠IgG,1:10000;山羊抗小鼠IgG1,1:4000;山羊抗小鼠IgG2a,1:1000),每孔100 μL,37℃孵育1.5 h。洗涤7次,加入TMB,室温15 min。加硫酸终止后,采用酶标仪于450nm波长处测定A值。
1.7 肿瘤预防实验模型构建第3次免疫后1周,在小鼠右后背胁处接种黑色素瘤细胞B16-MUC1,每只2.0 × 106个。隔天称体质量,用游标卡尺测量肿瘤的最大直径(a)和最小半径(b),计算肿瘤体积(V):V=1/2ab2,直至第23天第1只小鼠死亡,观察小鼠生存期。
1.8 统计学分析采用Graphpad Prism5统计软件对数据进行统计学分析。各组小鼠脾指数、SI、脾细胞培养上清中细胞因子IFN-γ、IL-2、IL-4和IL-10表达水平和脾细胞中T淋巴细胞亚群比例以x±s表示,组间样本均数比较采用单因素方差分析。以α=0.05为检验水准。
2 结果 2.1 各组小鼠脾指数和淋巴细胞增殖反应MUC1-MBP+ BCG组和MUC1-MBP+ Tα1组小鼠脾指数明显高于生理盐水组(P < 0.01)。非特异性淋巴细胞增殖反应:MUC1-MBP+ BCG组和MUC1-MBP+ Tα1组SI均高于生理盐水组(P < 0.05),以MUC1-MBP+BCG组升高最为明显。MUC1特异性淋巴细胞增殖反应:MUC1-MBP+BCG组和MUC1-MBP+Tα1组特异性SI均高于生理盐水组(P < 0.05)。见表 1。
| (n=7, x±s) | |||
| Group | Spleen index | SI | Specific SI |
| Normal saline | 0.003 9±0.000 7 | 1.457 0±0.359 9 | 1.429 0±0.179 9 |
| MUC1-MBP+BCG | 0.005 2±0.001 7** | 2.286 0±0.224 9* | 1.957 0±0.359 9* |
| MUC1-MBP+Tα1 | 0.006 1±0.000 8** | 1.914 0±0.498 1* | 1.843 0±0.269 9* |
| *P < 0.05, * * P < 0.01 vs normal saline group. | |||
与生理盐水组比较,MUC1-MBP+BCG组小鼠脾细胞培养上清中IFN-γ和IL-2水平明显升高(P < 0.05);IL-4和IL-10水平略升高,但差异无统计学意义(P>0.05)。与生理盐水组比较,MUC1-MBP+Tα1组小鼠脾细胞培养上清中IL-4水平明显升高(P < 0.01);IFN-γ、IL-2、IL-4和IL-10水平升高, 但差异无统计学意义(P>0.05)。见表 2。
| [n=7, x±s, ρB/(pg·L-1)] | ||||
| Group | IFN-γ | IL-4 | IL-2 | IL-10 |
| Normal saline | 152.90±49.49 | 47.14±13.50 | 145.00±44.91 | 42.86±13.50 |
| MUC1-MBP+ BCG | 471.40±135.00* | 72.86±17.99 | 471.40±179.90* | 53.57±8.99 |
| MUC1-MBP+ Tα1 | 200.00±95.74 | 113.10±44.99** | 185.70±89.97 | 57.14±17.99 |
| *P < 0.05, * * P < 0.01 vs normal saline group. | ||||
随着Tα1剂量的增加,相应的抗体效价也有所提高,并且高剂量的Tα1能促进抗体的产生。见表 3。抗体亚类检测结果显示:Tα1能够明显诱导IgG1的产生,并且有剂量依赖关系,而IgG2a产生不明显。见表 4。
| Antigen(MUC1-MBP)(50 μg) | Tα1(μg) | Titer of antibody |
| - | - | 0 |
| + | - | 1:500-1:1 000 |
| + | 15 | 1:500-1:2 000 |
| + | 30 | 1:1 000-1:4 000 |
| + | 60 | 1:4 000-1:8 000 |
| (n=5, x±s) | |||
| Group | IgG1 | IgG2a | IgG1/IgG2a |
| A | 0.0484±0.000 4 | 0.049 8±0.001 0 | 0.963 1±0.020 5 |
| B | 0.987 1±0.000 8* | 0.048 1±0.000 8 | 20.630 0±0.435 9 |
| C | 3.632 0±0.025 6** | 0.051 5±0.001 9 | 72.470 0±0.609 4 |
| D | 3.798 0±0.080 0** | 0.057 5±0.000 4 | 66.600 0±2.271 0 |
| E | 1.838 0±0.125 5** | 0.608 9±0.007 1 | 2.946 0±0.286 3 |
| *P < 0.05, * * P < 0.01 vs A group.A:Control; B:MUC1-MBP (50 μg); C:MUC1-MBP (50 μg)+ Tα1(5 μg); D:MUC1-MBP (50 μg)+ Tα1(130 μg); E:MUC1-MBP (50 μg)+ Tα1 (60 μg). | |||
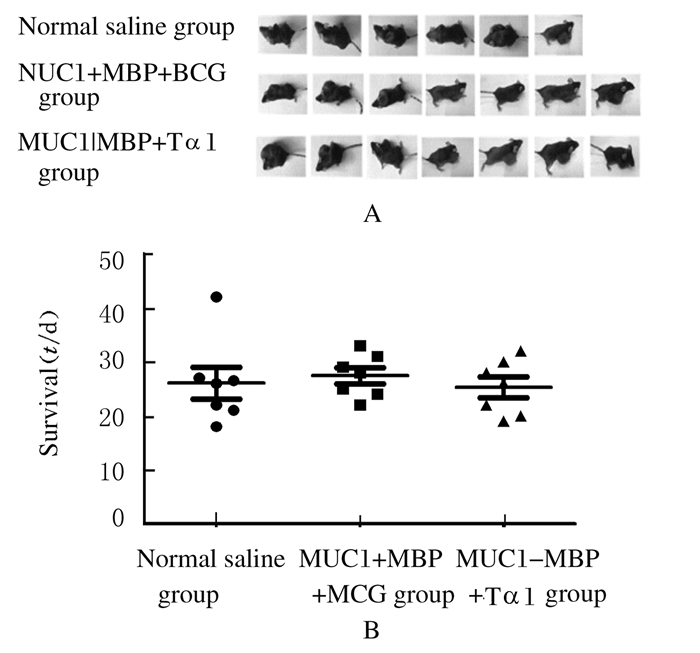
注射肿瘤细胞1周之内肿瘤生长缓慢,第8天生理盐水组最先触及肿瘤结节,第11天MUC1-MBP+Tα1组触及肿瘤结节,第14天MUC1-MBP+BCG组触及肿瘤结节。生理盐水组小鼠生存期为(26±4) d,MUC1-MBP+BCG组小鼠生存期为(28.7±6.3) d,MUC1-MBP+ Tα1组小鼠生存期为(28±6) d。见图 1。MUC1-MBP+BCG组和MUC1-MBP+Tα1组与生理盐水组小鼠生存期比较差异均无统计学意义(P>0.05)。
|
| A:Tumor growth situation; B: Survival time curve. 图 1 各组小鼠接种荷瘤23d后肿瘤生长情况和小鼠生存期 Figure 1 Tumor growth and survival curves of tumor-bearing mice in various groups 23 d after inoculation |
|
|
本文作者将BCG与MUC1-MBP联合作为阳性对照组,并与Tα1联合MUC1-MBP免疫C57BL/6小鼠进行对比。本研究免疫活性检测结果显示:MUC1-MBP+ BCG组和MUC1-MBP+Tα1组小鼠脾指数、有丝分裂原SI、MUC1多肽特异性SI均有所升高,说明MUC1-MBP联合Tα1和联合BCG均可诱导非特异性淋巴细胞增殖和特异性淋巴细胞增殖。由于CTL杀伤活性离不开Th1的辅助,因此,本文作者分析了诱导活化的Th类型。采用MUC1多肽刺激5 d,检测了脾脏特异性T淋巴细胞分泌的细胞因子IFN-γ、IL-2、IL-4和IL-10水平,结果显示:MUC1-MBP联合Tα1明显提高了IL-4和IL-10的分泌,而联合BCG提高了IFN-γ和IL-2的分泌水平,提示Tα1诱导MUC1特异的Th2型应答,而BCG却诱导MUC1特异的Th1应答,该结果与本文作者前期的研究[15-18]结果一致。抗体的产生提示体液免疫应答的激活,也提示Th2的活化。而且,IgG1在IL-4诱导下才能产生,IgG2a在IFN-γ诱导下产生,因此检测IgG1和IgG2a能间接提示Th2和Th1应答。本文作者进一步通过ELISA法检测对免疫小鼠的血清IgG和亚类IgG1和IgG2a进行分析,结果发现:当免疫3次后,与MUC1-MBP组比较,MUC1-MBP+ Tα1组产生了较高效价的MUC1特异性IgG,并随着Tα1剂量增加而升高,提示Tα1在促进MUC1-MBP产生体液免疫应答中有佐剂作用。进一步检测抗体亚类结果发现:随着Tα1剂量的增加,IgG1抗体的产生能力逐渐增强,而IgG2a未见产生,进一步提示Tα1诱导MUC1特异性Th2应答。
Th1应答不仅辅助CTL的杀伤,而其本身释放的IL-2、IFN-γ和TNF-α在治疗肿瘤中发挥重要的作用,Th2应答主要辅助体液免疫应答产生抗体,抗体在肿瘤治疗早期发挥作用,到晚期不仅发挥不了抗肿瘤作用,可能还会起到相反的作用[19-21]。因此,本文作者采用荷瘤鼠模型,深入探讨了Tα1联合MUC1-MBP抗肿瘤作用。本文作者将小鼠免疫3次后,给小鼠注射稳定转染MUC1的黑色素瘤细胞B16-MUC1,结果显示:Tα1联合MUC1-MBP作用下肿瘤生长在早期较对照组缓慢,而到后期与对照组无明显差别,未明显延长小鼠生存期,与本文作者的预期一致。而MUC1-MBP+BCG组作为阳性对照组也未见明显延长生存期,考虑可能是BCG活疫苗本身不稳定导致,其诱导产生的Th1应答强度较低,不足以诱导有效的抗肿瘤应答。
综上所述,Tα1促进MUC1-MBP诱导产生特异性Th2应答,明显促进体液免疫应答的产生,具有佐剂作用。Th2型应答的佐剂不适合应用于治疗性疫苗,但适合用于预防性疫苗。本研究结果也提示在临床中使用Tα1应该慎重,盲目应用有可能产生相反的作用。
| [1] | GoldsteinAL. From lab to bedside:emerging clinical applications of thymosin alpha-1[J]. Expert OpinBiolTher, 2009, 9(5): 593–608. |
| [2] | Naylor PH, Quadrini K, Garaci E, et al. Immunopharmacology of thymosin alpha 1 and cytokine synergy[J]. Ann NY Acad Sci, 2007, 1112: 235–244. DOI:10.1196/annals.1415.036 |
| [3] | Romani L, Moretti S, Fallarino F, et al. Jack of all trades:thymosin α1 and its pleiotropy[J]. Ann NY Acad Sci, 2012, 1269(1): 1–6. DOI:10.1111/j.1749-6632.2012.06716.x |
| [4] | Schulof RS, Lloyd MJ, Cleary PA, et al. A randomized trial to evaluate the immunorestorative properties of synthetic thymosin-alpha 1 in patients with lung cancer[J]. J Biol Response Mod, 1985, 4(2): 147–158. |
| [5] | Maio M, Mackiewicz A, Testori A, et al. Large randomized study of thymosin alpha 1 interferon alfa or both in combination with dacarbazine in patients with metastatic melanoma[J]. J Clin Oncol, 2010, 28: 1780–1787. DOI:10.1200/JCO.2009.25.5208 |
| [6] | Stefanini GF, Foschi FG, Castelli E, et al. Alpha-1 thymosin and transcatheter arterial chenoembolization in hepatocellular carinoma patients-a preliminary experience[J]. Hepatogastroenterology, 1998, 45(19): 209–215. |
| [7] | Cheng SQ, Wu MC, Chen H, et al. Anti-viral therapy using lamivudine and thymosin is helpful to prevent recurrence in hepatocellular carcinoma with coexisting active hepatitis B[J]. Zhonghua Zhong Liu Za Zhi, 2005, 27(2): 114–116. |
| [8] | Acres B, Limacher JM. MUC1 as a target antigen for cancer immunotherapy[J]. Expert Rev Vaccines, 2005, 4(4): 493–502. DOI:10.1586/14760584.4.4.493 |
| [9] | Nath S, Mukherjee P. MUC1:a multifaceted oncoprotein with a key role in cancerprogression[J]. Trends Mol Med, 2014, 20(6): 332–342. DOI:10.1016/j.molmed.2014.02.007 |
| [10] | Vassilaros S, Tsibanis A, Tsikkinis A, et al. Up to 15-year clinical follow-up of a pilot Phase Ⅲ immunotherapy study in stage Ⅱ breast cancer patients using oxidized mannan-MUC1[J]. Immunotherapy, 2013, 5(11): 1177–1182. DOI:10.2217/imt.13.126 |
| [11] | Quoix E, Ramlau R, Westeel V, et al. Therapeutic vaccination with TG4010 and first-line chemotherapy in advanced non-small-cell lung cancer:a controlled phase 2B trial[J]. Lancet Oncol, 2011, 12(12): 1125–1133. DOI:10.1016/S1470-2045(11)70259-5 |
| [12] | Wurz GT, Kao CJ, Wolf M, et al. Tecemotide:Anantigen-specific cancer immunotherapy[J]. Hum Vaccin Immunother, 2014, 10(11): 3383–3393. DOI:10.4161/hv.29836 |
| [13] | Hu B, Wang J, Guo Y, et al. Pre-clinical toxicity and immunogenicity evaluation of a MUC1-MBP/BCG anti-tumor vaccine[J]. Int Immunopharmacol, 2016, 33: 108–118. DOI:10.1016/j.intimp.2016.02.006 |
| [14] | Wang F, Ni W, Liu G, et al. Escherichia coli maltose-binding protein (MBP) directly induces mouseTh1activation through upregulating TLR2 and downregulating TLR4expressions[J]. Immunobiology, 2015, 220(6): 782–788. DOI:10.1016/j.imbio.2014.12.016 |
| [15] | 台桂香, 张凤吉, 朱迅. 重组人MUC1-MBP融合蛋白的抗肿瘤作用[J]. 中国肿瘤生物治疗杂志, 2003, 10(3): 202–205. |
| [16] | Fang F, Ma J, Ni W, et al. MUC1 and maltosebinding protein recombinant fusion protein combined with Bacillus Calmette-Guerin induces MUC1-specific and nonspecific anti-tumor immunity in mice[J]. Mol Med Rep, 2014, 10(2): 1056–1064. DOI:10.3892/mmr.2014.2306 |
| [17] | 赵小霞, 马吉春, 方芳, 等. 大肠杆菌麦芽糖结合蛋白(MBP)诱导小鼠Th1细胞的活化作用[J]. 中国免疫学杂志, 2009, 25(6): 504–507. |
| [18] | Ni W, Wang F, Liu G, et al. TLR9 played a more important role than TLR2 in the combination ofmaltose-bindingprotein and BCG-induced Th1 activation[J]. Mol Immunol, 2016, 79: 32–37. DOI:10.1016/j.molimm.2016.09.021 |
| [19] | Li Q, Zhang H, Yu L, et al. Down-regulation of Notch signaling pathway reverses the Th1/Th2 imbalance in tuberculosis patients[J]. Int Immunopharmacol, 2018, 54: 24–32. DOI:10.1016/j.intimp.2017.10.026 |
| [20] | Li L, Jing YB, Liu J, et al. Study on the correlation of the effect of entecavir on Th1/Th2 cytokines level in the treatment of chronic hepatitis[J]. Zhonghua Gan Zang Bing Za Zhi, 2017, 25(8): 606–611. |
| [21] | Kaminuma O, Saeki M, Nishimura T, et al. Differential contribution of adhesion molecules to Th1 and Th2 cell-mediated lung and bowel inflammation[J]. Biol Pharm Bull, 2017, 40(10): 1801–1805. DOI:10.1248/bpb.b17-00279 |
 2018, Vol. 44
2018, Vol. 44


