扩展功能
文章信息
- 肖燕, 王欢, 王淑敏, 高影
- XIAO Yan, WANG Huan, WANG Shumin, GAO Ying
- 肺癌并发抗利尿激素不适当分泌综合征2例报告及文献复习
- Lung cancer complicated with syndrome of inappropriate secretion of antidiuretic hormone:A report of 2 cases and literature review
- 吉林大学学报(医学版), 2017, 43(03): 643-645
- Journal of Jilin University (Medicine Edition), 2017, 43(03): 643-645
- 10.13481/j.1671-587x.20170335
-
文章历史
- 收稿日期: 2016-11-24
抗利尿激素不适当分泌综合征(syndrome of inappropriate secretion of antidiuretic hormone, SIADH)由Schwartz等[1]于1957年首先报道,SIADH又称Schwartz-Bartter综合征,是由于抗利尿激素(antidiuretic hormone, ADH)过量分泌导致体内水潴留、稀释性低钠血症、尿钠与尿渗透压升高的临床综合征[2]。SIADH是临床低钠血症的主要原因之一,其基础病因复杂且多样化,临床表现与血钠浓度明显相关,其病因包括恶性肿瘤、颅内病变、药物和渗量感受器/牵张感受器/压力感受器异常(包括肺部疾病及其他)。SIADH多为恶性肿瘤所致,恶性肿瘤约占SIADH病因的50%~70%,以肺癌最为常见,其中最常见的是小细胞肺癌(small cell lung cancer, SCLC)[3]。目前国内外关于肺癌并发SIADH的研究也多以SCLC为主,本研究中1例患者明确诊断为SCLC,另1例患者因未行病理检测不能明确分型,由于低钠血症为SCLC的独立预后不良因素,因此早期发现和诊断SIADH对肺癌患者的诊治及预后判断具有重要意义。本研究结合文献资料对2例肺癌并发SIADH患者的临床资料及诊治过程进行分析。
1 临床资料患者1,男性,48岁,2014年12月诊断为左肺肺癌(小细胞型)。患者于第2疗程化疗过程中开始出现乏力、食欲差和便秘等症状,2015年6月14日,血钠水平为116.8 mmol·L-1,补钠治疗后无好转。患者既往血钠水平均在正常值范围内,由于患者为SCLC,不除外异位抗利尿激素分泌,考虑肺癌并发SIADH可能性大,水潴留后引起稀释性低钠血症。严格限制液体量摄入后,6月19日患者血钠水平为130.2 mmol·L-1,完成第3疗程化疗后出院。既往:体健。查体:未见明显阳性体征。患者7次化疗前后血钠水平见图 1。辅助检查(第3疗程化疗前):离子,钠116.8 mmol·L-1,钾5.04 mmol·L-1,氯81.2 mmol·L-1。肾功能检查,肌酐65.6 μmol·L-1,尿素氮2.53 mmol·L-1,尿酸213 μmol·L-1;空腹血糖,5.22 mmol·L-1;肿瘤标志物,神经元特异性烯醇化酶67.5 μg·L-1(正常值为0~16.3 μg·L-1),癌胚抗原为正常值范围。气管镜刷片(2014年12月24日于吉林省肿瘤医院):小细胞恶性肿瘤,符合小细胞癌。肺CT:考虑左肺上叶中心型肺癌伴纵隔及左肺门淋巴结转移(图 2)。主要临床诊断:左肺肺癌(小细胞型)、SIADH。治疗方面单纯采用化疗,共行7个疗程。2年间患者肺癌反复进展,乏力、食欲差和便秘等症状反复,患者血钠水平多于每疗程化疗后好转,血钠水平维持在116~134 mmol·L-1。

|
| 图 1 患者每疗程化疗前后血钠水平 Figure 1 sodium levels of patient before and after each course of chemotherapy |
|
|
|
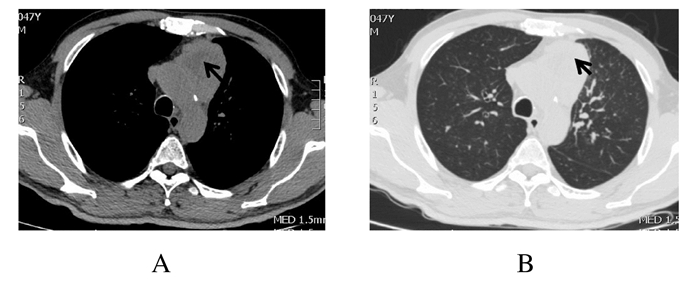
| A: Mediastinal window; B: Lung window. 图 2 左肺上叶中心型肺癌伴纵隔及左肺门淋巴结转移 Figure 2 Central lung cancer of left upper lobe with mediastinal and left lung door lymph node metastasis |
|
|
患者2,女性,79岁。2年前出现乏力,检查发现血钠水平偏低,后逐渐出现厌食、便秘和表情淡漠。2016年4月17日于本院老年病科住院,血钠水平为108.7 mmol·L-1,24小时尿钠水平为201.5 mmol·L-1,并出现嗜睡症状,查血清皮质醇、血浆促肾上腺皮质激素未见明显异常,给予限制液体量摄入及补钠治疗后好转。4月27日患者血钠水平为130.7 mmol·L-1,症状好转后出院。其后间断口服盐胶囊,多次复查血钠水平均低于正常值下限。10月27日因病情再次加重就诊于本科,血钠水平为120.4 mmol·L-1,血清皮质醇、血浆促肾上腺皮质激素结果提示激素分泌量及节律均正常。考虑垂体功能减退的可能性不大,鉴于患者出现顽固性低钠血症,不排除副肿瘤综合征。行肺CT检查,结果提示中心型肺癌(图 3)。既往:糖尿病病史5年。查体:未见明显阳性体征。辅助检查(2016年10月):离子,钾3.89 mmol·L-1,钠120.4 mmol·L-1,氯84.9 mmol·L-1;肾功能检查,肌酐55.4 μmol·L-1,尿素4.34 mmol·L-1,尿酸158 μmol·L-1;空腹血糖,11.90 mmol·L-1。肿瘤标志物(女性11项),神经元特异性烯醇化酶48.03 μg·L-1(正常值为 < 25 μg·L-1),其余10项均在正常值范围。24小时尿游离皮质醇正常。血清皮质醇、血浆促肾上腺皮质激素正常。肺CT:左肺上叶中心型肺癌伴纵隔淋巴结肿大。主要临床诊断:左肺肺癌、SIADH、2型糖尿病。10月31日给予托伐普坦口服试验性治疗,同时严格控制液体量摄入。11月2日患者血钠水平为135.6 mmol·L-1,临床症状明显好转后出院。
|
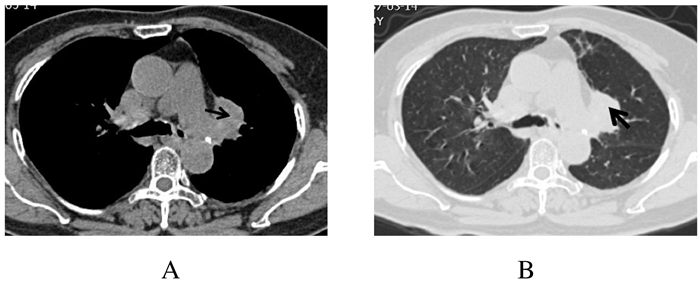
| A: Mediastinal window; B: Lung window. 图 3 左肺上叶中心型肺癌伴纵隔淋巴结肿大 Figure 3 Central lung cancer of left upper lobe with mediastinal lymph node enlargement |
|
|
SIADH的诊断标准尚不统一,有研究者[4]提出以下诊断标准:血钠水平小于135 mmol·L-1时,血浆渗透压小于275 mOsm·kg-1,尿渗透压大于100 mOsm·kg-1;除外肝硬化、肾功能衰竭和心力衰竭等其他引起低钠血症疾病;在未使用利尿剂或未严格限制钠摄入的情况下,尿钠水平大于40 mmol·L-1;甲状腺和肾上腺功能正常;血尿酸水平小于200 μmol·L-1,尿素氮水平小于4.5 mmol·L-1,肌酐水平小于80 μmol·L-1;通过输入生理盐水不能纠正低钠血症;限制液体摄入量治疗低钠血症有效。本研究中2例患者的相关检查结果中可以看出2例患者均符合SIADH的诊断。
肺癌患者,特别是SCLC患者常并发SIADH,其原因主要是肿瘤细胞异源性分泌ADH。此外,抗肿瘤药物使肿瘤细胞大量破坏释放ADH[5],导致不同程度的低钠血症。肺癌的主要化疗药物顺铂[6]可直接损伤肾小管上皮,影响重吸收,进而加重低钠血症。研究[7]表明:并发SIADH的SCLC患者预后更差。SIADH为SCLC的独立预后指标,同时低钠血症与患者的死亡率、发病率和住院时间有关[8]。随着肺癌发病率的逐年升高,国内关于肺癌并发SIADH的报道也越来越多,大部分患者多于确诊肺癌后发现SIADH,但并非所有的SIADH均发生在确诊肺癌后,本研究中患者2确诊肺癌2年前即患有严重的低钠血症,故在临床工作中,针对顽固性低钠血症患者应注意其是否为SIADH,进而注意排查恶性肿瘤,做到早期诊断及治疗,降低病死率。
本研究中患者1每个疗程化疗后血钠水平均能得到较好的纠正,但由于患者未严格限制液体量摄入,也未应用托伐普坦,故于下一疗程化疗前血钠水平均有明显减低。患者2未行肺癌病因治疗,仅单纯采取纠正低钠血症治疗,服用托伐普坦3d后血钠水平恢复正常,由于患者治疗时间尚短,长期预后及疾病进展情况有待后期随访,但关于该药物疗效及安全性的2项大型多中心、随机、双盲对照研究(SALT-1和SALT-2)[9]已经充分证实了托伐普坦升高血钠水平的有效性及安全性。SIADH引发的低钠血症病情严重程度与血钠水平、下降速度及病程长短明显相关。根据低钠血症的严重程度及发病时间针对性地制订个体化的治疗方案十分必要。低钠血症的过度治疗可导致严重的神经系统异常相关死亡率增加[10],在治疗SIADH过程中,要尽快纠正低钠血症,也要避免因血钠水平升高过快而引发的严重渗透性脱髓鞘综合征。由于SIADH的病情常随肿瘤的进展而加重,因此针对并发SIADH的肺癌患者,肺癌病因治疗及低钠血症对症治疗同等重要。
| [1] | Schwartz WB, Bennett W, Curelop S, et al. A syndrome of renal sodium loss and hyponatremia probably resulting from inappropriate secretion of antidiuretic hormone. 1957[J]. J Am Soc Nephrol, 2001, 12(12): 2860–2870. |
| [2] | Gitelman SE, Feldman BJ, Rosenthal SM. Nephrogenic syndrome of inappropriate antidiuresis:a novel disorder in water balance in pediatric patients[J]. Am J Med, 2006, 119(7 Suppl 1): S54–S58. |
| [3] | Gustafsson BI, Kidd M, Chan A, et al. Bronchopulmonary neuroendocrine tumors[J]. Cancer, 2008, 113(1): 5–21. DOI:10.1002/cncr.v113:1 |
| [4] | Gross P. Clinical management of SIADH[J]. Ther Adv Endocrinol Metab, 2012, 3(2): 61–73. DOI:10.1177/2042018812437561 |
| [5] | 覃晶, 蔡菊芬, 卢红阳. 小细胞肺癌伴发抗利尿激素异常分综合征诊治研究进展[J]. 实用医学杂志, 2014, 30(3): 489–491. |
| [6] | Iyer AV, Krasnow SH, Dufour DR, et al. Sodium-wasting nephropathy caused by cisplatin in a patient with small-cell lung cancer[J]. Clin Lung Cancer, 2003, 5(3): 187–189. DOI:10.3816/CLC.2003.n.033 |
| [7] | Wang X, Liu M, Zhang L, et al. Syndrome of inappropriate antidiuretic hormone secretion:A poor prognosis in small-cell lung cancer[J]. Arch Med Res, 2016, 47(1): 19–24. DOI:10.1016/j.arcmed.2015.12.006 |
| [8] | Spasovski G, Vanholder R, Allolio B, et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia[J]. Eur J Endocrinol, 2014, 170(3): G1–G47. DOI:10.1530/EJE-13-1020 |
| [9] | Schrier RW, Gross P, Gheorghiade M, et al. Tolvaptan, a selective oral vasopressin V2-receptor antagonist, for hyponatremia[J]. N Engl J Med, 2006, 355(20): 2099–2112. DOI:10.1056/NEJMoa065181 |
| [10] | Elhassan EA, Schrier RW. Hyponatremia:diagnosis, complications, and management including V2 receptor antagonists[J]. Curr Opin Nephrol Hypertens, 2011, 20(2): 161–168. DOI:10.1097/MNH.0b013e3283436f14 |
 2017, Vol. 43
2017, Vol. 43


