扩展功能
文章信息
- 孔繁学, 马翔, 范松涛, 卢建民, 秦秀虹, 邹吉扬
- KONG Fanxue, MA Xiang, FAN Songtao, LU Jianmin, QIN Xiuhong, ZOU Jiyang
- 玻璃体腔注射雷珠单抗和康柏西普联合青光眼引流阀植入治疗新生血管性青光眼的疗效
- Efficacy of intravitreal lucentis or conbercept injection combined with ahmed glaucoma valve implantation for treatment of neovascular glaucoma
- 吉林大学学报(医学版), 2017, 43(06): 1237-1242
- Journal of Jilin University (Medicine Edition), 2017, 43(06): 1237-1242
- 10.13481/j.1671-587x.20170631
-
文章历史
- 收稿日期: 2017-04-07
新生血管性青光眼(neovascular glaucoma, NVG)是源于虹膜与前房角新生血管(neovascularization, NV)收缩牵拉,导致房角进行性关闭,引起眼压(intraocular pressare, IOP)升高造成不可逆性视功能损害的继发性青光眼,属于难治性青光眼中最为棘手的一种,多继发于眼底及眼前段缺血性疾病,如增殖性糖尿病视网膜病变和视网膜中央静脉阻塞等。NVG的治疗方法主要包括对原发疾病的治疗、高眼压控制和减少NV生成。近年来眼科技术飞速发展,研究[1-2]表明:抑制视网膜缺血缺氧时产生的血管内皮生长因子(vascular endothelial growth factor,VEGF)能够有效阻止虹膜、脉络膜、角膜和视网膜NV的形成。玻璃体腔内注射抗VEGF药物联合青光眼引流阀(ahmed glaucoma valve,AGV)植入术治疗NVG成为国内外学者研究的热点,其安全性和有效性已经逐渐得到广泛认可[3-6]。目前上市的抗VEGF药物主要包括哌加他尼、雷珠单抗、贝伐单抗、阿柏西普和康柏西普,本研究分析近几年国内常用雷珠单抗和康柏西普治疗NVG的有效性和安全性,并进行比较。
1 资料与方法 1.1 一般资料回顾性分析2013年1月-2015年12月在本院行AGV(FP-7 AGV)植入术治疗的NVG患者的临床资料。NVG患者68例(68眼),其中男性37例(37眼),女性28例(28眼),年龄21~80岁,平均年龄为(53.69 ± 11.91)岁。本研究经本院伦理委员会批准。根据AGV植入术前是否进行玻璃体腔注药以及药物的不同分为雷珠单抗组、康柏西普组和对照组。详细记录患者术前的基本临床资料,包括最佳矫正视力(best corrected visual acuity, BCVA)、眼压(Goldmann眼压计测量)、抗青光眼用药数目、年龄、性别、NVG的原发病、手术史、晶状体的状态、术中丝裂霉素C应用的浓度和时间及玻璃体腔内注射抗VEGF药物后行AGV植入术间隔时间。纳入标准: ①全身和局部最大量应用抗青光眼药物后眼压仍高于21 mmHg的NVG患者;②有效随访时间满1年的患者;③术前检查前房角全部粘连关闭。排除标准:①年龄小于20岁;②眼局部感染性炎症性疾病;③有睫状体冷凝、青光眼滤过手术等手术史;④曾接受过抗VEGF药物治疗;⑤有玻璃体腔内注射抗VEGF药物或者AGV植入术禁忌证的患者。
1.2 治疗方法 1.2.1 术前处置玻璃体腔注药:AGV植入术前3~7 d行玻璃体腔注射雷珠单抗(诺华制药,10 g·L-1)或者康柏西普(成都康弘生物科技有限公司,10 g·L-1)。注射方法:患者仰卧,常规碘伏消毒铺巾,盐酸奥布卡因表面麻醉3次·10 min-1,生理盐水清洁结膜囊,距角膜缘约3.5 mm处睫状体平坦部垂直进针,玻璃体腔注射0.5 mg(0.05 mL)雷珠单抗或康柏西普,压迫30s,妥布霉素地塞米松眼膏涂眼。
1.2.2 AGV植入术雷珠单抗组和康柏西普组患者待虹膜NV消退后行AGV植入术;对照组患者首先局部及全身应用降眼压药物,必要时前房穿刺,待眼压平稳后行AGV植入术。采用2%利多卡因和0.75%布比卡因1: 1混合液行球后睫状神经节阻滞麻醉,在颞上做以穹隆部为基底的结膜瓣,暴露巩膜至赤道后。于拟放入引流盘处放置浸有0.4 g·L-1丝裂霉素C棉片3~5 min后,用约300 mL平衡盐溶液彻底冲洗。结扎AGV的引流管,用6-0丝线将引流盘缝于上、外直肌间巩膜面上,距角膜缘8~10 mm,修剪引流管,冲洗引流管以确保其通畅,做1/2巩膜厚度以角膜缘为基底的巩膜瓣。采用23 G针头巩膜瓣下在角膜缘后1.5 mm处穿刺,刺入前房,将引流管从穿刺口插入前房,平行于巩膜表面,10-0线缝合巩膜瓣及球结膜,妥布霉素地塞米松眼膏涂眼。
1.2.3 针对原发病变治疗NVG对屈光介质清晰的患者,玻璃体腔注药和AGV植入术前行全视网膜光凝术(PRP);对屈光介质不清晰者,先行抗VEGF药物治疗,待能窥清眼底时再行PRP。光斑直径200 μm,时间0.1~0.2 s,功率100~300 mW。
1.2.4 术后随访患者术后均于眼科门诊复诊,有效随访时间为1年,无失访患者。术后随访时间为术后2周, 1、3、6个月和1年。观察术后BCVA、眼压(Goldmann压平眼压计)、虹膜、房角、眼底NV情况、加用抗青光眼药物数目和并发症。手术疗效判断标准采用完全成功、条件成功和失败3种类型[5, 7]。①完全成功:指术后不用任何抗青光眼药物,眼压为6~21 mmHg,并且无严重眼部并发症[8];②部分成功:局部加用抗青光眼药物,眼压为6~21 mmHg,无严重并发症;③失败:术后局部用抗青光眼药物(种类≥ 3),连续2次眼压仍>21 mmHg,需进一步行抗青光眼手术; 眼压持续<6 mmHg; 出现严重的并发症; 因并发症需取出AGV。总成功率是指完全成功率和部分成功率之和。
1.3 统计学分析采用SPSS20.0统计软件进行统计学分析。患者年龄、眼压、抗青光眼药物数目和BCVA以x±s表示,BCVA小数视力行最小分辨角行对数(LogMAR)视力转换。符合正态分布和方差齐性的多组数据比较采用单因素方差分析,组间数据的两两比较采用LSD法;不满足正态分布和方差齐性的多组数据比较采用Kruskal-Wallis秩和检验,组间数据的两两比较采用Wilcoxon秩和检验;患者手术成功率多组间比较采用Kaplan-Meier生存曲线法分析,手术成功率组间两两比较采用Log-rank检验,随访中患者满足失败标准即终止分析;各组患者性别比较采用χ2检验;病因及术后并发症比较采用Fisher's确切概率法。检验水准为α = 0.05。
2 结果 2.1 各组患者基本资料本研究纳入患者68例,其中原发病糖尿病视网膜病变34例(34眼),视网膜中央静脉阻塞22例,视网膜分支静脉阻塞6例(6眼),眼缺血综合征6例6眼。术前BCVA为0.02~0.25,术前眼压为24.50~75.00mmHg, 平均眼压为(44.59±9.48)mmHg。雷珠单抗组患者26例(26眼),其中男性16例(16眼),女性10例(10眼),年龄23~80岁,平均年龄为(53.00±12.32)岁;康柏西普组患者21例(21眼),其中男性13例(13眼),女性8例(8眼),年龄21~79岁,平均年龄为(54.00±12.74)岁;对照组患者21例(21眼),其中男性14例(14眼),女性7例(7眼),年龄27~76岁,平均年龄为(54.24±11.05)岁。术前雷珠单抗组、康柏西普组和对照组患者平均眼压为(45.13± 8.94)、(44.39±10.62)和(44.11± 9.38) mmHg; 术前3组患者平均使用抗青光眼药物频数为(3.12±0.32)、(3.10±0.30)和(3.14±0.35)个。3组患者性别、平均年龄、NVG的病因、术前平均IOP、BCVA、术前平均使用抗青光眼药物频数和IOP比较差异均无统计学意义(P>0.05)。见表 1。
| Group | n | Gender | Age | Diagnosis | Baseline IOP/(P/mmHg) | BCVA(LogMAR) | Pre-medications | ||||
| Male | Female | DR | CRVO | BRVO | OIS | ||||||
| Control | 21 | 14 | 7 | 54.24±11.05 | 10 | 7 | 3 | 1 | 44.11±9.38 | 1.09±0.47 | 3.14±0.36 |
| Lucentis | 26 | 16 | 10 | 53.00±12.32 | 12 | 9 | 2 | 3 | 45.13±8.94 | 1.10±0.51 | 3.12±0.32 |
| Conbercept | 21 | 13 | 8 | 54.00±12.74 | 12 | 6 | 1 | 2 | 44.39±10.62 | 1.11±0.46 | 3.10±0.30 |
| P | 0.92 | 0.93 | 0.89 | 0.93 | 1.00 | 0.90 | |||||
| DR:Diabetic tretinopathy; CRVO:Central retinal vein occlusion; BRVO:Branch retinal vein occlusion; OIS:Ocular ischemia syndrome. | |||||||||||
雷珠单抗组患者26眼中,玻璃体腔注药后有23眼(88%)术后2~7 d虹膜和房角NV完全消退,3眼(12%)虹膜和房角NV部分消退;康柏西普组患者的21眼中,玻璃体腔注药后有19眼(90%)术后3~7 d虹膜和房角NV完全消退,2眼(10%)虹膜和房角NV仅残留少许NV,且明显萎缩;对照组患者因未注射抗VEGF药物,虹膜和房角NV持续存在。
2.3 术后各组患者平均IOP和使用抗青光眼药物频数雷珠单抗组、康柏西普组和对照组患者术后平均IOP均较术前明显降低(P<0.01)。3组患者术后平均IOP均随着术后时间延长呈升高趋势,雷珠单抗组和康柏西普组患者术后平均IOP在不同时间点均低于对照组(P<0.05),但组间两两比较差异无统计学意义(P>0.05)。3组患者术后平均使用抗青光眼药物频数均较术前明显减少(P<0.01)。3组患者术后平均使用抗青光眼药物频数伴随术后时间延长呈增加趋势,雷珠单抗组和康柏西普组患者术后平均使用抗青光眼药物频数在不同时间点均少于对照组,但差异无统计学意义(P>0.05)。见表 2。
| (x±s) | |||||||
| Group | n | Before operation | IOP | ||||
| 2 weeks after operation | 1 month after operation | 3 month safter operation | 6 months after operation | 1 year after operation | |||
| Control | 21 | 44.11±9.38 | 16.38±2.99△ | 18.14±3.65△ | 20.00±3.39△ | 21.38±4.30△ | 23.14±4.75△ |
| Lucentis | 26 | 45.13± 8.94 | 15.27±2.39△ | 15.88±4.41△ | 18.19±3.71△ | 19.73±3.32△ | 21.08±3.15△ |
| Conbercept | 21 | 44.39±1 0.62 | 14.95±3.03△ | 15.86±4.36△ | 18.10±3.40△ | 19.67±3.84△ | 21.00±3.80△ |
| Group | n | Before operation | Number of glaucoma medications | ||||
| 2 weeks after operation | 1 month after operation | 3 months after operation | 6 months after operation | 1 year after operation | |||
| Control | 21 | 3.14±0.36 | 0.14±0.36△ | 0.33±0.48△ | 0.67±0.58△ | 1.00±0.55△ | 1.62±0.80△ |
| Lucentis | 26 | 3.12±0.32 | 0.12±0.33△ | 0.23±0.59△ | 0.35±0.69△ | 0.58±0.70△ | 1.31±0.79△ |
| Conbercept | 21 | 3.10±0.30 | 0.10±0.30△ | 0.29±0.64△ | 0.33±0.73△ | 0.57±0.87△ | 1.38±0.92△ |
| Group | n | Before operation | BCVA (LogMAR) | ||||
| 2 weeks after operation | 1 month after operation | 3 months after operation | 6 months after operation | 1 year after operation | |||
| Control | 21 | 1.09±0.47 | 1.08±0.46 | 1.09±0.45 | 1.09±0.43 | 1.10±0.43 | 1.10±0.42 |
| Lucentis | 26 | 1.10±0.51 | 1.10±0.51 | 0.82±0.39*△ | 0.82±0.39*△ | 1.08±0.36 | 1.10±0.38 |
| Conbercept | 21 | 1.11±0.46 | 1.09±0.44 | 0.81±0.36*△ | 0.82±0.36*△ | 1.08±0.35 | 1.10±0.34 |
| *P<0.05 compared with control group; △P<0.05 compared with before operation. | |||||||
术后3组患者视力均呈先升高再降低的趋势。雷珠单抗组和康柏西普组患者在术后1个月视力达到最好状态,术后3个月后视力回落。对照组患者术后视力无明显改善。术后1和3个月雷珠单抗组和康柏西普组患者视力均明显优于对照组(P<0.05),雷珠单抗组和康柏西普组患者术后视力比较差异无统计学意义(P>0.05)。见表 2。
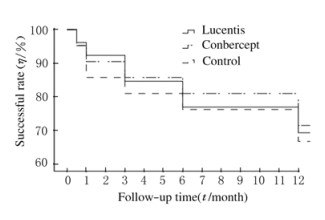
2.5 3组患者手术成功率随着术后时间延长,3组患者手术总成功率均降低,不同时间点手术成功率见表 3,生存分析显示3组患者手术成功率比较差异无统计学意义。见图 1。
| (η/%) | ||||||
| Group | n | Successful rate of operation | ||||
| 2 weeks after operation | 1 month after operation | 3 months after operation | 6 months after operation | 12 months after operation | ||
| Control | 21 | 95.24 | 85.71 | 80.95 | 76.19 | 66.67 |
| Lucentis | 26 | 96.15 | 92.31 | 84.62 | 76.92 | 69.23 |
| Conbercept | 21 | 95.24 | 90.48 | 85.71 | 80.95 | 71.43 |
| P | 0.98 | 0.75 | 0.91 | 0.92 | 0.95 | |
|
| 图 1 3组患者手术成功率的累积生存曲线 Figure 1 Cumulative survival curves of successful rates of operaton of patients in three groups |
|
|
术后并发症早期多见于虹膜睫状体炎、前房出血、浅前房、低眼压和引流管堵塞,3组患者术后并发症发生率比较差异无统计学意义(P>0.05)。患者术后中晚期并发症主要有包裹泡形成和引流管移位暴露,本研究入选患者中无眼内炎、脉络膜上腔出血、角膜失代偿及视网膜脱离等严重并发症。见表 4。
| [n(η/%)] | |||||||
| Group | n | Hyphema | Shallow anterior chamber | Olular Hypotension | Anterior uveitis | Tube occlusion/displacement/exposure | Encapsulated plate |
| Control | 21 | 10(48) | 5(24) | 2(10) | 9(43) | 2(10) | 2(10) |
| Lucentis | 26 | 11(42) | 7(27) | 3(12) | 9(35) | 3(12) | 3(12) |
| Conbercept | 21 | 9(43) | 6(29) | 3(14) | 7(33) | 4(19) | 1(5) |
| P | 0.93 | 0.94 | 0.89 | 0.78 | 0.63 | 0.93 | |
NVG在青光眼前期仅有虹膜或房角产生NV,滤过功能眼压正常;开角型青光眼期NV进入小梁网,IOP升高,部分患者通过局部药物或激光治疗可以控制IOP;闭角型青光眼期房角黏连关闭,IOP持续升高,药物和激光治疗不能控制,必须行手术治疗。目前公认房水引流阀植入术是难治性青光眼(包括NVG)的首选术式[9-10],尤其针对房角关闭的患者最为有效[11]。NVG的发病机制中,VEGF起关键性作用,是生理和病理性血管生成过程中发挥重要作用的细胞因子[12]。在缺氧和缺血等病理条件下诱发眼部NV形成[13]。降低眼内VEGF浓度抑制NV形成能更好地控制IOP[14],抗VEGF药物已成为NVG的一线用药。
既往国内外应用比较广泛的抗VEGF药物有贝伐单抗和雷尼单抗, 其用于玻璃体腔注射联合AGV植入术治疗NVG可取得良好疗效,但因为贝伐单抗为非适应证用药(美国食品医药管理局批准为抗癌药物),同时雷尼单抗价格偏高,使上述2种药物的应用受到一定限制。2014年康柏西普在国内上市后广泛应用于新生血管性眼病,但至今尚无关于雷尼单抗和康柏西普治疗NVG疗效比较的研究。本研究回顾性分析玻璃体腔注射2种不同抗VEFG药物联合AGV植入术治疗NVG的疗效和安全性,本研究结果显示:玻璃体腔注射不同药物后2~3 d开始有不同程度的虹膜房角NV消退, 与既往研究[7, 15]结果一致。术后平均IOP和抗青光眼药物频数均低于术前。术后均呈先升高再降低的趋势,术后早期(1~3个月)视力达到最佳状态,雷珠单抗组和康柏西普组患者BCVA均明显高于对照组,随后视力有降低趋势,虽然想要维持较好视力可能需要再次注射抗VEGF药物[6], 但这对于提高生活质量、增强患者治疗信心从而提高手术依从性均有很大帮助。Yalvac等[16]报道NVG植入房水引流阀的手术成功率为63.2%,Shen等[17]报道1和2年手术成功率为70%和60%,Tang等[6]报道6和12个月手术成功率分别为71.4%和68.4%。本研究中对照组患者6和12个月的手术总成功率分别为76%和67%,与上述既往报道结果相近。考虑手术成功率差异取决于病例数多少、青光眼类型、NVG有无联合其他手术、丝裂霉素有无应用以及患者年龄和种族等。本研究中各组患者手术成功率无明显差异,但统计结果显示雷珠单抗组和康柏西普组患者手术成功率均略高于对照组,且术后前房出血和虹膜睫状体炎发生率均略低于对照组,AGV植入术前的抗VEGF药物治疗能迅速减轻患者疼痛,减少术中术后并发症、改善手术预后[18]。关于该病的远期疗效报道较少,Netland[11]研究AGV治疗NVG的1、2和5年手术成功率分别为73.1%、61.9%和20.6%。
本研究中雷珠单抗组和康柏西普组患者均有不同程度的NV消退,未出现关于抗VEGF药物注射引发的并发症,进一步证实了抗VEFG药物治疗的安全性,3组患者AGV植入术后并发症发生率比较差异无统计学意义。患者术后早期多见虹膜睫状体炎、前房出血、浅前房、低眼压和引流管堵塞等,可能为很多因素导致,如虹膜房角的新生血管密度、术前不同程度的高眼压及术中术后IOP骤降等。针对性预防措施可行抗VEFG药物治疗减少NV、术前术后局部滴用抗生素滴眼液减轻炎症反应、术前积极降眼压、术中前房穿刺缓慢降低IOP、术中应用粘弹剂维持前房和IOP、采用可吸收缝线部分结扎引流管避免早期引流过强等。
综上所述,雷珠单抗和康柏西普多方面疗效指标比较均无明显差异。玻璃体腔注射抗VEGF药物联合AGV植入术可以有效、安全地治疗NVG,其短期和中期疗效已经被很多医师认可,但由于临床应用时间较短、病例数较少及抗VEGF药物价格昂贵等因素,其远期效果有待多中心大样本的长期随访研究证实。
| [1] | Gaudreault J, Fei D, Rusit J, et al. Preclinical pharmacokinetics of Ranibizumab (rhuFabV2) after a single intravitreal administration[J]. Invest Ophthalmol Vis Sci, 2005, 46(2): 726–733. DOI:10.1167/iovs.04-0601 |
| [2] | Hayreh SS. Neovascular glaucoma[J]. Prog Retin Eye Res, 2007, 26(5): 470–485. DOI:10.1016/j.preteyeres.2007.06.001 |
| [3] | Li Z, Zhou M, Wang W. A prospective comparative study on neovascular glaucoma and non-neovascular refractory glaucoma following Ahmed glaucoma valve implantation[J]. Chin Med J (Engl), 2014, 127(8): 1417–1422. |
| [4] | Kang JY, Nam KY, Lee SJ. The effect of intravitreal bevacizumab injection before Ahmed valve implantation in patients with neovascular glaucoma[J]. Int Ophthalmol, 2014, 34(4): 793–799. DOI:10.1007/s10792-013-9875-7 |
| [5] | Zhou MW, Wang W, Huang WB. Adjunctive with versus without intravitreal bevacizumab injection before Ahmed glaucoma valve implantation in the treatment of neovascular glaucoma[J]. Chin Med J (Engl), 2013, 126(8): 1412–1417. |
| [6] | Tang M, Fu Y, Wang Y, et al. Efficacy of intravitreal ranibizumab combined with Ahmed glaucoma valve implantation for the treatment of neovascular glaucoma[J]. BMC Ophthalmol, 2016, 16: 183–187. DOI:10.1186/s12886-016-0358-2 |
| [7] | 周民稳, 王伟, 王世明, 等. 不同材料的引流管覆盖物在房水引流阀植入术中的应用研究[J]. 中华眼科杂志, 2013, 49(2): 102–108. |
| [8] | Elmekawey H, Khafagy A. Intracameral ranibizumab and subsequent mitomycin C augmented trabeculectomy in neovascular glaucoma[J]. J Glaucoma, 2014, 23(7): 437–440. DOI:10.1097/IJG.0b013e3182946398 |
| [9] | Zhou M, Wang W, Huang W, et al. Use of Mitomycin C to reduce the incidence of encapsulated cysts following ahmed glaucoma valve implantation in refractory glaucoma patients:a new technique[J]. BMC Ophthalmol, 2014, 14: 107. DOI:10.1186/1471-2415-14-107 |
| [10] | 张秀兰. 新生血管性青光眼是否难治[J]. 中华眼科杂志, 2012, 48(6): 488–491. |
| [11] | Netland PA. The Ahmed glaucoma valve in neovascular glaucoma (An AOS Thesis)[J]. Trans Am Ophthalmol Soc, 2009, 107: 325–342. |
| [12] | Hollanders K, Van Bergen T, Van de Velde S, et al. Bevacizamab revisited:its use in different mouse models of ocular pathologies[J]. Curt Eye Res, 2015, 40(6): 611–621. DOI:10.3109/02713683.2014.943910 |
| [13] | Kowanetz M, Ferrara N. Vascular endothelial growth factor signaling pathways:therapeutic perspeetive[J]. Clin Cancer Res, 2006, 12(17): 5018–5022. DOI:10.1158/1078-0432.CCR-06-1520 |
| [14] | Haverly RF. Surgical management of neovascular glaucoma[J]. Tech Ophthalmol, 2010, 8: 87–93. DOI:10.1097/ITO.0b013e3181f14a44 |
| [15] | Lüke J, Nassar K, Lüke M, et al. Ranibizumah as adjuvant in the treatment of rubeosis iridis and neovascular glaucoma-results from a prospective interventional case series[J]. Graefes Arch Clin Exp Ophthalmol, 2013, 251(10): 2403–2413. DOI:10.1007/s00417-013-2428-y |
| [16] | Yalvac IS, Eksioglu U, Satana B. Long-term results of Ahmed glaucoma valve and Molteno implant in neovascular glaucoma[J]. Eye(Lond), 2007, 21(1): 65–70. |
| [17] | Shen CC, Salim S, Du H, et al. Trabeculectomy versus ahmed glaucoma valve implantation in neovascular glaucoma[J]. Clin Ophthalmol, 2011, 5: 281–286. |
| [18] | Wakabayashi T, Oshima Y, Sakaguchi H, et al. Iatravitreal bevacizumab to treat iris neovascularization and neovascular glaucoma secondary to ischemic retinal diseases in 41 consecutive cases[J]. Ophthalmol, 2008, 115(9): 1571–1581. DOI:10.1016/j.ophtha.2008.02.026 |
 2017, Vol. 43
2017, Vol. 43


