扩展功能
文章信息
- 司延芳, 莫冉冉, 李慧婷, 宋鹏, 李明娴
- SI Yanfang, MO Ranran, LI Huiting, SONG Peng, LI Mingxian
- 艾滋病伴肾上腺皮质功能减退症1例报告并文献复习
- AIDS complicated with adrenal insufficiency:A case report and literature review
- 吉林大学学报(医学版), 2017, 43(05): 1030-1033
- Journal of Jilin University (Medicine Edition), 2017, 43(05): 1030-1033
- 10.13481/j.1671-587x.20170532
-
文章历史
- 收稿日期: 2017-04-05
艾滋病即获得性免疫缺陷综合征(acquired immune dificiency syndrome, AIDS)与肾上腺皮质功能减退症(adrenal insufficiency, AI)临床表现缺乏特异性,且发病率均较低,临床医生诊断意识欠缺,极易发生误诊、漏诊和误治,而AIDS伴AI的诊断则更加困难。AIDS作为AI的一个重要病因越来越受到重视,而国内外对AIDS伴AI报道罕见。本院收治1例AIDS伴AI的患者,现将诊治经过进行总结,并进行相关文献复习,旨在提高人类免疫缺陷病毒(HIV)感染者并发AI的诊断率,有效降低死亡率。
1 临床资料 1.1 病例资料患者,男性,20岁。缘于7个月前无明显诱因出现乏力,就诊于当地医院,查血糖、甲状腺功能无明显异常,未经系统诊治自行出院,出院后上述症状反复出现。2个月前晕倒后致右侧额颞部损伤,伴抽搐,就诊于当地医院,诊断为“右侧额颞硬脑膜外血肿、蛛网膜下腔出血”,急诊行开颅血肿清除术,术前查HIV抗体可疑阳性,术后自觉乏力症状加重,并出现恶心、呕吐、消瘦和厌食等,给予对症治疗后症状略好转出院。出院4 d后上述症状再次出现,就诊于当地医院,给予补液、保护胃黏膜等对症支持治疗后症状未见明显好转,为求进一步系统诊治就诊于本院。近半年内体质量下降约5 kg。既往:带状疱疹病史2个月。2个月前晕倒后致右侧额颞硬脑膜外血肿、蛛网膜下腔出血,并行开颅血肿清除术,术后共输血3次。查体:血压90/60 mmHg,脉搏78 min-1,神情淡漠,言语欠流利;右侧额颞部头皮约7 cm手术切口,愈合良好;双上肢散在皮肤破溃,大小0.5 cm×0.5 cm,色素沉着;肝肋下3 cm;体质量指数(BMI)为15.63 kg·m-2,余查体未见异常。血常规:白细胞2.80×109 L-1,血红蛋白118 g· L-1,血小板53×109 L-1。血生化:钠离子121.0 mmol· L-1,氯离子82.9 mmol· L-1。肝功能:门冬氨酸氨基转移酶102.8 U· L-1,丙氨酸氨基转移酶121.1 U· L-1,γ-谷氨酰转肽酶84.6 U· L-1。复查肝功能:门冬氨酸氨基转移酶1 256.6 U· L-1,丙氨酸氨基转移酶974.6 U· L-1,γ-谷氨酰转肽酶108.8 U· L-1。甲状腺功能:促甲状腺激素17.70 mIU· L-1,FT3 3.07 pmol· L-1,FT4 13.71 pmol· L-1。泌乳素889.86 mIU· L-1,睾酮4.75 nmol· L-1。促肾上腺皮质激素(ACTH)(08:00)32.05 pmol· L-1;血清皮质醇(08:00):109.75 nmol· L-1。24 h尿游离皮质醇129.58 nmol·24 h-1。EB病毒衣壳抗原IgG抗体8.529 S/CO,EB病毒核心抗原IgG抗体5.033 S/CO。巨核细胞抗体IgG 7.431 S/CO,IgM 0.004 S/CO。T细胞亚群:辅助性T细胞(CD4+)0.3%,抑制/毒性T细胞(CD8+)79.4%,CD4+ /CD8+ 0.00。CD4+每微升2个。HIV抗体初筛试验阳性。结核T斑点阴性。痰培养:3 d未培养出真菌,正常菌群。痰结核菌涂片:未查到抗酸杆菌。真菌D-葡聚糖检测10 ng· L-1。抗核抗体系列、ANCA筛查与确证阴性。骨髓穿刺示有核细胞增生减低。垂体核磁未见异常。自带当地肺部CT示:右肺上叶炎症;双肺上叶及右肺下叶见结节影。肾上腺CT示双侧肾上腺显示欠清,肾上腺区未见明显异常密度影。
1.2 治疗和预后入院后给予补充糖皮质激素(8:00醋酸泼尼松5.0 mg口服、16:00醋酸泼尼松2.5 mg口服)、抗感染(头孢呋辛酯0.25 g,每天2次,口服)、改善肝功能(还原型谷胱甘肽1.8 g,每天1次,静脉输注)、纠正电解质紊乱、补液等对症治疗,12 d后患者乏力、恶心、呕吐症状消失,精神状态明显改善,食欲增加,复查电解质正常,建议出院后继续口服醋酸泼尼松(早上8点5.0 mg,下午4点2.5 mg)替代治疗,因患者HIV抗体初筛试验阳性,建议就诊于传染病医院进一步明确诊治。
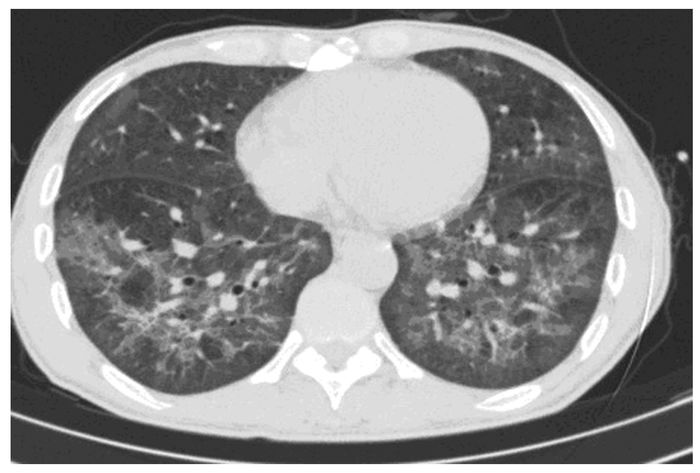
1.3 随访患者出院2周后就诊于长春市传染病医院,查HIV抗体初筛试验+确证试验阳性,开始抗HIV治疗。住院13 d时开始出现发热、咳嗽、胸闷,给予头孢曲松治疗1周病情无好转,最高体温达39.8℃。行肺部CT检查示双下肺弥漫分布的磨玻璃影(图 1)。高度怀疑“艾滋病并发卡氏肺孢子菌肺炎”。随后出现进行性加重的呼吸困难、抽搐、意识不清,血气分析显示氧分压45 mmHg,遂转入ICU继续治疗,给予经气管插管、呼吸机辅助通气,并行纤维支气管镜检查,肺泡灌洗液银染色提示存在卡氏肺囊虫,肺泡灌洗液培养出大量白色念珠菌,给予复方磺胺甲噁唑(SMZ-TMP)2片,每天3次,胃管入;卡泊芬净50 mg(首次70 mg),每天1次,静脉输注;甲强龙40 mg,每天2次,静脉输注,治疗3 d后,家属放弃治疗,要求出院,随访发现患者出院后半小时内死亡。
|
| 图 1 艾滋病并发卡氏肺孢子菌肺炎患者胸部CT表现 Figure 1 Appearence of chest CT in patient with AIDS complicated with pneumocystis carinii pneumonia |
|
|
2011年我国AIDS疫情估计[1]结果表明:全国AIDS疫情依然呈低流行态势,既往HIV感染者陆续进入发病期,AIDS发病率和死亡率持续增加。HIV感染后,造成CD4+ T淋巴细胞数量进行性减少,损坏细胞免疫功能,导致免疫功能缺陷,累及各个器官、系统,易患各种机会性感染和恶性肿瘤[2]。AIDS的国际诊断标准最主要的条件是卡波西肉瘤和机会性感染,实验室诊断为CD4+细胞计数下降和HIV抗体阳性。该患既往存在输血史,近半年明显消瘦,查体可见皮肤存在破溃,血常规提示三系降低,HIV抗体初筛试验阳性,查CD4+ /CD8+比例明显降低,CD4+每微升2个,进一步行HIV抗体确证试验阳性,AIDS诊断明确。
慢性AI早期症状缺乏特异性,且发病率较低,临床较为少见,临床医生诊断意识欠缺,因此早期诊断率不高[3]。主要表现为精神萎靡、疲乏无力、皮肤黏膜色素沉着、消瘦、食欲减退、恶心、呕吐、低血压、水电解质代谢紊乱及神经系统损害等症状[4]。根据病因可分为原发性、继发性2类。原发性者又称阿狄森病(Addison病),是由于自身免疫性疾病、结核、真菌、病毒等感染引起;较为少见的病因有AIDS、转移癌、淋巴瘤或白血病浸润、淀粉样变、肾上腺切除以及长期应用肾上腺酶系免疫抑制药物等原因破坏双侧肾上腺的绝大部分功能(约90%以上),从而导致肾上腺激素分泌不足[5]。继发性者是指下丘脑分泌促肾上腺皮质激素释放激素(CRH)或垂体分泌ACTH不足导致功能障碍后引起肾上腺皮质激素分泌不足[6]。原发性肾上腺皮质功能减退(PAI)最具特征的表现为全身皮肤色素沉着[3],暴露处、摩擦处、乳晕、瘢痕等处尤为明显。ACTH刺激试验是评估原发性和继发性AI的现行标准[7]。因条件所致,本院无法行ACTH刺激试验,且患者2个月前存在颅脑外伤史,鉴别原发与继发性肾上腺皮质功能减退症相对困难。考虑患者病史较短,以乏力、消瘦、食欲减退为主要表现,入院时存在严重电解质紊乱,ACTH上午8点32.05 pmol· L-1,皮质醇109.75 nmol· L-1,垂体核磁未见明显异常,患者AI诊断明确,虽无上述特征性表现,但考虑患者PAI可能性较大。
本例患者自身免疫性指标未见异常,可排除自身免疫性疾病所致AI。该患存在明显消瘦,BMI为15.63 kg·m-2,病程中无低热、咳嗽、咳痰和盗汗等结核中毒症状,结核T斑点阴性,肺CT未见结核病灶,肾上腺CT平扫未见钙化,考虑结核所致AI可能性不大。结合痰培养及真菌D-葡聚糖检测结果,考虑真菌所致AI可能性不大。患者既往无药物滥用史。综上所述,考虑患者AI与HIV感染有关。晚期AIDS患者常见的AI多由感染(巨细胞病毒、结核杆菌)、药物(酮康唑、蛋白酶抑制剂)、肿瘤(卡波西肉瘤、淋巴瘤)等引起[8]。患者结核T斑点阴性,肺CT未见结核病灶,肾上腺CT平扫未见钙化,无酮康唑及蛋白酶抑制剂等药物应用史,未见明确肿瘤证据,而患者存在肝脏肿大,肝功能明显异常,甲乙丙戊肝炎抗体阴性,巨细胞病毒IgG抗体升高,虽IgM抗体阴性(在感染早期及免疫缺陷患者可呈假阴性),但2个月前患者曾患带状疱疹,推测患者AIDS晚期因病毒感染所致AI可能性大。该患者辅助检查提示甲状腺、性腺和肾上腺等均存在不同程度的改变。这与Tripathy等[9]研究相同:在AIDS患者中甲状腺、肾上腺、性腺是最常累及的内分泌腺。
HIV感染是AI的一个重要危险因素。研究[10]显示:在多达60%的HIV感染者或A IDS患者尸检中发现AI。虽然肾上腺是HIV感染影响最常见的器官,但是HIV感染所致AI的临床诊断十分困难。首先,HIV感染和AI有很多相似症状,如消瘦、萎靡、虚弱和腹泻等;其次,AI的相关症状直到肾上腺皮质损害超过80%时才会表现出来[11];再次,HIV感染患者的皮质醇基线水平通常是正常或升高,仅有8 %~14%患者的皮质醇基线水平被发现低于正常范围[12]。因此,当患者出现无法解释的症状,如厌食、恶心、消瘦及更具特征性的表现(如体位性低血压、低钠血症或高钾血症时)应考虑到AI[13-14],临床医生应尽早为此类患者行ACTH刺激试验及ACTH、皮质醇检测,以准确判断HIV感染者是否伴有AI,及早的糖皮质激素替代治疗可有效改善HIV感染并发AI患者的临床症状及预后,降低死亡率[15-16]。
综上所述,文献检索显示国内外类似病例不多,特此报道旨在提高临床医生对HIV感染者并发AI的认识,提高该病的诊断率,并有效降低死亡率。
| [1] | 中华人民共和国卫生部, 联合国艾滋病规划署, 世界卫生组织. 2011年中国艾滋病疫情估计[J]. 中国艾滋病性病, 2012, 18(1): 1–5. |
| [2] | 张瑶, 韩冰, 王连双, 等. 艾滋病合并特殊感染及肿瘤的超声声像图与超声造影表现[J]. 河北医药, 2017, 39(10): 1514–1517. |
| [3] | 余剑波, 周倩云. 慢性肾上腺皮质功能减退症十例诊治分析[J]. 中国全科医学, 2015, 18(32): 3997–3998. DOI:10.3969/j.issn.1007-9572.2015.32.025 |
| [4] | 彭广波. 慢性肾上腺皮质功能减退症的临床治疗体会[J]. 世界最新医学信息文摘, 2016, 16(7): 172–173. |
| [5] | Pazderska A, Pearce SH. Adrenal insufficiency-recognition and management[J]. Clin Med, 2017, 17(3): 258–262. DOI:10.7861/clinmedicine.17-3-258 |
| [6] | 张妍, 王亮, 宋晓艳, 等. 以反复呕吐为首发表现的肾上腺皮质功能减退症一例报道及文献复习[J]. 空军医学杂志, 2014, 30(3): 146–148. |
| [7] | Struja T, Briner L, Meier A. Diagnostic accuracy of basal cortisol level to predict adrenal insufficiency in cosyntropin testing results from an observational cohort study with 804 patients[J]. Endocr Pract, 2017, 23(5): 228–232. |
| [8] | Lo J, Grinspoon SK. Adrenal function in HIV infection[J]. Curr Opin Endocrinol Diabetes Obes, 2010, 17(3): 205–209. DOI:10.1097/MED.0b013e3283394441 |
| [9] | Tripathy SK, Agrawala RK, Baliarsinha AK. Endocrine alterations in HIV-infected patients[J]. Indian J Endocr Metab, 2015, 19(1): 143–147. DOI:10.4103/2230-8210.146870 |
| [10] | Marik PE, Kiminyo K, Zaloga GP. Adrenal insufficiency in critically ill patients with human immunodeficiency virus[J]. Crit Care Med, 2002, 30(6): 1267–1273. DOI:10.1097/00003246-200206000-00018 |
| [11] | Bricaire F, Marche C, Zoubi D, et al. Adrenocortical lesions and AIDS[J]. Lancet, 1988, 1(8590): 881. |
| [12] | Villette JM, Bourin P, Doinel C, et al. Circadian variations in plasma levels of hypophyseal, adrenocortical and testicular hormones in men infected with human immunodeficiency virus[J]. J Clin Endocrinol Metab, 1990, 70(3): 572–577. DOI:10.1210/jcem-70-3-572 |
| [13] | Eledrisi MS, Verghese AC. Adrenal insufficiency in HIV infection:A review and recommendations[J]. Am J Med Sci, 2001, 321(2): 137–144. DOI:10.1097/00000441-200102000-00005 |
| [14] | Lo J, Grinspoon SK. Adrenal function in HIV infection[J]. Curr Opin Endocrinol Diabetes Obes, 2010, 17(3): 205–209. DOI:10.1097/MED.0b013e3283394441 |
| [15] | Freda PU, Wardlaw SL, Brudney K, et al. Primary adrenal insufficiency in patients with the acquired immunodeficiency syndrome:A report of five cases[J]. J Clin Endocrinol Metab, 1994, 79(6): 1540–1545. |
| [16] | 巩纯秀. 肾上腺危象处理[J]. 中国实用儿科杂志, 2016, 31(6): 425–428. |
 2017, Vol. 43
2017, Vol. 43


