扩展功能
文章信息
- 杨竹君, 侯旭, 于文雯, 闫阔, 申玉芹, 孙新华
- YANG Zhujun, HOU Xu, YU Wenwen, YAN Kuo, SHEN Yuqin, SUN Xinhua
- MT01对实验性牙移动大鼠牙周组织中TLR9、TRAF6和IL-6表达水平的影响
- Effects of MT01 on expressions of TLR9, TRAF6 and IL6 in periodontal tissue during experimental tooth movement of rats
- 吉林大学学报(医学版), 2017, 43(04): 752-756
- Journal of Jilin University (Medicine Edition), 2017, 43(04): 752-756
- 10.13481/j.1671-587x.20170418
-
文章历史
- 收稿日期: 2016-09-19
2. 吉林省牙发育及颌骨重塑与再生重点实验室, 吉林 长春 130021;
3. 吉林大学口腔医院儿童口腔科, 吉林长春 130021;
4. 吉林大学口腔医院牙周病科, 吉林 长春 130021
2. Jilin Provincial Key Laboratory of Tooth Development and Bone Remodel, Changchun 130021, China;
3. Department of Pediatric Dentistry, Stomatology Hospital, Jilin University, Changchun 130021, China;
4. Department of Periodontology, Stomatology Hospital, Jilin University, Changchun 130021, China
正畸牙移动是压力侧骨吸收伴随张力侧骨形成的骨改建的动力平衡过程。研究[1]认为:该过程可能是牙周组织在机械力作用下通过激活T细胞进而引发炎症反应造成的。许多免疫介质如炎症因子和生长因子等都参与正畸牙移动过程[2]。牙齿移动早期多伴有急性炎症反应,牙周血管扩张,大量白细胞游走迁移,随后反应减缓被慢性炎症反应替代。Toll样受体9(Toll-like receptors 9,TLR9) 作为TLRs家族中重要一员,其通过识别细菌和病毒DNA中的CpG基序或人工合成的寡脱氧核糖核酸(CpGoligodeoxy nucleo tides, CpG-ODN)参与炎症反应[3];肿瘤坏死因子受体相关因子6 (tumor necrosis factor receptor-associated factor 6, TRAF6) 作为TLR9信号转导过程中的关键分子,通过自身泛素化或以复合物形式调控炎症反应及炎症介质的释放; IL-6作为TLR9-TRAF6信号通路活化后释放的炎症介质之一,参与了牙移动过程中的骨代谢及炎症反应,加速牙槽骨吸收。目前TLR9信号通路在自身免疫性疾病领域中研究较多,TLR9信号的持续活化或失调可能引发如类风湿关节炎和系统性红斑狼疮等自身免疫性疾病[4-6], 但尚未见对于TLR9信号通路与正畸牙周组织改建的相关研究报道。
特定序列寡核苷酸MT01是本课题组根据人线粒体DNA序列设计的单链寡脱氧核苷酸(oligodeoxynucleotides,ODN)。前期的研究[7-9]表明:MT01能够抑制由TLR9激活引起的机体固有免疫应答,防止组织细胞受损,具有促成骨细胞分化的功能,能够减少大鼠正畸牙移动的距离。目前,MT01对牙移动过程中牙周组织成骨作用及对牙周炎抑制作用研究较多,但在牙移动过程中MT01对牙周组织炎症反应的影响及作用尚未见报道。本研究将通过建立正畸大鼠牙移动模型,观察牙移动过程中牙周组织IL-6和TLR9表达水平的变化,并通过MT01干预观察其对牙移动过程中牙周组织TLR9信号通路的影响,阐明MT01对实验性牙移动过程中牙周组织炎症反应的调控作用。
1 材料与方法 1.1 实验动物和主要试剂7周龄Wistar雄性大鼠30只,延边大学实验动物中心提供,生产许可证号:SCXK(吉)2011-0007,体质量(180±10) g。MT01 (5′-ACCCCCTCTACCCCCTCTACCCCCTCT-3′),吉林大学基础医学院分子生物学教研室设计,大连TaKaRa公司合成。组织细胞总RNA抽提试剂盒(广州Magen公司),逆转录试剂盒和PCR试剂盒(大连TaKaRa公司)。
1.2 实验分组所有大鼠均分笼饲养, 自由摄食饮水, 每12h昼夜交替。适应性饲养1周后,随机分为2组:无MT01干预组大鼠24只,右侧加力为实验组,左侧不加力为对照组;MT01干预组大鼠6只,左侧加力+MT01为实验组,右侧加力+PBS为对照组。
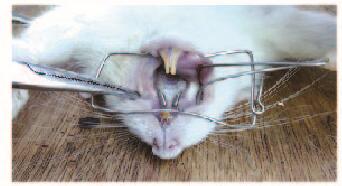
1.3 正畸牙移动模型的建立10%水合氯醛经腹腔麻醉(3 mL·100 g-1),使用牙科细金刚砂车针在实验动物上颌第一磨牙和左、右侧上颌切牙近牙龈缘处作深约0.20 mm浅固位沟, 再用0.20 mm不锈钢结扎丝将镍钛拉簧固定于上颌前牙与第一磨牙之间,以双侧切牙为支抗,0.49N力牵引上颌第一磨牙向近中移动。每天检查装置,如有脱落及时重新结扎。见图 1(封三)。
|
| 图 1 大鼠正畸牙移动模型 Figure 1 Model of orthodontic tooth movement of rats |
|
|
牙移动模型建立后,于MT01干预组大鼠左侧上颌第一磨牙颊侧牙龈黏膜下注射MT01 (20 mg·L-1)50 μL;并于右侧相同部位注射等量的PBS溶液。此后每3d注射1次,直至实验结束。
1.5 标本取材在无MT01干预组正畸加力后第3、7、14和21天各随机处死6只大鼠,获取上颌第一磨牙牙槽骨即刻提取RNA。MT01干预组的模型建立、给药及取材均待以上实验结果分析完成后进行。
1.6 总RNA的提取和质量控制总RNA的获取:取大鼠上颌第一磨牙近远中各约1.5mm宽的牙槽骨组织约60mg,HiPure Total RNA试剂盒分别提取上颌双侧第一磨牙近远中牙槽骨组织中的总RNA。NanoDrop 1000 Spectrophotometer核酸蛋白定量仪分别测定各样品总RNA浓度和纯度[A(260)/A(280)],结果显示:TLR9、TRAF6和IL-6RNA量充足,A(260)/A(280) 在1.8~2.0。逆转录试剂盒反转录合成cDNA,-20℃保存备用。
1.7 引物设计TLR9引物序列:上游引物5′-TGCTGCCCAGTTTGTCAGAG-3′,下游引物5′-ATGAGGCTTCAGTTCACAGGGTAG3′,扩增片段长度为171 bp。TRAF6引物序列:上游引物5′-TTTGGCGTCGGAGACACTTG-3′,下游引物5′-TCGCTTGAAGACTGGCTGGA-3′,扩增片段长度为180 bp。IL-6引物序列:上游引物5′-ATTGTATGAACAGCGATGATGCAC-3′,下游引物5′-CCAGGTAGAAACGGAACTCCAGA-3′, 扩增片段长度为150 bp。Actb引物序列:上游引物5′-GGAGATTACTGCCCTGGCTCCTA-3′,下游引物5′-GACTCATCGTACTCCTGCTTGCTG-3′,扩增片段长度为150 bp。
1.8 实时荧光定量PCR(RT-PCR)检测RT-PCR反应体系:上、下游引物(10 μmol·L-1)各0.5 μL,DyeⅡ0.5 μL,cDNA2 μL,SYBRPremixExTaq12.5 μL,蒸馏水补总体积至25 μL。反应条件:95℃、60s,95℃、5s,60℃、60s, 95℃延伸15s, 循环40次。采用M×3005P实时荧光定量PCR仪联机软件测定Ct值,确认反应的扩增曲线和熔解曲线,生成曲线为完全单一峰。以Actb为内参基因,采用相对定量2-ΔCt法计算实验组目的基因表达相对于对照组的变化倍数,代表实验组TLR9、TRAF6和IL-6mRNA的相对表达水平。
1.9 统计学分析采用SPSS17.0统计软件进行统计学分析。各组大鼠牙周组织中TLR9、TRAF6和IL-6mRNA相对表达水平以x±s表示,组间比较采用t检验。检验水准为双侧α=0.05。
2 结果 2.1 无MT01干预大鼠牙周组织中IL-6和TLR9mRNA表达水平无MT01干预大鼠各个时间点的实验组张力侧和压力侧牙周组织中IL-6mRNA表达水平均高于对照组(P < 0.05)。进一步分析,张力侧和压力侧牙周组织中IL-6mRNA表达水平在加力后3d即较对照组明显升高(P < 0.01),并随时间延长而增加,第7天达高峰且明显高于对照组(P < 0.01),第14天明显降低,但实验组仍高于对照组(P < 0.05), 第21天表达水平趋于稳定,与14d时比较差异无统计学意义(P > 0.05)。见表 1。
| (n=6, x±s) | |||||
| Group | IL-6 mRNA | ||||
| (t/d) 3 | 7 | 14 | 21 | ||
| Control | |||||
| Tension lateral | 1.000 0±0. 101 9 | 1.000 0±0.0810 | 1. 000 0±0. 066 5 | 1. 000 0±0.094 3 | |
| Compression lateral | 1. 000 0±0. 092 5 | 1.000 0±0.204 6 | 1. 000 0±0.010 6 | 1. 000 0±0.057 6 | |
| Experiment | |||||
| Tension lateral | 5.566 1 ±0. 503 9** | 11.4716 ± 0.890 5** | 1. 286 4±0. 111 7** | 4. 856 8±0. 103 9 ** | |
| Compression lateral | 2.188 6 ± 0. 114 7** | 12.097 8 ± 0.734 6 ** | 1. 427 3±0. 145 4** | 1. 366 0±0. 027 6 ** | |
| * P < 0.05, ** P < 0.01 compared with control group. | |||||
无MT01干预大鼠各个时间点的实验组张力侧和压力侧牙周组织中TLR9mRNA表达水平均高于对照组(P < 0.05)。进一步分析,牙周组织中TLR9mRNA表达水平在加力后的3~7d随时间延长而增加,第7天时表达水平达高峰且明显高于对照组(P < 0.01),在加力后的14~21 d逐渐降低,但组间比较差异仍有统计学意义(P < 0.01)。见表 2。
| (n=6, x±s) | |||||
| Group | TLR9 mRNA | ||||
| (t/d) 3 | 7 | 14 | 21 | ||
| Control | |||||
| Tension lateral | 1.000 0±0. 019 5 | 1.000 0±0.110 9 | 1. 000 0±0.010 6 | 1. 000 0±0.120 7 | |
| Compression lateral | 1.000 0±0. 123 5 | 1.000 0±0.064 3 | 1. 000 0±0.016 1 | 1.000 0±0.033 3 | |
| Experiment | |||||
| Tension lateral | 1.457 3±0.063 0** | 4.000 0±0.287 6** | 2.657 4 ± 0.099 3** | 2.445 3±0.075 0** | |
| Compression lateral | 1.259 9±0.104 4** | 2.639 0±0.1610** | 2.089 8 ± 0.247 8** | 1.713 2±0.045 5** | |
| * P < 0.05, ** P < 0.01 compared with control group. | |||||
加力7d后,MT01干预大鼠实验组张力侧和压力侧牙周组织中TLR9mRNA表达水平明显低于对照组(P < 0.01),实验组压力侧牙周组织中TRAF6mRNA表达水平明显低于对照组(P < 0.01), 实验组张力侧牙周组织中TRAF6mRNA表达水平与对照组比较有下降趋势,但组间比较差异无统计学意义(P > 0.05);实验组和对照组大鼠牙周组织中IL-6mRNA表达水平比较差异均无统计学意义(P > 0.05)。见表 3。
| (n=6, x±s) | |||
| Group | TLR9 mRNA | TRAF6 mRNA | IL-6 mRNA |
| Control | |||
| Tension lateral | 1. 000 0±0. 094 8 | 1. 000 0±0. 156 7 | 1. 000 0±0. 214 9 |
| Compression lateral | 4.179 5±0. 044 5 | 1. 234 0±0. 072 0 | 1. 914 1±0. 344 2 |
| Experiment | |||
| Tension lateral | 0.732 0±0. 092 4* | 0. 935 1±0. 024 8 | 0. 959 2±0. 139 2 |
| Compression lateral | 1.588 1 ±0. 302 2* | 0. 903 3±0. 351 5* | 2. 018 5±0. 167 9 |
| * P < 0.01 compared with control group. | |||
研究[10]表明:与正常牙周组织比较,正畸力作用下的牙周组织张力侧和压力侧炎症因子表达有不同程度升高。IL-6作为正畸牙移动的早期生物指标之一,在正畸牙移动和牙周炎的发生发展过程中起重要作用。研究[11]表明:IL-6参与牙移动的骨代谢过程,抑制牙周膜的代谢和修复功能,从而加速牙槽骨吸收。本研究结果显示:在牙移动3d后IL-6即有较高水平表达,且第7天表达水平达高峰,后呈下降趋势,但第21天时表达水平仍高于对照组且差异有统计学意义。TLRs作为模式识别受体(PRRs)中的主要家族,通过识别病原体相关分子模式(pathogen associated molecular pattern, PAMP)激活免疫细胞, 在天然免疫防御病原体中起重要作用。长期以来,天然免疫被认为是免疫系统的低级形式。随着近年来研究的不断深入,人们逐渐认识到天然免疫的另一方面:TLR在启动免疫防御反应的同时,也可能导致对机体有害的急慢性炎症反应和自身免疫反应的发生[12]。其中,TLR9为细胞内受体,主要存在于内质网、内体和溶酶体中,能识别细菌和病毒的核酸成分(DNA或RNA)[13]。本实验结果显示:无MT01干预大鼠,实验组张力侧和压力侧牙周组织中TLR9mRNA表达水平在加力3、7、14和21d均明显高于对照组,第7天时表达水平达高峰,表明即使无感染存在, 外力作用状态下的牙周组织细胞发出的信号也可以引发TLR9介导的免疫反应, 并参与组织的免疫调节。
本研究结果显示:正畸力作用7d时为牙周组织反应活跃期,TLR9和IL-6mRNA表达水平亦达高峰。基于上述结果,本研究选用MT01进行干预,检测牙移动7 d时相关细胞因子表达水平的结果显示:与对照组比较,实验组张力侧和压力侧TLR9mRNA及压力侧TRAF6 mRNA表达水平均明显降低。TRAF6是TRAFs家族一员,但与其他成员比较又有其独特的生理作用,即TRAF6参与肿瘤坏死因子受体(TNFR)和IL1-R/TLR超家族的信号转导,参与TLRs依赖MY-D88的活化反应[14-15],TRAF6与白细胞介素1受体相关激酶(IRAK)-1C末端反应诱导下游信号通路活化,如MAPK级联反应及NF-κB信号通路[16],活化的NF-κB引发白细胞黏附分子上调并产生促炎因子,最终促进炎症发生。所以本文作者推测:在MT01靶向抑制TLR9后,作为其信号转导过程中的重要分子TRAF6也受到明显抑制,并可能抑制最终炎症反应,从而抑制压力侧牙槽骨吸收程度,进而抑制正畸牙移动进程,该推测与前期研究[17]结果相符。本研究结果显示:2组大鼠牙周组织中IL-6mRNA表达水平比较差异无统计学意义,可能由于IL-6作为此通路活化后的末端因子,MT01虽在牙移动7d时对该通路有抑制作用,但其下游分子未必立即受到调控,因此在后期实验中可延长MT01的干预时间,进一步观察下游因子的变化情况。
| [1] | Graves DT, Kayal RA, Oates T, et al. Osteoimmunology in the oral cavity (periodontal disease, lesions of endodontic origin and orthodontic tooth movement)[J]. Osteoimmunology, 2016: 325–344. |
| [2] | Di DM, D'Apuzzo F, Feola A, et al. Cytokines and VEGF induction in orthodontic movement in animal models[J]. Biomed Res Int, 2012, 2012(5): 33–36. |
| [3] | Zhang D. A toll-like receptor that prevents infection by uropathogenic bacteria[J]. Science, 2004, 303(5663): 1522–1526. DOI:10.1126/science.1094351 |
| [4] | Lacerte P, Brunet A, Egarnes B, et al. Overexpression of TLR2 and TLR9 on monocyte subsets of active rheumatoid arthritis patients contributes to enhance responsiveness to TLR agonists[J]. Arthri Res Ther, 2016, 18(1): 1–14. DOI:10.1186/s13075-015-0906-9 |
| [5] | Devaraju P, Gulati R, Antony PT, et al. Susceptibility to SLE in South Indian Tamils may be influenced by genetic selection pressure on TLR2 and TLR9 genes[J]. Mol Immunol, 2015, 64(1): 123–126. DOI:10.1016/j.molimm.2014.11.005 |
| [6] | Rao H, Zeng Q, Liang Y, et al. Correlation between TLR9 expression and cytokine secretion in the clinical diagnosis of systemic lupus erythematosus[J]. Mediators Inflamm, 2015, 2015: 710720. |
| [7] | Yang G, Wan M, Zhang Y, et al. Inhibition of a C-rich oligodeoxynucleotide on activation of immune cells in vitro, and enhancement of antibody response in mice[J]. Immunology, 2010, 131(4): 501–512. DOI:10.1111/j.1365-2567.2010.03322.x |
| [8] | Xu H, Yuqin S, Chao Z, et al. A Specific oligodeoxy nucleotide promotes the differentiation of osteoblasts via ERK and p38 MAPK pathways[J]. Int J Mol Sci, 2012, 13(12): 7902–7914. DOI:10.3390/ijms13077902 |
| [9] | 王静, 孙新华, 冯志远, 等. 特定寡核苷酸对大鼠实验性牙移动的影响[J]. 吉林大学学报:医学版, 2011, 37(5): 812–816. |
| [10] | Meeran NA. Cellular response within the periodontal ligament on application of orthodontic forces[J]. J Indian Soc Periodontol, 2013, 17(1): 16–20. DOI:10.4103/0972-124X.107468 |
| [11] | Nokhbehsaim M, Deschner B, Winter J, et al. Contribution of orthodontic load to inflammationmediated periodontal destruction[J]. For Der Kie, 2010, 71(6): 390–402. |
| [12] | Liang J, Luan Y, Lu B, et al. Protection of ischemic postconditioning against neuronal apoptosis induced by transient focal ischemia is associated with attenuation of NF-κB/p65 activation[J]. PLos One, 2014, 9(5): 1–7. |
| [13] | Liu Z, He D, Zhang X, et al. Neuroprotective effect of early and short-time applying sophoridine in pMCAO rat brain:down-regulated TRAF6 and up-regulated p-ERK1/2 expression, ameliorated brain infaction and edema[J]. Brain Res Bull, 2012, 88(4): 379–384. DOI:10.1016/j.brainresbull.2012.04.003 |
| [14] | 米丛波, 刘红, 钱雅婧, 等. 正畸力作用下大鼠牙周组织中肝细胞生长因子的表达[J]. 牙体牙髓牙周病学杂志, 2010(11): 622–625. |
| [15] | 靳玫, 刘晓利, 唐超智, 等. Toll样受体在大鼠大脑皮层发育过程中的表达[J]. 郑州大学学报:医学版, 2017, 52(1): 41–44. |
| [16] | Yang JH, Li ZC, Kong WD, et al. Effect of orthodontic force on inflammatory periodontal tissue remodeling and expression of IL-6 and IL-8 in rats[J]. Asian Pac J Tropl Med, 2013, 6(10): 757–761. DOI:10.1016/S1995-7645(13)60133-9 |
| [17] | 冯志远. 寡核苷酸(ODN)促成骨细胞增殖活化的作用及机制研究[D]. 长春: 吉林大学, 2011. |
 2017, Vol. 43
2017, Vol. 43


