扩展功能
文章信息
- 石立强, 陈丽娜, 李洪宇, 谢立亚, 糜心雅, 苑广信, 孙晶波, 王曼力, 徐广宇, 韩笑, 赵南晰, 盛瑜, 杜培革, 安丽萍
- SHI Liqiang, CHEN Lina, LI Hongyu, XIE Liya, MI Xinya, YUAN Guangxin, SUN Jingbo, WANG Manli, XU Guangyu, HAN Xiao, ZHAO Nanxi, SHENG Yu, DU Peige, AN Liping
- 吉林大学学报(医学版), 2016, 42(04): 742-745
- Journal of Jilin University (Medicine Edition), 2016, 42(04): 742-745
- 10.13481/j.1671-587x.20160421
-
文章历史
- 收稿日期: 2016-01-04
酒精性肝炎作为进行性疾病,往往导致肝硬化和肝癌,其重症患者短期死亡率很高[1, 2]。小牛血去蛋白提取物(deproteiniz edextract of calf blood,DECB)是一种从小牛血清中提取的小分子生物活性物质,其中30%的有机成分包括低分子多肽、核苷、氨基酸和寡糖等。目前临床上DECB主要用于治疗脑细胞代谢障碍性疾病,同时还具有角膜修复功能[3, 4]。本课题组一直致力于DECB相关研究,改进其生产工艺,提高药效学活性,这种DECB生产工艺已经获得国家授权专利(专利号:201210434370.7)[5]。有研究[6, 7]表明:DECB具有消除氧自由基、促进细胞修复等作用。但其对肝组织的保护作用鲜少报道。本研究以DECB作为解酒及保肝剂,在构建小鼠酒精性肝损伤模型基础上,观察其解酒及保肝作用,并初步探讨其作用机制。
1 材料与方法 1.1 动物、主要试剂和仪器健康ICR小鼠60只,雄性,体质量( 20±2) g,由吉林省长春市亿斯实验动物技术有限责任公司提供(许可证号: 201500010623)。DECB由长春长庆药业有限公司提供,护肝片由黑龙江葵花药业股份有限公司提供(批号201408073),谷胱甘肽(GSH)、丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、丙二醛( MDA) 和甘油三酯(TG)试剂盒均购自南京建成生物工程研究所(批号分别为20150611、20150508、20150607、20150426和20150523)。SPX-250B-Z型恒温生化培养箱(上海博远实业有限公司),5430R低温高速离心机(美国Eppendorf公司),Infinite M200型酶标仪(瑞士TECAN公司)。
1.2 动物分组和给药健康ICR小鼠60 只适应性喂养3 d。随机分为对照组、模型组、阳性药物组和低、中、高剂量DECB组,每组10只。对照组小鼠给予生理盐水20 mL·kg -1,每天1 次,低、中和高剂量DECB组小鼠分别给予0.125、0.250和0.500 g·kg -1 DECB;阳性药物组小鼠给予护肝片0.63g·kg-1,模型组小鼠给予20 mL·kg -1生理盐水,连续灌胃给药30 d。
1.3 急性酒精性肝损伤模型制备除对照组外,其余各组小鼠均在末次给药1h后,一次性给予50%乙醇14mL·kg -1,空白组小鼠给予等量的生理盐水灌胃。记录各组小鼠的耐受酒精时间(从灌酒到翻正反射消失)和醉酒时间(从翻正反射消失到翻正反射重新开始)。造模结束后,模型组死亡1只小鼠,低剂量DECB组死亡2只小鼠,其他各组无死亡情况。
1.4 小鼠血清生化指标检测各组小鼠禁食16 h 后,取外周血,离心血清,按照试剂盒说明书方法测定ALT和AST活性。取小鼠肝脏,用冷生理盐水冲洗后制备10%肝匀浆,离心后取上清,参照试剂盒说明书方法测定TG、GSH及MDA水平。
1.5 小鼠肝组织HE染色取小鼠肝脏,用10%中性甲醛固定,常规石蜡包埋、切片,HE 染色,光镜下观察小鼠肝组织病理学表现。
1.6 统计学分析 采用SPSS 16.0统计软件进行统计学分析。小鼠酒精耐受时间和醉酒时间,血清ALT和AST活性,肝组织中TG、GSH和MDA水平均以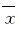 ±s表示,组间比较采用t检验。以p<0.05为差异有统计学意义。
±s表示,组间比较采用t检验。以p<0.05为差异有统计学意义。
与模型组比较,各剂量DECB组小鼠醉酒症状均明显减轻。 与模型组比较,高剂量DECB组和阳性药物组小鼠酒精耐受时间延长(P<0.05),醉酒时间缩短(P<0.05)。见表1。
(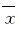 ±s,t/min) ±s,t/min) | |||
| Group | n | Endurance time | Drunk time |
| Control | 10 | - | - |
| Model | 9 | 11.10±3.13 | 167.63±16.12 |
| DECB | |||
| Low | 10 | 16.43±8.21 | 140.56±12.44 |
| Medium | 10 | 18.33±10.45 | 124.95±12.43 |
| High | 8 | 22.25±7.44 * | 117.51±16.28 * |
| Positive drug | 10 | 20.20±7.84 * | 120.43±15.36 * |
| “-”:No data. * P<0.05 vs model group. | |||
与对照组比较,模型组小鼠血清ALT和AST 活性均明显升高( P<0.05);与模型组比较,中、高剂量DECB组和阳性药物组小鼠血清ALT和AST 活性明显降低( P<0.05)。见表2
[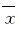 ±s,λB/(IU·L-1)] ±s,λB/(IU·L-1)] | |||
| Group | n | ALT | AST |
| Control | 10 | 20.03±2.41 | 36.02±7.71 |
| Model | 9 | 43.26±9.95 * | 58.41±7.88 * |
| DECB | |||
| Low | 10 | 37.86±7.53 | 49.25±6.25 |
| Medium | 10 | 27.27±8.62 △ | 43.46±7.23 △ |
| High | 8 | 26.95±4.47 △ | 40.21±4.44 △ |
| Positive drug | 10 | 25.72±8.22 △ | 40.66±9.58 △ |
| * P<0.05 vs control group; △ P<0.05 vs model group. | |||
与对照组比较,模型组小鼠肝组织GSH水平明显降低( P<0.05),MDA 和TG水平明显升高(P<0.05)。与模型组比较,中、高剂量DECB组和阳性药物组小鼠肝组织GSH水平明显升高(P<0.05) , 各剂量DECB组小鼠肝组织MDA和TG 水平明显降低(P<0.05)。见表3。
(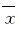 ±s) ±s) | ||||
| Group | n | GSH [wB /(mg·g-1)] | MDA [mB /(μmol·g-1)] | TG [cB /(mmol·L-1)] |
| Control | 10 | 5.47±1.62 | 8.59 ±4.08 | 0.18±0.04 |
| Model | 9 | 1.87±0.53 * | 35.06 ±18.91 * | 1.13±0.19 * |
| DECB | ||||
| Low | 10 | 2.35±0.78 | 19.39±11.19 △ | 0.74±0.34 △ |
| Medium | 10 | 3.92±1.64 △ | 19.34 ±8.55 △ | 0.51±0.27 △ |
| High | 8 | 2.99±0.87 △ | 17.76 ±6.06 △ | 0.63±0.25 △ |
| Positive drug | 10 | 4.20±0.93 △ | 15.72±11.41 △ | 0.42±0.36 △ |
| * P<0.05 vs control group; △ P<0.05 vs model group. | ||||
光镜下观察,对照组小鼠肝组织中肝细胞排列整齐,核仁清晰,肝细胞内胞浆丰富,呈红色,细胞核呈圆形,核内染色质呈现蓝色,肝窦大小正常,肝脏无异常病理改变;模型组小鼠肝组织可见肝索紊乱、胞质疏松,肝细胞呈现不同程度的变性改变,大量肝细胞表现为水样变性,细胞浆疏松呈网状结构,呈现淡红色,胞质内可见大小不一的脂滴空泡,可见淋巴细胞浸润,未见明显肝纤维化改变;不同剂量DECB组小鼠肝组织可见散在水样变性细胞,程度较模型组减轻,细胞轻度肿大。见图1(插页四)。
3 讨 论长期大量酒精摄入可引起酒精性肝病,其发病机制尚不清楚。近年来,学术界普遍认为氧化应激在酒精性肝损伤中起重要作用[8, 9]。在酒精氧化过程中消耗大量GSH,产生大量氧自由基(OH-、O2-、H2O2),引起氧化应激和线粒体功能障碍,进一步干扰脂肪酸代谢,加重脂肪积累,加速肝脏内细胞死亡[10, 11, 12, 13, 14]。本研究中酒精性肝损伤模型小鼠出现严重的酒精代谢导致的肝损伤,显示肝组织脂肪变性以及血清ALT和AST活性明显升高,肝组织中TG水平明显升高,出现脂肪变性;同时,肝脏发生较强的氧化应激,肝组织中GSH水平明显降低,脂质过氧化物MDA水平肝组织中明显升高;而DECB能明显降低血清ALT和AST活性和肝组织中TG和MDA水平,明显升高小鼠肝组织中GSH水平,提示DECB可以通过降低肝脏氧化应激程度改善酒精代谢所导致的急性肝损伤。DECB中起作用的主要成分为磷酸肌醇寡糖和小分子激活肽,其能够促进细胞对葡萄糖和氧的摄取和利用(不依赖于胰岛素),促进线粒体呼吸,从而提高ATP的周转,为细胞提供较高的能量。在低血氧以及能量需求量增加的情况下使葡萄糖的无氧代谢转向为有氧代谢,抑制乳酸合成,及时恢复肝脏必需的有氧代谢和能量供应,阻止受损肝组织细胞的进一步恶化,延长细胞生存时间,增加供血量[15, 16, 17, 18]。
综上所述,高剂量DECB对急性酒精性肝损伤有较明显的保护作用,可减轻酒精对肝脏的脂质过氧化损伤,降低血清转氨酶和TG水平,改善肝脏的组织病理学损伤,其作用机制可能是通过促进细胞对氧的摄取,促进血中葡萄糖进入细胞,明显延长缺氧细胞的生存时间,改善能量代谢,增强GSH对活性氧簇的清除能力,从而减轻酒精对肝细胞的直接损害,保护肝细胞并恢复肝功能。
| [1] | Brandon-Warner E, Schrum LW,Schmidt CM, et al. Rodent models of alcoholic liver disease: of mice and men[J]. Alcohol, 2012,46(8):715-725. |
| [2] | 吕晓梅,马丽杰.中药治疗急性肝损伤的研究进展[J].中国新药杂志,2016 ,25 (2):170-174. |
| [3] | Macheret IL, Khanenko NV. Drug therapy of patients with dyscirculatory encephalopathy[J].Lik Sprava,2002,7(3/4):84-87. |
| [4] | Lv H,Liu Z,Li X, et al.Effect of lacrimal plugs combined with deproteinized calf blood extract eye gel for filamentary keratitis[J].JOcul Biol Dis Infor ,2010,3(4):134-140. |
| [5] | 北华大学.小牛血去蛋白提取物及制备工艺[P].中国医药技术领域,201210434370.7.2013-02-06. |
| [6] | Chow JM,Shen SC,Huan SK, et al.Quercetin, but not rutin and quercitrin, prevention of H2O2-induced apoptosis via anti-oxidant activity and heme oxygenase 1 gene expression in macrophages[J]. Biochem Pharmacol,2005,69(12):1839-1851. |
| [7] | 亢泽春,刘少华,高 聪.鸡血藤总黄酮对酒精性肝损伤的保护作用及机制[J]. 中国老年学杂志,2013,23(33): 5951-5953. |
| [8] | Lucey MR,Mathurin P,Morgan TR.Alcoholic hepatitis [J].N Engl J Med,2009,360(10):2758-2769. |
| [9] | 屈胜胜.巴西莓对酒精性肝损伤的保护作用及机制研究[D].北京:北京中医药大学,2014. |
| [10] | Cohen JI,Nagy LE. Pathogenesis of alcoholic liver disease:interactions between parenchymal and non-parenchymal cells [J].J Dig Dis,2011, 12(1):3-9. |
| [11] | Schwartz JM, Reinus JF. Prevalence and natural history of alcoholic liver disease [J]. Clin Liver Dis,2012, 16(4):659-666. |
| [12] | Woo GA, O'Brien C. Long-term management of alcoholic liver disease [J].Clin Liver Dis,2012, 16(4):763-781. |
| [13] | Liu S, Lv XH, Sun ZX, et al. Hepatoprotective and antioxidant effects of baicalin against CCl4-induced hepatotoxicity [J]. J Chin Pharm Sci, 2015, 24 (8), 538-544. |
| [14] | 赵宗阁,王尊文,徐康森.国内小牛血、小牛血清去蛋白提取物注射液质量分析及其抗缺氧作用研究[J].药物分析杂志,2008,28(10):1637-1640. |
| [15] | 尹连红,于 浩,彭金咏.四氯化碳诱导肝损伤的分子机制及中药干预的研究进展[J] . 中国现代应用药学,2015,32(9):1147-1155. |
| [16] | Fedin AI,Starykh EP,Parfenov AS, et al.Pharmacotherapy of endothelial dysfunction in patients with atherosclerotic brain ischemia [J].Zh Nevrol Psikhiatr Im S S Korsakova,2013,113(10):45-48. |
| [17] | 王红英,刘 敏,刘 美,等.参龟固本酒对大鼠酒精性肝损伤的作用[J].西安交通大学学报:医学版,2015,36(5):707-710,714. |
| [18] | 蔡 琦,闫魏魏,王少坤,等.蛹虫草多肽对大鼠急性酒精性肝损伤的保护作用[J].临床肝胆病杂志,2016,32(4):669-672. |
 2016, Vol. 42
2016, Vol. 42


