扩展功能
文章信息
- 王宇, 穆尚强, 梅继文, 孙爽
- WANG Yu, MU Shangqiang, MEI Jiwen, SUN Shuang
- 可膨胀椎间融合器治疗腰椎间盘轻度退变的有限元分析
- Finite element analysis on lumbar intervertbral disc slight degeneration treated by expanded vertebra interbody fusion cage
- 吉林大学学报(医学版), 2016, 42(03): 565-569
- Journal of Jilin University (Medicine Edition), 2016, 42(03): 565-569
- 10.13481/j.1671-587X.20160328
-
文章历史
- 收稿日期: 2015-09-23
腰椎退行性改变是临床中最为常见的一种脊柱疾病,保守治疗无效时,脊柱的椎间融合是最终选择的手术方案[1]。在融合手术发展过程中出现了如生物型椎间融合器、金属型椎间融合器、复合材料型椎间融合器和可吸收型椎间融合器,其中金属型椎间融合器是最先问世的真正意义上的椎间融合器,包括BAK融合器、Ray-TFC融合器、LT融合器、TMC融合器及Axia-LIF融合器[2],所有类型的融合器均根据型号大小改变椎间隙的高度,为了能自由改变椎间高度和恢复正常脊柱生理弯曲,本文作者设计了可膨胀椎间融合器(expanded vertebra interbody fusion cage,EVIFC)(中国专利号:ZL 201420074686.4),其通过融合器前部分的膨胀撑顶来改变椎间隙角度,起到改变生理弯曲和椎间隙高度的目的,因其体积相对较小,椎间植入相对容易,操作简单。有限元方法可以验证EVIFC对脊柱融合的生物力学的影响[3]。通常建立腰4-5脊柱节段椎间盘摘除后模型和植入EVIFC模型,该模型包括上下2个椎体和相邻的终板、小关节、主要的韧带和椎间盘,以模拟较为真实的生物力学状态[4]。在持续压力下,模拟模型在不同载荷下力学强度发生改变[5],有限元模型可以直观地观测脊柱节段上产生的强度增加或减少。本实验建立EVIFC植入腰4-5椎间隙的三维有限元模型,并进行力学加载,旨在分析EVIFC在完整腰椎有限元模型中的力学分布及其对腰椎功能节段力学稳定性的影响,为其临床应用提供依据。
1 资料与方法 1.1 椎间盘摘除模型的建立选取23岁健康男性志愿者1人,签署知情同意书后进行腰椎正侧位X线检查,排除腰椎病变,对第三腰椎至骶骨进行精细扫描,扫描间隔为0.5 mm[6],将扫描所得数据以Dicom格式直接存入光盘中,然后将扫描数据导入计算机中,采用Mimics10.1软件建立几何实体模型,再划分网格单元,采用Pro/ E 5.0软件建立EVIFC模型,并导入Ansys软件中,在固有的三维坐标系中建立腰椎的几何模型[7]。建立椎间盘摘除的模型和植入EVIFC的模型。腰椎间盘摘除后模型中仍然包括椎体、小关节、纤维环、韧带、髓核和终板[8]。设定材料性质、单元类型并控制好网格划分精度,对腰椎和EVIFC模型划分网格。指定材料特性与以往有限元研究的数据相对应,包括腰椎周围多种韧带。完整的有限元模型包括201 756个元素。腰椎和附件的弹性模量及泊松比[9]。 见表 1。
| Material | Young’s modulus (P/MPa) | Poisson ratio | Transverse section (A/mm2) |
| Cortical bone | 12 000 | 0.300 | - |
| Cancellous bone | 100 | 0.200 | - |
| Endplate | 30 | 0.250 | - |
| Nucleus pulposus | 1 | 0.499 | - |
| Degenerative nucleus pulposus | 3 | 0.499 | - |
| Posterior elements | 3 500 | 0.250 | - |
| Annulus fibrosus | 50 | 0.450 | - |
| Ligament | 0.300 | - | |
| Anterior longitudinal ligament | 20 | - | 63.7 |
| Posterior longitudinal ligament | 20 | - | 20.0 |
| Ligamentum intertransversarium | 58.7 | - | 3.60 |
| Ligamentum flava | 19.5 | - | 40.0 |
| Interspinal ligaments | 11.6 | - | 40.0 |
| Supraspinous ligament | 15 | - | 30.0 |
| Capsule ligament | 32.9 | - | 60.0 |
| Cartilage end-plate | 3 000 | 0.250 | - |
| EVIFC | 3 000 | 0.440 | - |
根据实验方案,通过后方入路移除椎间盘,模拟完整椎间盘和韧带切除后建立模型,清除部分椎板、黄韧带、髓核和纤维环后路植入EVIFC。尽量减少椎体附件的破坏,保留小关节的完全,保留骨性终板[10]。EVIFC植入后建立三维模型,并将膨胀翼撑顶并固定在终板上。韧带张力设置为5%[11],模拟EVIFC植入后的张力值。在软骨下骨和终板界面之间设定紧密结合[12]。
1.3 有限元模型模拟力学的加载将腰4-5椎间盘摘除后模型和EVIFC植入后的模型划分网格,网格数量和分布力学特征按照文献[13]提供的数据划分。EVIFC和终板为膨胀翼张开撑顶,齿状咬合的相互作用,易形成应力集中的情况。建立四面体模型,并在Ansys软件中进行运算。为了得到有效的有限元模型,参考文献[14, 15],垂直轴向压缩力为500 N,扭力为15 N·m[16]。对2个模型施以相同的条件进行模拟运算,固定腰骶椎体,对腰4上终板施以连续的载荷。
加载条件1:模拟腰椎的垂直压缩运动,固定腰骶椎体,在腰3椎体上表面加载500 N的力。加载条件2:模拟腰椎的前屈运动,固定腰骶椎体,在腰3椎体上表面加载500 N的力+15 N·m的扭转力矩。加载条件3:模拟腰椎的后屈运动,固定腰骶椎体,在腰3椎体上表面加载500N的力+15 N·m的扭转力矩。加载条件4:模拟腰椎的侧弯运动,固定腰骶椎体,在腰3椎体上表面加载500N的力+15 N·m的扭转力矩。 加载条件5:模拟腰椎的旋转运动,固定腰骶椎体,在腰3椎体上表面加载500N的力+15 N·m的扭转力矩。
1.4 模型验证根据参考文献[17]所提供的方法和加载条件,本模型给予相同条件,约束L5 下表面自由度,在L4 上表面施加8 N·m的力矩分别模拟屈伸、侧屈和旋转时的受力状态,分析比较本模型的活动范围及其在腰4-5椎间盘上的最大应力值。根据其条件,在屈伸、侧屈和旋转时活动角度分别为10.2°、10.3°、4.5°,与文献[17]结果相近。腰4-5椎间盘上的最大应力为1.523 MPa,略小于文献[17]中模型的数据(1.6 MPa),两者数据接近。因此,通过模型验证,该研究建立的模型合理,可以进行有限元分析研究。
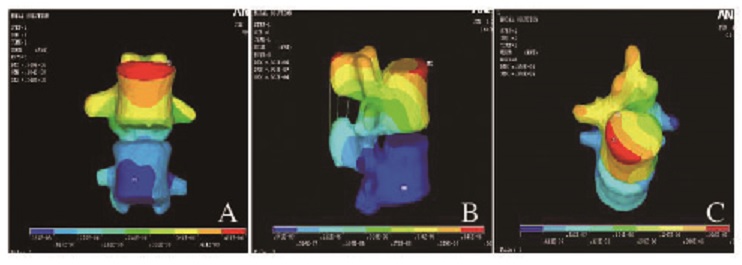
1.5 有限元分析将腰4-5椎间盘摘除后,固定腰5椎体下表面,在腰4椎体上表面加载屈曲、侧弯和旋转不同状态的载荷,比较单纯椎间盘摘除后无植入器械干预的情况下应力分布情况。见图 1(插页三)。在腰椎模型中植入EVIFC,将腰5和骶骨固定,腰3椎体上表面加载前屈、后伸、侧曲和旋转不同状态下的应力数据,比较各种不同力矩加载情况下的应力分布情况。见图 2(插页三)。
|
| 图1 腰4-5椎间盘摘除后屈曲、侧弯和旋转状态下模型的应力分布图 Fig.1 Diagram of stress distribution of model under flexion, later, latrending and rotation conditions of lumbar 4-5 after intervertebral diskresection |
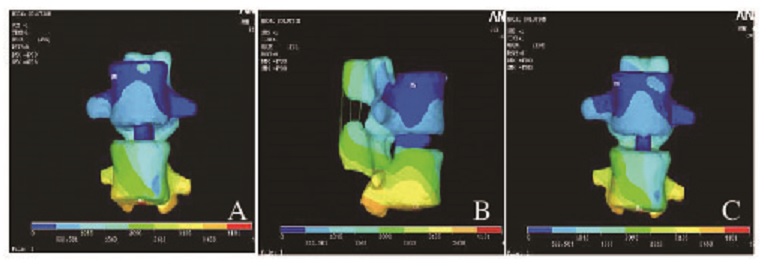
|
| 图2 植人EVIFC后在屈曲、侧弯和旋转状态下模型的应力 分布图 Fig.2 Diagram of stress distribution of model under flexion, lateral bending and rotation conditions after lmplantation of EVIFC |
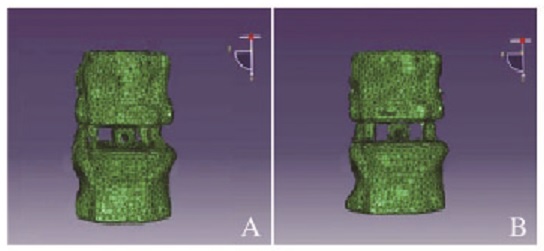
建立植入EVIFC有限元模型和EVIFC撑开后的有限元模型。见图 3(插页三)。
|
| 图3 EVIFC植人(A)和撑开后(B)的有限元模型 Fig.3 Finite element model after EVIFC implantation (A) and EVIFC expansion (B) |
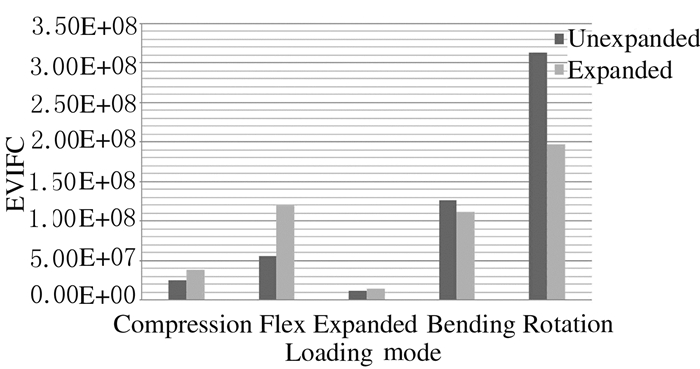
在500 N压力和15 N·m扭力条件下,计算植入EVIFC后应力值和植入EVIFC撑开后的有限元模型的应力值。在植入EVIFC模型中出现最大为3.128×108 MPa的应力值,在旋转模型中,2种模型出现了最大应力值差,其中植入EVIFC的应力值为3.128×108 MPa,植入EVIFC撑开后的应力值为1.968×108 MPa。在后伸模型运算数据中,2组EVIFC撑开后应力值的差值最小,所有的应力值多数集中在EVIFC的膨胀根部。见图 4。
|
| 图4 500 N载荷和15 N·m旋转扭力下植入EVIFC和植入EVIFC撑开后模型的压力值比较图 Fig.4 Comparison diagram of pressure values of model after EVIFC implantation and EVIFC expansion under 500 N load and 15 N·m rotation torque |
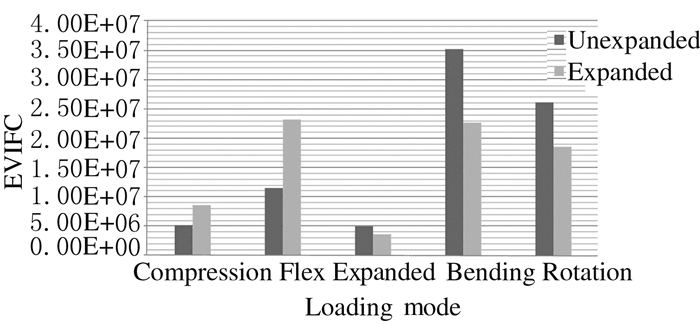
计算植入EVIFC的腰椎有限元模型在500 N垂直压力和15 N·m扭力下的终板应力强度峰值。与未撑开前比较,撑开的EVIFC应力较为均匀地分布在终板前后区域,最大峰值出现在未撑开的侧屈的状态下,应力值为3.513×108 MPa,而在EVIFC撑开时的应力值为2.262×108 MPa。见图 5。
|
| 图5 在500 N载荷和15 N·m旋转扭力下EVIFC闭合和撑开状态下上终板应力峰值比较图 Fig.5 Comparison diagram of stress values endplate after EVIFC implantation and EVIFC expension under 500 N load and 15 N·m rotation torque |
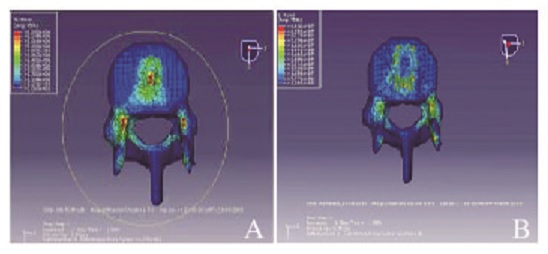
EVIFC撑开和未撑开时的有限元模型在500 N垂直载荷压力和15 N·m扭力作用下,分别计算在轴向压缩、屈伸、侧曲和旋转状态下终板应力值分布,因EVIFC外形轮廓为两头略圆,中央弧形隆起,相对于前后位置,中央接触易于集中,其外形与终板有匹配的弧形曲线,最大的接触区域在中心部位,故垂直载荷力加载时应力均集中于最为隆起区域,即终板中心的位置。当EVIFC前端撑开时,脊柱逐渐恢复正常生理弯曲,前端和中央压力分布更趋于均匀。此外,EVIFC为可膨胀融合器,相对体积可由小变大,植入时呈闭合状态,更易于操作;EVIFC未撑开时给终板带来更大的应力,最大应力值出现在旋转状态下。撑开的EVIFC在中心区域的应力值减小,考虑为撑开的前端分担了应力作用力的原故。见图 6(插页三)。
|
| 图6 500 N载荷和15N.m旋转扭力下闭合和撑开的EVIFC作用在终板上的应力分布图 Fig.6 Diagram of stress distribution of end-plate after EVIFC lmplantation and EVIFC expansionunder 500 N loading and 15N·m rotation torque |
有限元分析方法自应用于人体研究以来就极大地显示了其优越性;因常规的力学实验方法无法直接作用于人体,所以在对人体的力学研究方面,有限元数据模拟方法即成为一种有效手段[16]。
目前,有限元方法在骨科领域得到广泛的应用,许多依靠工程软件设计的医疗器械亦获得了较好的临床应用。采用有限元软件的优化设计功能,分析设计存在的不足,指导器械的设计和改进,可以在付出最小代价的情况下得到最大收益,以便更好地对医疗器械进行设计,保证良好的生物力学性能[17]。
本研究采用CT获取人体腰椎扫描数据,并采用Mimics10.1对数据进行重建,逆向成型为三维模型,再导入Ansys workbench软件中建模、划分网格和进行有限元分析。本研究结果显示:EVIFC撑开后,在前屈、后伸、侧弯和旋转等不同力学加载条件下,腰椎应力分布有所不同,EVIFC本身在500 N垂直载荷和15 N·m扭力下,其应力主要集中在融合器的膨胀根部。在旋转载荷下,2种状态的应力值差值最大,而后伸载荷时,2组应力值的差值最小。EVIFC在椎体终板上的力学分布图显示:EVIFC闭合时在终板上的轮廓图集中在中央区域,EVIFC撑开后其膨胀体能与椎体上下终板的轮廓相匹配。
本研究结果显示:融合器植入后与终板应力的匹配程度不同,所提供的支撑亦不相同,EVIFC可为椎体间隙内提供强有力的支撑,有足够的强度影响骨的塑形及生长,终板的应力为融合的成功提供了良好的生物力学环境。本研究结果显示:恢复脊柱的生长弯曲意义重大,融合器在整个终板的接触面积影响了其压力强度,建议融合器在终板上的接触面积应超过30%,以便为骨移植做准备[18]。
生物型椎间融合器、组合式融合器和B-twin融合器均有其优点和不足,如B-twin融合器在临床使用过程中发现了术后并发症,包括融合器移位或脱出、原发或相邻节段椎间盘突出,椎间隙高度丢失及椎体退变不稳,椎间隙感染及椎间植骨不融合等[19, 20, 21]。本研究最大的优点在于融合器体部可上下膨胀撑开,且融合器为中空结构。本研究结果提示:一个直径较大且中空的融合器和直径较小但坚固的融合器其融合效果相同,但中空融合器允许较大空间的植骨,以增加融合机会,临床中会优先选择[22, 23]。EVIFC通过箱体的膨胀实现了体积的增大,满足优先选择的条件,但因手术操作和解剖的原因,体积越小的融合器其操作越容易,这也是EVIFC设计的最大亮点。
本研究的不足之处:①未考虑术后融合后骨重塑型的情况和椎间隙内骨融合或骨吸收的情况;②有限元模型中的所有材料属性均按同质、线性弹性设置,与真实的人体结构存在差异,所以本研究取得结果可能与实际情况存在一定差异。虽然存在这些不足,但新设计的EVIFC在未撑开之前其形状类似于传统的椎间融合器,膨胀撑开以后即可改变融合器本身的体积、增加椎间隙的高度或恢复脊柱的生理弯曲。因此,EVIFC是一种适宜的椎体融合器械,为得到更为真实的数据以及验证其优势,仍需进一步行动物实验和临床试验。
| [1] | Koca OL,Eskitascioglu G,Usumez A. Three-dimensional finite-element analysis of functional stresses in different bone locations produced by implants placed in the maxillary posterior region of the sinus floor[J].J Prosthet Dent,2005 ,93(1):38-44. |
| [2] | Chang YI,Shin SJ,Baek SH.Three-dimensional finite element analysis in distal enmasse movement of the maxillary dentition with the multiloop edgewise archwire[J].Eur J Orthod,2004,26(3):339-345. |
| [3] | 马金梁,张记恩,刘克斌,等.一种新型腰椎间融合器的研制及生物力学评价[J].重庆医学,2014,43(4):465-468. |
| [4] | Wang M,Tang SJ,McGrady LM,et al.Biomechanical comparison of supplemental posterior fixations for two-level anterior lumbar interbody fusion[J].Proc Inst Mech Eng H,2012,227(3):245-250. |
| [5] | 石 岩,崔文岗,肖德明.腰椎椎间融合器临床研究进展[J].国际骨科学杂志,2013,34(1):45-48. |
| [6] | Zhang QH,Teo EC,Ng HW,et al.Finite element analysis of momentrotation relationships for human cervical spine[J].J Biomech,2006,39(1):189-193. |
| [7] | Ding JY,Qian S,Wan L,et al.Design and finite-element evaluation of a versatile assembled lumbar interbody fusion cage[J].Arch Orthop Trauma Surg,2010,130(4):565-571. |
| [8] | Chuah HG,Abd Rahim I,Yusof MI.Topology optimisation of spinal interbody cage for reducing stress shielding effect[J].Comput Methods Biomech Biomed Engin,2010,13(3):319-326. |
| [9] | Rihn JA,Makda J,Hong J,et al.The use of RhBMP-2 in single-level transforaminal lumbar interbody fusion:a clinical and radiographic analysis[J].Eur Spine J,2009,18(11):1629-1636. |
| [10] | Balseiro S,Nottmeier EW.Vertebral osteolysis originating from subchondral cyst end plate defects in transforaminal lumbar interbody fusion using rhBMP-2.Report of two cases [J].Spine J,2010,10(7):e6-e10. |
| [11] | Fabbri N,Rustemi E,Masetti C,et al.Severe osteolysis and soft tissue mass around total hip arthroplasty:description of four cases and review of the literature with respect to clinico-radiographic and pathologic differential diagnosis[J].Eur J Radiol,2011,77(1):43-50. |
| [12] | Yim EK,Darling EM,Kulangara K,et al.Nanotography-induced changes in focal adhesions,cytoskeletal organization,and mechanical properties of human mesenchymal stem cells[J].Biomaterials,2010,31(6):1299-1306. |
| [13] | Beuvelot J,Portet D,Lecollinet G,et al.In vitro kinetic study of growth and mineralization of osteoblast-like cells (Saos-2) on titanium surface coated with a RGD functionalized bispho -sphonate[J].J Biomed Mater Res B Appl Biomater,2009,90(2):873-881. |
| [14] | Corniola MV,Jgersberg M,Stienen MN,et al.Complete cage migration/subsidence into the adjacent vertebral body after posterior lumbar interbody fusion[J].J Clin Neurosci,2015,22(3):597-598. |
| [15] | Yamada K,Ito M,Akazawa T,et al.A preclinical large animal study on a novel intervertebral fusion cage covered with high porosity titanium sheets with a triple pore structure used for spinal fusion[J].European Spine J,2015:1-8. |
| [16] | Hart RA,Daniels AH,Bahney T,et al.Relationship of donor variables and graft dimension on biomechanical performance of femoral ring allograft[J].J Orthop Res,2011,29(12):1840-1845. |
| [17] | Razi AE,Spivak JM,Kummer FJ,et al.Biomechanical comparison of translaminar screw versus pedicle screw supplementation of anterior femoral ring allografts in one-level lumar spine fusion[J].Bull NYU Hosp Jt Dis,2011,69(4):298-302. |
| [18] | Suzuki T,Abe E,Miyakoshi N,et al.Anterior decompression and shortening reconstruction with a titanium mesh cage through a posterior approach alone for the treatment of lumbar burst fractures[J].Asian Spine J,2012,6(2):123-130. |
| [19] | 李菊根,杨进顺,谢楚海,等.可膨胀性椎间融合器治疗腰椎退行性疾病的术后并发症分析[J].中国矫形外科杂志,2012,20(12):1137-1139. |
| [20] | 周春光,宋跃明,屠重棋,等.多元氨基酸共聚物/磷酸钙复合材料椎间融合器的设计制备及压缩强度测试[J].生物医学工程学杂志,2011,28(6):1136-1140. |
| [21] | 丁金勇,钱 莘,吴小程,等.新型组合式腰椎间融合器的研制和生物力学评价[J].中国临床解剖学杂志,2009,27(5):588-591. |
| [22] | Le TV,Baaj AA,Dakwar E,et al.Subsidence of polyetheretherketone intervertebral cages in minimally invasive lateral retroperit oneal transpsoas lumbar interbody fusion[J].Spine,2012,37(14):1268-1273. |
| [23] | 刘家明,龙新华,周 扬,等.一期后路经椎间孔入路病灶清除椎体间非结构性植骨内固定治疗腰椎结核的疗效观察[J].解放军医学杂志,2015,40(11):938-942. |
 2016, Vol. 42
2016, Vol. 42


