扩展功能
文章信息
- 付鑫, 龚福梅, 丁宁, 朱静, 杨春光, 胡学军
- FU Xin, GONG Fumei, DING Ning, ZHU Jing, YANG Chunguang, HU Xuejun
- 类弹性蛋白展示NT-proBNP双抗原表位重组蛋白的制备和纯化
- Preparation and purification of recombinant proteins of elastin-like polypeptide for displaying two epitopes of NT-proBNP
- 吉林大学学报(医学版), 2020, 46(03): 458-463
- Journal of Jilin University (Medicine Edition), 2020, 46(03): 458-463
- 10.13481/j.1671-587x.20200305
-
文章历史
- 收稿日期: 2019-07-19
人体血浆中N端脑钠肽前体(N-terminal pro-brain natriuretic peptide, NT-proBNP)是检测无症状心衰和早期心衰的高灵敏性重要指标,对早期发现和治疗心衰患者、有效降低心衰患者的发病率及病死率具有重大意义[1-2]。另外,NT-proBNP还可作为诊断无症状晚期慢性肾脏疾病[3]和慢性阻塞性肺病[4]的独立检测指标,具有广泛的临床应用和研究价值[5]。目前市场上已经有多家商品化的NT-proBNP免疫检测试剂[6-7],其校准品来源广泛,包括人工合成、大肠杆菌(Escherichia coli, E.coli)、酵母和哺乳动物细胞表达的重组蛋白。上述几种来源的重组蛋白各有优势,但纯化重组蛋白大多数采用层析方法,且部分重组蛋白还不能直接用于检测,需增加去除融合标签这一步骤,生产方法繁琐且成本较高,成本可达0.1 mg/1000美元,因此成为制约其发展的主要因素。
类弹性蛋白(elastic-like polypeptide, ELP)是近十几年开发的一种融合标签,可通过可逆相变循环(inverse transition cycling, ITC)方法更简单、更经济地纯化蛋白[8]。ELP主要由五肽重复序列单元(VPGXG)n串联组成,其中客座残基X可以是除脯氨酸以外的任一种氨基酸,n代表ELP链中五肽重复次数[9-10]。外源蛋白和ELP融合后可同样保留ELP可逆相变的性质,利用温度诱导的多次ITC达到分离纯化蛋白的目的[11-12]。该方法操作简单、成本低且回收率高,适用于工业规模生产,纯化蛋白效率明显优于色谱等传统蛋白纯化方法,与层析法效果相近[13]。
本研究采用本实验室自行设计的客座残基为异亮氨酸的低相变温度(transition temperature, Tt)ELP蛋白[14]首次进行展示NT-proBNP双表位研究,在E.coli中高效表达ELP展示NT-proBNP的第13~20位和第63~71位氨基酸残基表位的重组蛋白,并通过温度诱导ITC方法,快速分离纯化具有NT-proBNP双表位抗原性的ELP重组蛋白,为低成本、高效快速地制备出NT-proBNP检测校准品奠定基础。
1 材料与方法 1.1 菌株和主要试剂E. coli BL21(DE3)和E. coli JM109购自美国Novagen公司。基因合成全部由南京金斯瑞生物科技有限公司完成。HRP标记小鼠来源抗人NT-proBNP的第13~20位氨基酸表位的单克隆抗体(13G1213-20)、小鼠来源抗人NT-proBNP的第63~71位氨基酸表位的单克隆抗体(15C463-71)购自美国HyTest公司,硫酸卡那霉素(终浓度为50 mg·L-1)、DNase(终浓度50 mg·L-1)及HRP标记的羊抗小鼠IgG抗体购自南京生工生物工程有限公司, ECL发光试剂盒购自美国Tanon公司, TMB显色液购自美国Sigma公司。
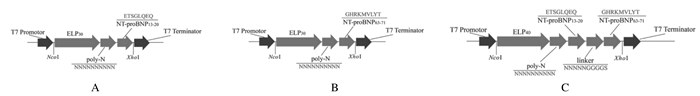
1.2 ELP展示NT-proBNP抗原表位基因设计、合成和克隆为了获得具有抗原抗体结合能力的NT-proBNP双抗原表位融合蛋白,首先进行ELP展示单抗原表位研究,评估特异抗体与展示表位的结合能力,在此基础上进一步进行展示双表位研究。为此,分别设计了2个ELP展示NT-proBNP单个表位及1个展示双表位的融合基因。选取编码30~40个VPGIG串联碱基序列,通过编码柔链的氨基酸残基序列与编码NT-proBNP特异表位氨基酸残基序列相连,形成融合基因;为减小2个表位的相互影响,2个表位之间也通过编码柔链序列相连,基因结构和表达框见图 1。所选取NT-proBNP表位分别为编码NT-proBNP的第13~20位氨基酸残基ETSGLQEQ碱基序列和编码第63~71位氨基酸残基GHRKMVLYT碱基序列。ELP与NT-proBNP表位之间的柔链氨基酸残基序列为NNNNNNNNNN,2个表位之间的柔链氨基酸残基序列为NNNNNGGGGS(其中N代表天冬氨酸残基、G代表甘氨酸残基、S代表丝氨酸残基)。根据E.coli密码子偏好性,委托南京金斯瑞生物科技有限公司合成上述3个基因,并将融合基因克隆至pET-28a(+)的NcoⅠ和XhoⅠ酶切位点上构建表达载体。3个基因分别命名为ELP-E13-20、ELP-E63-71和ELP-E(13-20)-(63-71)。
|
| A: Diagram of ELP-E13-20 fusion gene; B: Diagram of ELP-E63-71 fusion gene; C: Diagram of ELP-E(13-20)-(63-71) fusion gene. 图 1 ELP展示NT-proBNP抗原表位基因结构图 Fig. 1 Diagrams of gene structures of ELP for displaying NT-proBNP epitopes |
|
|
分别将携带ELP-E13-20、ELP-E63-71和ELP-E(13-20)-(63-71)基因的表达载体转入E.coli BL21(DE3)中,37 ℃过夜培养。挑取单克隆菌株接种到含有卡那霉素(终浓度50 mg·L-1)的LB培养基中振荡培养。次日以1:100接种到自动诱导培养基中大量培养,经28℃诱导表达24 h后留取600nm处吸光度(A)值为1的菌量,以诱导前菌液为阴性对照进行Western blotting鉴定。自动诱导培养基配方:5%的20×NPS 20 mL,2%的50×5052 8 mL和0.1%的1mol·L-1 MgSO2 0.4 mL加入ZY配置成400 mL体系培养基。其中ZY由10 g·L-1胰蛋白胨和5 g·L-1酵母提取物加入ddH2O配制而成,pH=7.2;20×NPS由0.1 mol·L-1 PO42-、0.025 mol·L-1 SO42-、0.05 mol·L-1NH4+、0.1 mol·L-1 Na+和0.05 mol·L-1 K+加入ddH2O配制而成,pH=7.4;50×5052由0.5%甘油、0.05%葡萄糖和0.2% α-乳糖加入ddH2O配制而成。
1.4 ELP展示NT-proBNP抗原表位重组蛋白的纯化将大量培养后的菌液低温离心收集菌体,沉淀用约25 mL无盐PBS(0.02 mol·L-1)重悬,保存于-80℃冰箱。菌液经反复冻融2次后置于冰浴中超声破碎(条件:80 W,破碎时间2 s,破碎间隔3 s,总时间20 min),10 000 r·min-1、4 ℃离心10 min,弃除沉淀,将上清移入新管中并加入DNase(终浓度50 mg·L-1),冰浴20 min,10 000 r·min-1离心10 min,弃除沉淀,上清移入新管。处理后的上清进行ITC蛋白纯化,向上清液中添加NaCl固体至终浓度为2 mol·L-1,37℃水浴20 min溶解,10 000 r·min-1于30 ℃离心10 min后弃上清;沉淀加入20 mL预冷无盐PBS重悬,冰浴20 min,10 000 r·min-1于4 ℃离心10 min后弃沉淀,再将上清移入新管。此即为一轮ITC。经过4轮ITC纯化处理后,得到纯化的NT-proBNP特异抗原表位重组蛋白。
1.5 ELP展示NT-proBNP抗原表位重组蛋白的纯度鉴定和Tt测定取80 μL纯化后蛋白样品加入20 μL 5×Loading Buffer混匀,99 ℃裂解制样并进行SDS-PAGE冰上电泳,通过凝胶显示单一蛋白条带鉴定重组蛋白纯度。采用BCA定量法测定蛋白浓度,并采用PBS(0.02 mol·L-1)将蛋白稀释至终浓度为10 μmol·L-1,取100 μL加入酶标版中,以1 ℃为梯度测定从23 ℃到40 ℃重组蛋白溶液于波长为350nm处A值,每个温度设置3个平行结果,当A(350)值为最大A值1/2时,该温度即为ELP重组蛋白的Tt。
1.6 ELP展示NT-proBNP抗原表位重组蛋白特异性分析采用ELISA法测试重组蛋白在pH值为7.4时与相应抗体的结合特异性,以0.02 mol·L-1无盐PBS作为空白对照孔。将纯化蛋白在PBS缓冲液中以10 μmol·L-1浓度梯度稀释,每孔设置3个平行孔,4 ℃包被于96孔板上过夜孵育。其中ELP展示单抗原表位ELP-E13-20和ELP-E63-71重组蛋白采用直接ELISA方法检测,分别对应抗NT-proBNP的13~20及63~71表位的鼠源单克隆抗体13G1213-20和15C463-71。TMB显色,终止反应后测定各孔A(450)值,以蛋白浓度为横坐标,各浓度点测定A(350)值为纵坐标,应用GraphPad Prism绘制四参数逻辑拟合曲线。
ELP展示双抗原表位ELP-E(13-20)-(63-71)重组蛋白采用2种方法检测,方法一同上述方法,分别与13G1213-20和15C463-71单克隆抗体孵育行直接ELISA检测并做拟合曲线;方法二采用双抗体夹心ELISA方法,以单克隆抗体15C463-71 (抗体1:1 000稀释,终浓度为7.0 mg·L-1)捕获抗原蛋白,单克隆抗体13G1213-20 (1:1 000稀释,终浓度为0.7 mg·L-1)为检测抗体,TMB显色,终止反应后测定各孔A(450)值,以蛋白浓度为横坐标,各浓度点测定A(450)值为纵坐标,应用GraphPad Prism绘制15C463-71和13G1213-20检测系统的log-log双对数校准曲线。
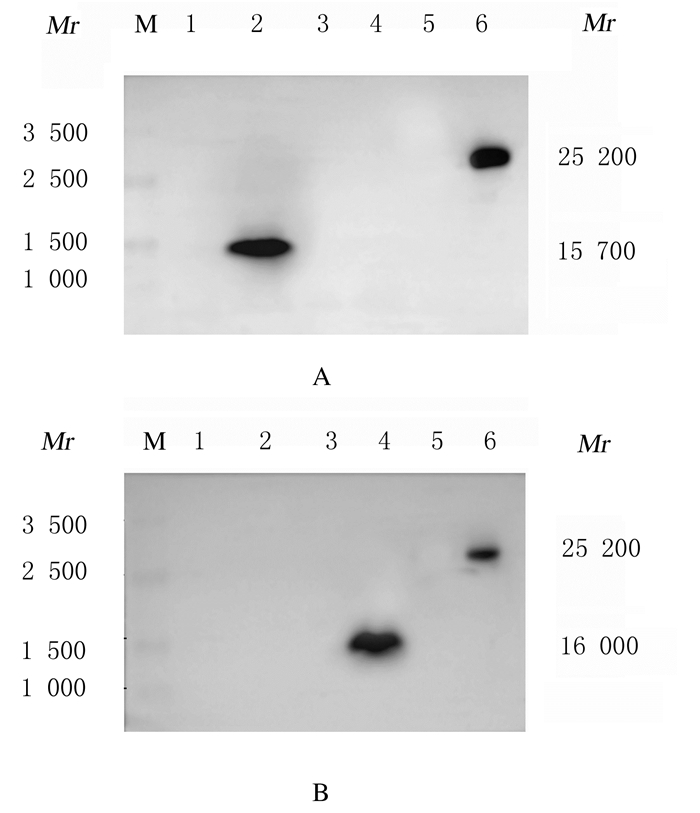
2 结果 2.1 ELP展示NT-proBNP抗原表位重组蛋白表达将重组质粒转入E.coli BL21(DE3)宿主后,自动诱导表达24 h,以诱导前收集菌液为阴性对照,分别采用13G1213-20和15C463-712个单克隆抗体对蛋白表达情况进行Western blotting法检测的结果表明:重组蛋白ELP-E13-20、ELP-E63-71和ELP-E(13-20)-(63-71)在自动诱导条件下均获得高效表达(图 2),同时证明ELP所展示的表位均能与相应抗体特异结合。3种重组蛋白的相对分子质量与理论相对分子质量相符,分别为157 00、160 00和252 00。
|
| A: 13G1213-20 antibody; B: 15C463-71 antibody.M: Protein marker; Lane 1: ELP-E13-20 without induction; Lane 2: ELP-E13-20 with induction; Lane 3: ELP-E63-71 without induction; Lane 4: ELP-E63-71 with induction; Lane 5: ELP-E(13-20)-(63-71) without induction; Lane 6: ELP-E(13-20)-(63-71) with induction. 图 2 Western blotting法检测NT-proBNP重组蛋白表达电泳图 Fig. 2 Electrophoregram of expressions of recombinant proteins of NT-proBNP detected by Western blotting method |
|
|
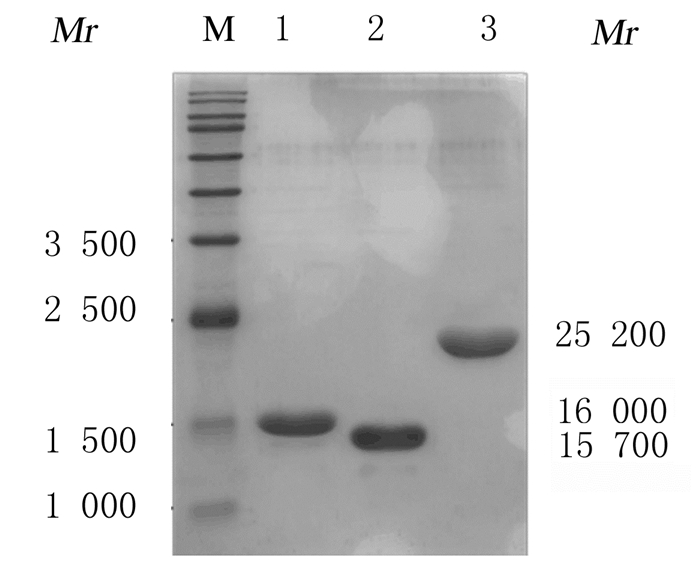
采用ITC方法将自动诱导24 h后的ELP-E13-20、ELP-E63-71和ELP-E(13-20)-(63-71)重组蛋白从菌体中分离出来。通过4次ITC纯化,SDS-PAGE电泳检测显示上述3种重组蛋白均获得纯化(图 3),经BCA法检测,每升自动诱导表达培养基中可纯化2.0~2.5 mg重组蛋白。纯化条带相对于理论值的位置较低,可能是盐离子浓度对蛋白的影响导致,这也是ELP在SDS-PAGE蛋白电泳检测时的常见现象[8, 15]。测定蛋白浓度为10 μmol·L-1时ELP-E13-20、ELP-E63-71和ELP-E(13-20)-(63-71)重组蛋白Tt分别为(29.7±0.5)℃、(28.5±0.25)℃和(30.8±0.2)℃。
|
| M: Protein marker; Lane 1: ELP-E13-20; Lane 2: ELP-E63-71; Lane 3: ELP-E(13-20)-(63-71). 图 3 SDS-PAGE法检测纯化的NT-proBNP重组蛋白电泳图 Fig. 3 Electrophoregram of purified recombinant proteins of NT-proBNP detected by SDS-PAGE method |
|
|
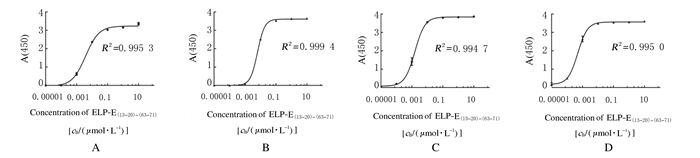
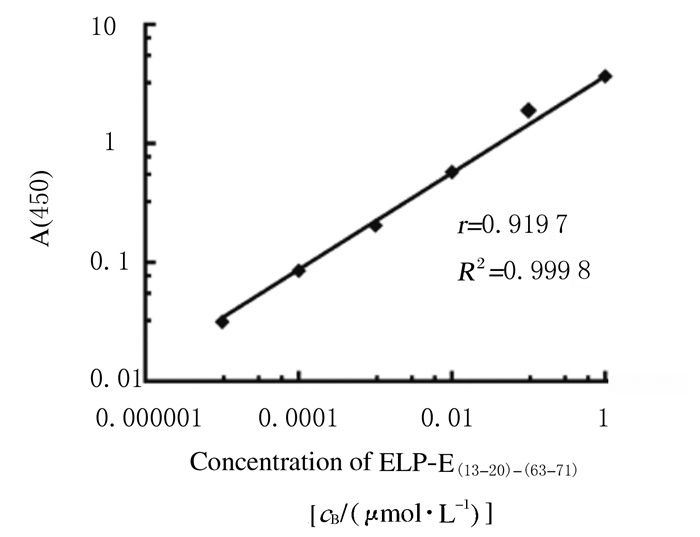
采用直接ELISA方法分别检测13G1213-20和15C463-71抗体与ELP展示抗原表位重组蛋白的结合能力见图 4。3种蛋白的参数逻辑拟合曲线显示:重组蛋白浓度与A值呈现良好的S形曲线,相关系数(R2)均在0.99以上,拟合优度高。13G1213-20和15C463-71单克隆抗体可以分别与ELP展示NT-proBNP双抗原表位重组蛋白上的表位结合,说明双抗原表位间柔链设计合理。采用夹心ELISA方法分别将15C463-71和13G1213-20单克隆抗体作为捕获抗体和检测抗体,定量检测ELP-E(13-20)-(63-71)重组蛋白样品标准曲线,见图 5。双对数线性回归分析显示:ELP-E(13-20)-(63-71)与A(450)值呈双对数线性剂量依赖关系,其中相关系数(r)= 0.9197 (P < 0.01),其绝对值为0.8~1.0,说明两者之间存在极强的相关关系,可信度高;R2=0.999 8,说明回归直线对观测值的拟合程度非常好。
|
| A: Immunoassay for ELP-E13-20 using 13G1213-20 antibody; B: Immunoassay for ELP-E63-71 using15C463-71 antibody; C: Immunoassay for ELP-E(13-20)-(63-71) using 13G2213-20 antibody; D: Immunoassay for ELP-E(13-20)-(63-71) using 15C463-71 antibody. 图 4 直接ELISA法检测13G1213-20和15C463-71抗体与ELP展示抗原表位重组蛋白的结合能力 Fig. 4 Binding abilities of 13G1213-20 and 15C463-71 antibodies and recombinant proteins of ELP for displaying epitopes detected by direct ELISA method |
|
|
|
| 15C463-71 was a capture antibody and 13G213-20 was a detection antibody; r=0.919 7, P < 0.01. 图 5 夹心ELISA法测定ELP-E(13-20)-(63-71)重组蛋白标准曲线 Fig. 5 Standard curve of recombinant protein of ELP-E(13-20)-(63-71) detected by Sandwich ELISA method |
|
|
本研究采用ELP展示NT-proBNP线性表位,探索了低成本、高效地制备NT-proBNP检测校准品的方法。NT-proBNP相对分子质量为8 600,属于低相对分子质量多肽,目前生产NT-proBNP的普遍策略是利用基因工程与其他蛋白融合并在E.coli中表达[16-19]。与脑钠肽融合的常用蛋白:硫氧还蛋白(Trx)、谷胱甘肽-S-转移酶(GST) [18]、Ssp dnaB微型蛋白内含子[19]和人血清白蛋白(human serum albumin, HSA) [20]等。KIM等[21]采用来自肝片吸虫的Fh8多肽作为融合标签高效生产NT-proBNP,可纯化出大量NT-proBNP重组蛋白,但是需使用蛋白酶将NT-proBNP从融合蛋白上切割下来才能进一步用作检测校准品。上述方法中大多数需利用层析法纯化蛋白,而且重组蛋白不能直接用于检测,增加了获取大量目的蛋白的生产步骤和生产成本。
本研究采用的ELP融合标签是一种通过可逆相变直接纯化的重组蛋白,其与靶蛋白融合后可以在E.coli中高效、可溶地表达,该技术是更简单、更经济的纯化蛋白方法。目前临床对NT-ProBNP的检测通常运用免疫学夹心法[22]来测定样本浓度,本课题组选择2个抗原表位与ELP融合用于夹心ELISA法检测。研究[23]表明:心衰患者血浆中NT-proBNP是O-糖基化蛋白,其中心区域第28~56位氨基酸残基部位被糖基化,所以该区域表位的抗体很难被识别。为了确保人血浆中NT-proBNP检测的准确性,HyTest公司推荐其筛选出的15C463-71-13G1213-20抗体组合作为捕获抗体-检测抗体[24],其可分别与NT-proBNP多肽的第63~ 71位和第13~20位氨基酸残基表位高效结合,所以本课题组最终选用以上2段多肽作为展示双表位,不受糖基化影响,适用于NT-proBNP精确检测系统。
本课题组首先对ELP展示NT-proBNP单表位的研究显示:在无需去除ELP融合标签的情况下,展示NT-proBNP部分线性表位的重组蛋白仍具有抗原性,且无论在变性条件下还是非变性条件下均能与相应特异抗体结合,进而设计ELP通过10个天冬氨酸残基(N)的柔链展示NT-proBNP双特异抗原表位,并采用NNNNNGGGGS柔链序列将双表位隔开,以减小表位之间空间位阻,充分将2个表位展示出来。夹心ELISA法测定ELP-E(13-20)-(63-71)双对数曲线显示:本课题组设计的NT-proBNP重组蛋白无需将ELP融合标签切割下来就能够同时与相应的捕获抗体和检测抗体结合,该设计也不需要融合表达全部NT-proBNP多肽序列,只选取2个表位进行表征即可作为检测校准品。
综上所述,选取ELP标签作为融合蛋白展示NT-proBNP特异抗原表位提供了一种低成本、纯化携带多个特异抗原表位的方法,为生产其他多肽抗原检测校准品提供了思路。
| [1] |
MCKIE P M, BURNETT J C. NT-proBNP:the gold standard biomarker in heart failure[J]. J Am Coll Cardiol, 2016, 68(22): 2437-2439. DOI:10.1016/j.jacc.2016.10.001 |
| [2] |
LUCHNER A, VON HAEHLING S, HOLUBARSCH C, et al. Indications and clinical implications of the use of the cardiac markers BNP and NT-proBNP[J]. Dtsch Med Wochenschr, 2017, 142(5): 346-355. DOI:10.1055/s-0042-117368 |
| [3] |
TIRMENSTAJN-JANKOVIC B, DIMKOVIC N, PERUNICIC-PEKOVIC G, et al. Anemia is independently associated with NT-proBNP levels in asymptomatic predialysis patients with chronic kidney disease[J]. Hippokratia, 2013, 17(4): 307-312. |
| [4] |
LABAKI W W, XIA M, MURRAY S, et al. NT-proBNP in stable COPD and future exacerbation risk:Analysis of the SPIROMICS cohort[J]. Respir Med, 2018, 140: 87-93. DOI:10.1016/j.rmed.2018.06.005 |
| [5] |
CAO ZP, JIA YQ, ZHU BL. BNP and NT-proBNP as diagnostic biomarkers for cardiac dysfunction in both clinical and forensic medicine[J]. Int J Mol Sci, 2019, 20(8): E1820. DOI:10.3390/ijms20081820 |
| [6] |
SEMENOV A G, TAMM N N, APPLE F S, et al. Searching for a BNP standard:Glycosylated proBNP as a common calibrator enables improved comparability of commercial BNP immunoassays[J]. Clin Biochem, 2017, 50(4/5): 181-185. |
| [7] |
SUN HZ, WANG W, ZHAO HJ, et al. Internal quality control status for BNP and NT-proBNP in China from 2014 to 2017[J]. J Clin Lab Anal, 2019, 33(1): e22643. DOI:10.1002/jcla.22643 |
| [8] |
MEYER D E, CHILKOTI A. Purification of recombinant proteins by fusion with thermally responsive polypeptides[J]. Nat Biotechnol, 1999, 17(11): 1112-1115. DOI:10.1038/15100 |
| [9] |
KUNA M, MAHDI F, CHADE A R, et al. Molecular size modulates pharmacokinetics, biodistribution, and renal deposition of the drug delivery biopolymer elastin-like polypeptide[J]. Sci Rep, 2018, 8(1): 7923. |
| [10] |
VERHEUL R, SWEET C, THOMPSON D H. Rapid and simple purification of elastin-like polypeptides directly from whole cells and cell lysates by organic solvent extraction[J]. Biomater Sci, 2018, 6(4): 863-876. DOI:10.1039/C8BM00124C |
| [11] |
XIA W, LU H, LI Y. Purification of chicken IgY by binding capture using elastin-like polypeptide-tagged immunoglobulin-binding domain of streptococcal protein G[J]. Vet Immunol Immunopathol, 2017, 192: 13-19. DOI:10.1016/j.vetimm.2017.09.002 |
| [12] |
KE C, XIONG H, ZHAO C, et al. Expression and purification of an ArsM-elastin-like polypeptide fusion and its enzymatic properties[J]. Appl Microbiol Biotechnol, 2019, 103(6): 2809-2820. DOI:10.1007/s00253-019-09638-w |
| [13] |
FONG B A, WOOD D W. Expression and purification of ELP-intein-tagged target proteins in high cell density E. coli fermentation[J]. Microb Cell Fact,, 2010, 9: 77. DOI:10.1186/1475-2859-9-77 |
| [14] |
林衡, 李军明, 张立超, 等. 疏水性ELP基因设计与基因库构建[J]. 微生物学通报, 2013, 40(4): 584-592. |
| [15] |
TRABBIC-CARLSON K, LIU L, KIM B, et al. Expression and purification of recombinant proteins from Escherichia coli:Comparison of an elastin-like polypeptide fusion with an oligohistidine fusion[J]. Protein Sci, 2004, 13(12): 3274-3284. |
| [16] |
SOLEH M T, FOO J Y, BAILEY U M, et al. A rapid and cost-effective method of producing recombinant proBNP and NT-proBNP variants in Escherichia coli for immunoassay of heart failure[J]. Biotechnol Lett, 2014, 36(1): 133-140. |
| [17] |
李梦阳, 杨春光, 孙慎侠, 等. 人源骨架蛋白FN3展示脑钠肽前体N端抗原表位研究[J]. 上海交通大学学报(医学版), 2016, 36(11): 1558-1561. DOI:10.3969/j.issn.1674-8115.2016.11.004 |
| [18] |
ALA-KOPSALA M, RUSKOAHO H, LEPPÄLUOTO J, et al. Single assay for amino-terminal fragments of cardiac A- and B-type natriuretic peptides[J]. Clin Chem, 2005, 51(4): 708-718. DOI:10.1373/clinchem.2004.039891 |
| [19] |
SUN ZY, CHEN JY, YAO HW, et al. Use of Ssp dnaB derived mini-intein as a fusion partner for production of recombinant human brain natriuretic peptide in Escherichia coli[J]. Protein Expr Purif, 2005, 43(1): 26-32. DOI:10.1016/j.pep.2005.05.005 |
| [20] |
DING Y, PENG Y, DENG L, et al. The effects of fusion structure on the expression and bioactivity of human brain natriuretic peptide (BNP) albumin fusion proteins[J]. Curr Pharm Biotechno, 2014, 15(9): 856-863. DOI:10.2174/1389201015666141012182106 |
| [21] |
KIM Y S, KARISA N, JEON W Y, et al. High-level production of N-terminal pro-brain natriuretic peptide, as a calibrant of heart failure diagnosis, in Escherichia coli[J]. Appl Microbiol Biotechnol, 2019, 103(12): 4779-4788. DOI:10.1007/s00253-019-09826-8 |
| [22] |
APPLE F S, PANTEGHINI M, RAVKILDE J, et al. Quality specifications for b-type natriuretic peptide assays[J]. Clin Chem, 2005, 51(3): 486-493. DOI:10.1373/clinchem.2004.044594 |
| [23] |
SCHELLENBERGER U, O'REAR J, GUZZETTA A, et al. The precursor to B-type natriuretic peptide is an O-linked glycoprotein[J]. Arch Biochem Biophys, 2006, 451(2): 160-166. DOI:10.1016/j.abb.2006.03.028 |
| [24] |
SEFERIAN K R, TAMM N N, SEMENOV A G, et al. Immunodetection of glycosylated NT-proBNP circulating in human blood[J]. Clin Chem, 2008, 54(5): 866-873. DOI:10.1373/clinchem.2007.100040 |
 2020, Vol. 46
2020, Vol. 46


