扩展功能
文章信息
- 张晓萌, 王惠敏, 杨宇斌, 朱轩言, 田子璐, 朱松
- ZHANG Xiaomeng, WANG Huimin, YANG Yubin, ZHU Xuanyan, TIAN Zilu, ZHU Song
- 可光固化聚氨酯粘接剂的制备及其对传统丙烯酸树脂粘接剂性能的影响
- Preparation of light-curable polyurethane adhesive and its effect on properties of traditional acrylic resin adhesives
- 吉林大学学报(医学版), 2020, 46(02): 365-371
- Journal of Jilin University (Medicine Edition), 2020, 46(02): 365-371
- 10.13481/j.1671-587x.20200226
-
文章历史
- 收稿日期: 2019-11-25
目前,光固化复合树脂以其优异的机械性能、美学性能及操作简便性几乎完全取代了银汞合金成为现代口腔医学不可缺少的修复材料。然而,与银汞合金修复相比,复合树脂修复治疗的失败率却增加了2.0~3.5倍。国内外临床数据调查[1]显示:树脂修复体的年失败率高达8%,平均寿命只有5.7年。研究[2-6]表明:目前的丙烯酸酯单体粘接系统亲水性较大,其高含量的亲水性单体导致粘接体系在潮湿的口腔环境中容易吸收过多的水份,使固化后的聚合物网络结构出现降解,从而使得树脂-牙本质的粘接界面完整性产生缺陷,进而引发树脂修复体的水解甚至断裂。因此,对传统的丙烯酸树脂单体粘接剂进行功能改性,研发新型耐水解的粘接剂已成为众多学者的研究方向之一[2, 7]。
聚氨酯(polyurethane, PU)作为最具商业价值和生物安全性的医用高分子材料之一,以其优异的力学性能和生物相容性被广泛应用于医学领域。PU的耐潮湿、耐溶剂和较高的粘接性能等特性使其在口腔医学粘接修复领域的应用具有较大潜力[8]。国内外研究[9-10]显示:将医用PU粘接剂直接应用于口腔的粘接修复领域中,由于其不易固化或固化条件口腔不耐受以及无法与光固化树脂材料很好地结合等,不能应用于临床。本研究制备一种可光固化PU粘接剂,检测其加入到现有商品粘接剂后对粘接剂的吸水值和溶解值、双键转化率和微剪切强度的影响,综合评价PU粘接剂对传统丙烯酸树脂粘接剂性能的影响,以期为新型耐水解性树脂粘接剂的研究和临床应用提供参考依据。
1 材料与方法 1.1 实验材料和仪器通用型粘接剂Single Bond Universal(SBU)和全酸蚀粘接剂Single Bond 2(SB2)(3MESPE公司,美国),自酸蚀粘接剂SE Bond(SE)(Clearfil公司,日本)。聚醚三元醇(蓝星东大公司,中国),异氟尔酮二异氰酸酯(isophorone diisocyanate, IPDI)、甲基丙烯酸羟乙酯(2-hydroxyethyl methacrylate,HEMA)、丙烯酸异冰片酯、甲基丙烯酸甲酯、丙酮、樟脑醌和4-二甲基氨基苯甲酸乙酯(Sigma公司,美国)。傅里叶转换红外光谱仪(FT-IR)(Nicolet iS10,Thermo Scientific公司,美国), 光固化灯(维润V200,桂林维润医疗科技有限公司),电子分析天平(MATTELER AE240,北京晨曦勇创科技有限公司),电热恒温鼓风干燥箱(DGG-9070B,上海森信实验仪器有限公司),万能试验机(AG-X plus,岛津公司,日本),低速金刚石切割机(SYJ-160,沈阳科晶自动化设备有限公司)。
1.2 PU粘接剂的制备与表征将7.992 g IPDI和0.096 g二月桂酸二丁基锡加入三颈瓶中,68℃油浴下冷凝管冷凝,机械搅拌。再逐滴加入24 g聚醚三元醇(相对分子质量为3 000),反应时间为3 h。使用FT-IR观察无羟基特征峰后,向反应中加入3.12 g HEMA,反应持续2 h后获得聚氨酯丙烯酸酯预聚体,采用红外光谱仪观察无羟基基团后,关闭反应。将产物中的剩余溶剂用真空旋蒸仪除净。通过FT-IR对合成的预聚体进行红外结构表征。PU粘接剂由聚氨酯丙烯酸酯预聚体、稀释剂丙烯酸异冰片酯和甲基丙烯酸甲酯、光引发剂樟脑醌、4-二甲基氨基苯甲酸乙酯和丙酮溶剂组成。其中聚氨酯丙烯酸酯预聚体、丙烯酸异冰片酯、甲基丙烯酸甲酯和丙酮的质量比为6:1.5:1.5:1,光引发剂樟脑醌和助发剂4-二甲基氨基苯甲酸乙酯共占1%~3%的总质量。在本课题组的前期研究中,所合成的聚氨酯单独使用时不能够完全渗透至酸蚀后的牙本质小管内发挥粘接作用,因此在本研究中尝试将PU粘接剂与现有商品粘接剂(SBU、SB2和SE)混合作为新型牙本质粘接剂。在预实验时设计了90%、80%和70% PU 3种混合比例,尽管90%PU和80%PU组的吸水值和溶解值低于70%PU组,但前两者在微剪切实验的试样制备过程中均出现了树脂修复体脱落的现象,未脱落试样的测试结果也较低,因此,最终选择了PU添加质量分数为70%。在避光条件下PU粘接剂分别与SBU、SB2和SE按照质量分数比为70:30进行配置并超声震荡混匀,作为实验组,不加PU粘接剂的SBU、SB2和SE作为对照组。
1.3 各组粘接剂吸水值和溶解值的检测根据标准YY 1042-2011要求,将各组样品滴入圆盘形模具(内径直径15.0 mm±0.1 mm,深度1.0 mm±0.1 mm),光照固化(n=5)。LED蓝光固化灯光源(900 mW·cm-2)统一距离试件表面1 mm。将所有试件放置于含硅胶的干燥器中,37℃恒温保存,每隔24 h监控质量变化直至达到稳定值m1(质量减少量小于0.1 mg)。测量并计算各试件体积V(mm3)。将试件在去离子水中浸泡7 d后取出,用滤纸吸干表面水分,称质量后记为m2。再放置于干燥器内干燥,直至质量再次恒定记为m3。吸水值(water sorption, Wsp)和溶解值(water solubility, Wsl)可由下列公式计算(单位:μg·mm-3): Wsp=(m2-m3)/V, Wsl= (m1- m3)/V。m1为试件浸水前质量(μg),m2为试件浸水后质量(μg),m3为再恒定质量(μg),V为试件的体积(mm3)。公式中Wsp和Wsl的计算均为单位体积(mm3)质量的变化,即已将体积变化的因素考虑在内。
1.4 各组粘接剂双键转化率测定将各组粘接剂涂布均匀薄层于溴化钾压片上,采集样品固化前的FT-IR吸收光谱,再对样品进行光固化,并立即测定样品固化后的FT-IR吸收光谱。以苯环(C…C)为内标(1 609 cm-1),计算C=C双键在峰值1 638 cm-1处的吸光度(A)值变化。双键转化率= 1-固化后A(1638)/A(1609)/固化前A(1638)/A(1609)×100%。
1.5 各组粘接剂微剪切强度测试在患者知情同意的情况下,收集于吉林大学口腔医院拔除的磨牙,要求磨牙结构完好且无龋坏,将离体牙用75%乙醇消毒后保存在4℃生理盐水中。用低速切割机在流水下磨去磨牙的牙釉质层,以完全暴露牙本质。经自凝树脂包埋后用600目碳化硅砂纸湿性打磨形成粘接面,将粘接剂均匀涂抹在牙本质上,将圆孔胶贴贴在粘接面上,限定粘接面积,再将复合树脂Z250充填在圆孔硅胶贴内形成高约2 mm的树脂柱。光固化24 h后,将万能试验机的剪切压头加载于粘接界面,加载速度为1 mm·min-1,记录断裂时的最大剪切力,计算微剪切强度。微剪切强度(MPa)=最大剪切力(N)/粘接面积(mm2)。
1.6 统计学分析采用SPSS19.0统计软件进行统计学分析。各组粘接剂的Wsp、Wsl、双键转换率和微剪切强度均符合正态分布,以x±s表示,两组间样本均数比较采用两独立样本t检验。以P<0.05为差异有统计学意义。
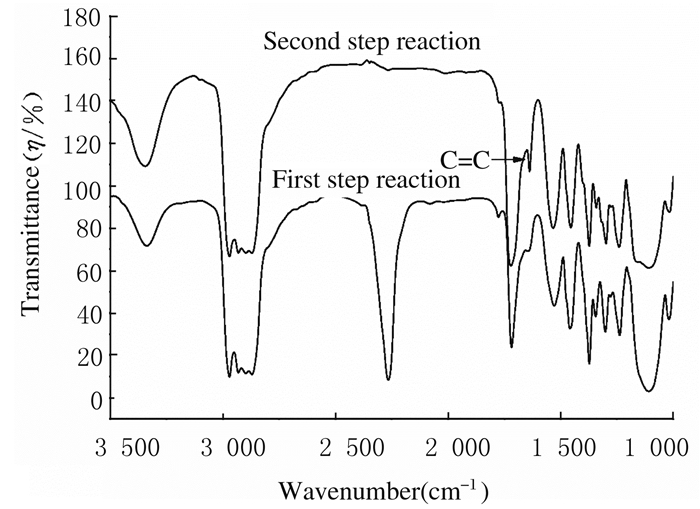
2 结果 2.1 聚氨酯丙烯酸酯预聚体的FT-IR表征聚氨酯丙烯酸酯预聚体合成过程及产物所涉及的主要化学结构式如图 1所示,FT-IR见图 2。由FT-IR可见在3 340 cm-1处为聚醚三元醇中的OH与IPDI中的NCO反应生成的氨基甲酸酯键(-NHCOO-)中的N-H峰,1 720 cm-1处为羰基(C=O)吸收峰,在加入HEMA后于1 637 cm-1处出现了C=C双键的特征吸收峰。FT-IR对产物结构的结果分析与预期产物一致,成功合成含有可光固化基团(C=C)的聚氨酯预聚体。

|
| 图 1 溶液聚合法合成光固化聚氨酯的反应步骤及化学反应式 Fig. 1 Reaction steps and chemical reaction formulas of solution polymerization for synthesizing light-curing polyurethane |
|
|
|
| 图 2 溶液聚合法合成聚氨酯丙烯酸酯预聚体的FT-IR步骤图 Fig. 2 FT-IR steps of synthesizing polyurethane acrylate prepolymer by solution polymerization |
|
|
与SBU、SB2和SE对照组比较,加入PU后的相应实验组粘接剂吸水值明显降低(t=15.479, P < 0.05;t=19.703, P < 0.05;t=11.795, P < 0.05);与SBU和SB2对照组比较,相应实验组粘接剂的溶解值明显降低(t=29.845, P < 0.05;t=28.862, P < 0.05)。见表 1。
| (n=5, x±s, μg·mm-3) | |||||||||||||||||||||||||||||
| Material | Wsp | Wsl | |||||||||||||||||||||||||||
| SBU control | 108.73±9.35 | 45.07±3.27 | |||||||||||||||||||||||||||
| SBU-70%PU | 42.14±2.07* | 4.86±0.42* | |||||||||||||||||||||||||||
| SB2 control | 98.53±6.39 | 62.88±4.89 | |||||||||||||||||||||||||||
| SB2-70%PU | 43.30±3.53△ | 7.81±1.27△ | |||||||||||||||||||||||||||
| SE control | 61.67±5.52 | 1.96±0.91 | |||||||||||||||||||||||||||
| SE-70%PU | 38.63±0.19# | 3.57±1.61# | |||||||||||||||||||||||||||
| * P < 0.05 vs SBU control group; △ P < 0.05 vs SB2 control group; # P < 0.05 vs SE control group. | |||||||||||||||||||||||||||||
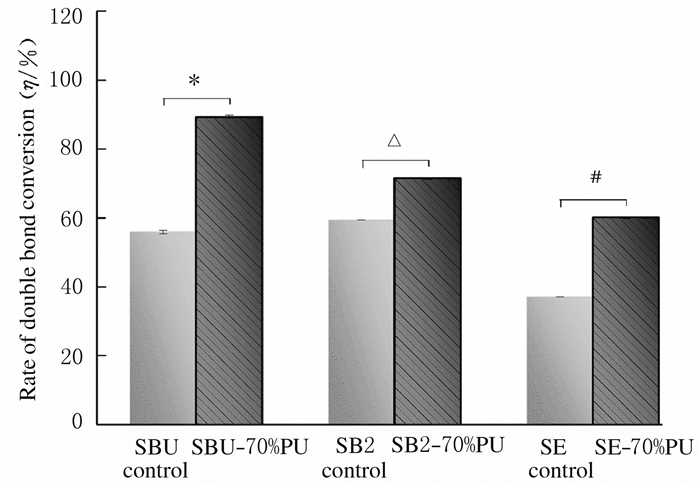
各组粘接剂双键转化率比较情况:SBU-70%PU组>SBU对照组,SB2-70%PU组>SB2对照组,SE-70%PU组>SE对照组,各组间比较差异均有统计学意义(t=-11.612, P < 0.05;t=7.213, P < 0.05;t=-15.031, P < 0.05)。见图 3。
|
| * P < 0.05 vs SBU control group; △ P < 0.05 vs SB2 control group; # P < 0.05 vs SE control group. 图 3 FT-IR法检测各组粘接剂的双键转化率 Fig. 3 Rates of double bond conversion of adhesives in various groups detected by FT-IR method |
|
|
各组粘接剂微剪切强度比较情况: SB2-70%PU组微剪切强度大于SB2对照组(t=-2.515, P < 0.05),SBU-70%PU组和SE-70%PU组与其对照组比较差异无统计学意义(P>0.05)。见图 4。

|
| * P < 0.05 compared with SB2 control group. 图 4 各组粘接剂的微剪切强度 Fig. 4 Micro-shear bond strengths of adhesives in various groups |
|
|
20世纪60年代末,自BUONOCORE成功采用37%磷酸处理牙体硬组织表面以后,树脂粘接剂逐渐发展并得到广泛应用。目前,临床常用的商品树脂粘接剂主要由功能单体或交联单体、光引发剂、抑制剂或稳定剂、溶剂以及无机填料组成[3]。其中亲水性较好的单体如HEMA,因具有优异的渗透能力而被大量添加到商品粘接剂中,以促进疏水性组分和亲水性组分混合,防止产生相分离,同时还可与相对亲水的牙本质之间进行有效结合。然而,HEMA的引入同时也使得牙本质-粘接界面有大量羟基存在,即使在树脂粘接剂充分光固化后,粘接层仍具有很高的吸水性和溶解性,可逐渐造成整个粘接界面的水解降解,机械性能降低,进而引发继发龋,最终导致修复失败[10-11]。因此如何降低商品粘接剂的亲水性及吸水溶解性、增强材料的耐水解性是目前学者们在牙本质粘接领域的研究重点之一。PU是一类具有优异生物相容性、化学多功能性和良好力学性能的软硬段交替组成的聚合物,其中硬链段为多异氰酸酯和小分子扩链剂组成,软链段由低聚物多元醇(主要包括聚酯或聚醚多元醇)组成,是可根据聚多元醇种类的不同而获得不同性能的PU,即聚酯型PU和聚醚型PU。一般而言,醚键比酯基具有更好的耐水性,因此聚醚型PU展现出比聚酯型PU更好的耐水解稳定性。此外,PU聚合物与传统的丙烯酸树脂单体类粘接剂相比,相对分子质量较大,分子链段也较长,交联后形成的聚合物网络结构不易发生水解降解[2, 12-13]。
本研究设计合成一种光固化型PU粘接剂以改善上述存在的问题。通过聚醚三元醇、IPDI和HEMA为原材料, 用红外光谱监控整个合成过程,确保HEMA成功接枝,从而获得可光固化PU。根据临床使用步骤的不同,目前商品粘接剂分为酸蚀-冲洗和自酸蚀两类。为了更充分、全面地评估新合成的PU对现有商品粘接剂性能的影响,本研究中选用了最新一代的通用型粘接剂(SBU)、有金标准之称的两步法酸蚀-冲洗粘接剂(SB2)和经典的自酸蚀粘接剂(SE)作为研究对象。分别在3种商品粘接剂中加入新合成的PU粘接剂,在不影响粘接性能的前提下,提高粘接剂的耐水解性,进一步提升临床光固化复合树脂的粘接修复效果。本研究中吸水值/溶解值实验结果表明:在3种商品粘接剂中加入70%PU后,其吸水值均发生明显降低。其中,在商品粘接剂SBU和SB2中加入70%PU后,溶解值也明显降低。商品粘接剂中含有的HEMA单体、磷酸和羧酸等亲水性物质,使粘接剂聚合后的网络结构易从口腔环境中以“结合水”等形式吸收水分子,导致网络结构链增塑、软化和断裂;而且,逐渐降解的网络结构也会溶解释放未聚合的单体和一些其他小分子物质。随着时间的延长,粘接剂的粘接强度下降,粘接界面的不稳定性增强,修复体的使用寿命缩短,甚至危害人体健康[2, 14-15]。PU材料是一类较单体物质而言相对分子质量较大的低聚物,分子链段相对较长,固化后分子链之间为高交联密度,从而降低了聚合物链膨胀的能力,抵抗水渗透的能力增强[17], 水分子难以进入并对其产生降解。因此,在加入了PU成分后,各组粘接剂的吸水值和溶解值均得到改善。BOARO等[16]的研究显示:SE的溶解值为负数,是由于材料的疏水性使其溶解性和吸水性均降低,导致材料本身的水分子难以溶出,或被结合在材料内部,使材料质量增加。这也可能是本研究中SE组吸水值较大但溶解值相对较低的原因。
在光固化材料中,通常以双键转化率作为评估其聚合能力和固化性能的重要参数。较高的转化率使材料的聚合物网络结构相对致密,不易吸收水分,因此材料的吸水溶解性也较低,也不易有单体游离析出,对维持机械性能的长期稳定性发挥着重要作用。粘接剂材料的双键转化率与单体类型和体系粘度密切相关[17]。本实验中3种商品粘接剂以Bis-GMA单体为主体,含有刚性的芳香结构,并且相邻单体中的-OH和C=O之间能够产生强烈的分子间氢键作用。这些因素均限制了单体在聚合过程中的流动性,进而限制了带双键的树脂单体的移动[18]。尽管粘接剂中含有稀释单体和乙醇或丙酮等溶剂有效降低了材料的粘度体系,但同时也降低了单位体积内含双键成分的浓度,因而最终导致双键发生碰撞的概率减少。而PU粘接剂中不含刚性较强的苯环结构,富含柔韧性较好且相对易移动的醚键,有利于光引发时含双键成分的移动和碰撞。另有研究[19-21]表明:商品粘接剂中的树脂单体相对分子质量较小,在牙本质表面的扩散速率较快且渗透性较强。因此在光固化后未发生聚合的树脂单体和从聚合物中溶解析出的单体也是产生牙髓细胞刺激作用的主要原因,可引发不同程度的牙髓-牙本质复合体的不可逆生物学行为。总之,通过在粘接体系中引入PU材料,在提高体系双键转化率的同时又降低了粘接材料固化后的吸水值和溶解值,有利于减少树脂单体的游离和析出,进而减缓粘接材料对牙髓细胞的刺激作用。
微剪切粘接强度测试是评估树脂粘接剂粘接强度性能的常用方法之一,适宜的微剪切强度是实现良好修复粘接效果的基础[22]。本研究中微剪切实验结果显示:在加入质量分数为70%的可光固化PU后,3个实验组粘接剂的微剪切强度均未发生下降,其中全酸蚀粘接剂SB2的实验组较相应对照组的微剪切强度明显升高。由于本研究所合成的PU无苯环结构,材料的刚性不足,因此当PU的含量过高时会降低粘接剂材料的机械性能,同时还会增加粘接体系的粘稠度而影响其与牙体组织的渗透作用。但加入适量的PU有助于粘接体系双键转化率的提高,增强粘接体系的聚合,使材料的交联固化效果更好,同时也降低了水分子的渗透和水解作用,从而确保与牙体组织的有效粘接。
综上所述,本研究合成的可光固化PU粘接剂在与商品粘接剂共混后,所获得的粘接剂具有较低吸水性和溶解性,良好的光固化性能,且不会降低与牙本质的粘接强度,该粘接体系的研制有望使粘接界面的耐水解稳定性得到改善,为新型树脂-牙本质粘接剂的研究提供参考依据。
| [1] |
SPENCER P, YE Q, SONG L Y, et al. Threats to adhesive/dentin interfacial integrity and next generation bio-enabled multifunctional adhesives[J]. J Biomed Mater Res B Appl Biomater, 2019, 107(8): 2673-2683. DOI:10.1002/jbm.b.34358 |
| [2] |
GONG H H, GUO X W, CAO D F, et al. Photopolymerizable and moisture-curable polyurethanes for dental adhesive applications to increase restoration durability[J]. J Mater Chem B, 2019, 7(5): 744-754. DOI:10.1039/C8TB01716F |
| [3] |
VAN LANDUYT K L, SNAUWAERT J, DE MUNCK J, et al. Systematic review of the chemical composition of contemporary dental adhesives[J]. Biomaterials, 2007, 28(26): 3757-3785. DOI:10.1016/j.biomaterials.2007.04.044 |
| [4] |
NISHITANI Y, YOSHIYAMA M, DONNELLY A M, et al. Effects of resin hydrophilicity on dentin bond strength[J]. J Dent Res, 2006, 85(11): 1016-1021. DOI:10.1177/154405910608501108 |
| [5] |
TAY F R, PASHLEY D H. Have dentin adhesives become too hydrophilic?[J]. J Can Dent Assoc, 2003, 69(11): 726-731. |
| [6] |
TAUSCHER S, ANGERMANN J, CATEL Y, et al. Evaluation of alternative monomers to HEMA for dental applications[J]. Dent Mater, 2017, 33(7): 857-865. DOI:10.1016/j.dental.2017.04.023 |
| [7] |
XU R C, YU F, HUANG L, et al. Isocyanate-terminated urethane-based dental adhesive bridges dentinal matrix collagen with adhesive resin[J]. Acta Biomater, 2019, 83: 140-152. DOI:10.1016/j.actbio.2018.11.007 |
| [8] |
张佳慧, 冯丹, 宫海环, 等. 聚氨酯在牙体修复材料中的应用[J]. 口腔医学, 2016, 36(3): 266-268. |
| [9] |
AKINDOYO J O, BEG M D H, GHAZALI S, et al. Polyurethane types, synthesis and applications-a review[J]. RSC Adv, 2016, 6(115): 114453-114482. DOI:10.1039/C6RA14525F |
| [10] |
宫海环, 郭晓伟, 高平, 等. 新型耐水解牙本质粘结剂的制备及其体外细胞毒性研究[J]. 口腔生物医学, 2017, 8(3): 145-149. |
| [11] |
TJADERHANE L. Dentin bonding:can we make it last?[J]. Oper Dent, 2015, 40(1): 4-18. |
| [12] |
ZHANG C H, ZHANG N, WEN X J. Synthesis and characterization of biocompatible, degradable, light-curable, polyurethane-based elastic hydrogels[J]. Biomed Mater Res A, 2007, 82(3): 637-650. |
| [13] |
朱文强.丙烯酸酯改性聚氨酯胶粘剂的研制[D].柳州: 广西工学院, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10594-1011285942.htm
|
| [14] |
MALACARNE J, CARVALHO R M, DE GOES M F, et al. Water sorption/solubility of dental adhesive resins[J]. Dent Mater, 2006, 22(10): 973-980. DOI:10.1016/j.dental.2005.11.020 |
| [15] |
ARGOLO S, MATHIAS P, AGUIAR T, et al. Effect of agitation and storage temperature on water sorption and solubility of adhesive systems[J]. Dent Mater J, 2015, 34(1): 1-6. DOI:10.4012/dmj.2014-033 |
| [16] |
BOARO L C, GONCÇALVES F, GUIMARÃES T C, et al. Sorption, solubility, shrinkage and mechanical properties of "low-shrinkage" commercial resin composites[J]. Dent Mater, 2013, 29(4): 398-404. DOI:10.1016/j.dental.2013.01.006 |
| [17] |
WANG J, YU Q S, YANG Z Y. Effect of hydrophobic surface treated fumed silica fillers on a one-bottle etch and rinse model dental adhesive[J]. J Mater SciMater Med, 2017, 29(1): 10. |
| [18] |
AL-ANI A A S S, SCARABELLO STAPE T H, MUTLUAY M, et al. Incorporation of dimethyl sulfoxide to model adhesive resins with different hydrophilicities:Physico/mechanical properties[J]. J Mech Behav Biomed Mater, 2019, 93: 143-150. DOI:10.1016/j.jmbbm.2019.02.015 |
| [19] |
ELIAS S T, SANTOS A F D, GARCIA F C P, et al. Cytotoxicity of universal, self-etching and etch-and-rinse adhesive systems according to the polymerization time[J]. Braz Dent J, 2015, 26(2): 160-168. DOI:10.1590/0103-6440201300294 |
| [20] |
KIERKLO A, PAWINSKA M, TOKAJUK G, et al. Cytotoxicity evaluation of three light-cured dentin adhesive materials on human gingival fibroblasts, ex vivo[J]. Adv Med Sci, 2012, 57(2): 385-390. DOI:10.2478/v10039-012-0038-2 |
| [21] |
PORTO I C C M, OLIVEIRA D C, RAELE R A, et al. Cytotoxicity of current adhesive systems:in vitro testing on cell cultures of primary murine macrophages[J]. Dent Mater, 2011, 27(3): 221-228. DOI:10.1016/j.dental.2010.10.006 |
| [22] |
FORNAZARI I A, WILLE I, MEDA E M, et al. Effect of surface treatment, silane, and universal adhesive on microshear bond strength of nanofilled composite repairs[J]. Oper Dent, 2017, 42(4): 367-374. DOI:10.2341/16-259-L |
 2020, Vol. 46
2020, Vol. 46


