2. State Key Laboratory of Urban Water Resource and Environment(Harbin Institute of Technology), 150090 Harbin, China
二氧化锰(MnO2)胶体广泛存在于工程水体和天然水环境[1-4]。在工程应用中,高锰酸钾(KMnO4)还原和溶解态锰的氧化都产生MnO2胶体[5-9];在天然水体中,矿物的风化和生物过程均能产生MnO2胶体。这些生成的胶体,在水中的凝聚行为将会影响到与之相关的无机、有机污染物的去除、迁移和归趋[10-12]。而水体中存在的人造或天然有机物与胶体相互作用,对人工和天然胶体的凝聚有重要影响。进而可能影响到胶体本身,也包括水中相关污染物的去除或在水环境中的迁移和归趋[3,12,13]。
纳米颗粒在水环境中的凝聚动力学是水环境领域重要的课题[14]。研究结果表明,影响纳米颗粒在水中凝聚的因素众多,如静电排斥作用、水化作用、空间位阻作用、范德华作用等。天然有机物(如腐植酸和富里酸)存在时,由于吸附在纳米颗粒表面的大分子有机物增加了颗粒之间的空间位阻作用,纳米颗粒的凝聚速率降低,增加了纳米颗粒的流动性[14]。生物大分子存在时也增加了纳米颗粒在水环境中的凝聚稳定性[15],低浓度工业表面活性剂对纳米颗粒的凝聚动力学也有降低[16]。MnO2胶体在天然有机物和生物大分子存在水体中的凝聚动力学已有研究,天然有机物通过吸附在MnO2颗粒表面,增加颗粒间的空间位阻作用力,进而阻止了MnO2胶体在水环境中的凝聚[17]。然而,有关工业表面活性剂(聚乙二醇,PEG)和天然表面活性剂(表面活性素)对MnO2胶体凝聚动力学的影响尚未有研究报道。因此,本文将研究这些水中常见表面活性剂存在时,MnO2凝聚动力学,并探讨其影响的机理。
1 实验 1.1 实验材料高锰酸钾(KMnO4)、硫代硫酸钠(Na2S2O3)、碳酸氢钠(NaHCO3)、氢氧化钠(NaOH)、硝酸(HNO3)、硝酸钙(Ca(NO3)2)、硝酸钠(NaNO3)均为分析纯,购于上海国药集团有限公司,PEG(分子量:2000、6000)购于天津科密欧化学试剂有限公司,表面活性素(纯度:98%,分子式:C53H93N7O13,分子量:1036.34462)源于西格玛奥德里奇公司。所有药品均未经过纯化,均采用超纯水配制储备液待用(18.2 MΩ cm)。所有实验使用的溶液均利用NaHCO3和NaOH调节至pH=7.0,缓冲浓度为1mmol·L-1。
1.2 MnO2胶体制备及表征MnO2胶体制备采用,无氧条件下,KMnO4被稀Na2S2O3等当量还原生成[17]。反应计量关系见式(1):
| $8MnO_{4}^{-}+3{{S}_{2}}O_{3}^{2-}+2{{H}^{+}}=6SO_{4}^{2-}+8Mn{{O}_{2}}+{{H}_{2}}O$ | (1) |
磁力搅拌器以150 r·min-1搅拌的高锰酸钾溶液,用氦气吹30 min,保持氦气吹脱,将等当量的Na2S2O3缓慢滴入。得到棕褐色胶体,保持搅拌12 h。并在低温下避光保存备用。
制备的MnO2胶体的粒度检测基于动态光散射法检测原理,利用英国马尔文激光粒度仪(Zetasizer,ZS90,UK)检测分析其粒度分布。粒度分布范围是20.03-150.62 nm,检测响应强度加权平均水力直径为75.43 ± 1.23 nm。新制备MnO2胶体的Zeta(ζ)电位采用毛细管检测池,利用英国马尔文激光粒度仪检测,进行20次检测。其检测结果为47.98 ± 3.24 mV。当表面活性剂存在时,液体样品准备与下述凝聚实验准备方法相同。
1.3 吸附试验为探究凝聚机理,考察了凝聚实验中采用的表面活性剂在MnO2表面吸附情况。含26.1 mg·L-1 MnO2胶体体系中投加一定量的表面活性剂储备液,保证体系中最终表面活性剂含量为20 mgTOC·L-1。经过2h吸附平衡之后,通过高速离心(20000 r·min-1)分离去除MnO2之后,检测上清也中残余表面活性剂的浓度,进而计算出MnO2胶体对有机表面活性剂的吸附量,计算公式见式(2)。
| $Q=\frac{{{C}_{0}}-C}{{{C}_{Mn{{O}_{2}}}}}$ | (2) |
式中,Q是MnO2胶体对表面活性剂的吸附量,C0是表面活性剂的初始浓度,20 mgTOC·L-1;C是离心分离后上清液中的表面活性剂浓度;CMnO2是吸附试验中MnO2胶体的浓度,26.1 mg·L-1。
1.4 凝聚实验为定量表达纳米二氧化锰(nMnO2)在阳离子溶液中的凝聚动力学,采用时间分辨的动态光散射法检测在各种盐溶液(NaNO3、Ca(NO3)2)中,nMnO2胶体水力直径随时间的变化。由于,检测结果中响应强度加权平均水力直径最为稳定可靠,因此直径利用响应强度加权平均水力直径作为描述nMnO2尺寸变化的数据。在这部分实验中,将一定量的阳离子使用液加入含有提前计算好体积的nMnO2母液的DLS检测皿中,保证最终溶液是1mL。nMnO2浓度为30 μmol·L-1。检测皿立即在漩涡振荡器上震荡1s后马上进行水力直径检测立即开始,水力直径检测采用连续自动检测模式,每个自动采样时间间隔为30s,检测时间10-90 min不等。
1.5 凝聚动力学的确定MnO2胶体的初期凝聚动力学常数k正比于其初期水力直径增长率[18],见式(3):
| $k\propto \frac{1}{{{N}_{0}}}{{\left( \frac{d{{D}_{h}}\left( t \right)}{dt} \right)}_{t\to 0}}$ | (3) |
式中N0是初始颗粒浓度,Dh(t)是t时刻相应强度加权平均水力直径。dDh(t)/dt是凝聚初期t时刻的水力直径不超过初始直径1.5倍(1.50Dh,0)范围内水力直径的随时间增长的速率。它的值是dDh(t)/dt通过最小二乘法得到。这个方法也被用在其他纳米材料凝聚动力学中[19, 20]。
颗粒附着效率(α)也称为逆稳定率(1/W),用来定量描述MnO2胶体凝聚动力学。它是检测的凝聚速率常数(k)与扩散控制条件下的凝聚速率常数(kfast,不随阳离子浓度改变而改变)的比值。由于在所有凝聚实验中,MnO2胶体浓度相同,一定阳离子浓度下凝聚初期水力直径变化斜率就可以用来计算α值[18],见式(4):
| $\alpha =\frac{1}{W}=\frac{k}{{{k}_{fast}}}=\frac{{{\left( \frac{d{{D}_{h}}\left( t \right)}{dt} \right)}_{t\to 0}}}{{{\left( \frac{d{{D}_{h}}\left( t \right)}{dt} \right)}_{t\to 0,fast}}}$ | (4) |
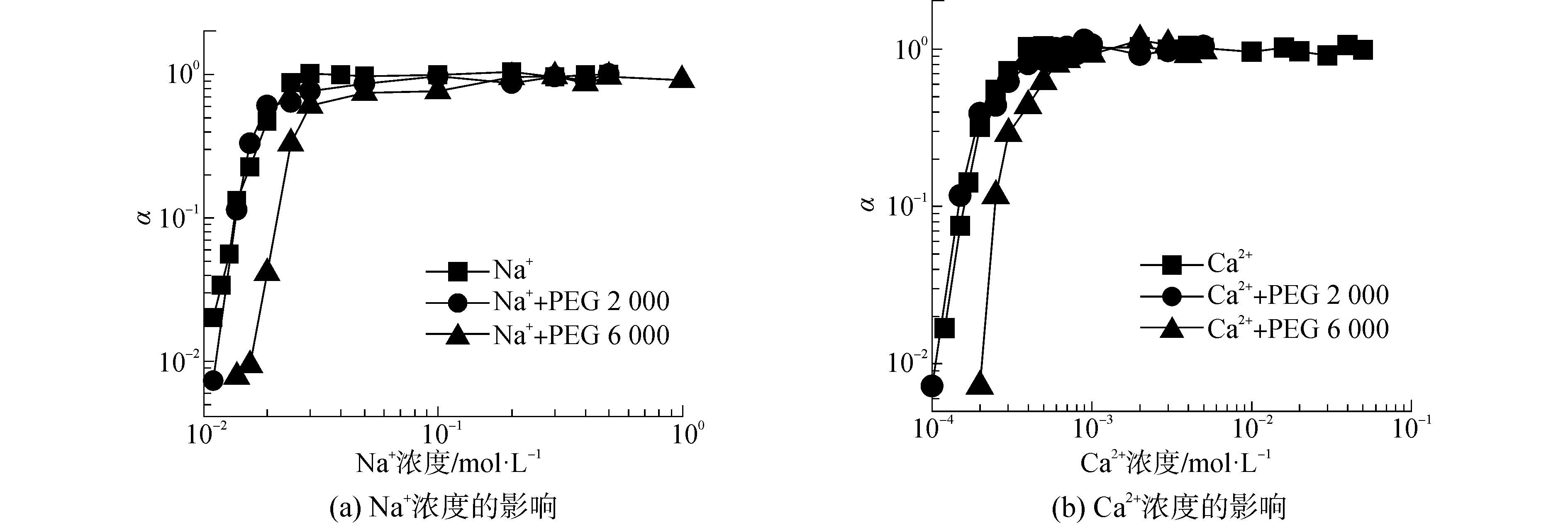
图 1给出了MnO2胶体的凝聚动力学规律,符合经典DLVO理论。如图 1(a)所示,在NaNO3溶液中,当NaNO3溶液浓度小于0.01 mol·L-1时,MnO2凝聚很微弱,几乎可以忽略;当NaNO3浓度增加到0.12 mol·L-1时,凝聚附着率为0.02,继续增加NaNO3浓度,凝聚附着率迅速增加,这一阶段称为反应控制凝聚或慢速凝聚阶段,直到NaNO3浓度为0.03 mol·L-1时,凝聚附着率达到最大值1.0,即达到扩散控制的快速凝聚阶段。因此,MnO2胶体的临界聚沉浓度为0.03 mol·L-1 NaNO3。图 1(b)还显示了在Ca(NO3)2溶液中MnO2胶体的凝聚。由图可知,达到MnO2快速凝聚阶段的临界聚沉浓度为4×10-4 mol·L-1 Ca(NO3)2。
|
| 图1 MnO2胶体在PEG溶液中凝聚附着率变化规律 Figure 1 Attachment efficiency of MnO2 colloids in the presence of PEG |
大分子表面活性剂PEG广泛存在与众多工业废水中,其对MnO2胶体凝聚的影响必然影响与MnO2胶体有关的水处理技术的应用,天然水体中存在的PEG也可能对MnO2胶体凝聚产生相应的影响。图 1显示了不同分子量PEG存在时,MnO2胶体在一价及二价阳离子溶液中的凝聚情况。与没有表面活性剂存在时相似,大分子表面活性剂存在时,纳米MnO2颗粒的凝聚均表现出经典DLVO类型的动力学。即在很低阳离子浓度时,没有显著的凝聚现象,当阳离子浓度升高到一定范围时,凝聚速率迅速增加,直至扩散控制的最大凝聚速率为止。不同分子量PEG表现出阻止MnO2凝聚的规律不尽相同。在分子量为2000 Da的PEG2000存在时,一价和二价离子溶液中,MnO2胶体凝聚均没有显著改变。临界聚沉浓度仍然约为0.03 mol·L-1 NaNO3和4×10-4 mol·L-1 Ca(NO3)2。然而,更大分子量的PEG6000能阻止MnO2凝聚。其临界聚沉浓度约为0.05 mol·L-1 NaNO3和8×10-4 mol·L-1 Ca(NO3)2。
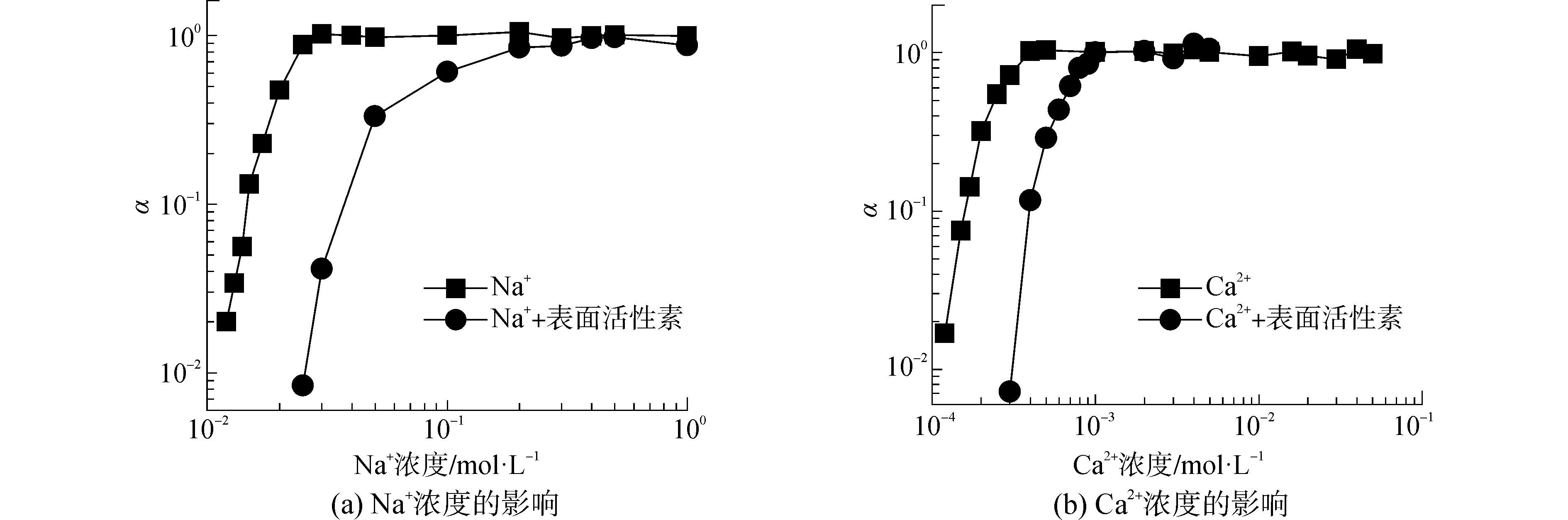
表面活性素是一种脂肽类生物表面活性剂,广泛应用于工业生产,因此,在工程水体中经常出现,这些表面活性剂的存在也会影响相应技术在水和废水处理中的应用。同时,环境中的枯草芽孢杆菌也会分泌产生表面活性素,对天然水体中的MnO2胶体的迁移也有一定影响。因此,考察表面活性素对MnO2凝聚的影响,如图 2所示。
|
| 图2 MnO2胶体在表面活性素溶液中凝聚附着率变化规律 Figure 2 Attachment efficiency of MnO2 colloids in the presence of surfactin |
图 2所示表面活性素存在时,MnO2胶体依然表现出经典DLVO类型的凝聚行为。然而,当NaNO3和CaC(NO3)2浓度分别为0.025 mol·L-1或3×10-4 mol·L-1时,才观察到MnO2的显著凝聚。这比没有表面活性素存在时的0.012 mol·L-1和1×10-4 mol·L-1有较大提高,这说明表面活性素阻碍了MnO2胶体的凝聚。临界聚沉浓度值也具有一致的结果,表面活性素存在时,MnO2的临界聚沉浓度分别为0.1 mol·L-1 NaNO3和10×10-4 mol·L-1 Ca(NO3)2均升高明显,也证明了凝聚被表面活性素抑制。
综上所述,工业表面活性剂PEG的分子量是PEG阻止MnO2胶体凝聚的重要因素。分子量越大,抑制纳米颗粒凝聚能力越强。表面活性素能显著抑制MnO2胶体凝聚。
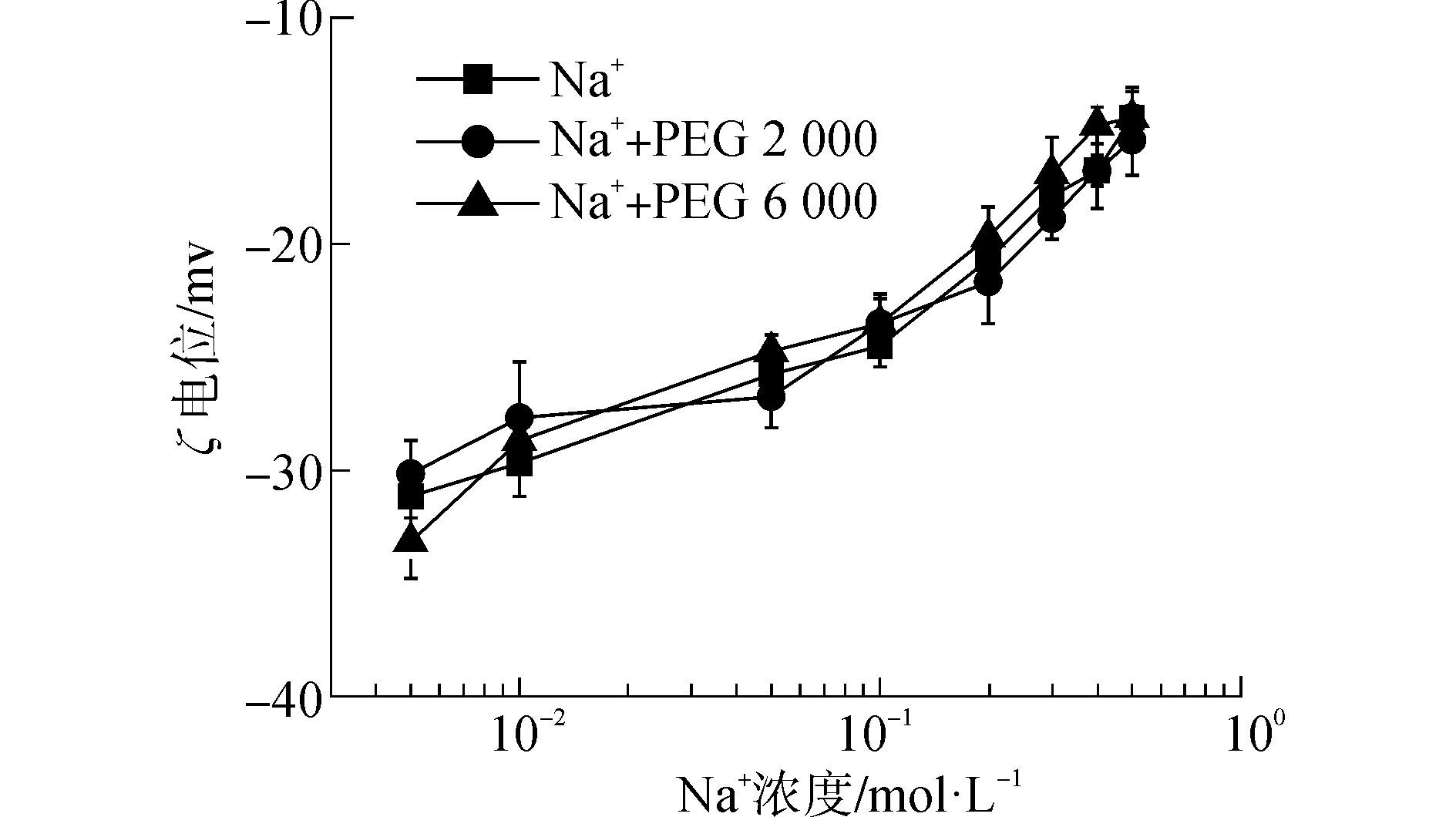
2.2 PEG抑制MnO2凝聚的机理为探讨PEG阻碍MnO2凝聚的机理,检测了PEG存在时,不同阳离子浓度下MnO2胶体的ζ电位。如图 3所示,溶液中无PEG时,随一价阳离子Na+浓度增加,MnO2胶体的ζ电位由-33 mV升高到-15 mV,这说明随Na+浓度的增加,钠在MnO2颗粒表面的吸附,降低了MnO2胶体的表面负电位,进而降低了胶体颗粒间的静电排斥作用,导致了MnO2胶体的凝聚。
|
| 图3 MnO2胶体在PEG溶液中ζ电位随Na+浓度增加的变化规律 Figure 3 MnO2 colloidal ζ potential as function of Na+ concentration in the presence of PEG |
从图 3中还可以看到,PEG2000存在时,相同Na+浓度条件下,MnO2胶体的ζ电位变化微弱,可以忽略。说明溶液中PEG2000并不改变MnO2胶体表面的电荷。表 1显示了MnO2胶体对PEG的吸附,如表所示,有一定量的PEG2000被MnO2颗粒吸附。这说明吸附在MnO2表面的PEG2000对胶体间静电作用影响微弱。结合图 1的凝聚实验结果可以推断,PEG对空间位阻等作用影响也很微弱。图 3还显示更大分子量的高分子表面活性剂PEG6000对MnO2表面的静电作用影响也很微弱。吸附试验结果显示,MnO2胶体对PEG6000的吸附量达0.04mg·g-1(见表 1)。因此,大分子量的PEG产生更大的空间位阻作用可能是Na+溶液中,PEG6000阻止MnO2胶体凝聚的主要原因。
| 表面活性剂 | 吸附量(mgTOC·g-1 MnO2) |
| PEG2000 | 0.03 |
| PEG6000 | 0.04 |
| 表面活性素 | 0.1 |
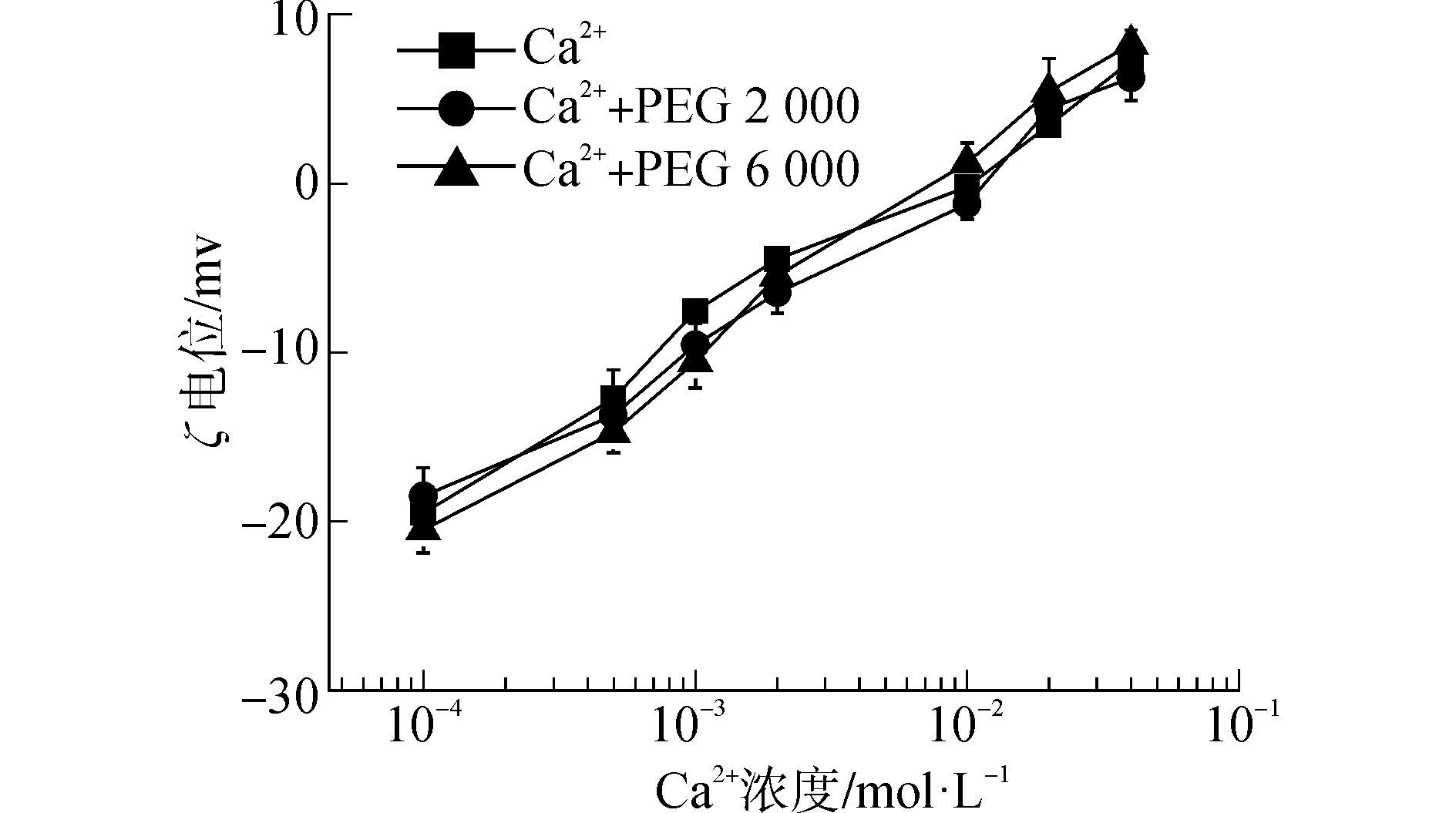
如图 4所示,与一价阳离子Na+相比,二价阳离子Ca2+能更有效降低纳米MnO2的ζ电位,ζ电位从-20 mV升高到5 mV。因此,二价阳离子能更有效降低MnO2胶体表面静电排斥作用,进而更高效地促进MnO2胶体的凝聚。
与一价阳离子Na+相似,有机高分子表面活性剂PEG存在时,MnO2有一定吸附量,在相同浓度二价阳离子Ca2+溶液中的ζ电位变化可以忽略(见图 4)。而表 1证实了两种分子量的PEG在MnO2表面有一定吸附量,这说明,在二价阳离子溶液中,PEG对MnO2胶体凝聚阻碍作用可能也主要是由于增加了空间位阻作用。因此,小分子量的PEG吸附产生的空间位阻太小,对MnO2胶体凝聚影响不大;相反,随着分子量增大,空间位阻增大,因此PEG6000能更高效地阻碍MnO2接近,进而降低了MnO2凝聚速率。与之相似,有研究显示天然有机物的分子量对纳米颗粒的凝聚有一定影响[21],分子量大的有机物产生的空间位阻效应更大,能更有效地组织纳米颗粒的凝聚。
|
| 图4 MnO2胶体在PEG溶液中ζ电位随Ca2+浓度增加的变化规律 Figure 4 MnO2 colloidal ζ potential as function of Ca2+ concentration in the presence of PEG |
凝聚实验显示,表面活性素能更强地降低MnO2胶体的凝聚速率。为探究其阻碍MnO2胶体凝聚动力学的机理,检测了不同阳离子浓度下,表面活性素存在时,MnO2胶体的ζ电位(见图 5)。
|
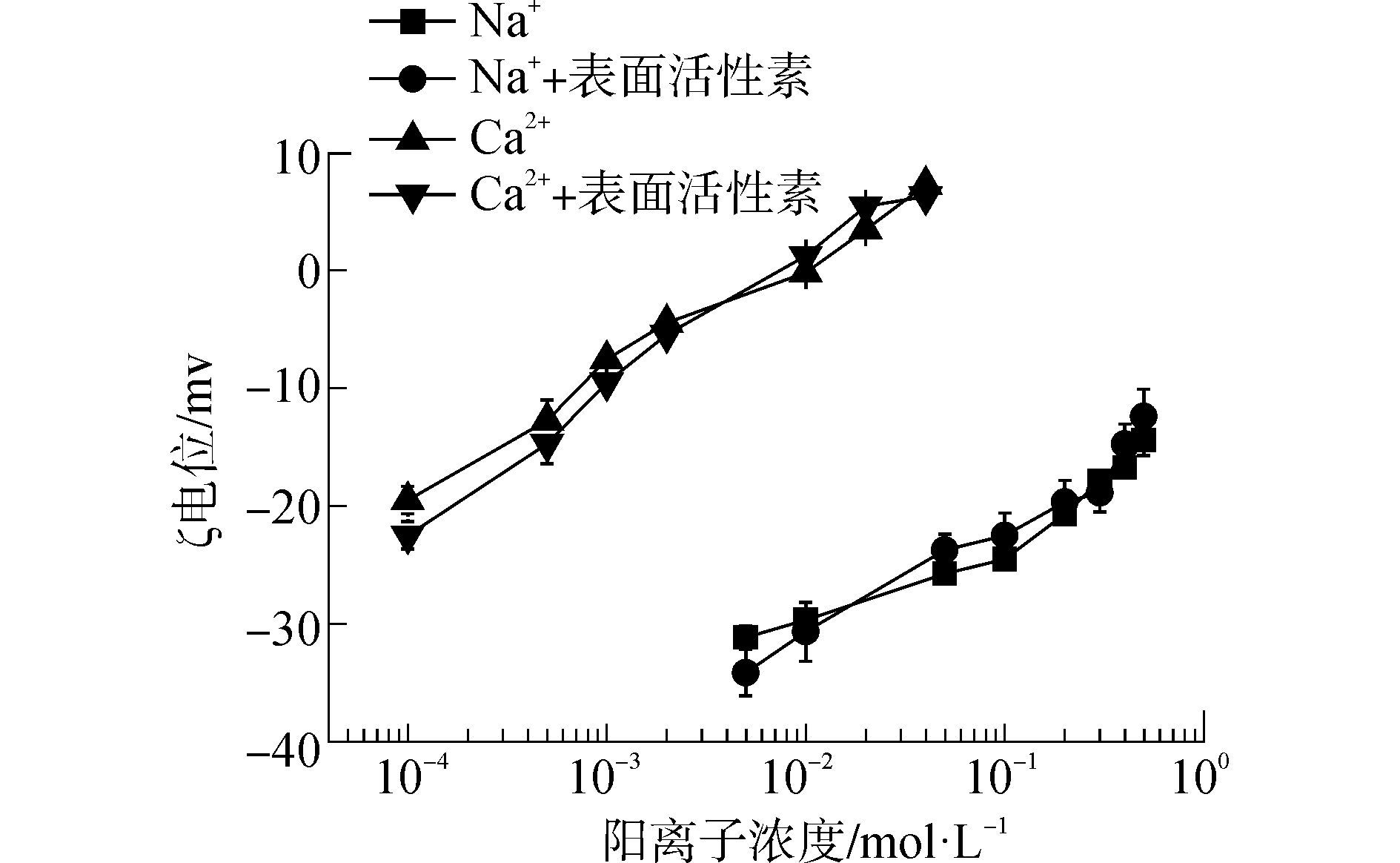
| 图5 MnO2胶体在表面活性素溶液中ζ电位随阳离子浓度增加的变化规律 Figure 5 MnO2 colloidal ζpotential as function of cation concentration in the presence of surfactin |
从图 5中可以看到,随着Na+浓度的增加,溶液中ζ电位从-35 mV升高到-12 mV;而随着Ca2+浓度的增加,溶液中ζ电位从-20 mV升高到6 mV。由此可见,随着阳离子浓度的增加,ζ电位升高,降低了MnO2颗粒表面电荷。但对于一价和二价阳离子,表面活性素的存在均不能显著改变MnO2胶体的ζ电位(见图 5)。因此可以推断,MnO2胶体表面静电排斥作用,依然可能是表面活性素存在时,纳米MnO2凝聚发生的主要原因。由表 1可知,表面活性素在MnO2胶体表面的吸附量达0.1 mg·g-1。因此,MnO2胶体凝聚动力学显著降低的可能原因是由于MnO2胶体粒子之间空间位阻的大幅度增加,而空间位阻的增加主要是由吸附的表面活性素形成有机物吸附层而产生的。
3 结论1) 研究了MnO2在水溶液中的凝聚动力学,一价和二价阳离子均能导致MnO2胶体的凝聚,其临界聚沉浓度约为0.03 mol·L-1 NaNO3和4×10-4 mol·L-1 Ca(NO3)2。主要是由于随着阳离子浓度的增加,吸附阳离子的量增加降低屏蔽了MnO2胶体表面的负电荷,降低其表面电位,导致凝聚作用增强。
2) PEG对MnO2胶体的凝聚动力学影响不显著,PEG2000对纳米MnO2胶体凝聚几乎没有影响,临界聚沉浓度依然是0.03 mol·L-1 NaNO3和4×10-4 mol·L-1 Ca(NO3)2,而PEG6000存在时,临界聚沉浓度有所升高,约为0.05 mol·L-1 NaNO3和8×10-4 mol·L-1 Ca(NO3)2。生物表面活性剂——表面活性素对MnO2胶体的凝聚动力学具有显著影响,能很大程度地阻碍MnO2胶体凝聚,其临界聚沉浓度约为0.05 mol·L-1 NaNO3和8×10-4 mol·L-1 Ca(NO3)2。
3) MnO2胶体表面电荷分析和表面活性剂吸附的研究结果表明,表面活性剂在MnO2胶体表面有一定量的吸附,吸附的表面活性剂层产生的空间位阻是表面活性剂阻碍MnO2胶体凝聚的主要原因。
4) 大分子生物表面活性剂——表面活性素在MnO2表面吸附量最大,产生的空间位阻最大,因此阻止MnO2胶体凝聚的能力最强;对于吸附量相近的工业表面活性剂PEG,分子量成为产生不同空间位阻的主要原因,即分子量越大,产生的空间位阻能力越强,降低纳米MnO2凝聚速率的能力越强。
| [1] | FERREIRA J R, LAWLOR A J, BATES J M, et al. Chemistry of riverine and estuarine suspended particles from the Ouse-Trent system, UK[J]. Colloids and surfaces a:physicochemical and engineering aspects, 1997, 120(1/2/3): 183–198. |
| [2] | LIENEMANN C P, TAILLEFERT M, PERRET D, et al. Association of cobalt and manganese in aquatic systems:chemical and microscopic evidence[J]. Geochimica et cosmochimica acta, 1997, 61(7): 1437–1446. |
| [3] | HERSZAGE J, AFONSO M D S, LUTHER III G W. Oxidation of cysteine and glutathione by soluble polymeric MnO2[J]. Environmental science & technology, 2003, 37(15): 3332–3338. |
| [4] | ZHANG Huichun, HUANG C H. Oxidative transformation of triclosan and chlorophene by manganese oxides[J]. Environmental science & technology, 2003, 37(11): 2421–2430. |
| [5] | ANDRZEJEWSKI P, NAWROCKI L, NAWROCKI J. The role of manganese dioxide (MnO2) in the process of N-nitrosodimethylamine (NDMA) formation during reaction of dimethylamine (DMA) with some oxidants in water solutions[J]. Ochrona srodowiska, 2009, 31(4): 25–29. |
| [6] | JIANG Jin, PANG Suyan, MA Jun. Oxidation of triclosan by permanganate (Mn(VII)):importance of ligands and in situ formed manganese oxides[J]. Environmental science & technology, 2009, 43(21): 8326–8331. |
| [7] | LOOMER D B, AI T A, BANKS V J, et al. Manganese valence in oxides formed from in situ chemical oxidation of TCE by KMnO4[J]. Environmental science & technology, 2010, 44(15): 5934–5939. |
| [8] | AL-THABAITI S A, AL-NOWAISER F M, OBAID A Y, et al. Formation and decomposition of water soluble colloidal manganese dioxide during the reduction of MnO4-by cysteine. A kinetic study[J]. Journal of dispersion science and technology, 2008, 29(10): 1391–1395. |
| [9] | MA Jun, GRAHAM N. Controlling the formation of chloroform by permanganate preoxidation-destruction of precursors[J]. Journal of water supply:research and technology-AQUA, 1996, 45(6): 308–315. |
| [10] | WIGGINTON N S, HAUS K L, HOCHELLA M F JR. Aquatic environmental nanoparticles[J]. Journal of environmental monitoring, 2007, 9(12): 1306–1316. |
| [11] | BUFFLE J, LEPPARD G G. Characterization of aquatic colloids and macromolecules 1. structure and behavior of colloidal materia[J]. Environmental science & technology, 1995, 29(9): 2169–2175. |
| [12] | VILLALOBOS M, BARGAR J, SPOSITO G. Mechanisms of Pb(II) sorption on a biogenic manganese oxide[J]. Environmental science & technology, 2005, 39(2): 569–576. |
| [13] | YANG Kun, LIN Daohui, XING Baoshan. Interactions of humic acid with nanosized inorganic oxides[J]. Langmuir, 2009, 25(6): 3571–3576. |
| [14] | PETOSA A R, JAISI D P, QUEVEDO I R, et al. Aggregation and deposition of engineered nanomaterials in aquatic environments:role of physicochemical interactions[J]. Environmental science & technology, 2010, 44(17): 6532–6549. |
| [15] | SALEH N B, PFEFFERLE L D, ELIMELECH M. Influence of biomacromolecules and humic acid on the aggregation kinetics of single-walled carbon nanotubes[J]. Environmental science & technology, 2010, 44(7): 2412–2418. |
| [16] | BOUCHARD D, ZHANG Wei, POWELL T, et al. Aggregation kinetics and transport of single-walled carbon nanotubes at low surfactant concentrations[J]. Environmental science & technology, 2012, 46(8): 4458–4465. |
| [17] | HUANGFU Xiaoliu, JIANG Jin, MA Jun, et al. Aggregation kinetics of manganese dioxide colloids in aqueous solution:influence of humic substances and biomacromolecules[J]. Environmental science & technology, 2013, 47(18): 10285–10292. |
| [18] | HOLTHOFF H, EGELHAAF S U, BORKOVEC M, et al. Coagulation rate measurements of colloidal particles by simultaneous static and dynamic light scattering[J]. Langmuir, 1996, 12(23): 5541–5549. |
| [19] | CHENG K L, ELIMELECH M. Aggregation and deposition kinetics of fullerene (C60) nanoparticles[J]. Langmuir, 2006, 22(26): 10994–11001. |
| [20] | SMITH B, WEPASNICK K, SCHROTE K E, et al. Colloidal properties of aqueous suspensions of acid-treated, multi-walled carbon nanotubes[J]. Environmental science & technology, 2009, 43(3): 819–825. |
| [21] | LOUIE S M, TILTON R D, LOWRY G V. Effects of molecular weight distribution and chemical properties of natural organic matter on gold nanoparticle aggregation[J]. Environmental science & technology, 2013, 47(9): 4245–4254. |



