扩展功能
文章信息
- 李林, 徐淑华, 赵建设
- LI Lin, XU Shu-Hua, ZHAO Jian-She
- 23例MRI误、漏诊局灶性皮质发育不良患儿(FCD)术后回顾性读片再认识
- Postoperative image reading for children with focal cortical dysplasia misdiagnosed or missed by magnetic resonance imaging: A retrospective analysis of 23 cases
- 国际神经病学神经外科学杂志, 2020, 47(2): 186-190
- Journal of International Neurology and Neurosurgery, 2020, 47(2): 186-190
-
文章历史
收稿日期: 2020-01-05
修回日期: 2020-03-05
2. 日照市人民医院放射科, 山东 日照 276800
2. Department of Radiology, Ri Zhao people's hospital, Rizhao, Shandong 276800
局灶性皮质发育不良(focal cortical dysplasia,FCD)是属于脑皮质发育畸形的一个亚型,也是儿童顽固性癫痫常见病因之一,相关文献[1]报道所占比例超过30%以上,但是药物治疗效果却不理想,外科手术切除致痫灶是彻底治愈本病的唯一有效手段。术前对致痫灶进行准确的评估与定位对于手术方案的制定起着至关重要的作用。由于磁共振3D高分辨成像具有多参数、多方位及软组织分辨率高的优势等特点,其检出和识别FCD病灶的能力,较常规MRI序列大大提高[2],成为术前定位器质性病灶的首选检查方法。然而,由于部分FCD病灶较局限、且隐匿,缺乏典型MRI征象[3],MRI对此部分患儿的术前器质性定位变得尤为困难,从而会出现漏诊及误诊的情况。本研究收集了23例术前MRI读片漏诊或误诊的FCD患儿的MRI及其病理学资料,对其进行深度分析及再认识,找出异常放电区域脑结构的异常及MRI特征。既往,这方面国内外报道较为少见,本研究将会帮助临床医生在术前准确识别此部分FCD患儿的MRI征象,这对外科医生进行术前的准确评估、定位及手术方案的制定都将起着至关重要的作用。
1 资料与方法 1.1 一般资料收集2014年5月—2019年6月间经术后病理证实的误诊及漏诊的23例FCD患儿MRI及病理学资料,男15例,女8例,年龄6个月~8.9岁,中位年龄3.2岁。病理标准[4]为国际抗癫痫联盟协会(International League Against Epilepsy,ILAE)于2011年发布的最新病理学分类:单纯型(Ⅰ、Ⅱ型)和结合型(Ⅲ型)。该研究通过了本院伦理委员会的审核,争取了患儿监护人的知情同意并自愿签署知情同意书。
1.2 设备及参数使用Ingenia 3.0T超导磁共振扫描仪(Philips),对于不能主动配合的患儿,检查前给予5%水合氯醛(0.4~0.5 mL/kg)口服, 使其进入深睡眠状态再行检查。高分辨3D-T1W:最小TR,最小TE,TI 310 ms,翻转角10°,FOV 290 mm×290 mm,矩阵285×285;高分辨3D-T2 FLAIR序列,TR 80.5ms,TE 66.5 ms,TI 315 ms,翻转角10°,FOV 290 mm×290 mm,矩阵285×285。其他常规序列:T1W,TE 13.5 ms,TR 767.0 ms,FOV 290 mm×290 mm,矩阵265×265,层厚5 mm,间隔1 mm;T2W,TE 125 ms,最小TR,FOV 285 mm×285 mm,矩阵265×265,层厚5 mm,间隔1 mm;T2-FLAIR序列,TE 170 ms,TR 13 000 ms,FOV 285 mm×285 mm,矩阵265×265,层厚5 mm,间隔1 mm。
1.3 图像分析由3名具有10年以上工作经验的影像科高年资医师进行回顾性图像分析。主要观察原异常放电区域MRI征象:①局部脑沟形态异常;②局部脑回形态异常;③局部节段性或脑叶萎缩/发育不全与白质体积缩小;④T2WI/FLAIR灰白质内异常信号灶。上述①、②、③的参考标准均为与对侧比较,位置采用标准对称轴位及冠状位来观察。
2 结果23例经术后病理证实的FCD患儿,术前MRI读片为阴性或诊断错误,病理学示Ⅰ型17例,Ⅱ型6例。术后重新阅术前片发现术区异常改变:①局部脑沟形态异常5例(21.74%)(图 1),表现为脑沟宽窄不等2例、脑沟深宽1例、脑沟边缘不规整2例;病理学示Ⅰa型2例,表现为成熟神经元,其内仅为放射状层状结构不良,Ⅰb型1例,为异形神经元(少量)伴切线方向结构不良,Ⅱa型2例,病理学示其内大量异形神经元(体积较大、数量较多),术前MRI读片均为阴性。②局部脑回形态异常7例(30.43%),其中脑回形态失常3例、单纯脑回轻度增大3例、局部脑回略变小1例;病理示Ⅰb型3例,表现为灰白质分界模糊伴少量异形神经元,Ⅱa型4例,表现为切线方向的结构不良伴大量异形神经元,术前读片诊断为先天发育异常3例,4例为阴性。③局部白质体积缩小4例(17.39%),病理示Ⅰc型1例,为各方向的皮层结构不良伴或不伴异形神经元,Ⅱa型3例,灰白质分界模糊伴大量异形神经元,术前均诊断为髓鞘化延迟。④局部白质内片状T2WI/FLAIR信号略增高2例(8.70%),病理示Ⅱb型,1例为标本内气球样变细胞及大量异形神经元,另1例病灶内无气球样变细胞,术前1例诊断为髓鞘化不良、1例为阴性。⑤节段性脑萎缩2例(8.70%),均为Ⅰ型,未见明显异形神经元,仅为轻微层状结构不良,病理学无法区分各亚型,术前读片诊断为局限性蛛网膜下腔增宽。⑥3例(13.04%)为皮层下多发团状及条片状异常信号灶,病理示Ⅱb型,为病灶内大量气球样变细胞及异形神经元,患儿术前诊断为结节硬化(图 2)。
|
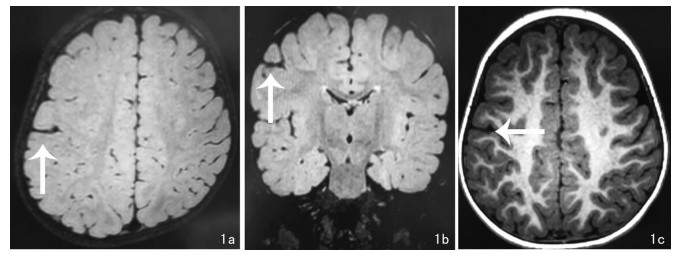
| 1a(轴位)、1b(冠状位)分别为3D高分辨T2WI-FLAIR,右侧额顶叶交界区异常形态脑沟,脑沟宽窄不等、且边缘不规整(箭头所示);1c(轴位)为3D高分辨T1WI, 右侧额顶叶交界区异常脑沟周围灰白质分界模糊(箭头所示) 图 1 典型病例1,女,2岁,FCDⅠa型MRI成像 |
|
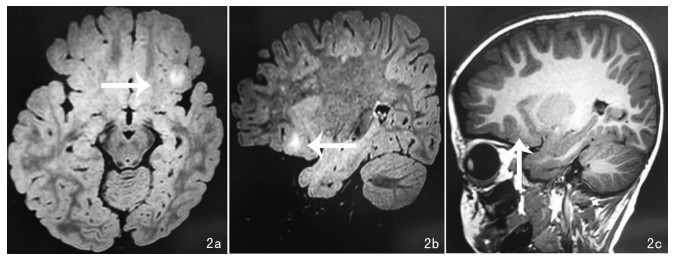
| 2a(轴位)、2b(矢状位)为3D高分辨T2WI-FLAIR,左侧额叶皮层下可见团状高信号灶,边界模糊(箭头所示);2c为3D高分辨T1WI, 左额叶低信号灶,伴周围灰白质分界模糊(箭头所示) 图 2 典型病例2,男, 5岁, FCDⅡa型MRI成像 |
儿童FCD发病机制为胚胎期神经元及胶质细胞的分化、增值、迁徙等环节发生异常所导致的局部脑皮层的发育畸形,而产生一系列病理变化[5、6]。本病主要临床症状为癫痫发作及部分认知功能的损害,抗癫痫药物治疗效果较差,不能够很好的控制患儿癫痫发作,给患儿及整个家庭带来了沉重负担。近年来,外科手术切除致痫灶逐渐成为治愈FCD所致癫痫的唯一有效手段[7],而手术切除致痫灶成败最关键的是术前准确评估与定位,由于MRI在中枢神经系统病变中的明显优势,成为了FCD术前器质性病变定位的主要影像学检查手段,相关文献报道[8、9]MRI阳性FCD患儿手术预后要明显好于阴性患儿,原因可能为MRI阳性FCD患儿定位与评估可能更准确,临床手术方案的制定也会更加完善。然而对于部分发病较隐匿的FCD患儿,MRI检查却不能够很好的识别其轻微脑结构异常而导致漏诊,部分非典型MRI征象的FCD患儿容易导致误诊为其它病变,给术前评估及手术方案的制定带来了较大困难。
本研究中,我们收集了23例术前误诊及漏诊的FCD患儿的MRI资料,对其影像学特征进行深分析。其中5例FCD术前MRI读片为阴性,术后经过深分析、阅片,发现原致痫区域(手术切除区域)与健侧(对侧)比较脑沟形态的异常,可为脑沟宽窄不等、边缘不规整等多种改变,相关文献[10]也曾报道,FCD有时候仅仅只表现为局部脑沟形态的异常,此时仅仅依靠MRI无法明确诊断,因为脑沟形态异常本身并无特异性,必须密切结合临床脑电等相关检查,才能最终确定病变及异常放电区域,这与我们的研究是一致的。7例局灶性脑回形态的轻微结构异常,包括脑回形态的轻度失常,略增大或变小,常规读片很容易漏诊或误诊,术前4例读片阴性,3例诊断为先天发育异常,分析原因为轻度脑回异常MRI征象不典型,诊断较困难,回顾性阅片后,给我们的提示是:癫痫患儿MRI检查后必须三维重建标准对称的轴位及冠状位,结合临床脑电等检查来确定局灶性轻微脑结构异常,同时两侧对比也是临床常用的排除脑轻微结构异常的常用方法。局部脑白质体积缩小4例,术前诊断为髓鞘化延迟,回顾性阅片后认为,髓鞘化延迟一般是一种弥漫性脑髓鞘化落后,不会出现在局部白质内[11],这也提示我们,如果遇到局灶性白质体积缩小的癫痫患儿,应该想到FCD的可能。局部白质内片状T2WI/FLAIR信号略增高2例,术前1例诊断为髓鞘化不良、1例为阴性,回顾性分析:经元移行的方向是从内向外进行的[12],如果在终末阶段导致神经元移行停滞的因素出现,那么少量神经元就会停留在位置较深的白质内,表现为T2WI/FLAIR略高信号,此种情况与髓鞘化不良鉴别较为困难。节段性脑萎缩2例,术前读片诊断为局限性蛛网膜下腔增宽,此种表现缺乏特异性,且不是FCD的典型MRI特征,故术前较难做出正确诊断,回顾性读片后的出的结论为,脑萎缩是一种细胞数目减少,脑组织体积缩小,脑室和蛛网膜下腔扩大的病理状态[13],局灶性脑萎缩主要病因有外伤及炎症等损伤后遗所致,当癫痫患儿遇到局灶性脑萎缩时,需要结合相关病史来做出正确诊断。本组中3例FCDⅡ型患儿术前诊断为结节硬化,表现为皮层下单发或多发团状及条片状异常信号灶,结节硬化症,临床表现为智力低下、癫痫、皮脂腺瘤三联征,MRI征象为室管膜下多发细颈状异常信号灶突入脑室,呈波浪状或锯齿状改变,皮层及皮层下多发异常信号灶[14],常多发,而FCD一般为单发局灶性病变较常见,增强扫描未钙化结节强化较明显,此点可作为二者的鉴别要点,回顾性阅片后,认为结合临床症状及典型MRI征象不难鉴别。
本组中节段性脑萎缩2例均为Ⅰ型,但术后病理学无法区分各亚型,原因可能是萎缩脑组织不具备典型皮层六层结构[15],从而无法区分异形神经元及皮层结构不良。其余病例均可以准确到各亚型,Ⅰ型中病理学表现以轻度皮层结构不良与少量异形神经元为主,其病理学表现较轻微,又因为FCD磁共振征象是病理特征的宏观表现[16],故相应MRI征象不明显或不典型从而导致漏诊或误诊的发生。Ⅱ型患儿的主要病理学改变为大量异形神经元伴或不伴气球样变细胞,如果不伴有气球样变细胞时,MRI征象主要为灰白质分界模糊,当位于脑沟、回附近较隐匿时容易漏诊;当患儿伴有气球样变细胞时,基本是以误诊为主,因为此征象较为显著,是MRI上tansmantle征(T2WI或T2 FLAIR序列白质内向脑室方向延伸锥形高信号)形成的主要病理学基础[17],但此征象却不是FCD的特异征象,容易与其它疾病混淆,本组中有3例患儿术前层误诊为结节硬化。通过本文分析与总结,结合其病理学特征,我们对MRI不典型及局灶性脑结构改变轻微的FCD患儿有了更深刻及新的认识,提示我们只有密切结合患儿病史及临床症状,采用标准位置MRI成像及多人阅片的模式,才能够对此部分患儿做到不漏诊及误诊的发生。相信随着影像学新技术的不断发展[18]及对FCD病变的深刻认识,MRI术前正确诊断率将会大大提高。
| [1] |
Kakita A. Surgical pathologic features of cerebral cortical lesions taken from 600 patients with intractable epilepsy[J]. Brain Dev, 2013, 35(8): 793-801. |
| [2] |
Veersema TJ, Ferrier CH, van Eijsden P, et al. Seven tesla MRI improves detection offocal cortical dysplasia in patients with refractory focal epilepsy[J]. Epilepsia Open, 2017, 2(2): 162-171. |
| [3] |
Hong SJ, Bernhardt BC, Caldairou B, et al. Multimodal MRI profiling of focal cortical dysplasia type II[J]. Neurology, 2017, 88(8): 734-742. |
| [4] |
Blümcke I, Thom M, Aronica E, et al. The clinicopathologic spectrum of focal cortical dysplasias:A consensus classification proposed by an ad hoc Task Force of the ILAE Diagnostic Methods Commission[J]. Epilepsia, 2011, 52(1): 158-174. |
| [5] |
Foldvary-Schaefer N, Bautista J, Andermann F, et al. Focal malformations of cortical development[J]. Neurology, 2004, 62(6 Suppl 3): 14-19. |
| [6] |
Taylor DC, Falconer MA, Bruton CJ, et al. Focal dysplasia of the cerebral cortex in epilepsy[J]. J Neurol Neurosurg Psychiatry, 1971, 34(4): 369-387. |
| [7] |
Jayalakshmi S, Nanda SK, Vooturi S, et al. Focal Cortical Dysplasia and Refractory Epilepsy:Role of Multimodality Imaging and Outcome of Surgery[J]. AJNR Am J Neuroradiol, 2019, 40(5): 892-898. |
| [8] |
Elsharkawy AE, Alabbasi AH, Pannek H, et al. Outcome of frontal lobe epilepsy surgery in adults[J]. Epilepsy Res, 2008, 81(2-3): 97-106. |
| [9] |
徐翠萍, 杜薇, 遇涛, 等. 儿童和青少年额叶癫痫患者术后急性发作及长期疗效分析[J]. 中华神经外科杂志, 2016, 32(4): 344-348. |
| [10] |
Sacino MF, Ho CY, Whitehead MT, et al. Resective surgery for focal cortical dysplasia in children:a comparative analysis of the utility of intraoperative magnetic resonance imaging (iMRI)[J]. Childs Nerv Syst, 2016, 32(6): 1101-1107. |
| [11] |
Sharma P, Powell KL, Wlodek ME, et al. Delayed myelination and neurodevelopment in male seizure-prone versus seizure-resistant rats[J]. Epilepsia, 2018, 59(4): 753-764. |
| [12] |
孙国强, 等. 实用儿科放射诊断学. 北京: 人民军医出版社, 2011: 35-43.
|
| [13] |
Moon Y, Moon WJ, Kim JO, et al. Muscle Strength Is Independently Related to Brain Atrophy in Patients with Alzheimer's Disease[J]. Dement Geriatr Cogn Disord, 2019, 47(4-6): 306-314. |
| [14] |
Jesmanas S, Norvainyt K, Gleiznien R, et al. Different MRI-defined tuber types in tuberous sclerosis complex:Quantitative evaluation and association with disease manifestations[J]. Brain Dev, 2018, 40(3): 196-204. |
| [15] |
Fauser S, Essang C, Altenmüller DM, et a1. Long-term seizure outcome in 211 patients with focal cortical dysplasia[J]. Epilepsia, 2015, 56(1): 66-76. |
| [16] |
Tassi L, Garbelli R, Colombo N, et al. Electroclinical, MRI and surgical outcomes in 100 epileptic patients with type II FCD[J]. Epileptic Disord, 2012, 14(3): 257-266. |
| [17] |
Colombo N, Tassi L, Deleo F, et al. Focal cortical dysplasia type Ⅱa and Ⅱb:MRI aspects in 118 cases proven by histopathology[J]. Neuroradiology, 2012, 54(10): 1065-1077. |
| [18] |
Sakaguchi Y, Kidokoro H, Ogawa C, et al. Longitudinal Findings of MRI and PET in West Syndrome with Subtle Focal Cortical Dysplasia[J]. Am J Neuroradiol, 2018, 39(10): 1932-1937. |
 2020, Vol. 47
2020, Vol. 47




