扩展功能
文章信息
- 马刘佳, 郑云锋, 康平, 胡国良
- MA Liu-Jia, ZHENG Yun-Feng, KANG Ping, HU Guo-Liang
- 血管紧张素转换酶基因多态性与自发性蛛网膜下腔出血后脑血管痉挛的相关性研究
- A study on the association between angiotensin converting enzyme gene polymorphism and cerebral vasospasm in patients with spontaneous subarachnoid hemorrhage
- 国际神经病学神经外科学杂志, 2019, 46(5): 528-531
- Journal of International Neurology and Neurosurgery, 2019, 46(5): 528-531
-
文章历史
收稿日期: 2019-04-08
修回日期: 2019-09-02
脑血管痉挛(cerebral vasospasm, CVS)是蛛网膜下腔出血(subarachnoid hemorrhage, SAH)患者最常见的并发症之一,直接影响远端脑血管灌注,严重者可导致脑梗死发生,显著增加SAH患者的病残率和死亡率[1-3]。因此,早期识别与预防CVS发生对SAH患者远期预后具有重要意义。有研究发现SAH患者血管紧张素转换酶(angiotensin-converting enzyme, ACE)表达异常,并与CVS存在一定时间相关性,提示ACE可能参与CVS发生过程[4, 5]。本研究以166例自发性SAH患者为研究对象,探讨ACE基因插入(insertion, I)/缺失(deletion, D)多态性及其血清水平与CVS的相关性,为临床工作提供参考。
1 对象与方法 1.1 研究对象连续性选择2014年10月至2017年1月于我院神经外科治疗的自发性SAH患者纳入研究,纳入标准:①年龄>18岁或≤80岁; ②SAH诊断明确,并经头颅CT/MR检查确认; ③首次发病,且由发病到住院<24 h; ④出生并长期生活于陕西地区的汉族人,彼此无血缘关系; ⑤一般临床资料完整; ⑥患者及家属完全知情同意。排除标准:①创伤性SAH; ②病情严重,发病早期即出现脑疝、死亡; ③合并其他严重神经、精神疾病; ④合并严重肝肾功能障碍、自身免疫疾病、严重感染、恶性肿瘤、严重凝血功能障碍,或近期口服抗血小板、抗凝药物; ⑤妊娠期女性。本研究共纳入166例患者,其中男97例,女69例,平均年龄(50.2±11.4)岁。本研究通过本院伦理委员会审核批准。
所有研究对象按照有无合并CVS分为CVS组和对照组,其中CVS组72例,包括男42例,女30例,平均年龄(48.9±10.2)岁; 对照组94例,包括男55例,女39例,平均年龄(51.1±12.7)岁,两组患者性别,年龄差异均无统计学意义(χ2=2.005, P=0.157; t=0.643, P=0.521)。CVS的诊断标准:SAH发病3 d~2周内; 患者临床症状经治疗好转或稳定后再次恶化或进行性加重; 经颅多普勒(transcranial Doppler, TCD)超声检查大脑中动脉峰值平均血流速度(peak mean flow velocity, PMFV)≥140 cm/s,或大脑后动脉PMFV≥90 cm/s,并排除再出血、脑积水、感染和电解质紊乱等因素后可诊断为CVS。
1.2 研究方法 1.2.1 一般临床资料收集所有入组患者临床资料,主要包括患者性别、年龄、体重指数、吸烟史、饮酒史、高血压史、糖尿病史、Fisher分级和Hunt-Hess分级等。
1.2.2 血清ACE测定分别于入院时,及入院后第4、7、10、13天抽取外周静脉血,采用ELISA法检测患者血清ACE水平,试剂盒购自武汉博士德生物工程有限公司,严格按照使用说明进行操作。
1.2.3 基因组DNA提取采集清晨空腹时外周静脉血用于实验室检查,部分样本采用DNA提取试剂盒(天根生化科技有限公司,北京)提取全血基因组DNA。
1.2.4 PCR扩增PCR反应体系主要包括:上下游引物各1 μl(上游:5'-CTGGAGACCACTCC CATCCTTTCT-3';下游:5'-GATGTGGCCATCACATTCGTCAGAT-3',均由上海生工生物技术有限公司合成)、dNTP混合物2 μL、TaqDNA聚合酶0.25 μL、模板DNA 1 μl、10×Buffer 2.5 μl。反应条件:95℃预变性4 min,然后按照变性95℃ 20 s、退火65℃ 30 s、延长72℃ 50 s的顺序循环30周期,最后72℃延长3 min。
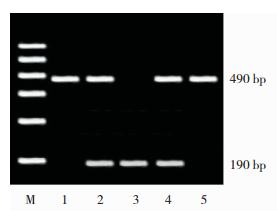
1.2.5 基因型判读取PCR扩增产物进行电泳,紫外灯下观察并摄片,有且只有1条490 bp电泳带记为Ⅱ基因型,有且只有1条190 bp电泳带记为DD基因型,490 bp和190 bp电泳带同时存在时记为ID基因型,见图 1。
|
| 图 1 ACE基因I/D多态性PCR-RFLP结果 |
采用SPSS 19.0统计软件分析处理,计量资料结果以均数±标准差(x±s)表示,多组均数比较采用方差分析,组间两两比较采用SNK-q检验,两组均数比较采用t检验; 计数资料结果以构成百分比(%)表示,组间比较采用χ2检验。基因型分布采用Hardy-Weinberg平衡定律检验。单因素分析P<0.05的参数采用二分类多因素logistic回归分析法评价ACE基因多态性与SAH患者CVS的相关关系。P<0.05为差异有统计学意义。
2 结果 2.1 两组患者一般临床资料比较如表 1,本研究结果显示,CVS组患者年龄、性别、体重指数、高血压、糖尿病、吸烟、饮酒等指标与对照组比较,差异均无统计学意义(P>0.05);两组在发热、Hunt-Hess分级和Fisher分级三项指标上差异均具有统计学意义(P<0.05)。
| 项目 | CVS组(n=72) | 对照组(n=94) | t/χ2 | P |
| 年龄(岁) | 48.9±10.2 | 51.1±12.7 | 1.196 | 0.248 |
| 男性 | 42(58.3) | 55(58.5) | 0.001 | 0.982 |
| 体重指数(kg/m2) | 23.7±4.1 | 24.0±3.8 | 0.468 | 0.645 |
| 高血压 | 44(61.1) | 46(48.9) | 2.435 | 0.119 |
| 糖尿病 | 9(12.5) | 8(8.5) | 0.706 | 0.401 |
| 吸烟 | 28(38.9) | 30(31.9) | 0.872 | 0.350 |
| 饮酒 | 16(22.2) | 16(17.0) | 0.709 | 0.400 |
| 发热 | 16(22.2) | 7(7.4) | 7.457 | 0.006 |
| Hunt-Hess分级 | 6.855 | 0.009 | ||
| Ⅰ+Ⅱ | 50(69.4) | 81(86.2) | ||
| Ⅲ+Ⅳ+Ⅴ | 22(30.6) | 13(13.8) | ||
| Fisher分级 | 6.638 | 0.010 | ||
| Ⅰ+Ⅱ | 39(54.2) | 69(73.4) | ||
| Ⅲ+Ⅳ | 33(45.8) | 25(26.6) |
如表 2,CVS组患者入院时及入院第4、7、10、13天血清ACE水平均显著高于对照组,差异有统计学意义(P<0.05);但两组血清ACE水平随时间推移均无显著变化(P>0.05)。
| 组别 | 例数(n) | 入院时 | 第4天 | 第7天 | 第10天 | 第13天 | F | P |
| CVS组 | 72 | 295.5±48.4 | 296.5±50.3 | 291.0±47.6 | 288.0±53.2 | 293.9±50.4 | 0.357 | 0.845 |
| 对照组 | 94 | 279.8±45.8 | 279.4±49.2 | 275.1±47.2 | 269.2±51.8 | 277.8±46.8 | 0.774 | 0.546 |
| t | 2.136 | 2.196 | 2.142 | 2.297 | 2.129 | |||
| P | 0.048 | 0.042 | 0.047 | 0.035 | 0.048 |
如表 3,不同基因型患者入院时,及入院第4、7、10、13日血清ACE水平差异具有统计学意义(P<0.05);但每种基因型患者血清ACE水平随时间推移均无显著变化(P>0.05)。
| 组别 | 例数(n) | 入院时 | 第4天 | 第7天 | 第10天 | 第13天 | F | P |
| Ⅱ | 47 | 260.7±39.2 | 246.4±47.0 | 255.4±40.9 | 237.8±46.6 | 248.3±35.4 | 0.998 | 0.411 |
| ID | 70 | 286.4±45.1 | 293.0±48.4 | 281.5±50.7 | 278.7±53.0 | 286.7±48.6 | 0.872 | 0.482 |
| DD | 49 | 311.7±57.2 | 316.7±54.4 | 308.0±48.8 | 313.3±57.2 | 317.5±60.5 | 0.242 | 0.918 |
| F | 13.820 | 24.783 | 14.682 | 24.774 | 23.705 | |||
| P | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 |
ACE组和对照组比较,两组ACE基因I/D位点基因型和等位基因分布频率差异均具有统计学意义(P<0.05),见表 4。
| 基因型/等位基因 | CVS组(n=72) | 对照组(n=94) | χ2 | P |
| Ⅱ | 17(23.6) | 30(31.9) | 7.086 | 0.029 |
| ID | 26(36.1) | 44(46.8) | ||
| DD | 29(40.3) | 20(21.3) | ||
| Ⅰ | 60(41.7) | 104(55.3) | 6.080 | 0.014 |
| D | 84(58.3) | 84(44.7) |
如表 5,采用二分类多因素logistic回归法分析,结果显示对于自发性SAH患者,携带ACE基因I/D位点D等位基因是发生CVS的危险因素。
| 变量 | B | SE | Wals | OR | 95%CI | P |
| D等位基因 | 0.387 | 0.208 | 3.467 | 1.473 | (1.068~2.610) | 0.021 |
| 发热 | 0.223 | 0.320 | 0.486 | 1.250 | (1.014~4.115) | 0.035 |
| 高Hunt-Hess分级 | 0.632 | 0.462 | 1.873 | 1.882 | (1.234~3.035) | 0.011 |
| 高Fisher分级 | 0.515 | 0.368 | 1.960 | 1.674 | (1.166~3.310) | 0.017 |
本研究发现ACE基因I/D多态性与自发性SAH后CVS发生密切相关,携带D等位基因是CVS发生的危险因素,可显著增加CVS发病风险。
CVS的具体发生机制复杂,可能涉及炎症反应、血管舒张/收缩因子失衡、血管壁结构变化等多方面因素[6, 7]。
ACE是肾素-血管紧张素系统(renin-angiotensin system, RAS)的重要成员之一,有研究发现SAH患者脑脊液ACE水平显著增高,并与CVS发生具有一定时间相关性,表现为出血后脑脊液ACE水平逐渐增高,于1周时达到高峰,之后逐渐降至基线水平[4]。然而,SAH患者血清ACE水平动态变化过程目前研究尚无统一结论,多数研究结果显示SAH后血清ACE水平随时间无明显变化[8]。但王平等[9]研究发现SAH后血清AT Ⅱ水平立即开始逐渐增高,24 h达到高峰,1周时逐渐回落。本研究CVS和对照组血清ACE水平在发病13 d内与基线比较均无明显变化,但CVS组患者入院时基线血清ACE水平较对照组显著升高,提示SAH患者血清ACE水平可能与CVS存在一定相关性。
既往研究证实ACE基因I/D多态性与ACE生成及活性密切相关,DD基因型人群血清ACE水平最高,ID基因型次之,Ⅱ基因型最低[10],本研究结果与既往研究相符,携带DD基因型患者血清ACE水平在各时间点均为最高。同时,还有研究发现ACE基因I/D多态性与缺血性卒中和脑出血易感性相关[11, 12]。但是,目前关于ACE基因I/D多态性与SAH易感性研究相对较少,且结论不一,与SAH后CVS相关性研究更鲜有报道。本研究结果显示ACE基因I/D多态性与自发性SAH后CVS发生密切相关,DD基因型是CVS发生的危险因素,可显著增加CVS发病风险。该结果间接说明了CVS组患者血清ACE水平较对照组明显升高的原因。另外,多因素分析结果还显示发热、高Hunt-Hess等级和高Fisher等级与SAH患者发生CVS密切相关,提示对于合并发热、高Hunt-Hess等级和高Fisher等级的自发性SAH患者,更加需要仔细评估其发生CVS的可能性,及时予以相关处理,选择更合适的治疗方案。
最后,需指出,一方面,本研究尚存在诸多不足,本研究纳入样本量较小,其结果期待多中心大样本研究证据进一步验证; 另一方面,CVS发病机制十分复杂,不仅与局部复杂多变病理生理状况相关,还可能是多基因共同表达的结果,ACE基因多态性与其他因素、其他基因相互作用的具体机制有待进一步研究。
| [1] |
Pepa GMD, Scerrati A, Albanese A, et al. Protective effect of external ventricular drainage on cerebral vasospasm. A retrospective study on aneurysmal SAH treated endovascularly[J]. Clin Neurol Neurosurg, 2014, 124: 97-101. DOI:10.1016/j.clineuro.2014.06.030 |
| [2] |
Wu L, Chen G. Signaling Pathway in Cerebral Vasospasm After Subarachnoid Hemorrhage:News Update[J]. Acta Neurochir Suppl, 2016, 121: 161-165. |
| [3] |
李泽, 张志银, 刘志刚, 等. 运动诱发电位对脑动脉瘤蛛网膜下腔出血后迟发性脑血管痉挛的诊断性意义分析[J]. 国际神经病学神经外科学杂志, 2017, 44(6): 611-615. |
| [4] |
庞刚, 肖泉, 曾敬初, 等. 蛛网膜下腔出血后脑脊液血管紧张素转换酶的变化[J]. 广西医学, 2001, 23(6): 1323-1325. DOI:10.3969/j.issn.0253-4304.2001.06.001 |
| [5] |
Griessenauer CJ, Tubbs RS, Foreman PM, et al. Association of renin-angiotensin system genetic polymorphisms and aneurysmal subarachnoid hemorrhage[J]. J Neurosurg, 2018, 128(1): 86-93. DOI:10.3171/2016.9.JNS161593 |
| [6] |
Boulouis G, Labeyrie MA, Raymond J, et al. Treatment of cerebral vasospasm following aneurysmal subarachnoid haemorrhage:a systematic review and meta-analysis[J]. Eur Radiol, 2017, 27(8): 3333-3342. DOI:10.1007/s00330-016-4702-y |
| [7] |
邹长林. 炎症在蛛网膜下腔出血中的作用及机制研究进展[J]. 国际神经病学神经外科学杂志, 2017, 44(1): 83-86. |
| [8] |
肖泉, 唐秀文, 庞刚, 等. 蛛网膜下腔出血后脑血管痉挛与血管活性物质的关系[J]. 中国现代神经疾病杂志, 2002, 2(5): 292-294. DOI:10.3969/j.issn.1672-6731.2002.05.008 |
| [9] |
王平. 蛛网膜下腔出血后患者脑血管痉挛与血浆内皮素血管紧张素及一氧化氮变化的相关性分析[J]. 中国实用神经疾病杂志, 2014(16): 24-25. |
| [10] |
Das S, Roy S, Sharma V, et al. Association of ACE gene I/D polymorphism and ACE levels with hemorrhagic stroke:comparison with ischemic stroke[J]. Neurol Sci, 2015, 36(1): 137-142. DOI:10.1007/s10072-014-1880-8 |
| [11] |
Zhao J, Qin X, Li S, et al. Association between the ACE I/D polymorphism and risk of ischemic stroke:an updated meta-analysis of 47, 026 subjects from 105 case-control studies[J]. J Neurol Sci, 2014, 345(1-2): 37-47. DOI:10.1016/j.jns.2014.07.023 |
| [12] |
Malueka RG, Dwianingsih EK, Sutarni S, et al. The D allele of the angiotensin-converting enzyme (ACE) insertion/deletion (I/D) polymorphism is associated with worse functional outcome of ischaemic stroke[J]. Int J Neurosci, 2018, 128(8): 697-704. DOI:10.1080/00207454.2017.1412962 |
 2019, Vol. 46
2019, Vol. 46




