扩展功能
文章信息
- 李朝阳, 赵之晗, 冯国栋, 杜芳, 王静, 张红鸭, 杨毅宁, 代文, 刘婷婷, 贺莹, 周慧敏, 边婷, 安星月, 蔡铮, 赵钢
- LI Chao-Yang, ZHAO Zhi-Han, FENG Guo-Dong, DU Fang, WANG Jing, ZHANG Hong-Ya, YANG Yi-Ning, DAI Wen, LIU Ting-Ting, HE Ying, ZHOU Hui-Min, BIAN Ting, AN Xing-Yue, CAI Zheng, ZHAO Gang
- 结核性脑膜炎和疱疹病毒脑膜脑炎脑脊液细胞学检查的特点分析
- Cytological features of cerebrospinal fluid in tuberculous meningitis and herpes virus meningoencephalitis
- 国际神经病学神经外科学杂志, 2018, 45(6): 551-555
- Journal of International Neurology and Neurosurgery, 2018, 45(6): 551-555
-
文章历史
收稿日期: 2018-07-24
修回日期: 2018-10-23
2. 复旦大学附属中山医院神经内科, 上海市 200032;
3. 中国人民解放军第四五一医院神经内科, 陕西省西安市 710054
结核性脑膜炎(tuberculous meningitis, TBM)和疱疹病毒脑膜脑炎(herpes viral meningoencephalitis, HVME)是常见的中枢神经系统感染性疾病,都具有病原检出率低、病情危重和死亡率高的特点[1-3]。部分TBM患者临床表现、脑脊液生化和影像学检查不仅不典型,且与HVME具有相似性,导致两者的早期鉴别诊断十分困难。中枢神经系统感染时,脑脊液细胞的数量和类型都会发生变化,而这些变化可以通过脑脊液细胞学检查得到反映。本文对西京医院神经内科经下一代基因测序(next-generation sequencing, NGS)技术确诊的28例TBM和27例HVME患者进行了脑脊液细胞学检查及动态观察,以期通过分析两者脑脊液细胞学特点,为临床提供辅助诊断依据。
1 对象与方法 1.1 研究对象 1.1.1 结核性脑膜炎组(TBM组)TBM组共28例,其中男12例,女16例;年龄3~82岁,平均年龄32岁。全部病例具有头痛、易激惹、呕吐、发热、颈项强直、抽搐、局灶性神经缺损或意识障碍等临床表现,符合结核性脑膜炎诊断标准[4]。脑脊液NGS均检出结核分枝杆菌DNA片段,脑脊液改良抗酸染色[5, 6]均为阳性。经脑脊液结核分枝杆菌培养证实9例,Gene-Xpert证实19例。患者首次脑脊液标本采自发病后的2~28 d,此前均未进行抗结核治疗,其中病程3 d以内(3天组)患者7例。脑脊液外观无色透明(无色透明组)19例,非无色透明(非无色透明组)9例(其中黄色透明或混浊7例,无色微混1例,淡红混浊1例)。有15例患者进行了脑脊液细胞学动态观察(7例2次,4例3次,2例4次,1例5次,1例7次),标本采集间隔时间为3~255 d,其中首次腰穿与第二次腰穿间隔时间为3~35 d。15例动态观察患者中有4例死亡,其中首次腰穿脑脊液无色透明3例。24例经抗结核治疗好转(未死亡组),4例无效死亡(死亡组)。
1.1.2 疱疹病毒脑膜脑炎组(HVME组)HVME组共27例,男17例,女10例,年龄22~78岁,平均年龄43岁。全部病例具有头痛、发热、颈项强直、意识障碍、认知障碍或癫痫发作等脑膜脑炎临床表现[7],脑脊液NGS均检出疱疹病毒DNA片段,并经PCR证实。其中单纯疱疹病毒1型6例,单纯疱疹病毒2型4例,水痘﹣带状疱疹病毒10例,EB病毒4例,人类巨细胞病毒1例,人类疱疹病毒7型1例,猪疱疹病毒1例。患者首次脑脊液标本采自发病后的2~7 d,此前均未进行抗病毒治疗,其中病程3 d以内(3天组)患者8例。脑脊液无色透明26例,红色混浊1例。有17例患者进行了脑脊液细胞学动态观察(8例2次,6例3次,3例4次),标本采集间隔时间为3~10 d,其中首次腰穿与第二次腰穿间隔时间为3~7 d。所有病例均好转出院。
1.2 方法脑脊液细胞学检查采用粟氏玻片离心沉淀法[8]。脑脊液标本送检后,先行白细胞计数;再取新鲜脑脊液0.5 ml,加入粟氏细胞涂片离心沉淀器,500~800转/min,离心3~5 min;待脑脊液的有形成分全部沉淀在玻片上后,取下玻片进行May-Grunwald-Giemsa (MGG)染色。光学显微镜10×100倍下进行细胞学分类计数。
1.3 统计学方法采用SPSS 24.0软件对数据进行统计分析。对于偏态分布或者方差不齐的数据,使用中位数和四分位数间距[M(P25, P75)]进行集中和离散程度描述,采用非参数检验(Mann-Whitney U检验)进行统计学分析;正态分布和方差齐性的数据用均数±标准差(x±s)进行集中和离散程度描述,采用两独立样本t检验进行统计学分析。检验水准为双侧α=0.05,P < 0.05表示差异具有统计学意义。
2 结果 2.1 首次腰穿结果TBM组嗜中性粒细胞比例显著高于HVME组(P < 0.01),HVME组小淋巴细胞比例显著高于TBM组(P < 0.01);3天组嗜中性粒细胞和小淋巴细胞比例两组间差异均无统计学意义(均P>0.05)。HVME组有6例查见红细胞和/或含铁血黄素吞噬细胞(吞噬细胞),并与TBM组有显著差异(P < 0.01);其中单纯疱疹病毒1型1例,水痘﹣带状疱疹病毒1例,EB病毒2例,人类巨细胞病毒1例,猪疱疹病毒1例。HVME组有2例患者查见细胞内包涵体,其中单纯疱疹病毒1型1例,人类巨细胞病毒1例。脑脊液白细胞计数、单核细胞、大淋巴细胞、大淋巴样细胞、嗜酸性粒细胞、嗜碱性粒细胞和有丝分裂细胞比例两组间均无明显差异(均P>0.05)。见表 1、表 2。
| 指标 | TBM组(n=28) | HVME组(n=27) | t/z | P |
| 白细胞(×106/L) | 152.00(93.75, 330.00) | 172.00(63.50, 275.00) | 0.41 | 0.68 |
| 大淋巴细胞(%) | 0.05 ± 0.21 | 0.07 ± 0.23 | 0.12 | 0.73 |
| 小淋巴细胞(%) | 51.93 ± 31.11 | 79.31 ± 22.65 | 14.22 | < 0.01 |
| 单核细胞(%) | 7.79 ± 4.39 | 13.07 ± 10.69 | 3.00 | 0.09 |
| 嗜中性粒细胞(%) | 39.52 ± 31.40 | 6.17 ± 17.96 | 23.15 | < 0.01 |
| 浆细胞(%) | 0.55 ± 0.52 | 0.43 ± 0.38 | 1.01 | 0.30 |
| 大淋巴样细胞(%) | 0.02 ± 0.09 | 0.15 ± 0.33 | 0.86 | 0.39 |
| 嗜酸性粒细胞(%) | 0.02 ± 0.09 | 0.25 ± 0.80 | 1.79 | 0.07 |
| 嗜碱性粒细胞(%) | 0.03 ± 0.13 | 0.17 ± 0.44 | 1.31 | 0.19 |
| 吞噬细胞(%) | 0.00 ± 0.00 | 0.25 ± 0.54 | 3.66 | < 0.01 |
| 有丝分裂细胞(%) | 0.09 ± 0.20 | 0.13 ± 0.22 | 0.72 | 0.48 |
| 注:除白细胞以[M(P25, P75)]表示外,其余指标以(x±s)表示。 | ||||
| 指标 | TBM 3天组(n=7) | HVME 3天组(n=8) | t/z | P |
| 白细胞(×106/L) | 483.00(307.00, 680.50) | 429.00(209.50, 616.00) | 0.69 | 0.49 |
| 大淋巴细胞(%) | 0.21 ± 0.39 | 0.13 ± 0.23 | 0.30 | 0.76 |
| 小淋巴细胞(%) | 48.79 ± 36.15 | 60.19 ± 32.13 | 0.70 | 0.48 |
| 单核细胞(%) | 15.28 ± 5.17 | 18.59 ± 9.32 | 0.81 | 0.42 |
| 嗜中性粒细胞(%) | 34.73 ± 30.18 | 20.08 ± 29.73 | 1.10 | 0.27 |
| 浆细胞(%) | 0.71 ± 0.81 | 0.44 ± 0.50 | 0.86 | 0.39 |
| 大淋巴样细胞(%) | 0.07 ± 0.19 | 0.06 ± 0.18 | 0.10 | 0.92 |
| 嗜酸性粒细胞(%) | 0.07 ± 0.19 | 0.06 ± 0.18 | 0.10 | 0.92 |
| 嗜碱性粒细胞(%) | 0.07 ± 0.19 | 0.13 ± 0.23 | 0.50 | 0.62 |
| 吞噬细胞(%) | 0.00 ± 0.00 | 0.19 ± 0.37 | 1.37 | 0.17 |
| 有丝分裂细胞(%) | 0.07 ± 0.19 | 0.13 ± 0.23 | 0.50 | 0.62 |
| 注:除白细胞以[M(P25, P75)]表示外,其余指标以(x±s)表示。 | ||||
TBM死亡组脑脊液白细胞计数和嗜中性粒细胞比例均高于未死亡组,小淋巴细胞比例则低于未死亡组,但均无统计学差异(均P>0.05,见表 3)。TBM非无色透明组脑脊液白细胞计数和嗜中性粒细胞比例均显著高于无色透明组(均P < 0.01,见表 4)。
| 指标 | 未死亡组(n=24) | 死亡组(n=4) | t/z | P |
| 白细胞(×106/L) | 140.00(90.00, 278.50) | 393.50(290.25, 538.50) | 0.96 | 0.34 |
| 嗜中性粒细胞(%) | 36.61±32.15 | 57.00±21.82 | 1.43 | 0.24 |
| 注:白细胞以[M(P25, P75)]表示,嗜中性粒细胞以(x±s)表示。 | ||||
| 指标 | 无色透明组(n=19) | 非无色透明组(n=9) | t/z | P |
| 白细胞(×106/L) | 140.00(73.50, 198.00) | 678.00(265.00, 917.00) | 2.98 | < 0.01 |
| 嗜中性粒细胞(%) | 27.26±24.39 | 65.40±29.67 | 3.61 | < 0.01 |
| 注:白细胞以[M(P25, P75)]表示,嗜中性粒细胞以(x±s)表示。 | ||||
TBM组:经过抗结核治疗,有6例患者脑脊液白细胞计数和嗜中性粒细胞比例下降,其中3例随着病情反复脑脊液白细胞计数和嗜中性粒细胞比例再次升高。5例患者脑脊液白细胞计数和嗜中性粒细胞比例先升高,后下降,其中1例病情反复2次。4例死亡患者,3例脑脊液白细胞计数和嗜中性粒细胞比例升高,1例无变化;第二次腰穿脑脊液为非无色透明者3例,其中2例由无色透明转变为非无色透明。
HVME组:经过抗病毒治疗,有15例患者脑脊液白细胞计数和嗜中性粒细胞比例下降;2例在白细胞计数升高的同时,嗜中性粒细胞比例下降。
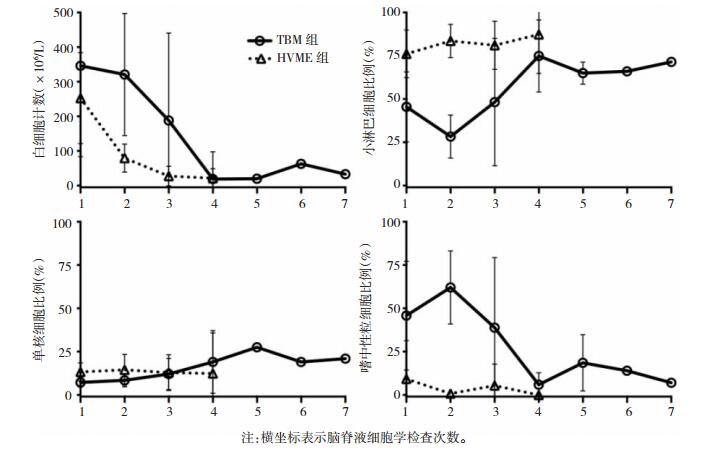
治疗后的TBM组脑脊液白细胞计数和嗜中性粒细胞比例下降及小淋巴细胞比例上升的速度较HVME组缓慢,且呈波动性。见图 1。
|
| 图 1 TBM组和HVME组脑脊液细胞学动态观察 |
脑脊液结核分枝杆菌和病毒培养阳性是诊断TBM和HVME的金标准,但两者的阳性率都只有5%左右[5, 6]。脑脊液Gene-Xpert和改良抗酸染色的阳性检出率,常受到细菌数量多少的影响,且分枝杆菌属和部分其他细菌也皆可呈抗酸染色阳性[9, 10]。NGS技术具有高灵敏度、高准确性和高通量等优点,在检测未知病原体和对已知病原体分型方面具有独特的优势[11],为中枢神经系统感染早期精准诊断提供了病原学依据。但目前NGS技术在检测RNA病毒方面仍面临诸多问题[12],且高成本使其不能作为常规检查开展。脑脊液细胞学是诊断神经系统疾病的重要检查手段之一,具有快速、简便、准确和成本低的优点,可为临床辅助诊断提供帮助。
本研究TBM组嗜中性粒细胞比例显著高于HVME组,而小淋巴细胞比例显著低于HVME组,表明两组脑脊液细胞反应类型不同,TBM表现为混合型细胞反应,HVME则以淋巴细胞反应为主。部分HVME患者也可出现嗜中性粒细胞比例增高,但持续时间较短,多在发病后数小时~72 h下降[13]。本研究中3天组嗜中性粒细胞和小淋巴细胞比例在TBM组和HVME组中均无差异,表明在病程早期,两组脑脊液细胞学特点具有相似性,均表现为嗜中性粒细胞反应[14]。
TBM组(32.14%, 9/28)首次腰穿非无色透明脑脊液比率高于HVME组(3.7%, 1/27),表明未经治疗TBM患者较HVME患者的脑脊液更易出现非无色透明改变。TBM非无色透明组脑脊液白细胞计数和嗜中性粒细胞比例均显著高于无色透明组,提示脑脊液外观性状的改变与细胞反应有关。本文TBM组4例死亡患者,脑脊液白细胞计数和嗜中性粒细胞比例均高于未死亡患者,提示两者上升幅度的大小与患者病情轻重程度相关。TBM死亡组首次腰穿有3例脑脊液为无色透明,其中2例随后转变为非无色透明,提示脑脊液外观性状的改变是病情变化的标志之一。
既往认为并发出血的脑炎或脑膜炎多由单纯疱疹病毒感染引起,但本研究中HVME组经NGS分型后,在单纯疱疹病毒1型、水痘﹣带状疱疹病毒、EB病毒、人类巨细胞病毒和猪疱疹病毒感染病例中均查见吞噬细胞,表明其他类型疱疹病毒感染也可引起出血。HVME组查见吞噬细胞的6例患者中,有5例脑脊液为无色透明,说明在并发颅内出血时,脑脊液细胞学检查在脑脊液无色透明性状发生改变前即可帮助确诊。本文在2例HVME患者中查见细胞内包涵体,而包涵体是疱疹病毒感染的特征性表现之一,对于疱疹病毒感染具有诊断意义[13]。
本研究的动态观察发现,当病情好转或反复时,脑脊液白细胞计数和细胞学分类也随之发生相应改变。治疗后的TBM组脑脊液白细胞计数和嗜中性粒细胞比例下降速度、小淋巴细胞比例上升速度均较HVME组缓慢,且呈波动性,表明了TBM病程长于HVME,并易因疗效不佳或耐药而出现病情反复。
本研究结果表明,TBM和HVME脑脊液细胞学特点不仅可以为临床辅助诊断提供帮助,还可作为病情观察、疗效判定和预后评估的客观指标,具有十分重要的临床意义。
| [1] |
McGill F, Griffiths MJ, Solomon T. Viral meningitis:current issues in diagnosis and treatment[J]. Curr Opin Infect Dis, 2017, 30(2): 248-256. |
| [2] |
Kennedy PGE, Quan PL, Lipkin WI. Viral Encephalitis of Unknown Cause:Current Perspective and Recent Advances[J]. Viruses, 2017, 9(6): 138-146. DOI:10.3390/v9060138 |
| [3] |
Wilkinson RJ, Rohlwink U, Misra UK, et al. Tuberculous meningitis[J]. Nat Rev Neurol, 2017, 13(10): 581-598. DOI:10.1038/nrneurol.2017.120 |
| [4] |
Marais S, Thwaites G, Schoeman JF, et al. Tuberculous meningitis:a uniform case definition for use in clinical research[J]. Lancet Infect Dis, 2010, 10(11): 803-812. DOI:10.1016/S1473-3099(10)70138-9 |
| [5] |
Feng GD, Shi M, Ma L, et al. Diagnostic accuracy of intracellular mycobacterium tuberculosis detection for tuberculous meningitis[J]. Am J Respir Crit Care Med, 2014, 189(4): 475-481. DOI:10.1164/rccm.201309-1686OC |
| [6] |
Chen P, Shi M, Feng GD, et al. A highly efficient Ziehl-Neelsen stain:identifying de novo intracellular Mycobacterium tuberculosis and improving detection of extracellular M. tuberculosis in cerebrospinal fluid[J]. J Clin Microbiol, 2012, 50(4): 1166-1170. DOI:10.1128/JCM.05756-11 |
| [7] |
Steiner I, Budka H, Chaudhuri A, et al. Viral meningoencephalitis:a review of diagnostic methods and guidelines for management[J]. Eur J Neurol, 2010, 17(8): 999-1009. DOI:10.1111/j.1468-1331.2010.02970.x |
| [8] |
粟秀初, 楼玉珍. 脑脊液细胞玻片离心沉淀仪的改进及其使用价值[J]. 神经精神疾病杂志, 1981, 7(4): 256-260. |
| [9] |
Li H, Turhan V, Chokhani L, et al. Identification and differentiation of clinically relevant mycobacterium species directly from acid-fast bacillus-positive culture broth[J]. J Clin Microbiol, 2009, 47(12): 3814-3820. DOI:10.1128/JCM.01534-09 |
| [10] |
McHugh KE, Sturgis CD, Procop GW, et al. The cytopathology of Actinomyces, Nocardia, and their mimickers[J]. Diagn Cytopathol, 2017, 45(12): 1105-1115. DOI:10.1002/dc.v45.12 |
| [11] |
Wilson MR, Naccache SN, Samayoa E, et al. Actionable diagnosis of neuroleptospirosis by next-generation sequencing[J]. N Engl J Med, 2014, 370(25): 2408-2417. DOI:10.1056/NEJMoa1401268 |
| [12] |
Chen G, Qiu Y, Zhuang Q, et al. Next-generation sequencing library preparation method for identification of RNA viruses on the Ion Torrent Sequencing Platform[J]. Virus Genes, 2018, 54(4): 536-542. |
| [13] |
粟秀初, 孔繁元. 神经系统脑脊液细胞学. 北京: 人民军医出版社, 2001: 65-66.
|
| [14] |
杨毅宁.脑脊液细胞学检查的临床应用[J]. 2017, 40(12): 916-919.
|
 2018, Vol. 45
2018, Vol. 45




