扩展功能
文章信息
- 罗龙, 杨晓苏
- LUO Long, YANG Xiao-Su
- 易误诊为病毒性脑炎的成人抗N-甲基-D-天门冬氨酸受体脑炎(附16例临床分析)
- Adult anti-N-methyl-D-aspartic acid receptor encephalitis easily misdiagnosed as viral encephalitis: a clinical analysis of 16 cases
- 国际神经病学神经外科学杂志, 2017, 44(3): 289-293
- Journal of International Neurology and Neurosurgery, 2017, 44(3): 289-293
-
文章历史
收稿日期: 2017-01-16
修回日期: 2017-05-04
抗NMDA受体脑炎是自身免疫性脑炎的一种,2007年由Dalmau等[1]首次在“脑炎”患者脑脊液中检测出抗NMDA抗体而命名,2010年国内首次报道抗NMDAR脑炎[2]。随着对该病的关注,发现的病例逐渐增多,现将我院自2014年12月至2016年6月收治的16例成人抗NMDA受体脑炎病例报道如下,并结合文献进行分析。
1 临床资料 1.1 一般资料及临床表现本组16例患者,男性9例,女性7例,年龄18~52岁,平均(30±13.84) 岁;平均病程(52±17.96) d。其一般信息及临床表现如下表。
| 病例序号 | 性别 | 年龄(岁) | 病程(d) | 前驱症状 | 首发症状 | 主要临床表现 | ||||
| 精神行为异常 | 癫痫发作 | 不自主运动 | 自主神经功能障碍 | 其他 | ||||||
| 1 | 男 | 18 | 63 | - | 癫痫 | - | + | - | - | |
| 2 | 男 | 21 | 31 | - | 癫痫 | - | + | - | - | |
| 3 | 女 | 20 | 53 | 呼吸道感染 | 精神行为异常 | + | - | +# | 低热、出汗 | 低通气障碍 |
| 4 | 男 | 46 | 76 | - | 精神行为异常 | + | - | + | - | |
| 5 | 女 | 27 | 39 | - | 精神行为异常 | + | - | - | 低热、出汗 | |
| 6 | 男 | 22 | 84 | - | 癫痫 | - | + | - | 低热、出汗 | 低通气障碍 |
| 7 | 男 | 20 | 42 | 呼吸道感染 | 精神行为异常 | + | +* | - | - | |
| 8 | 男 | 19 | 49 | 消化道感染 | 精神行为异常 | + | - | - | 低热、出汗、心动过速 | |
| 9 | 女 | 52 | 35 | - | 精神行为异常 | + | + | + | - | |
| 10 | 女 | 21 | 37 | - | 精神行为异常 | + | - | - | - | |
| 11 | 男 | 22 | 39 | - | 癫痫 | - | +* | - | 低热、出汗 | |
| 12 | 男 | 18 | 56 | - | 癫痫 | + | + | - | 出汗 | |
| 13 | 女 | 42 | 46 | 呼吸道感染 | 精神行为异常 | + | - | + | 低热、出汗 | |
| 14 | 女 | 44 | 52 | - | 精神行为异常 | + | - | - | - | |
| 15 | 男 | 50 | 50 | - | 癫痫 | - | +* | - | - | |
| 16 | 女 | 38 | 81 | - | 癫痫 | - | + | +# | 出汗 | 低通气障碍 |
| 注:*为同时有癫痫持续状态;3为仅有肢体不自主运动,不伴面部不自主运动。 | ||||||||||
血白细胞增高10例,中性粒细胞显著增高4例。血沉加快5例,C-反应蛋白升高7例。肌酸激酶增高6例。11例患者血清NMDA受体抗体阳性。见表 2。
| 病例序号 | 白细胞 | 中性粒细胞 | 血沉 | 肌酸激酶 | 头部MRI | 脑电图 | 是否合并畸胎瘤 |
| 1 | ↑ | - | - | ↑ | - | 轻中度异常 | - |
| 2 | - | - | - | ↑ | + | 重度异常 | - |
| 3 | ↑ | ↑ | ↑ | - | + | - | - |
| 4 | ↑ | - | - | - | - | 中度异常 | - |
| 5 | ↑ | - | - | - | + | - | - |
| 6 | - | - | - | - | - | 中度异常 | - |
| 7 | ↑ | ↑ | ↑ | - | - | 重度异常 | - |
| 8 | ↑ | ↑ | ↑ | ↑ | + | 轻度异常 | - |
| 9 | - | - | - | - | + | - | - |
| 10 | - | - | - | - | + | 轻中度异常 | - |
| 11 | ↑ | - | ↑ | ↑ | - | 重度异常 | - |
| 12 | - | - | - | ↑ | + | 轻度异常 | - |
| 13 | ↑ | ↑ | ↑ | - | - | - | - |
| 14 | ↑ | - | - | - | + | 轻中度异常 | - |
| 15 | ↑ | - | - | ↑ | - | 中度异常 | - |
| 16 | - | - | - | - | - | 重度异常 | + |
所有16例患者均进行了一次以上腰穿。5例CSF初压大于180 mmH2O,11例初压正常。4例CSF白细胞增加分别为12×106/L~80×106/L。糖均正常,4例氯增高,4例蛋白轻度增加(0.54~0.92) g/L。全部患者脑脊NMDA受体抗体阳性。见表 3。
| 病例序号 | 压力(mmH2O) | 白细胞数(×106/L) | 蛋白(g/L) | 葡萄糖 | 氯化物 | 病毒学(CSF) | 病毒学(血) | 抗NMDA抗体(CSF) | 抗NMDA抗体(血) |
| 1 | 正常 | 正常 | 正常 | 正常 | - | - | - | + | + |
| 2 | 正常 | 正常 | 正常 | 正常 | - | - | - | + | + |
| 3 | 正常 | 正常 | 正常 | 正常 | ↑ | - | 呼吸道合胞病毒IgM | + | + |
| 4 | 正常 | 12 | 0.54 | 正常 | - | - | 呼吸道合胞病毒IgM | + | + |
| 5 | 220 | 正常 | 正常 | 正常 | - | - | - | + | - |
| 6 | 正常 | 正常 | 正常 | 正常 | ↑ | - | - | + | - |
| 7 | 320 | 80 | 0.74 | 正常 | - | - | - | + | + |
| 8 | 正常 | 正常 | 正常 | 正常 | - | - | 腺病毒IgM | + | + |
| 9 | 275 | 正常 | 正常 | 正常 | - | - | - | + | + |
| 10 | 正常 | 正常 | 正常 | 正常 | ↑ | - | - | + | - |
| 11 | 正常 | 18 | 0.90 | 正常 | - | - | 单纯疱疹病毒1抗体IgM | + | + |
| 12 | 正常 | 正常 | 正常 | 正常 | - | - | - | + | - |
| 13 | 360 | 13 | 0.92 | 正常 | - | - | 呼吸道合胞病毒IgM | + | + |
| 14 | 正常 | 正常 | 正常 | 正常 | ↑ | - | - | + | + |
| 15 | 正常 | 正常 | 正常 | 正常 | - | - | - | + | - |
| 16 | 190 | 正常 | 正常 | 正常 | - | - | - | + | + |
本组患者均行头部MRI检查。其中8例未见明显异常;8例见异常信号灶,病灶多见于额、颞叶、脑干,1例位于延髓、脑桥、双侧额颞叶、左侧岛叶、右枕叶,多发片状异常信号灶;1例位于右侧额叶、左侧基底节、中脑右侧份及延髓,多发小片状异常信号灶;4例额颞叶异常信号灶;1例颅内多发异常信号并多发脑膜异常强化;1例右侧海马异常信号。见表 2。
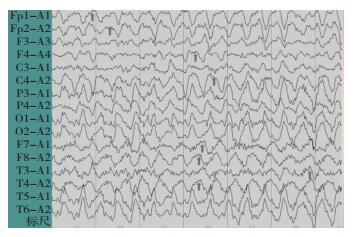
全部患者均行脑电图检查,4例患者无异常,3例轻度异常,2例轻-中度异常,3例中度异常,4例重度异常,其中1例出现δ刷。4例重度异常者表现为:基本节律差,发作期及发作间期见普遍较多δ波为主慢波及痫性波,部位可以一侧额区或颞区为主,也可双侧同时广泛受累,未见以顶枕区异常波单独出现者。见表 2、图 1。
|
| 图 1 1例38岁的女性患者,双侧各导联可见广泛的δ刷(箭头所示)。 |
本组病例中,有5例在确诊前曾诊断为病毒性脑炎,抗病毒治疗无效,后改用免疫治疗才改善,所有病例从发病至确诊平均时间为(17±4.26) d。本组16例患者均接受了免疫治疗,4例仅用激素治疗,3例仅用免疫球蛋白治疗,8例使用激素加免疫球蛋白联合治疗,1例使用激素联合淋巴细胞血浆置换治疗。激素治疗的13例为甲泼尼龙500~1000 mg/d静脉输注,连续治疗3~5 d,然后逐渐减量。免疫球蛋白用量为0.4g /kg/d,5 d为一疗程,剂量及疗程视临床情况调整。除上述治疗外,根据患者病情,分别加用了控制癫痫发作及精神症状的对症支持治疗。1例合并畸胎瘤的女性患者予外科手术切除。11例出院时基本恢复正常;5例存在不同程度的功能障碍,3例有认知功能障碍及精神症状,2例有运动障碍或癫痫发作。电话随访1~18个月,16例随访患者中12例完全恢复,4例遗留不同程度的后遗症,包括1例间断癫痫发作,2例言语功能障碍和肢体活动障碍(其中1例出院5月后复发,表现为说话减少、双下肢无力且不灵活,血及脑脊液NMDA抗体阳性。),1例有精神症状,表现为言语错乱,有攻击行为。
2 讨论NMDA受体脑炎的病因和发病机制复杂,仍不十分清楚,既往认为与肿瘤相关,目前认为系各种病因诱发了抗NMDAR抗体,后者攻击NMDAR而发病[3]。该病可见于任何年龄,好发年轻成人、青少年、儿童,女性多于男性,最常合并卵巢畸胎瘤[4]。其典型的临床症状是精神行为异常、癫痫、意识障碍、中枢性通气不足及自主神经紊乱。有学者[5-7]将其临床表现分为5期:① 前驱期:早期多为非特异前驱症状。本组16例患者4例有发热、头痛前驱史。② 精神症状/癫痫发作期:主要表现为精神行为异常、癫痫发作。本组16例患者9例以精神行为异常为首发症状,7例以癫痫为首发症状,精神行为异常表现为幻觉、做事丢三落四、不能自行回家、胡言乱语、答非所问、自唱、自舞,攻击他人,7例癫痫均是全面强直阵挛发作。③ 无应答期:常表现为口头语言减少和模仿语言、抵制睁眼、对疼痛刺激无反应。本组有患者表现为言语减少、缄默不语。④ 运动过多期:主要表现为不自主运动和自主神经功能紊乱,不自主运动可表现为口舌面及肢体局部或全身的异常运动,异常运动被认为是该病的特征性表现。本组表现为口舌面和(或)肢体不自主运动5例、泌涎增多2例、出汗增多8例、低热6例、心动过速1例。⑤ 恢复期。
本病的脑脊液压力、细胞数改变、蛋白水平无特异性,可出现寡克隆带,确诊该病的依据是脑脊液NMDAR抗体(+)[8],且抗体滴度与患者结局密切关联[9]。MRI可正常,也可表现为额颞叶、边缘系统、基底核、小脑和脑干等处出现异常信号。脑电图常出现局灶性或弥漫性慢波或节律失常,痫样放电或δ刷,δ刷被认为具有特异性[10],常与持续性癫痫相伴随[11],本组1例患者出现δ刷。
抗NMDAR脑炎目前尚无统一的诊断标准。Graus等[12]于2016年提出抗NMDAR脑炎的诊断标准,指出同时满足以下3项标准可拟诊为抗NMDAR脑炎:⒈快速起病(病程 < 3个月),临床表现具备其中6项主要症状中的至少4项,如伴发畸胎瘤则只需满足6项主要症状中的至少3项:① 异常行为(精神症状)或认知功能障碍;② 语言功能障碍(连续的无法被打断的强制语言、言语减少、缄默);③ 癫痫发作;④ 运动障碍、异动症或肌强直/异常姿势;⑤ 意识水平下降;⑥ 自主神经功能障碍或中枢通气不足。⒉至少有其中一项检查的异常发现:① 异常脑电图(局灶性或弥漫性慢波或节律失常、痫样放电或异常δ刷);② 脑脊液细胞数增多或出现寡克隆带。⒊可排除其他可能的病因。同时满足以下3项标准可确诊为抗NMDAR脑炎:(1) 临床表现出现上述⒈中6项症状中的1项或多项;(2) 抗NMDAR(GluN1亚基)IgG抗体阳性(抗体检测应包括脑脊液,如仅有血清样本,血清检测抗体阳性后需再做验证检测方可认为自身抗体结果阳性);(3) 合理的排除其他病因。由于本病早期临床表现与病毒性脑炎相似,故病初常被误诊为病毒性脑炎,但抗病毒治疗无好转,结合典型临床表现、特异性抗体检测、畸胎瘤的发现及治疗转归,可相鉴别。
另外,病毒感染与抗NMDA脑炎的关系至今仍不明确。众所周知,遗传和环境因素可触发自身免疫反应[13],感染导致自身免疫性疾病首次提出已超过了100年。事实上,许多自身免疫性脱髓鞘疾病可能由感染引发的[14],包括多发性硬化、急性播散性脑脊髓膜炎和视神经脊髓炎等。感染打破中枢神经系统免疫耐受的机制是多方面的,包括分子模拟、抗原的表达改变、选择性剪接、翻译后修饰、蛋白质错误折叠、隐性神经抗原暴露、抗原表位扩展、免疫失调等[15, 16]。在感染致抗NMDAR脑炎的报道中,目前发现的感染源包括单纯疱疹病毒、水痘带状疱疹病毒、腮腺炎病毒、肠道病毒、肺炎支原体[17]。但是,感染致抗NMDAR脑炎的机理仍待研究。有研究认为病原抗体结合到GluN1明显增加NMDAR通道的开放时间[18],随着时间的推移,受体交联和内化导致NMDAR减少,同时伴有电流的减少[19],病原抗体消除后,NMDA受体的内化和临床症状可恢复[20]。本组5例血清病毒检测阳性的患者,抗病毒治疗后无好转或病情稳定后又再次复发加重,使用免疫治疗后才好转。
有研究认为单纯疱疹性脑炎(herpes simplex encephalitis, HSE)后抗NMDAR脑炎比经典的抗NMDAR脑炎具有更强的抗原性[21],HSE可以触发多种中枢神经系统自身免疫性疾病。有文献报道HSE感染后,同时合并有多巴胺2受体抗体(D2R)和抗NMDAR抗体阳性[22]。其他中枢神经系统感染也可能类似于HSE触发抗NMDAR脑炎。因此,当有病毒感染,特别是HSE时,有必要行NMDAR抗体检测。
由于该病与免疫相关,因此诊断后建议立即开始一线免疫治疗[23],包括糖皮质激素、丙种球蛋白、血浆置换,单药疗效不佳时建议联合用药或换用其它药物[24]。有研究表明[4]一线免疫治疗和(或)肿瘤切除4周后只有53%患者症状改善。一线治疗未改善的患者,接受二线免疫治疗,如利妥昔单抗、环磷酰胺,或长程免疫治疗如吗替麦考酚酯、硫唑嘌呤,能改善预后。对伴肿瘤的患者,肿瘤切除术联合免疫治疗能缩短患者病程[25]。有文献[26]报道约75%的患者能痊愈或遗留轻度后遗症,死亡率接近4%。本病可复发。有研究者[3]对25例患者随访观察发现6例患者复发,复发时间0.5~13年,平均为2年,首次发病未接受免疫治疗、不伴肿瘤的患者更易于复发。有研究[27]报道年龄>12岁、初始的mRS评分(modified Rankin scale,改良Rankin量表)≤3分提示预后良好。本组1例5月后复发。对复发性脑炎的患者尤其应警惕自身免疫性脑炎。
3 结语临床上对于以癫痫发作、精神异常、记忆下降、运动障碍或自主神经功能紊乱为主要表现的急性或亚急性起病的脑病患者,除了考虑病毒性脑炎以外,还要重点考虑抗NMDAR脑炎等自身免疫性脑炎可能,应及时完善血清及脑脊液抗NMDAR抗体及其他自身免疫性抗体的检查,同时要排查体内肿瘤,特别是畸胎瘤。
| [1] |
Dalmau J, Tuzun E, Wu H Y, et al. Paraneoplastic anti-N-methyl-D-aspartate receptor encephalitis associated with ovarian teratoma[J]. Ann Neurol, 2007, 61(1): 25-36. DOI:10.1002/ana.v61:1 |
| [2] |
许春伶, 赵伟秦, 李继梅, 等. 抗N-甲基-D-天冬氨酸受体脑炎一例[J]. 中华神经科杂志, 2010, 43(11): 781-783. DOI:10.3760/cma.j.issn.1006-7876.2010.11.011 |
| [3] |
Gabilondo I, Saiz A, Galan L, et al. Analysis of relapses in anti-NMDAR encephalitis[J]. Neurology, 2011, 77(10): 996-999. DOI:10.1212/WNL.0b013e31822cfc6b |
| [4] |
Titulaer MJ, Mccracken L, Gabilondo I, et al. Treatment and prognostic factors for long-term outcome in patients with anti-NMDA receptor encephalitis:an observational cohort study[J]. Lancet Neurol, 2013, 12(2): 157-165. DOI:10.1016/S1474-4422(12)70310-1 |
| [5] |
Iizuka T, Sakai F, Ide T, et al. Anti-NMDA receptor encephalitis in Japan:long-term outcome without tumor removal[J]. Neurology, 2008, 70(7): 504-511. DOI:10.1212/01.wnl.0000278388.90370.c3 |
| [6] |
Iizuka T, Sakai F. Anti-nMDA receptor encephalitis——clinical manifestations and pathophysiology[J]. Brain Nerve, 2008, 60(9): 1047-1060. |
| [7] |
Barry H, Hardiman O, Healy DG, et al. Anti-NMDA receptor encephalitis:an important differential diagnosis in psychosis[J]. Br J Psychiatry, 2011, 199(6): 508-509. DOI:10.1192/bjp.bp.111.092197 |
| [8] |
陈向军, 邓波. 自身免疫性脑炎的诊断标准及其临床指导意义[J]. 中国临床神经科学, 2016, 24(3): 336-340. |
| [9] |
Hughes EG, Peng X, Gleichman AJ, et al. Cellular and synaptic mechanisms of anti-NMDA receptor encephalitis[J]. J Neurosci, 2010, 30(17): 5866-5875. DOI:10.1523/JNEUROSCI.0167-10.2010 |
| [10] |
Schmitt SE, Pargeon K, Frechette ES, et al. Extreme delta brush:a unique EEG pattern in adults with anti-NMDA receptor encephalitis[J]. Neurology, 2012, 79(11): 1094-1100. DOI:10.1212/WNL.0b013e3182698cd8 |
| [11] |
Veciana M, Becerra JL, Fossas P, et al. EEG extreme delta brush:An ictal pattern in patients with anti-NMDA receptor encephalitis[J]. Epilepsy Behav, 2015, 49: 280-285. DOI:10.1016/j.yebeh.2015.04.032 |
| [12] |
Graus F, Titulaer MJ, Balu R, et al. A clinical approach to diagnosis of autoimmune encephalitis[J]. Lancet Neurol, 2016, 15(4): 391-404. DOI:10.1016/S1474-4422(15)00401-9 |
| [13] |
Miller FW, Pollard KM, Parks CG, et al. Criteria for environmentally associated autoimmune diseases[J]. J Autoimmun, 2012, 39(4): 253-258. DOI:10.1016/j.jaut.2012.05.001 |
| [14] |
Venkatesan A, Johnson RT. Infections and multiple sclerosis[J]. Handb Clin Neurol, 2014, 122: 151-171. DOI:10.1016/B978-0-444-52001-2.00007-8 |
| [15] |
Atassi MZ, Casali P. Molecular mechanisms of autoimmunity[J]. Autoimmunity, 2008, 41(2): 123-132. DOI:10.1080/08916930801929021 |
| [16] |
来海欧, 杨金升. NMDA受体与癫痫发病机制的研究现状[J]. 国际神经病学神经外科学杂志, 2008, 35(1): 72-76. |
| [17] |
Venkatesan A, Benavides DR. Autoimmune encephalitis and its relation to infection[J]. Curr Neurol Neurosci Rep, 2015, 15(3): 3. DOI:10.1007/s11910-015-0529-1 |
| [18] |
Gleichman AJ, Spruce LA, Dalmau J, et al. Anti-NMDA receptor encephalitis antibody binding is dependent on amino acid identity of a small region within the GluN1 amino terminal domain[J]. J Neurosci, 2012, 32(32): 11082-11094. DOI:10.1523/JNEUROSCI.0064-12.2012 |
| [19] |
Moscato EH, Peng X, Jain A, et al. Acute mechanisms underlying antibody effects in anti-N-methyl-D-aspartate receptor encephalitis[J]. Ann Neurol, 2014, 76(1): 108-119. DOI:10.1002/ana.24195 |
| [20] |
Leypoldt F, Armangue T, Dalmau J. Autoimmune encephalopathies[J]. Ann N Y Acad Sci, 2015, 1338: 94-114. DOI:10.1111/nyas.12553 |
| [21] |
Schein F, Gagneux-Brunon A, Antoine JC, et al. Anti-N-methyl-D-aspartate receptor encephalitis after Herpes simplex virus-associated encephalitis:an emerging disease with diagnosis and therapeutic challenges[J]. Infection, 2016. https://link.springer.com/article/10.1007/s15010-016-0959-y
|
| [22] |
Mohammad SS, Sinclair K, Pillai S, et al. Herpes simplex encephalitis relapse with chorea is associated with autoantibodies to N-Methyl-D-aspartate receptor or dopamine-2 receptor[J]. Mov Disord, 2014, 29(1): 117-122. DOI:10.1002/mds.25623 |
| [23] |
Jensen P, Kondziella D, Thomsen G, et al. Anti-NMDAR encephalitis:demonstration of neuroinflammation and the effect of immunotherapy[J]. Neurology, 2015, 84(8): 859. DOI:10.1212/WNL.0000000000001278 |
| [24] |
Wang H. Efficacies of treatments for anti-NMDA receptor encephalitis[J]. Front Biosci (Landmark Ed), 2016, 21: 651-663. DOI:10.2741/4412 |
| [25] |
Bai Y, Guan Q, Jiang J, et al. Treatment principles of ovarian teratoma with anti-N-methyl-D-aspartate receptor encephalitis[J]. Arch Gynecol Obstet, 2016, 294(3): 623-629. DOI:10.1007/s00404-016-4050-9 |
| [26] |
Dalmau J, Lancaster E, Martinez-Hernandez E, et al. Clinical experience and laboratory investigations in patients with anti-NMDAR encephalitis[J]. Lancet Neurol, 2011, 10(1): 63-74. DOI:10.1016/S1474-4422(10)70253-2 |
| [27] |
Zekeridou A, Karantoni E, Viaccoz A, et al. Treatment and outcome of children and adolescents with N-methyl-D-aspartate receptor encephalitis[J]. J Neurol, 2015, 262(8): 1859-1866. DOI:10.1007/s00415-015-7781-9 |
 2017, Vol. 44
2017, Vol. 44




