扩展功能
文章信息
- 朱蔚文, 廖卫平, 易咏红, 宋兴旺
- ZHU Wei-Wen, LIAO Wei-Ping, YI Yong-Hong, SONG Xing-Wang
- CLN5基因复合杂合突变致青少年型神经元腊样脂褐质沉积症的临床特征及基因分析
- Clinical features and gene analysis of juvenile neuronal ceroid lipofuscinosis induced by compound heterozygous mutation in CLN5 gene
- 国际神经病学神经外科学杂志, 2017, 44(2): 113-117
- Journal of International Neurology and Neurosurgery, 2017, 44(2): 113-117
-
文章历史
收稿日期: 2017-02-09
修回日期: 2017-04-09
神经元蜡样脂褐质沉积病 (neuronal ceriod lipofuscinoses, NCLs) 是一组遗传性神经系统变性疾病,以进行性神经元变性坏死和视网膜萎缩为主要病理变化,电镜下可发现特征性脂褐素样物沉积于神经元、皮肤上皮细胞和淋巴细胞的溶酶体中。目前发现引起NCLs的致病基因有13个,多呈常染色体隐性遗传,儿童期发病多见,偶见以常染色体显性遗传方式发病的成年人患者。迄今在国内已有CLN1基因、CLN2基因和CLN3基因突变的病例报道[1]。我科近期发现1例CLN5等位基因的2号外显子及3号外显子各有1个位点发生突变、临床表现为青少年型神经元腊样脂褐质沉积症的病例,现将该病例及其父母、弟弟的临床特征及基因分析结果报告如下。
1 资料与方法 1.1 临床资料患者,女性,9岁,出生时顺产,婴幼儿期生长发育与同龄儿童相近。6岁开始出现反应迟钝、注意力不集中,渐渐地写字越来越差,学习困难,成绩明显下降,对所学的知识基本遗忘。7岁时视力开始下降,曾在眼科检查,结果:双眼屈光不正、双眼弱视和双眼卵黄样黄斑病变。目前佩戴近视、散光眼镜,戴镜纠正视力为0.2。8岁始患者出现反复持碗摔落,9岁某次发热时出现发作性“惊吓样”全身不自主抖动,此后经常出现发作性肢体抽动或行走时突发后倾摔倒,目前行走欠稳易跌倒。神经系统专科查体:接触可,情感反应幼稚,反应慢,对答基本对题,能写自己名字,但不能写出完整句子,无法回忆起曾学过的诗词,计算力差,勉强完成10以内加减,理解力欠佳,完成复杂指令困难,自发言语少,构音含糊;双眼可见自发眼震、水平性和旋转性眼震,余颅神经检查未见明显异常;四肢肌力正常,肌张力稍偏低,双侧指鼻试验、跟膝胫试验完成笨拙欠准;Romberg征阳性,四肢腱反射对称正常,未引出病理征;脑膜刺激征阴性。体查期间可见多次手部突发短促抽动。
患儿父亲视力、言语、理解能力尚可,否认癫痫发作史、否认行走活动异常;体查可见水平性及旋转性眼震,指鼻稍笨拙,Romberg征可疑阳性。患儿弟弟8岁,视力、智力良好,否认癫痫发作史、否认行走活动异常;体查可见水平性眼震,指鼻稍笨拙,Romberg征阴性。患者母亲视力正常,理解能力稍差,对患儿的病情反复多次解释后才能勉强理解,其余神经系统体查未发现明显阳性体征。患儿一位姑姑有癫痫发作史、智力差、行走欠稳 (具体情况不详)。
1.2 检查方法对患者进行头颅MRI+MRA、24小时视频脑电图检查,并进行全外显子基因测序 (北京迈基诺基因科技有限责任公司),并对其家庭成员进行相关基因检测。患儿弟弟行头颅MRI检查。
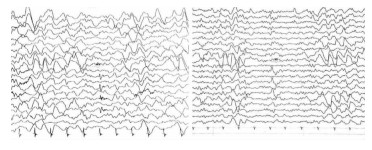
2 结果 2.1 动态脑电图背景为后头部8~9 Hz α节律,可见弥漫性高幅2.5~3.5 Hz慢活动中-长程出现,以后头部明显,偶见右前中颞部单个尖波、尖慢波发放。见图 1。
|
| 图 1 患者脑电图改变 |
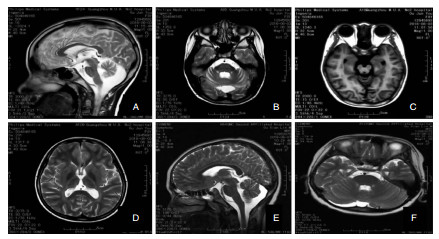
患者头颅MRI检查示小脑半球及蚓部明显萎缩,脑干轻度萎缩,第四脑室、枕大池明显扩大,双侧大脑半球沟回略增宽,双侧颞叶、枕叶皮质轻度萎缩,双侧侧脑室扩大。见图 2A、图 2B、图 2C、图 2D。
|
| 图 2 患者及患者弟弟MRI图像 A:小脑萎缩明显;B、C:桥脑、中脑和海马萎缩;C、D:颞叶、额叶、枕叶轻度萎缩;E、F:患者弟弟小脑轻度萎缩。 |
患者弟弟头颅MRI检查示小脑、脑干轻度萎缩,余未见明显异常。见图 2E、图 2F。
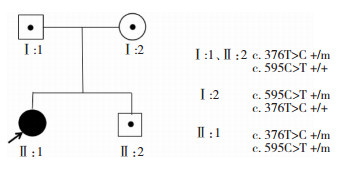
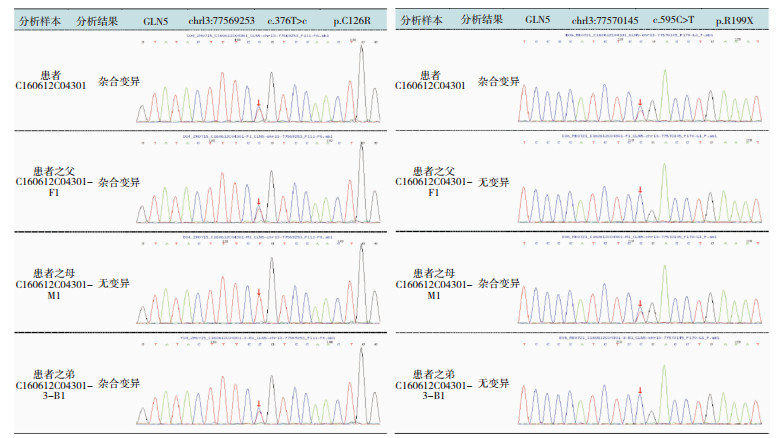
2.3 全外显子组测序结果患者CLN5基因2号外显子第376对碱基胸腺嘧啶T突变为胞嘧啶C,该变异为错义突变,来源于父亲,患者弟弟该位点发现同样的碱基突变。患者母亲该位点无变异。患者CLN5基因3号外显子第595对碱基胞嘧啶C突变为胸腺嘧啶T,该变异为无义突变,来源于母亲。患者父亲、弟弟该位点无变异。见图 3、图 4。
|
| 图 3 CLN5基因复合杂合突变致JNCL患者家系图 |
|
| 图 4 患者及家人CLN5基因突变位点测序图 |
神经元蜡样脂褐质沉积病 (NCL) 典型的临床症状为进行性视力减退、智能倒退、癫痫以及运动障碍;其共同的病理特征为大脑和小脑皮质神经元进行性死亡、视网膜细胞变性坏死,残余的神经元细胞内有大量脂褐质沉积 (其内容物主要为线粒体ATP合成酶C亚基、脂蛋白结合蛋白A和D、β-淀粉样蛋白等)。迄今发现的13个NCL致病基因分别编码溶酶体酶 (PPT1和TPP1)、溶酶体跨膜蛋白和内质网跨膜蛋白、多种功能尚未明确的组织蛋白酶和可溶性蛋白等[2]。通过RT-PCR研究发现在小鼠胚胎发育全程的海马、脑室区和小脑均检测到CLN2、CLN3和CLN5三种基因mRNA持续的表达,并且在时空上与神经祖细胞中干细胞标志物的表达相一致,这表明,CLN2、CLN3和CLN5基因可能在早期胚胎发生中发挥重要作用[3]。目前的研究提示,这些NCL相关蛋白能影响彼此的表达或活性,因此,一旦其中某种NCL蛋白功能障碍将会导致溶酶体或内质网的一系列功能障碍 (如代谢产物不能正常降解、氧化应激与NO转导通路受阻和线粒体呼吸链无法正常工作等),直接或间接引起神经元自噬障碍、凋亡程序异常启动,影响脑的正常发育和导致特征性溶酶体病理改变[2]。因此,不同NCL基因突变可引起相似的病理改变和临床表型。另一方面,同一基因的不同位点突变可能导致不同临床表型,如CLN8基因突变既可引起“严重”的临床表型,如婴儿期发病、难以控制的癫痫发作、严重视力减退、共济失调、痴呆和早逝;亦可引起“温和”的临床表型,如成年起病的进行性肌阵挛性癫痫,但并不影响视力。前者被认为是由于突变位点导致蛋白质功能完全丧失,后者是突变位点仅降低蛋白质的活性[4]。
NCL的分类开始时是以患者起病年龄为依据分为婴儿型、晚婴型、青少年型和成人型等,随着多个致病基因相继被发现,逐渐倾向于根据致病基因进行分类。Gewalin等[5]通过对440例患者进行基因型和临床表型的meta分析发现两者在起病年龄方面既有明显相关性同时又具有多样性,例如CLN3突变均引起青少年型NCL, CLN4突变均引起成人型NCL;但CLN1突变可引起婴儿型NCL且起病年龄均早于3岁,也可导致成年早期型NCL;CLN5突变可以引起晚婴型和青少年型NCL,CLN6突变的患者年龄分布呈现成人型和婴儿型“双峰”趋势等。因此,单靠患者起病年龄为依据是无法推测致病基因的。相反,通过基因检测得到基因型诊断可以在尚无典型的临床表型及病理改变不明显时预测到病程进展,具有较高临床诊断价值。目前,大多数专家建议NCL主要依靠基因分类,其次根据发病年龄及临床特点分类。由于到目前为止尚无明确有效的延迟或停止疾病进展的综合治疗方案,因此,对NCLs的疾病管理策略主要是控制症状而不是“治愈”疾病,同时及早对病人及其家庭进行遗传诊断和生育指导尤其必要。
CLN5基因位于13号染色体q21-32区,编码1个由407个氨基酸组成的多肽链,是位于溶酶体和内质网中的可溶性糖蛋白。Schmiedt等[6]发现CLN5具有蛋白水解酶样降解作用,能降解转运到溶酶体中的成熟的多肽链;体外结合分析和免疫共沉淀试验显示CLN5蛋白与CLN2蛋白和CLN3蛋白之间有相互作用。Lyly等[7]发现CLN5蛋白与CLN1、CLN2、CLN3、CLN6和CLN8等蛋白有相互作用,提示CLN5蛋白对NCL发病既有启动也有修饰作用。CLN5型被称为“芬兰变异型”,因为该遗传病家族最早在芬兰被发现,但主要为散发病例。CLN5型发病年龄从4至17岁不等,临床表现包括精神运动功能倒退、共济失调、肌阵挛性癫痫和视力下降。目前在CLN5基因上已发现40多个引起临床表型的突变点,其中本病例发现的CLN5基因突变位点exon3 c595C>T的纯合子突变已有一例报道,患者为意大利裔,其临床表型为JNCL[8];本病例另一个杂合突变位点exon2 c376T>C通过检索HGMD数据库和www.ucl.ac.uk/ncl/mutation.shtml未见报道,因此本例为新发现的具有JNCL临床表型的CLN5基因复合杂合突变病例。患者弟弟检测到CLN5基因d376T>C突变,检查发现有眼球震颤、MRI显示有轻度小脑脑干萎缩,父亲也存在眼球震颤和轻微小脑性共济失调症状 (未做头颅MRI),提示该位点杂合突变可以影响CLN5蛋白的功能并产生部分临床表征,倘若同时出现CLN5基因其它位点杂合突变时,可能产生典型的临床表现和病理改变。因此,我们要重视这种复合杂合突变在遗传学上的意义,对有遗传病风险人群应该进行相关基因筛查和生育指导。
| [1] | 毕鸿雁, 姚生, 卜定芳, 等. 婴儿型神经元蜡样质脂褐素沉积病棕榈酰蛋白硫酯酶1基因的二个新突变[J]. 中华儿科杂志, 2006, 17(5): 345–348. |
| [2] | Radke J, Stenzel W, Goebel HH, et al. Human NCL neuropathology[J]. Biochim Biophys Acta, 2015, 1852: 2262–2266. DOI:10.1016/j.bbadis.2015.05.007 |
| [3] | Fabritius AL, Vesa J, Minye HM, et al. Neuronal ceroid lipofuscinosis genes, CLN2, CLN3 and CLN5 are spatially and temporally co-expressed in a developing mouse brain[J]. Exp Mol Pathol, 2014, 97: 484–491. DOI:10.1016/j.yexmp.2014.10.003 |
| [4] | Kousi M, Lehesjoki AE, Mole SE. Update of the mutation spectrum and clinical correlations of over 360 mutations in eight genes that underlie the neuronal ceroid lipofuscinoses[J]. Hum Mutat, 2012, 33(1): 42–63. DOI:10.1002/humu.21624 |
| [5] | Aungaroon G, Hallinan B, Jain P, et al. Correlation among genotype, phenotype, and histology in neuronal ceroid lipofuscinoses:an individual patient data meta-analysis[J]. Pediatr Neurol, 2016, 60: 42–48. DOI:10.1016/j.pediatrneurol.2016.03.018 |
| [6] | Schmiedt ML, Bessa C, Heine C, et al. The neuronal ceroid lipofuscinosis protein CLN5:new insights into cellular maturation, transport, and consequences of mutations[J]. Hum Mutat, 2010, 31(3): 356–365. DOI:10.1002/humu.v31:3 |
| [7] | Lyly A, von Schantz C, Heine C, et al. Novel interactions of CLN5 support molecular networking between Neuronal Ceroid Lipofuscinosis proteins[J]. BMC Cell Biol, 2009, 10: 83. DOI:10.1186/1471-2121-10-83 |
| [8] | Santorelli FM, Garavaglia B, Cardona F, et al. Molecular epidemiology of childhood neuronal ceroid-lipofuscinosis in Italy[J]. Orphanet J Rare Dis, 2013, 8: 19. DOI:10.1186/1750-1172-8-19 |
 2017, Vol. 44
2017, Vol. 44




