2. 528000, 佛山市第一人民医院MR室;
3. 510800 广州, 广东省人民医院核医学科PET/CT中心
2. Department of MRI, the First People's Hospital of Foshan, Foshan 528000, China;
3. Department of PET/CT Center, Guangdong General Hospital, Guangzhou 510800, China
胰腺实性假乳头状瘤(solid pseudopapillary tumor,SPT)在临床工作中并不少见,其首次由Frantz提出,由于组织形态结构具有多样性曾多次被命名,最终于1996年由世界卫生组织将其统一命名为SPT,分为良性、交界性、恶性,其中恶性SPT被命名为实性假乳头状癌(solid pseudopapillary carcinoma,SPC)[1-2]。有关胰腺SPT的CT和MRI诊断的报道不在少数,由于良、恶性SPT的CT和MRI征象存在重叠,其诊断与鉴别诊断仍存在一定难度,笔者归纳并分析了良、恶性胰腺SPT的CT和MRI的几个特征性诊断要点,以期提高胰腺SPT诊断的准确率。
1 资料与方法 1.1 一般资料病例纳入标准:①2012年至2017年经广州市第一人民医院、佛山市第一人民医院手术病理确诊的胰腺良性SPT和SPC患者;②临床与CT、MRI资料完整。病例排除标准:①CT或MRI图像伪影较重,影响观察;②存在大量腹水、胰腺或胰周其他病变干扰。最终纳入38例良性SPT和10例SPC患者,38例良性SPT中女性35例[平均年龄(26.7±4.3)岁]、男性3例[平均年龄(44.7±5.6)岁],10例SPC中女性3例[平均年龄(35.2±3.8)岁]、男性7例[平均年龄(50.8±3.3)岁]。48例患者中32例良性SPT、8例SPC出现上腹部不适。所有患者均进行了CT、MRI平扫及动态增强扫描。所有患者检查前均签署了知情同意书。
1.2 CT扫描患者检查前禁食10 h以上,扫描前0.5 h饮水1000 mL。所有CT扫描资料来源于两台CT机,其中一台采用荷兰Philips Brilliance 256层iCT扫描仪(探测器组合0.625 mm×256),扫描范围自膈顶至肝、脾下缘,包括整个胰腺;扫描层厚:1~2 mm,扫描速度:0.27 s/r;螺距:0.915,电压:80 kV,电流:100 mAs,X线管旋转:360°/0.4 s。另一台采用日本Toshiba Aquilion 64层CT扫描机,电压:120 kV,电流:200 mAs,层厚1~2 mm;探测器:0.625 mm×128。增强扫描均采用对比剂碘普罗胺(拜耳医药保健有限公司广州分公司)注射液,用高压注射器经前臂肘正中静脉注射,注射速率4~5 mL/s,注射体积90~100 mL。分别于注射后25 s、55~65 s、120 s行动脉期、门脉期及实质期的扫描。
1.3 MRI扫描采用荷兰Philips Achieva 1.5T MRI扫描仪,上腹部专用4US线圈;患者取仰卧位,头先进,轴位扫描。扫描参数:轴位单次激发快速自旋回波(SS-FSE),T2加权扫描,重复时间3200 ms,回波时间85 ms,矩阵288×224,层厚4 mm,激励次数3,视野20 cm×15 cm;梯度回波T1加权扫描,重复时间8.5 ms,回波时间4 ms,矩阵288×192,层厚4 mm,激励次数3,视野22 cm×22 cm。增强扫描对比剂采用钆喷酸葡胺(广州康臣药业有限公司),0.1 mmol/kg,高压注射器注射,速率1.5 mL/s。
1.4 CT和MRI征象分析由2名腹部放射专业副主任医师在不了解病情或不知道病理结果的情况下分别对图像进行分析,结论不一致时讨论并达成共识。征象分析内容包括:病灶的部位、大小、形态、密度或信号、胰管扩张、周围血管或组织是否受侵犯等,其中,病灶的包膜、钙化、瘤内出血、胰管扩张、周围血管或组织是否受侵犯等情况需要着重观察。
2 结果 2.1 一般征象病灶部位:胰腺体尾部较头颈部多见,48例患者中28例病灶位于胰腺体尾部,20例病灶位于胰头颈部。病灶大小:良性SPT与SPC病灶平均直径范围分别约为(4.83±0.63)和(4.86±0.56)cm。病灶形态:无特异性,多呈圆形或椭圆形。病灶质地:良性SPT与SPC的囊实性特点无特异性,39例病灶呈囊实性,9例呈实性。
2.2 CT和MRI征象38例良性SPT瘤体包膜均完整、边缘清楚,T1、T2均呈低信号,增强后呈延迟强化(图 1、图 2);10例SPC中9例包膜局部显示不清、欠完整(图 3)。18例良性SPT与6例SPC钙化均呈点状、结节状或弧线状(图 4)。11例良性SPT与6例SPC瘤内出血,CT平扫呈片絮状稍高密度影,MRI呈T1稍高信号,T2低信号(图 5)。良性SPT与SPC胰管扩张均呈管状或串珠状改变,7例良性SPT胰管扩张,其中4例位于胰头颈部,3例位于胰腺体部;5例SPC胰管扩张,其中3例位于胰头颈部,2例位于胰腺体部。38例良性SPT均未见周围血管受侵犯;4例SPC可见病灶周围血管受侵犯,表现为血管局部管壁模糊(图 6)。38例良性SPT均未见周围组织受侵犯;5例SPC可见病灶周围组织受侵犯,表现为瘤-组织边缘模糊,局部包膜不完整(图 7)。
|
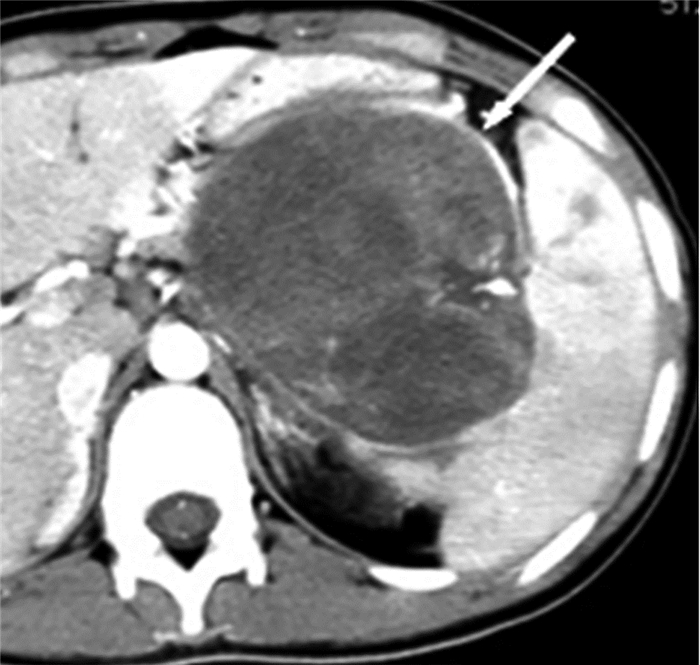
图 1 胰腺良性实性假乳头状瘤患者CT增强扫描图 患者女性,31岁。图中,箭头示包膜环形强化。CT:计算机体层摄影术。 Figure 1 Enhanced CT image of a solid pseudopapillary panceatic tumor |
|
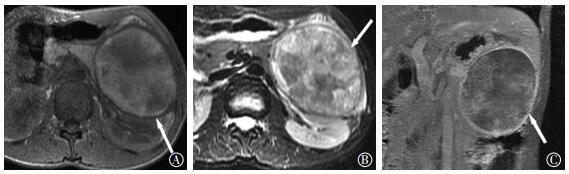
图 2 胰腺良性实性假乳头状瘤患者MRI扫描图 患者女性,25岁。图中,A、B:T1加权像、T2加权像包膜完整并呈低信号;C:增强扫描包膜环形强化。MRI:磁共振成像。 Figure 2 MRI images of a solid pseudopapillary panceatic tumor |

|
图 3 胰腺实性假乳头状癌患者CT增强扫描图 患者男性,58岁。图中,箭头示包膜不完整。CT:计算机体层摄影术。 Figure 3 Enhanced CT image of a solid pseudopapillary panceatic carcinoma |

|
图 4 胰腺良性实性假乳头状瘤患者CT平扫图 图中,A:患者女性,32岁,瘤内点状、条状及弧形钙化;B:患者女性,25岁,点状钙化;C:患者男性,51岁,结节状钙化。CT:计算机体层摄影术。 Figure 4 Plain CT images of solid pseudopapillary panceatic tumor |
|
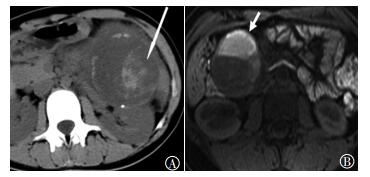
图 5 胰腺良性实性假乳头状瘤患者瘤内出血CT和MRI图 图中,A:CT平扫图,患者女性,47岁,箭头示瘤内出血,CT平扫呈片絮状稍高密度影;B:MRI T1加权图,患者女性,45岁,箭头示T1加权像分层混杂高低信号影。CT:计算机体层摄影术;MRI:磁共振成像。 Figure 5 CT and MRI images of solid pseudopapillary panceatic tumor with intratumoral hemorrhage |
|
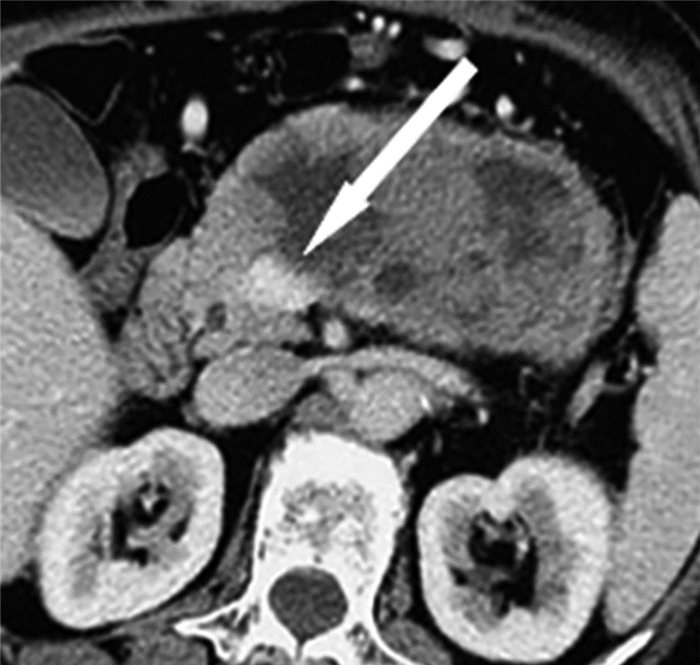
图 6 胰腺实性假乳头状癌患者 CT增强扫描图患者男性,62岁,箭头示肿瘤侵犯周围肠系膜上静脉,血管壁模糊。CT:计算机体层摄影术。 Figure 6 Enhanced CT image of a solid pseudopapillary panceatic carcinoma |

|
图 7 胰腺实性假乳头状癌患者CT增强扫描图 患者男性,49岁,肿瘤侵犯周围胰腺组织,箭头示肿瘤与正常胰腺组织分界不清。CT:计算机体层摄影术。 Figure 7 Enhanced CT image of a solid pseudopapillary panceatic carcinoma |
胰腺SPT的发病机制目前尚不清楚,但其病理组织形态已明确,由实性和假乳头状结构的细胞组成[3]。其发生率占胰腺外分泌肿瘤的1%~2%,好发于年轻女性[4],本研究38例良性SPT患者中女性为35例,平均年龄(26.7±4.3)岁。SPT可发生于胰腺各个部位,但以胰腺体尾部多见[5],本研究48例患者中有28例病灶位于胰腺体尾部。SPT以囊实性多见,本研究39例病灶为囊实性。我们收集的病例来自两家不同医院,所用CT机型与扫描参数不尽相同,但对于图像质量、病变征象的分析未造成干扰。
3.1 良、恶性胰腺SPT的CT和MRI特征性征象 3.1.1 包膜SPT瘤体周边可见包膜,这一征象在胰腺其他病变中不可见,故SPT瘤体边界一般与周围组织分界清楚。包膜含有丰富的纤维结缔组织,CT平扫显示欠清,动态增强扫描包膜呈渐进性强化,于静脉期或延迟期显示清晰;T1或T2加权像大部分呈低信号,动态增强扫描延迟强化,强化程度可高于周围胰腺组织。良性SPT瘤体包膜一般完整,而SPC包膜可见局部不完整或显示不清[6],本研究10例SPC中9例包膜局部显示不清、欠完整,提示肿瘤突破包膜向周围组织侵犯。
3.1.2 钙化文献报道胰腺SPT钙化占病灶总数的30%[6-7],本研究48例病灶钙化占50.0%,其中良性SPT钙化占47.4%(18/38),SPC占60.0(6/10)%,病例数较少可能是本研究钙化比例大于文献报道的原因。钙化是良性SPT和SPC特征性的征象,一般出现在瘤内实性成分或包膜处,多呈点状、结节状或弧线状,CT平扫呈高密度,T1、T2加权像均呈低信号,良性SPT和SPC钙化的出现可能与瘤内出血坏死有关[8]。
3.1.3 瘤内出血胰腺SPT由实性和假乳头状结构的细胞组成,实性结构细胞围绕瘤内纤维血管呈团片状排列,假乳头状结构细胞围绕纤维血管呈假乳头状排列,远离纤维血管的细胞容易坏死、出血并囊变[9]。瘤内出血为良性SPT和SPC区别于胰腺其他肿瘤性病变的重要征象[3]。新鲜出血CT平扫呈稍高密度,陈旧出血CT平扫显示欠清。瘤内出血T1加权像呈高信号,T2加权像呈稍低信号,增强后无强化。本研究48例病灶瘤内出血17例,其中良性SPT瘤内出血11例(占28.9%),SPC瘤内出血6例(占60.0%),该结果比文献报道的比例略高[9],可能是由于病例数较少的原因。
3.1.4 胰腺胰管扩张良性SPT和SPC发生于胰头颈部或胰体部时,引起胰管扩张不多见[10],但有文献报道瘤体压迫或侵犯近端胰管可致远端胰管扩张[11],CT或MRI可见胰管扩张呈管状或串珠状。本研究48例病灶中胰管扩张12例:7例良性SPT胰管扩张,其中4例位于胰头颈部,3例位于胰腺体部;5例SPC胰管扩张,其中3例位于胰头颈部,2例位于胰腺体部。
3.1.5 侵犯血管或周围组织当瘤体较大时,胰腺良性SPT对周围血管或组织表现为推压,分界清晰。而SPC可突破瘤体包膜,对周围的血管或组织进行侵犯,CT或MRI表现为局部包膜模糊、中断,与邻近血管或组织分界不清,这一特点为良性SPT与SPC相鉴别的重要征象[3, 12-13]。
3.2 鉴别诊断与总结包膜、钙化、胰管扩张、瘤内出血是良性SPT和SPC具有特征性的征象,结合患者的年龄特点可作出较为准确的诊断。侵犯血管或周围组织是鉴别SPT良恶性的重要征象。临床工作中掌握以上CT和MRI征象有助于良、恶性胰腺SPT的准确诊断。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 高强负责论文命题的提出和设计、病例收集、图像分析以及论文撰写;贺小红负责病例扫描、研究设计指导、论文审阅;邵丹负责协助病例收集、图像分析以及数据归纳;魏新华负责图像阅读、数据分析;江新青负责参数校正、数据分析及论文修订。
| [1] | Coleman KM, Doherty MC, Bigler SA. Solid-pseudopapillary tumor of the pancreas[J]. Radiographics, 2003, 23(6): 1644–1648. DOI:10.1148/rg.236035006 |
| [2] | Ulusan S, Bal N, Kizilkilic O, et al. Case report: solid-pseudopapillary tumour of the pancreas associated with dorsal agenesis[J]. Br J Radiol, 2005, 78(929): 441–443. DOI:10.1259/bjr/91312352 |
| [3] |
周洁, 曾旭文, 梁治平, 等.
胰腺实性假乳头状瘤的CT和MRI征象及病理回顾[J]. 中国CT和MRI杂志, 2016, 14(8): 1–3.
DOI:10.3969/j.issn.1672-5131.2016.08.001 Zhou J, Zeng XW, Liang ZP, et al. The imaging features and pathological analysis of solid pseudopapillary tumors of pancreas[J]. Chin J CT and MRI, 2016, 14(8): 1–3. DOI:10.3969/j.issn.1672-5131.2016.08.001 |
| [4] |
许春苗, 曲金荣, 李辛, 等.
胰腺实性假乳头状瘤的CT征像和病理的对照[J]. 实用放射学杂志, 2011, 27(4): 564–567.
DOI:10.3969/j.issn.1002-1671.2011.04.024 Xu CM, Qu JR, Li X, et al. The Comparison on CT Features and Pathology of Solid Pseudopapillary Neoplasm of the Pancreas[J]. J Pract Radiol, 2011, 27(4): 564–567. DOI:10.3969/j.issn.1002-1671.2011.04.024 |
| [5] |
温锋, 孙巍, 梁宏元, 等.
胰腺实性假乳头状瘤的影像诊断[J]. 中国临床医学影像杂志, 2011, 22(3): 195–197.
DOI:10.3969/j.issn.1008-1062.2011.03.016 Wen F, Sun W, Liang HY, et al. The image diagnosis of solid-pseudopapillary tumor of pancreas[J]. J Chin Clin Med Imaging, 2011, 22(3): 195–197. DOI:10.3969/j.issn.1008-1062.2011.03.016 |
| [6] |
胡小红, 王成林, 刘鹏程, 等.
胰腺实性假乳头状瘤的CT表现[J]. 中国CT与MRI杂志, 2012, 10(6): 76–78.
DOI:10.3969/j.issn.1672-5131.2012.06.025 Hu XH, Wang CL, Liu PC, et al. CT manifestestation of solid pseudopapillary tumor of the pancreas[J]. Chin J CT and MRI, 2012, 10(6): 76–78. DOI:10.3969/j.issn.1672-5131.2012.06.025 |
| [7] | Buetow PC, Buck JL, Pantongrag-Brown L, et al. Solid and papillary epithelial neoplasm of the pancreas:imaging-pathologic correlation on 56 cases[J]. Radiology, 1996, 199(3): 707–711. DOI:10.1148/radiology.199.3.8637992 |
| [8] |
钟熹, 汤日杰, 李建生, 等.
胰腺实性假乳头状瘤的CT表现[J]. 中国CT和MRI杂志, 2015, 13(9): 90–92, 102.
DOI:10.3969/j.issn.1672-5131.2015.09.028 Zhong X, Tang RJ, Li JS, et al. CT features of solid pseudopapillary tumor of the pancreas[J]. Chin J CT and MRI, 2015, 13(9): 90–92, 102. DOI:10.3969/j.issn.1672-5131.2015.09.028 |
| [9] |
马义, 朱斌.
胰腺实性假乳头状瘤的临床及影像学表现分析[J]. 医学影像学杂志, 2016, 26(4): 662–665.
Ma Y, Zhu B. The clinical manifestations and imaging features of the solid pseudopapillary tumors of pancreas[J]. J Med Imaging, 2016, 26(4): 662–665. |
| [10] |
李靖, 黎海亮, 曲金荣, 等.
胰腺实性假乳头状瘤多层螺旋CT和MRI表现[J]. 临床放射学杂志, 2016, 35(11): 1707–1711.
DOI:10.13437/j.cnki.jcr.2016.11.020 Li J, Li HL, Qu JR, et al. Imaging Features of Solid Pseudopapillary Neoplasm Of the Pancreas on MSCT and MRI[J]. J Clin Radiol, 2016, 35(11): 1707–1711. DOI:10.13437/j.cnki.jcr.2016.11.020 |
| [11] |
喻奇志, 于小平, 段智.
胰腺实性假乳头状癌的CT特征及病理对比研究(附11例报道)[J]. 放射学实践, 2012, 27(12): 1343–1346.
DOI:10.3969/j.issn.1000-0313.2012.12.018 Yu QZ, Yu XP, Duan Z. The CT characteristics of solid pseudopapillary carcinoma of pancreas (SPC) and pathological analysis (repost of 11 case and review of literature)[J]. Radiol Practice, 2012, 27(12): 1343–1346. DOI:10.3969/j.issn.1000-0313.2012.12.018 |
| [12] |
张发林, 雍昉.
巨大胰腺实性假乳头状瘤2例影像学诊断分析[J]. 国际放射医学核医学杂志, 2010, 34(1): 61–62.
DOI:10.3760/cma.j.issn.1673-4114.2010.01.018 Zhang FL, Yong F. Imaging diagnosis and analysis of solid-pseudopapillary tumor of the pancreas on two cases[J]. Int J Radiat Med Nucl Med, 2010, 34(1): 61–62. DOI:10.3760/cma.j.issn.1673-4114.2010.01.018 |
| [13] | Antoniou EA, Damaskos C, Garmpis N, et al. Solid Pseudopapillary Tumor of the Pancreas:A Single-center Experience and Review of the Literature[J]. In Vivo, 2017, 31(4): 501–510. DOI:10.21873/invivo.11089 |
 2018, Vol. 42
2018, Vol. 42


