2. 300070, 天津医科大学基础医学院细胞生物学系
2. Derpartment of Cell Biology, Institute of Medicine, Tianjin Medical University, Tianjin 300070, China
临床上,放疗是治疗肿瘤的主要且有效的手段,但是射线在杀伤肿瘤细胞的同时会对患者机体带来骨损伤[1-2]。临床数据表明肿瘤放疗可导致骨组织减少8%~23%[3]。长期的放疗可以导致患者产生骨密度减少、骨质疏松、骨变薄、骨折、骨坏死等骨损伤[4]。小鼠全身受到2 Gy照射后,骨密度明显减少,进一步的研究结果表明小鼠全身受2 Gy照射后,早期会出现破骨细胞数量的增加和功能的提升[5-6]。
MC3T3-E1细胞系是源于C57BL/6小鼠颅盖骨的成骨细胞系,是研究成骨细胞的良好模型[7]。Notch信号转导通路对成骨细胞的增殖、分化和功能有重要影响[8-9]。转基因小鼠实验结果表明,Notch通路对成骨细胞的分化具有抑制作用[10]。Notch信号通路胞内结构域(Notch intracellular domain,NICD)是Notch信号通路中重要的信号分子,其在Notch信号通路中起关键的承上启下作用。
我们利用RNA干扰技术抑制NICD表达建立稳定抑制NICD表达的MC3T3-E1细胞株,并于体外诱导分化为前体成骨细胞和成骨细胞。在辐射损伤后,对前体成骨细胞和成骨细胞的生长和功能基因的变化进行了观察。
1 材料与方法 1.1 细胞和主要试剂MC3T3-E1细胞系购买于中国医学科学院基础医学研究所。DMEM培养基、胎牛血清(美国Gibco公司);Opti-MEM培养基、Lipofectamine 2000转染试剂、Trizol试剂、M-MLV逆转录酶试剂盒、实时定量PCR(real-time quantitative PCR,qRT-PCR)试剂盒(美国Invitrogen公司);G418、Roche Cell Proliferation ELISA、5-溴-2’-脱氧尿嘧啶核苷(5-bromo-2’-deoxyuridine,BrdU)(colorimetric)试剂盒(德国Sigma-Aldrich公司);蛋白浓度测定试剂盒(上海生工生物工程有限公司);鼠源β-actin单抗(日本Santa Cruz Biotechnology公司);兔源NICD多抗(美国Millipore公司)。
1.2 仪器设备137Cs γ射线放射源(加拿大Gamma Ⅱ40,吸收剂量率0.99 Gy/min);CFX96TouchTM Real time PCR仪、ChemiDoc TMXRS+成像系统、Mini-PROTEAN®Tetra电泳槽、Sub-Cell®GT Cell水平小型电泳槽、Trans-Blot®半干转印槽、Gene Pulser MXcellTM电穿孔系统(美国Bio-Rad公司);M200酶标仪(瑞士Tecan公司);Nanodrop 2000 UV-Vis分光光度计、HEPA Class100二氧化碳培养箱(美国Thermo公司);倒置显微镜(上海蔡康光学仪器厂);-80℃超低温冰箱(美国Thermo Forma公司);4℃冰箱(广东容声电器股份有限公司);-20℃冰箱(日本三洋电器);高速台式离心机(上海嘉鹏科技有限公司);5430R小型台式高速冷冻离心机(德国Eppendorf);低速离心机(安徽中科中佳科学仪器有限公司);微量恒温器(绍兴市卫星医疗设备制造有限公司)。
1.3 MC3T3-E1细胞的培养、传代及诱导分化将MC3T3-E1细胞系细胞加入含10%胎牛血清、青霉素(100 U/mL)和链霉素(100 pg/mL)的DMEM完全培养液中,置于37℃、5% CO2、饱和湿度恒温培养箱中培养,每2 ~ 3 d更换培养液1次。待细胞贴壁生长至70% ~ 80%融合时,弃去培养液,PBS清洗,消化,室温离心5 min(1000 r/min,离心半径5 cm),用于细胞实验。
MC3T3-E1细胞贴壁生长至70%~80%融合时,根据文献[11]和[12]将培养液更换为成骨细胞分化培养液(osteoblast differentiation medium,OBDM)培养,同样每2 ~ 3 d更换培养液1次,培养8 d左右则可分化为前体成骨细胞,培养18 d左右分化为成熟的成骨细胞。OBDM完全培养液中含有10-8 mol/L β甘油磷酸钠、50 μg/mL维生素C和10-8 mol/L地塞米松。
1.4 细胞照射将培养5 d的前体成骨细胞和培养15 d的成骨细胞以137Cs γ射线放射源分别进行2 Gy照射。同时,参照文献[13],继续培养3 d后,将细胞样品用于实验分析。
1.5 RNA提取及逆转录用Trizol法提取细胞样品中的RNA。根据M-MLV逆转录试剂盒说明书进行逆转录。逆转录后的cDNA分装,置于-20℃冰箱中保存备用。
1.6 利用RNA干扰技术建立稳定抑制NICD表达的MC3T3-E1细胞株选取NICD序列1691作为干扰位点,干扰序列设计、合成和表达载体pGPH1/GFP/Neo构建由上海吉码公司完成。NICD的RNA干扰序列正反向分别是5’-CACCGCATATGTATGCCAGGTTATGT-TCAAG-3’和5’-AGACATAACCTGGCATACATATG-CTTTTTTG -3’。
将生长良好的MC3T3-E1细胞置于96孔板中,每孔100 μL,含细胞1×104个,培养过夜。每孔换用无抗生素的完全培养基100 μL,培养过夜。将4 μg的NICD的RNA干扰序列载体DNA加入250 μL无血清的Opti-MEM培养基中。加入5 μL Lipofectamine 2000于250 μL相同的无血清Opti-MEM培养基中。将上述两种液体混匀,室温下放置30 min,使cDNA和Lipofectamine 2000形成复合物。弃去转染培养液,将之前形成的复合物加到96孔板中,每孔100 μL,培养24 h后,用G418进行筛选,成功转染后的细胞将具有G418抗性。倒置荧光显微镜下观察结果。
1.7 细胞增殖实验根据colorimetric试剂盒说明书进行操作,将照射后3 d的MC3T3-E1细胞离心(1000转/min,离心半径为5 cm)弃去培养基,用PBS洗3遍,每孔加入100 μL已经加入胎牛血清和L-谷氨酰胺的α-MEM培养基。每孔加入10 μL BrdU标记溶液(终浓度为10 μmol/L)后,置于37℃、5% CO2、饱和湿度的细胞培养箱中继续培养2 h。弃去培养液,每孔加入200 μL FixDenat溶液,室温孵育30 min后,弃去。每孔加入连接有过氧化物酶的BrdU单抗(anti-BrdU-POD)100 μL,室温孵育90 min后,弃去。使用PBS洗3遍,弃去PBS,每孔加入100 μL TMB(四甲基联苯胺)底物溶液室温孵育5~30 min,直至显色足够进行检测为止。置于BioTek Synergy HT多功能微孔板检测仪上,测定每孔在370 nm和492 nm波长处的吸光度值。
1.8 qRT-PCR根据Platinum®SYBR® Green qPCR Super Mix-UDG with ROX试剂盒说明书,用qRT-PCR仪进行qRT-PCR反应。反应条件:50℃ 2 min,94℃ 3 min;94℃ 15 s,60℃ 20 s,72℃ 1 min,40个循环。采用2-△△Ct方法[14]来评价目的基因mRNA的表达水平。靶基因引物由Invitrogen公司合成,序列见表 1。
| 表1 成骨细胞功能靶基因引物序列 Table 1 The primer sequences of target genes in osteoblasts |
用哺乳动物细胞总蛋白抽提试剂裂解细胞提取蛋白。使用二喹啉甲酸(BCA)蛋白浓度测定试剂盒测定蛋白浓度。使用十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE)分离抽提蛋白,在转印槽内进行半干转,将目的蛋白转到硝酸纤维素膜上,4℃封闭过夜,分别用各靶蛋白的一抗与相应二抗孵育、洗脱及化学发光显色,最后用BIO-RAD Chemi-DocTM XRS+成像系统检测蛋白表达。其中,兔源NICD多抗的工作浓度为1 : 500,抗兔源的NICD二抗的工作浓度为1 : 5000;鼠源β-Actin单抗的工作浓度为1 : 1000,抗鼠源β-Actin的二抗的工作浓度为1 : 5000。
1.10 统计学分析采用OriginPro 8绘图分析软件进行柱状图的绘制,用SPSS 12.0统计软件处理数据,对各细胞增殖、相关功能基因的表达实验数据进行分析,各组数据均来自正态分布总体,符合正态分布和方差齐性。使用Student-Newman-Keuls进行组间显著性差异分析,并对组间进行t检验,P < 0.05表示差异具有统计学意义。
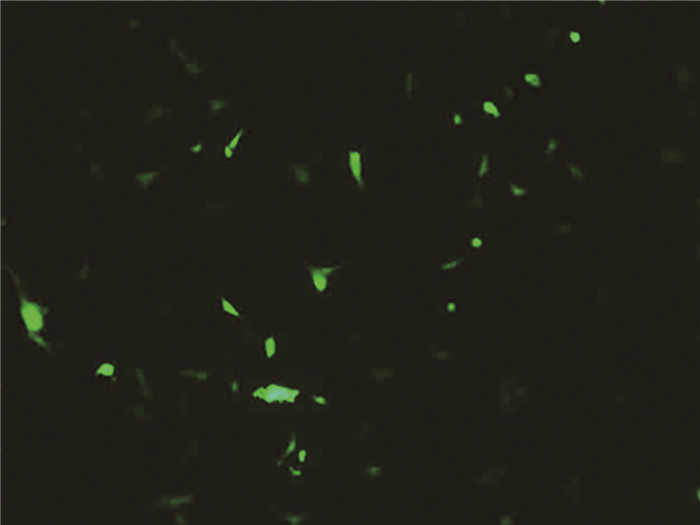
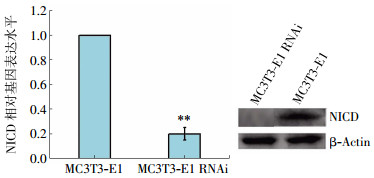
2 结果 2.1 稳定抑制NICD表达的MC3T3-E1细胞株的NICD表达水平NICD的RNA干扰序列表达载体pGPH1/GFP/Neo转染MC3T3-E1细胞,经G418筛选,在荧光显微镜下可见转染MC3T3-E1的细胞有荧光出现,并随着培养时间延长,带有荧光的细胞增多(图 1)。对该细胞进行qRT-PCR和Western blot检测,结果表明,与对照组MC3T3-E1相比,NICD的表达水平明显降低,两者之间的差异有统计学意义(t=4.774,P < 0.01)(图 2)。
|
图 1 倒置荧光显微镜(×20)下RNA干扰Notch信号通路胞内结构域的MC3T3-E1细胞 Figure 1 Notch intracellular domain RNAi MC3T3-E1 cells under the inverted fluorescence microscope (×20) |
|
图 2 实量定量PCR和Western blot检测NICD表达水平 Figure 2 Real-time quantitative PCR and Western blot examined Notch intracellular domain(NICD) expression in NICD RNAi MC3T3-E1 and MC3T3-E1 cells 图中,RNAi:RNA干扰;NICD:Notch信号通路胞内结构域;β-Actin:β肌动蛋白;**表示与对照组MC3T3-E1相比,NICD的表达水平明显降低,两者之间的差异有统计学意义(t=4.774,P < 0.01)。 |
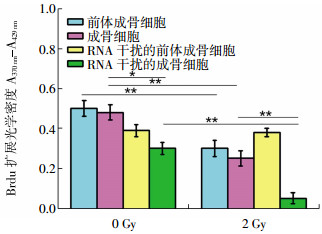
MC3T3-E1和NICD RNA干扰的MC3T3-E1细胞分别在OBDM中培养5 d和15 d,各自分别接受2 Gy照射,3 d后进行BrdU掺入实验。各种细胞BrdU掺入量依次是:前体成骨细胞>成骨细胞>NICD RNA干扰的前体成骨细胞>NICD RNA干扰的成骨细胞。RNA干扰的成骨细胞与成骨细胞相比BrdU掺入量下降,差异有统计学意义(t=2.828,P < 0.05),这表明RNA干扰抑制成骨细胞的增殖。与0 Gy相比,经过2 Gy照射后,前体成骨细胞和成骨细胞以及NICD RNA干扰的成骨细胞的BrdU掺入量明显下降,差异有统计学意义(t=3.365、3.451、3.213,均P < 0.01)。照射前后,NICD RNA干扰的前体成骨细胞BrdU掺入量没有明显改变,这表明NICD RNA干扰抑制前体成骨细胞和成骨细胞的增殖。2 Gy照射对NICD低表达的前体成骨细胞增殖的抑制作用不敏感,差异无统计学意义(t=0.714,P>0.05),但对成骨细胞增殖的抑制作用明显,差异有统计学意义(t=3.377,P < 0.01)(图 3)。
|
图 3 2 Gy照射对MC3T3-E1和NICD RNA干扰的MC3T3-E1细胞增殖的影响 Figure 3 Effect of 2 Gy radiation on proliferation of MC3T3-E1 and Notch intracellular domain(NICD) RNAi MC3T3-E1 cells 图中,Brdu:5-溴-2′-脱氧尿嘧啶核苷;NICD:Notch信号通路胞内结构域。除RNA干扰的前体成骨细胞外,2 Gy照射组各细胞增殖状况与0 Gy对照组相比,差异有统计学意义(t=3.365、3.451、3.213,均P < 0.01);成骨细胞与RNA干扰的成骨细胞增殖相比,差异有统计学意义(t=2.828,P < 0.05);2 Gy照射组成骨细胞与RNA干扰的成骨细胞增殖相比,差异有统计学意义(t=3.377,P < 0.01);*表示P < 0.05;**表示P < 0.01。 |
qRT-PCR检测各靶细胞功能基因表达水平,以0 Gy、2 Gy照射的细胞cDNA为模板,通过qRT-PCR分别检测各受照剂量细胞的成骨特异性转录因子2(Runt-related transcription factor 2,Runx2)、碱性磷酸酶(alkaline phosphatase,ALP)、骨保护素(osteoprotegerin,OPG)、核因子κB受体活化因子配体(receptor activator of nuclear factor κB ligand,RANKL)、巨噬细胞集落刺激因子(macrophage-colony stimulating factor,M-CSF)和β肌动蛋白(β-Actin)的mRNA表达量(图 4)。辐射对各细胞功能基因(Runx2、ALP、RANNKL、OPG和M-CSF)表达的影响如下。①Runx2:与0 Gy相比,2 Gy照射后的前体成骨细胞表达小幅度上调,差异有统计学意义(t=2.353,P < 0.05),成骨细胞表达小幅度下调,差异有统计学意义(t=2.342,P < 0.05),NICD RNA干扰的前体成骨细胞和成骨细胞的表达小幅度下调,差异有统计学意义(t=2.353、2.543,P < 0.05)。②ALP:与0 Gy相比,2 Gy照射后的前体成骨细胞、成骨细胞和NICD RNA干扰的前体成骨细胞表达上调,差异有统计学意义(t= 3.182、3.345、3.555,P < 0.05),NICD RNA干扰的成骨细胞表达下调,差异有统计学意义(t=5.045,P < 0.01)。③RANKL:与0 Gy相比,2 Gy照射后成骨细胞和NICD RNA干扰的前体成骨细胞表达上调,差异有统计学意义(t= 3.299,P < 0.05;t=10.212,P < 0.01),前体成骨细胞表达下调,差异有统计学意义(t=2.541,P < 0.05),NICD RNA干扰的成骨细胞表达变化不明显,差异无统计学意义(t=0.765,P>0.05)。④OPG:与0 Gy相比,2 Gy照射后的前体成骨细胞、成骨细胞和NICD RNA干扰的成骨细胞表达下调,差异有统计学意义(t=2.994、2.782、2.544,P < 0.05),NICD RNA干扰的前体成骨细胞的表达上调,差异有统计学意义(t=5.841,P < 0.01)。⑤M-CSF:与0 Gy相比,2 Gy照射后前体成骨细胞的表达下调,差异有统计学意义(t=2.379,P < 0.05),成骨细胞的表达上调,差异有统计学意义(t=2.353,P < 0.05),NICD RNA干扰的前体成骨细胞表达为不明显上调,差异无统计学意义(t=0.752,P>0.05),NICD RNA干扰的成骨细胞表达明显下调,差异有统计学意义(t=7.453,P < 0.01)。

|
图 4 实时定量PCR检测辐射对MC3T3-E1 RNAi和MC3T3-E1细胞的前体成骨细胞及成骨细胞中各基因表达水平的影响 Figure 4 Real-time quantitative PCR detects the effect of radiation on genes expression in the precursor osteoblasts and osteoblasts derived from MC3T3-E1 and Notch intracellular domain RNAi MC3T3-E1 cells 图中,ALP:碱性磷酸酶;Runx2:成骨特异性转录因子2;M-CSF:巨噬细胞集落刺激因子;RANKL:核因子κB受体活化因子配体;OPG:骨保护素;*表示,0 Gy与2 Gy照射后相比,各基因表达水平之间的差异有统计学意义(t=2.342 ~ 3.555,均P < 0.05);**表示,0 Gy与2 Gy照射后相比,各基因表达水平之间的差异有统计学意义(t=5.045 ~10.212,均P < 0.01)。 |
Notch信号转导通路在细胞的增殖、生长、分化和凋亡等生理过程中至关重要。在哺乳动物中,Notch信号通路有多种受体和配体,这些配体和受体都是单跨膜蛋白,需要细胞之间的相互作用才能激活。当相邻细胞的Notch配体和受体结合后,诱导靠近跨膜区域的Notch受体细胞内部分的C端被切割,NICD释放,进入细胞核内。在细胞核内没有NICD时,CSL(人为CBF1,鼠为RBPJ,果蝇为Suppressor of hairless,线虫为Lag1)和组蛋白去乙酰复合物(histone deccetylase complexes, HDAC)与DNA结合,抑制转录。NICD进入细胞核后,替换该复合物,与CSL和Mastermind-like蛋白形成三元复合体,将CSL蛋白原来的转录抑制作用转换为激活作用[15]。NICD在Notch信号通路中起到了非常重要的作用。在成骨细胞分化早期,NICD过表达可以导致成骨细胞数量减少,进而导致骨质疏松;但在成骨细胞分化晚期,NICD过表达将会影响成骨细胞的成熟,导致成骨细胞不能形成正常的骨组织。当NICD表达被干扰抑制后,成骨细胞激活破骨细胞的作用明显减少[16-18]。已有文献报道,2 Gy照射全身的小鼠出现明显骨丢失[5]。所以我们选用了MC3T3-E1细胞,经2 Gy照射后,来探讨NICD表达下调对成骨细胞的增殖和功能的影响。
我们用RNA干扰技术抑制MC3T3-E1细胞的NICD表达,在荧光倒置显微镜下观察到该转染细胞生长良好,qRT-PCR和Western blot实验结果表明NICD表达下调,表明NICD RNA干扰的MC3T3-E1细胞模型设置良好。为了观察NICD RNA干扰的MC3T3-E1细胞受到2 Gy照射损伤后对其增殖的影响,采用BrdU掺入法进行分析。BrdU可代替胸腺嘧啶核苷插入复制的DNA双链中,这种置换可稳定存在,并带到子代细胞中。用免疫学方法检测DNA中BrdU的含量,从而可以判断细胞的增殖能力。2 Gy照射剂量对前体成骨细胞、成骨细胞以及NICD RNA干扰的成骨细胞的增殖抑制作用是明显的,但2 Gy照射对NICD RNA干扰的前体成骨细胞的增殖无明显影响,这表明NICD低表达对MC3T3-E1的前体成骨细胞的增殖有保护作用。
为了揭示NICD RNA干扰的MC3T3-E1细胞受辐射损伤后的功能变化,我们分析了相关基因Runx2、ALP、RANKL、OPG和M-CSF的表达。Runx2是成骨细胞分化和骨质形成过程中一种重要的转录因子,是成骨细胞定向分化的重要标志。由MC3T3-E1细胞分化的前体成骨细胞经2 Gy照射后Runx2表达上升,而经NICD RNA干扰的前体成骨细胞受到2 Gy照射后Runx2表达下降可知,NICD RNA干扰对经2 Gy照射后的前体成骨细胞的定向分化有抑制作用。Wei等[19]通过抑制Runx2相关的AMP依赖的蛋白激酶降解,使Runx2表达降低,进而发现可以抑制成骨细胞分化。有文献表明Runx2过表达的转基因小鼠会表现出骨质减少症状[20]。抑制Runx2表达会减少成骨细胞的分化,同时ALP水平也会出现降低[21]。ALP是成骨细胞分化的重要标志性分子[22]。NICD RNA干扰的成骨细胞经2 Gy照射后ALP的表达水平下调,说明NICD表达下调能抑制受2 Gy照射后的成骨细胞的分化,减少骨质损伤。
成骨细胞对破骨细胞具有调控作用,这种调控是通过OPG/RANK/RANKL(RANK:核因子κB受体活化因子)系统来发挥作用的。成骨细胞表达的RANKL与破骨细胞表达的RANK结合,能诱导促进破骨细胞前体细胞分化为破骨细胞。OPG是成骨细胞表达的分泌性乙二醇蛋白,与RANKL竞争性地结合RNAK,但是并不能对破骨细胞发挥促进作用[23]。经2 Gy照射后的成骨细胞对RANKL的表达上调,这表明照射后的成骨细胞能提高破骨细胞的功能;NICD RNA干扰的MC3T3-E1细胞的成骨细胞经2 Gy照射后RANKL的表达水平下调,但并没有表现出降低破骨细胞的功能作用。经2 Gy照射后的前体成骨细胞和成骨细胞对OPG的表达下调,这表明辐射损伤后的细胞激活了破骨细胞的功能;而NICD RNA干扰的前体成骨细胞的OPG表达上调,表现出抑制破骨细胞功能的作用。M-CSF在破骨细胞的分化中起着非常重要的作用,其可以增强RANKL诱导的破骨细胞的骨吸收能力[24-25],照射后成骨细胞的M-CSF表达上升,促进了破骨细胞功能。相比之下,NICD RNA干扰的成骨细胞经2 Gy照射后,对M-CSF的表达明显下降,降低了破骨细胞功能。
本研究结果证实,抑制NICD表达可降低MC3T3-E1诱导的前体成骨细胞的增殖与分化,降低成骨细胞的增殖,从而减少骨质损伤。同时,抑制NICD表达的前体成骨细胞及成骨细胞通过调节Runx2、ALP、RANKL、OPG、M-CSF等基因的表达抑制前体成骨细胞分化,实现对破骨细胞功能的调节与抑制作用,进而减少骨丢失。这表明,NICD在辐射引起的成骨细胞与破骨细胞功能及分化的抑制中起到了重要的作用。此外,Runx2、ALP、RANKL、OPG、M-CSF等基因在辐射损伤的成骨细胞与破骨细胞之间的调节中至关重要。本研究为后续探究辐射后的骨重塑提供了有力依据。
利益冲突 本研究有署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 边佩鲜负责实验的实施、数据的提供、论文的起草与修订;杨冰、王静雅负责实验的实施与数据的提供;孙元明负责论文的审阅;龙伟负责论文命题的提出及方法设计。
| [1] | Brown SA, Guise TA. Cancer treatment-related bone disease[J]. Crit Rev Eukaryot Gene Expr, 2009, 19(1): 47–60. DOI:10.1615/CritRevEukarGeneExpr.v19.i1.20 |
| [2] |
杨文峰, 杨志祥, 胡燕, 等.
《外照射放射性骨损伤诊断标准》解读[J]. 国际放射医学与核医学杂志, 2012, 36(4): 227–230.
DOI:10.3760/cma.j.issn.1673-4114.2012.04.008 Yang WF, Yang ZX, Hu Y, et al. Explanation of Diagnostic Criteria for External Radiation Bone Injury[J]. Int J Radiat Med Nucl Med, 2012, 36(4): 227–230. DOI:10.3760/cma.j.issn.1673-4114.2012.04.008 |
| [3] | Hopewell JW. Radiation-therapy effects on bone density[J]. Med Pediatr Oncol, 2003, 41(3): 208–211. DOI:10.1002/mpo.10338 |
| [4] | Willey JS, Lloyd SA, Nelson GA, et al. Space Radiation and Bone Loss[J]. Gravit Space Biol Bull, 2011, 25(1): 14–21. |
| [5] | Willey JS, Lloyd SA, Robbins ME, et al. Early increase in osteoclast number in mice after whole-body irradiation with 2 Gy X rays[J]. Radiat Res, 2008, 170(3): 388–392. DOI:10.1667/RR1388.1 |
| [6] | Hamilton SA, Pecaut MJ, Gridley DS, et al. A murine model for bone loss from therapeutic and space-relevant sources of radiation[J]. J Appl Physiol (1985), 2006, 101(3): 789–793. DOI:10.1152/japplphysiol.01078.2005 |
| [7] | Chaves NAH, Machado D, Yano CL, et al. Antioxidant defense and apoptotic effectors in ascorbic acid and β-glycerophosphate-induced osteoblastic differentiation[J]. Dev Growth Differ, 2011, 53(1): 88–96. DOI:10.1111/j.1440-169X.2010.01232.x |
| [8] |
唐泉, 杨冰, 仲蕾蕾, 等.
电离辐射对MC3T3细胞增殖和Notch1、Jagged1基因表达的影响[J]. 辐射损伤与辐射工艺学报, 2012, 30(6): 374–377.
Tang Q, Yang B, Zhong LL, et al. Effects of ionizing radiation on MC3T3 cell proliferation and expression of Notch1 and Jagged1[J]. J Radiat Res Radiat Process, 2012, 30(6): 374–377. |
| [9] | Lai EC. Notch signaling:control of cell communication and cell fate[J]. Development, 2004, 131(5): 965–973. DOI:10.1242/dev.01074 |
| [10] | Siebel C, Lendahl U. Notch Signaling in Development, Tissue Homeostasis, and Disease[J]. Physiol Rev, 2017, 97(4): 1235–1294. DOI:10.1152/physrev.00005.2017 |
| [11] | Zanotti S, Canalis E. Notch and the skeleton[J]. Mol Cell Biol, 2010, 30(4): 886–896. DOI:10.1128/MCB.01285-09 |
| [12] | Bo Y, Yan L, Gang Z, et al. Effect of calcitonin gene-related peptide on osteoblast differentiation in an osteoblast and endothelial cell co-culture system[J]. Cell Biol Int, 2012, 36(10): 909–915. DOI:10.1042/CBI20110562 |
| [13] | Pérez-Campo FM, May T, Zauers J, et al. Generation and characterization of two immortalized human osteoblastic cell lines useful fo r epigenetic studies[J]. J Bone Miner Metab, 2017, 35(2): 150–160. DOI:10.1007/s00774-016-0753-z |
| [14] | Schmittgen TD, Livak KJ. Analyzing real-time PCR data by the comparative C(T) method[J]. Nat Protoc, 2008, 3(6): 1101–1108. DOI:10.1038/nprot.2008.73 |
| [15] | Gordon WR, Arnett KL, Blacklow SC. The molecular logic of Notch signaling-a structural and biochemical perspective[J]. J Cell Sci, 2008, 121(Pt 19): 3109–3119. DOI:10.1242/jcs.035683 |
| [16] | Mead TJ, Yutzey KE. Notch signaling and the developing skeleton[J]. Adv Exp Med Biol, 2012, 727: 114–130. DOI:10.1007/978-1-4614-0899-4_9 |
| [17] | Engin F, Yao Z, Yang T, et al. Dimorphic effects of Notch signaling in bone homeostasis[J]. Nat Med, 2008, 14(3): 299–305. DOI:10.1038/nm1712 |
| [18] | Bai S, Kopan R, Zou W, et al. NOTCH1 regulates osteoclastogenesis directly in osteoclast precursors and indirectly via osteoblast lineage cells[J]. J Biol Chem, 2008, 283(10): 6509–6518. DOI:10.1074/jbc.M707000200 |
| [19] | Wei J, Shimazu J, Makinistoglu MP, et al. Glucose Uptake and Runx2 Synergize to Orchestrate Osteoblast Differentiation and Bone Formation[J]. Cell, 2015, 161(7): 1576–1591. DOI:10.1016/j.cell.2015.05.029 |
| [20] | Franceschi RT, Xiao G. Regulation of the osteoblast-specific transcription factor, Runx2:responsiveness to multiple signal transduction pathways[J]. J Cell Biochem, 2003, 88(3): 446–454. DOI:10.1002/jcb.10369 |
| [21] | Liu W, Toyosawa S, Furuichi T, et al. Overexpression of Cbfa1 in osteoblasts inhibits osteoblast maturation and causes osteopenia with multiple fractures[J]. J Cell Biol, 2001, 155(1): 157–166. DOI:10.1083/jcb.200105052 |
| [22] | Harada H, Tagashira S, Fujiwara M, et al. Cbfa1 isoforms exert functional differences in osteoblast differentiation[J]. J Biol Chem, 1999, 274(11): 6972–6978. DOI:10.1074/jbc.274.11.6972 |
| [23] | Pivonka P, Zimak J, Smith DW, et al. Theoretical investigation of the role of the RANK-RANKL-OPG system in bone remodeling[J]. J Theor Biol, 2010, 262(2): 306–316. DOI:10.1016/j.jtbi.2009.09.021 |
| [24] | Hodge JM, Collier FM, Pavlos NJ, et al. M-CSF potently augments RANKL-induced resorption activation in mature human osteoclasts[J/OL]. PLoS One, 2011, 6(6): e21462[2018-01-24]. http://journals.plos.org/plosone/article?id=10.1371/journal.pone.0021462. DOI: 10.1371/journal.pone.0021462. |
| [25] |
韩英, 杨冰, 唐泉, 等.
电离辐射对原代成骨细M-CSF表达的影响[J]. 国际放射医学核医学杂志, 2013, 37(1): 5–8.
DOI:10.3760/cma.j.issn.1673-4114.2013.01.002 Han Y, Yang B, Tang Q, et al. Effects of radiation on macrophage colony stimulating factor in primary osteoblasts[J]. Int J Radiat Med Nucl Med, 2013, 37(1): 5–8. DOI:10.3760/cma.j.issn.1673-4114.2013.01.002 |
 2018, Vol. 42
2018, Vol. 42


