放射性核素全身骨显像是通过放射性核素检测骨组织的代谢异常,常用的显像剂为99Tcm-MDP。骨显像的原理是骨骼的主要无机盐成份--羟基磷灰石晶体,依靠化学吸附和离子交换从血液中获取99Tcm-MDP,并通过SPECT显像。99Tcm-MDP SPECT骨显像具有灵敏度高,能观察全身骨组织病变等特点,广泛用于骨外伤、感染、瘤样病变、转移性骨肿瘤等诊断。相关研究显示,外伤、手术创伤、放疗、各种原发及转移性肿瘤、大量胸腹腔积液、明显渗出及弥漫性炎性病变等均可引起99Tcm-MDP的非特异性摄取,但本例患者并无确切证据显示其双肺浓聚影与以上原因有关。本文通过综合分析患者病史、检查结果,并查阅文献,对本例患者双肺弥漫性摄取99Tcm-MDP的原因做出了比较合理的解释。
1 患者资料患者男性,52岁,因“腰骶部及双下肢疼痛且活动受限1年”入院。患者1年前无明显诱因出现腰骶部疼痛,进行性加重,伴活动受限。2017年4月在当地医院行MRI检查,结果提示:腰椎椎体多发骨质破坏并椎旁软组织占位,遂入我院骨科进一步诊治。该患者在治疗前签署了知情同意书。
患者入院后实验室检查结果:血红蛋白为132 g/L(正常值为130~175 g/L),红细胞为4.6×1012/L(正常值为4.3×1012/L~5.8×1012/L),血小板为138×109/L(正常值为125×109/L~350×109/L),尿素为5.82 mmol/L(正常值为2.86~8.20 mmol/L),肌酐水平为84 μmol/L(正常值为59~104 μmol/L),钙为2.38 mmol/L(正常值为2.1~2.6 mmol/L),降钙素原为0.31 ng/mL(正常值为 < 0.05 ng/mL),尿本周蛋白(+)。除降钙素原稍增高、尿本周蛋白异常外,其他检验结果均未见明显异常。红细胞沉降率、球蛋白、β2微球蛋白、轻链蛋白均未检查。患者行99Tcm-MDP SPECT全身骨显像结果示:双肺未见异常显影,多处肋骨、脊柱放射性分布不均(图 1中A)。CT显像示:胸腰椎、骨盆多发骨质破坏,第3腰椎节段周围软组织病变累及椎管;双侧胸腔积液并伴双肺下叶部分肺不张;双肺细支气管炎可能性。患者无特殊既往史及家族史。有明确的手术指征后,患者于2017年5月3日全身麻醉下行L3椎体肿瘤切除+钉棒系统内固定术,术后病理提示:L3椎体浆细胞瘤。患者术后恢复尚可。
|
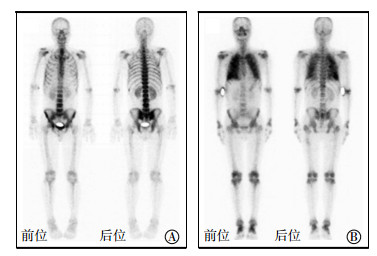
图 1 患者男性,52岁,多发性骨髓瘤,两次入院99Tcm-MDP SPECT全身骨显像图 图中,A:2017年4月27日全身骨显像示双肺未见异常显影,多处肋骨、脊柱放射性分布不均;B:2017年7月3日全身骨显像示双肺弥漫性异常放射性增高,L3椎体代谢异常,考虑术后改变;多根多处肋骨、T10、T12椎体代谢活跃,考虑受侵。 |
患者于2017年6月30日再次入院,入院后的实验室检查结果:血红蛋白为71 g/L,红细胞为2.5×1012/L,血小板为95×109/L,球蛋白为42 g/L(正常值为20~40 g/L),β2微球蛋白为33.91 mg/L(正常值为0.8~2.2 mg/L),轻链蛋白为5.72 g/L(正常值为0.93~2.42 g/L),尿本周蛋白(+),尿素为18.45 mmol/L,肌酐水平为596 μmol/L,钙为3.46 mmol/L,红细胞沉降率为96.0 mm/h(正常值为0~15 mm/h),降钙素原为3.52 ng/mL。行99Tcm-MDP SPECT全身骨显像结果示:双肺弥漫性异常放射性增高影;L3椎体代谢异常,考虑为术后改变;多处肋骨、T10、T12椎体代谢活跃,考虑受侵(图 1中B)。CT结果示:L3椎体浆细胞瘤术后L3椎体棘突及双侧附件缺如,L1、L2、L4椎体内可见内固定植入物,胸腰椎骨质密度降低,并可见多发骨质破坏(图 2中A);骨盆骨质密度降低,并可见多发骨质破坏(图 2中B);肺部双侧有少量胸腔积液并双肺下叶部分肺不张,双肺散在片絮状模糊影,考虑为炎性病变(图 2中C)。骨髓细胞形态学检查结果:浆细胞极度增生,其中幼浆细胞占0.5%,成熟浆细胞占22.5%,符合多发性骨髓瘤的骨髓象(图 3)。临床诊断为多发性骨髓瘤,合并急性肾功能衰竭、高钙血症、骨髓造血功能障碍及肺部感染。
|
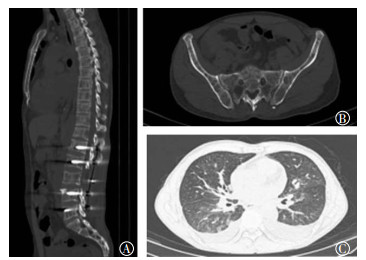
图 2 患者男性,52岁,多发性骨髓瘤,2017年6月30日入院脊柱、骨盆、肺部CT图像 图中,A:L3椎体浆细胞瘤术后L3椎体棘突及双侧附件缺如,L1、L2、L4椎体内可见内固定植入物,胸腰椎骨质密度降低,并可见多发骨质破坏;B:骨盆骨质密度降低,并可见多发骨质破坏;C:肺部有双侧少量胸腔积液并双肺下叶部分肺不张,双肺散在片絮状模糊影,考虑炎性病变。 |
|
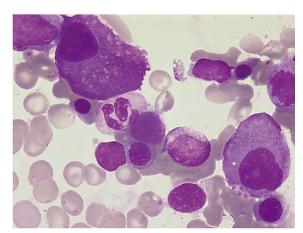
图 3 患者男性,52岁,多发性骨髓瘤,2017年6月30日入院骨髓细胞形态学检查(瑞氏染色,×400)。图中显示浆细胞极度增生,其中幼浆细胞占0.5%,成熟浆细胞占22.5%,符合多发性骨髓瘤的骨髓象。 |
多发性骨髓瘤的肿瘤细胞起源于骨髓中的浆细胞,浆细胞是B淋巴细胞发育到最终功能阶段的细胞。多发性骨髓瘤是B细胞淋巴瘤的一种,又称为浆细胞瘤[1],它的特征表现为骨髓浆细胞异常增生,伴有功能异常的单克隆免疫球蛋白或轻链蛋白过度生成,主要临床表现为广泛的溶骨性骨质破坏、肾功能损伤、高钙血症、贫血、感染等[2]。
多发性骨髓瘤常可致肾功能不全,主要原因是骨髓瘤细胞产生大量异常的单克隆免疫球蛋白或轻链蛋白,并经肾小球滤过进入肾小管,当其超出肾小管重吸收的能力时形成特殊管型,阻塞肾小管,引起肾功能受损[3]。肾功能不全使肾小球滤过率降低,肾排磷功能下降,血磷酸盐潴留,并与Ca2+结合引起血钙水平降低;高血磷同时可抑制肾脏分泌1α-羟化酶,使活性维生素D3(1,25-(OH)2-D3)生成障碍,引起小肠吸收及肾小管重吸收Ca2+减少,也使血钙含量降低[4];低血钙及高血磷使甲状旁腺代偿性增生,甲状旁腺激素分泌增多,继发性甲状旁腺功能亢进引起患者血钙升高,出现高钙血症[5]。高钙血症或血Ca×PO4>5.5 mmol/L时Ca2+将沿浓度梯度被动转运至细胞,并与线粒体结合形成非晶体状的羟磷灰石钙沉积或含Mg2+的晶体状钙磷复合物,若此类物质沉积于双肺组织中,则形成肺转移性微钙化[6-7]。转移性微钙化灶吸附99Tcm-MDP的原理与骨显像相似,即组织中的羟基磷灰石依靠化学吸附和离子交换从血液中获取99Tcm-MDP,并通过SPECT显影。不同类型的钙化灶与99Tcm-MDP的亲和能力有明显差异。研究显示,新形成的钙化灶与99Tcm-MDP的亲和能力比陈旧性钙化灶强[8];非晶体状的羟基磷灰石钙化与99Tcm-MDP的亲和能力比含Mg2+的晶体状钙磷复合物强[9]。双肺组织中若广泛存在新形成的钙化灶及非晶体状的羟基磷灰石钙化灶,就更易摄取99Tcm-MDP,并通过SPECT显像。
除了转移性钙化灶,还有其他原因引起骨外组织异常摄取99Tcm-MDP,例如:外伤、手术创伤、放疗、各种原发及转移性肿瘤、大量胸腹腔积液、明显渗出及弥漫性炎性病变等均有可能引起99Tcm-MDP的非特异性摄取[10]。本例患者无外伤及放疗史,既往仅接受过L3椎体手术,相关影像学检查未提示双肺及胸壁存在原发或转移性肿瘤,故可排除外伤、手术创伤、放疗、各种原发及转移性肿瘤引起99Tcm-MDP非特异性摄取的可能性,但不能完全排除大量胸腹腔积液、明显渗出及弥漫性炎性病变引起99Tcm-MDP非特异性摄取的可能性,本例患者为少量胸水及双肺较局限的炎性病变,若出现99Tcm-MDP非特异性摄取,SPECT不应表现为双肺前后位的弥漫性浓聚影。此外,结合患者病史及肾功能不全、高钙血症等临床表现,对于引起99Tcm-MDP双肺弥漫性显影的原因我们更倾向于转移性微钙化。诊断依据是多发性骨髓瘤可引起肾功能不全,通过诱发继发性甲状旁腺功能亢进导致高钙血症,此时Ca2+沿浓度梯度被动转运至肺泡细胞及支气管上皮细胞,与线粒体结合形成非晶体状的羟基磷灰石钙化灶,摄取99Tcm-MDP,因此SPECT表现为双肺弥漫性显影。
骨外组织转移性钙化灶非常微小,通过其他影像学检查手段很难发现。当双肺出现弥漫性转移性微钙沉积时,因Ca2+与细胞线粒体结合,抑制细胞有氧代谢,引起细胞缺氧及死亡,将出现严重的呼吸衰竭,患者预后极差[11]。虽然99Tcm-MDP显像对肺转移性微钙化的阳性诊断率偏低,但仍不失为一种可行的诊断及疗效评估的手段,可指导临床医师尽早采取积极的对症治疗,改善患者预后,降低病死率。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 陈婷负责研究命题的提出、设计,查阅文献,论文起草及修订;刘超负责数据、图像的获取、提供与分析;邓智勇负责研究命题的提出、设计及指导。
| [1] | Palumbo A, Anderson K. Multiple myeloma[J]. N Engl J Med, 2011, 364: 1046–1060. DOI:10.1056/NEJMra1011442 |
| [2] | Tan D, Chng WJ, Chou T, et al. Management of multiple myeloma in Asia: resource-stratified guidelines[J/OL]. Lancet Oncol, 2013, 14(12): e571-581[2017-11-20]. http://www.sciencedirect.com/science/article/pii/S1470204513704042?via%3Dihub. DOI: 10.1016/S1470-2045(13)70404-2. |
| [3] | Lescoat A, Rioux-Leclercq N, Vigneau C. Demonstration of the cause of acute renal failure in a case of IgD multiple myeloma[J]. Br J Haematol, 2014, 168(2): 162. DOI:10.1111/bjh.13177 |
| [4] | Keung YK, Norris S, Elks M, et al. Spurious hyperparathyroidism in a patient with multiple myeloma, hypercalcemia, and renal failure[J]. Am J Hematol, 1995, 50(1): 72. DOI:10.1002/ajh.2830500127 |
| [5] | Hsu HL. Multiple splenic tumors, hypercalcemia, and acute renal failure isolated splenic sarcoidosis[J/OL]. Gastroenterology, 2011, 140(1): e7-8[2017-11-20]. http://www.sciencedirect.com/science/article/pii/S0016508510003458?via%3Dihub. DOI: 10.1053/j.gastro.2010.01.062. |
| [6] | Kerr DN. Hypercalcemia and metastatic calcification[J]. Cardiovasc Res, 1998, 36(3): 293–297. DOI:10.1016/S0008-6363(97)00243-5 |
| [7] | Agarwal KK, Karunanithi S, Jain S, et al. Ovarian carcinoma producing parathyroid hormone-related protein causing hypercalcemia and metastatic calcification detected on 18F-FDG PET-CT[J]. Indian J Nucl Med, 2013, 28(4): 237–239. DOI:10.4103/0972-3919.121973 |
| [8] | Castaigne C, Martin P, Blocklet D. Lung, gastric, and soft tissue uptake of Tc-99m MDP and Ga-67 citrate associated with hypercalcemia[J]. Clin Nucl Med, 2003, 28(6): 467–471. DOI:10.1097/01.RLU.0000067505.24908.5C |
| [9] | Aso Y, Sato A, Tayama K, et al. Parathyroid carcinoma with metastatic calcification identified by technetium-99m methylene diphosphonate scintigraphy[J]. Internal Med, 1996, 35(5): 392–395. DOI:10.2169/internalmedicine.35.392 |
| [10] |
邹珍, 常娅妮, 武志芳.
常见的99Tcm-MDP骨扫描骨外摄取研究进展[J]. 国际放射医学核医学杂志, 2017, 41(2): 137–155.
DOI:10.3760/cma.j.issn.1673-4114.2017.02.011 Zou Z, Chang YN, Wu ZF. Extraosseous findings on bone scintigraphy and research progress of its mechanism[J]. Int J Radiat Med Nucl Med, 2017, 41(2): 137–155. DOI:10.3760/cma.j.issn.1673-4114.2017.02.011 |
| [11] | Matsuo T, Tsukamoto Y, Tamura M, et al. Acute respiratory failure due to 'pulmonary calciphylaxis' in a maintenance haemodialysis patient[J]. Nephron, 2001, 87(1): 75–79. DOI:10.1159/000045887 |
 2018, Vol. 42
2018, Vol. 42


