2. 528000, 佛山市第一人民医院医学病理科
2. Department of Pathology, the First People's Hospital, Foshan 528000, China
Rosai-Dorfman病(Rosai-Dorfman disease,RDD)又称窦组织细胞增生症伴巨大淋巴结病(sinus cell hyperplasia with massive lymphadenopathy,SHML),是一种罕见的良性淋巴组织增生性疾病,Rosai和Dorfman[1]于1969年对其做了详细研究并正式命名。根据病变累及范围可分为淋巴结型、结外型和混合型3种亚型,以淋巴结型最常见,表现为无痛性淋巴结肿大,常伴有发热;结外型罕见,可累及皮肤、上呼吸道(鼻腔、副鼻窦)、软组织、眼眶、中枢神经系统[2]。发生于骨且不伴淋巴结受累的结外型RDD罕见,至2017年3月国内外仅有24例关于骨RDD的报道(国内6例),该病因临床及影像学表现缺乏特异性从而易被误诊。本文报道2例骨骼RDD并复习相关文献,旨在拓展视野,以提高对该罕见疾病的认识。
1 资料与方法 1.1 病例资料病例1:男,28岁,于2012年2月至我院就诊,主因右肩部间断胀痛6个月余加重3 d入院。查体:体温38.1℃,右肩关节外旋受限,深度叩击痛,软组织未见肿胀及破溃。实验室检查:外周血WBC 18.98×109个/L,RBC 2.25×1012个/L,血红蛋白62 g/L,血沉28 mm/h,肝、肾功能正常,肿瘤12项未见异常。曾行骨髓穿刺抽出少许骨髓组织约0.3 cm,镜下有效成分太少不符合诊断条件,随后行开窗手术取右肱骨病变组织,经病理形态学及免疫组化确诊为右肱骨RDD。
病例2:女,39岁,于2013年6月至我院就诊,主因反复左枕部头痛10个月入院。患者10个月前无明显诱因出现左枕部轻度头痛,此后反复发作,无发热、头昏、呕吐,无视物不清,无肢体乏力。查体:左枕部局限性隆起,约1.5 cm×1.5 cm,质硬,固定,轻度压痛,无波动感,未见红肿。实验室检查:WBC 4.92×109个/L,中性粒细胞比值0.685,嗜酸性粒细胞0.016×109个/L,血红蛋白浓度119 g/L,血沉25 mm/h,肝、肾功能正常,肿瘤8项未见异常。手术切除物经病理形态学及免疫组化确诊为左顶骨RDD,头皮及脑膜均见累及。
1.2 影像学检查病例1:仅行数字化X线摄影(digital radiography,DR)检查,使用德国西门子AXIOM Aristos MX DR机,行正、斜位摄影。
病例2:CT扫描仅行常规平扫,使用日本东芝Aquilion 64排螺旋CT扫描机。MRI检查使用美国GE Signa Excite HD 3.0T超导型MR成像系统,采用SE T1WI(TR为500 ms,TE为20 ms)和FSE T2WI(TR为4500 ms,TE为80 ms)。增强T1WI对比剂为Gd-DTPA,浓度0.5 mol/L,剂量0.1 mL/kg,自肘静脉注药30 s后开始增强扫描,包括轴面、冠状面及矢状面,患者于增强扫描前签署知情同意书。影像学分析由2名有丰富骨关节影像诊断经验的高年资影像科医师完成。
1.3 病理切片制备标本中软组织和骨组织经10%中性甲醛固定,骨组织先进行脱钙处理,采用常规石蜡包埋切片,行苏木精-伊红染色及免疫组织化学标记,免疫组织化学标记采用Envision两步法。
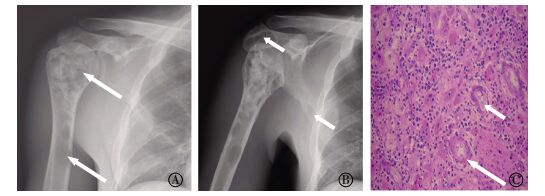
2 结果 2.1 影像学表现病例1:DR示右肱骨近中段骨髓腔条片状以低密度为主的溶骨性骨破坏,部分密度不均匀增高,未见骨膜反应,周围软组织未见肿块,伴右侧肩胛骨多发类似病灶(图 1中A、B),拟诊为慢性骨髓炎。
|
图 1 骨RDD患者X线表现和病理图 患者男性,28岁,图中,A:DR正位片示右肱骨中上段骨髓腔以低密度为主的混杂密度破坏,范围较广(长箭头);B:DR斜位片示右肩峰、右肩胛骨体部低密度破坏,密度均匀(短箭头),未见明显硬化与骨膜反应;C:光镜下见组织细胞(长箭头),胞浆内可见吞噬形态完整的淋巴细胞或浆细胞(短箭头,苏木精-伊红染色,×10);RDD:Rosai-Dorfman病;DR:数字化X线摄影。 Figure 1 X-ray findings and pathology figure of bone Rosai-dorfman disease patient |
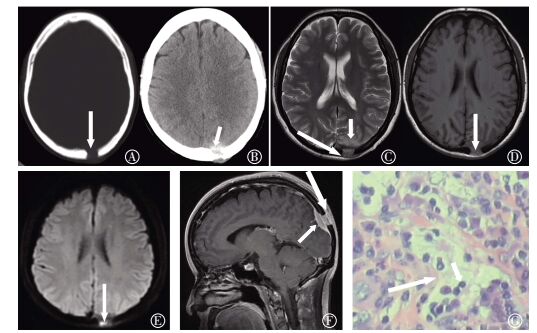
病例2:CT平扫骨窗示左侧顶骨后部局灶性骨破坏,范围约1.1 cm × 0.9 cm,破坏区呈低密度,边界清晰,未见钙化,累及板障与颅骨内外板,边缘未见硬化(图 2中A)。脑组织窗示顶骨破坏区临近头皮及脑膜增厚(图 2中B),未见钙化、坏死。MRI示左顶骨后部近中线处局限性骨质破坏,病灶自板障向颅骨内外板侵蚀合并周围软组织肿块,邻近左顶叶轻度受压并轻度水肿,病变T1WI及T2WI均呈中等信号,弥散加权成像(diffusion-weighted imaging,DWI)病灶部分呈高信号,注射Gd-DTPA后T1WI增强扫描显著强化(图 2中C~F),拟诊为嗜酸性肉芽肿。
|
图 2 颅骨RDD患者CT、MRI表现和病理图 患者女性,39岁,图中,A:CT平扫骨窗示左顶骨低密度骨质破坏,累及颅骨内外板及板障(长箭头),边缘未见硬化,密度均匀;B:CT平扫脑组织窗示顶骨骨破坏区周围软组织增厚(短箭头);C:轴位T2WI示左顶骨病灶呈稍高信号(长箭头),邻近脑实质水肿(短箭头);D:轴位T1WI示病灶呈中等信号(长箭头);E:轴位DWI示部分病灶呈高信号(长箭头);F:Gd-DTPA增强矢状面示病灶显著强化,侵犯头皮(长箭头)及邻近脑膜(短箭头);G:光镜下示纤维组织间见大量成片的合体细胞样组织细胞(长箭头),胞质丰富淡染,胞质内见淋巴细胞伸入(短箭头,苏木精-伊红染色,×20);RDD:Rosai-Dorfman病;DWI:弥散加权成像。 Figure 2 CT and MRI findings and pathology figure of skull Rosai-Dorfman disease patient |
病例1于DR中显示骨质破坏处凿开肱骨,刮取病灶及周围骨质,镜下呈明暗相间的结节状结构,明区可见片状分布的组织细胞,胞浆内可见吞噬形态完整的淋巴细胞(图 1中C)。免疫组化:窦组织细胞S-100(+),CD68(+),CD1a(-),CD23(-)。确诊为骨RDD。
病例2术中所见左顶骨大小约1 cm×1 cm的缺损,可见头皮及脑膜累及,肿瘤全切除,镜下病灶纤维组织间见大量成片的合体细胞样组织细胞,胞质丰富淡染,可见核仁,胞质内见中性粒细胞、浆细胞和淋巴细胞(图 2中G)。免疫组化:组织细胞S-100(+),CD68(+),CD1a(-),CD23(-),Ki-67约3%(+)。确诊为骨RDD。
3 讨论有关RDD最大宗的病例报告(包含423例)[2]来自耶鲁大学病案室,平均发病年龄为20.6岁,男性比女性更常见(58% vs. 42%);大多数患者表现为双侧颈部淋巴结无痛性肿大,43%的患者有淋巴结外侵犯,骨的累及明显罕见,只有33例(7%),其中24例并发淋巴结病,6例(1.4%)合并结外其他组织累及,仅3例(0.7%)表现为骨的单独发病。截至目前,国内仅有6例原发于骨且不伴有淋巴结累及的报道。骨RDD可发生在中轴骨和四肢骨,相对好发于长骨、颅骨及指(趾)骨等,大多为孤立性病灶,也有多灶性发生的报道[3],青年人多见,最小者仅10个月[4]。骨RDD临床多表现为局部胀疼、肿胀,可伴有低热和WBC升高、血沉加快、轻度贫血,但均不具有特异性,临床与影像学常误诊其为肿瘤或炎症性病变,其通常呈自限性病程,部分患者可自行消退[2, 5]。因此,正确诊断尤为重要,可避免患者过度的侵袭性治疗。
迄今为止,RDD的病因及发病机制尚不明确,部分学者认为RDD可能为某种感染因子导致淋巴结窦组织细胞异常增殖,使活性淋巴细胞的免疫功能抑制或丧失所致的一种免疫反应障碍性疾病[6]。病理学镜下呈明暗相间的结节状结构,明区可见一类体积大的组织细胞,其胞浆丰富,内见吞噬形态完整的淋巴细胞、浆细胞、嗜中性粒细胞和红细胞,被称之为淋巴细胞的吞噬现象或“伸入运动”。从病理学角度来看,明暗相间的结节状结构、淋巴细胞的吞噬现象以及组织细胞免疫化学S-100和CD68阳性、CD1a阴性,是诊断该病的可靠依据[7]。相对于淋巴结内RDD,骨发生的RDD吞噬炎细胞的组织细胞数量相对少,淋巴细胞伸入或吞噬现象不显著,故不易被查见[4, 8]。正如病理学家Kroft[7]所谓的RDD“如此熟悉却又神秘莫测”,极易将其误诊为炎症性病变、肉芽肿性疾病、IgG4相关性疾病、炎性肌纤维母细胞瘤、纤维组织细胞瘤、Langerhans细胞增生症等。
据文献描述,长骨RDD的X线表现通常是髓腔内溶骨性破坏,病灶大小为0.5~5.0 cm,可伴病理性骨折,病灶的边缘模糊或清晰但很少硬化[5, 9-12],中央钙化少见,长骨骨皮质破坏和周围软组织肿块很少发生[13-14],虽然髓腔内病变可以累及骨皮质或突破皮质累及周围软组织,但骨膜反应相对更少见[15]。国内仅见零星个案报道[16-19],其X线共同特点是病灶表现为低密度破坏影,不具有明确的硬化边。本组多数病灶与上述文献报道类似,至于病例1肱骨部分病灶密度不均匀增高,可能提示患者病程较长,破坏区一定程度上存在修复性成骨,首诊时误判为死骨,结合患者WBC升高,导致误诊为慢性骨髓炎。有文献报道骨RDD表现为单纯的成骨性破坏或者以硬化为主的骨破坏极其罕见[20]。骨RDD经皮质类固醇药物治疗和放疗可愈合,完全愈合的特征可能是病灶的边缘变薄、硬化,最终趋于消失[21]。
颅骨被认为是骨的孤立病变最常见的累及部位[5]。本组病例2颅骨病灶累及板障并突破颅骨内外板,侵犯邻近软组织,与长骨表现迥异,融骨性破坏伴软组织受累可能是颅骨RDD的特征之一[13-14]。颅骨嗜酸性肉芽肿也常表现为类圆形或卵圆形溶骨性骨缺损,自板障向内外板侵蚀的同时伴有软组织肿块,影像学表现与骨RDD类似,因此导致病例2首诊误诊,确诊依赖病理和免疫组织化学特征。骨RDD可以原发于骨组织,也可为临近的软组织肿块造成的骨侵蚀,CT扫描主要用于观察破坏区细节。MRI骨髓腔内病灶多为T1WI等或稍高信号、T2WI高信号,T2WI脂肪抑制序列及DWI通常呈高信号,T2WI脂肪抑制序列图像上病灶周围骨髓斑片状高信号提示可能存在水肿,当软组织受累时通常呈现类似骨髓内病灶的信号,MRI增强扫描常表现为病灶区域显著强化[22-23]。本组病例2的病灶信号和强化表现与以上文献报道一致。病例2病灶DWI表现为高信号,可能与病理学所见病灶内淋巴细胞、浆细胞、中性粒细胞和嗜酸性粒细胞成片浸润导致局部水分子扩散障碍有关。
RDD也可表现为无症状的多骨受累,有时DR很难发现微小病灶。放射性核素扫描常表现为病灶的核素摄取增加,对发现骨骼多发病灶的灵敏度较高,但难以区分病灶实体与灶周反应[24],对评估病变细节有所限制。快速扫描序列和大范围脂肪抑制DWI的应用,使MRI发现骨骼病灶的灵敏度和特异度相对提高,可尝试用于可疑部位的筛查,但由于MRI费用昂贵不利于全身扫描筛查。SPECT/CT既可满足全身成像的要求又可同时实现CT成像,可清晰显示局部骨结构改变,有助于RDD的系统性筛查,同时也便于随访观察、比对。
综上所述,骨骼RDD罕见,当青少年人群骨髓腔内单发或多发融骨性破坏、未伴明确硬化边与骨膜反应时应考虑到该病的可能,该病影像学表现没有特异性,须与骨髓炎、嗜酸性肉芽肿、Langerhans细胞增生症、淋巴瘤、浆细胞瘤、脑膜瘤、转移瘤等鉴别,确诊依赖病理形态和免疫组织化学特征。然而,由于骨RDD病理特征性细胞不明显和其不均匀性分布,可导致病理学误诊。当临床、影像、病理诊断不一致时,多学科讨论是获得正确诊断的必要条件。
| [1] | Rosai J, Dorfman RF. Sinus histiocytosis with massive lymphadenopathy. A newly recognized benign clinicopathological entity[J]. Arch Pathol, 1969, 87(1): 63–70. |
| [2] | Foucar E, Rosai J, Dorfman RF. Sinus histiocytosis with massive lymphadenopathy. Current status and future directions[J]. Arch Dermatol, 1988, 124(8): 1211–1214. DOI:10.1001/archderm.1988.01670080023011 |
| [3] | Li SY, Yan ZJ, Jhala N, et al. Fine needle aspiration diagnosis of Rosai-Dorfman disease in an osteolytic lesion of bone[J]. Cytojournal, 2010, 7: 12. DOI:10.4103/1742-6413.65058 |
| [4] |
王蔚, 陈炳旭, 陈晓东, 等.
累及骨和软骨Rosai-Dorfman病2例报告并文献复习[J]. 国际病理科学与临床杂志, 2012, 32(2): 124–129.
DOI:10.3969/j.issn.1673-7347.2012.02.007 Wang W, Chen BX, Chen XD, et al. Rosai-Dorfman disease of bone and cartilage:two case reports and review of the literature[J]. Int J Pathol Clin Med, 2012, 32(2): 124–129. DOI:10.3969/j.issn.1673-7347.2012.02.007 |
| [5] | Demicco EG, Rosenberg AE, Björnsson J, et al. Primary Rosai-Dorfman disease of bone:a clinicopathologic study of 15 cases[J]. Am J Surg Pathol, 2010, 34(9): 1324–1333. DOI:10.1097/PAS.0b013e3181ea50b2 |
| [6] | Davis BM, Mueller J, Netterville J. Pathology quiz case-Sinus histiocytosis with massive lymphadenopathy(Rosai-Dorfman disease)[J]. Arch Otolaryngol Head Neck Surg, 2006, 132(4): 455–456. DOI:10.1001/archotol.132.4.455 |
| [7] | Kroft SH. Rosai-Dorfman disease:familiar yet enigmatic[J]. Semin Diagn Pathol, 2016, 33(5): 244–253. DOI:10.1053/j.semdp.2016.05.008 |
| [8] |
张良运, 郭莉, 罗小平, 等.
颅骨Rosai-Dorfman病的病理诊断临床分析[J]. 中南医学科学杂志, 2014, 42(4): 367–369.
Zhang LY, Guo L, Luo XP, et al. Clinical and pathological diagnosis of skull Rosai-Dorfman disease[J]. Med Sci J Centr South Chin, 2014, 42(4): 367–369. |
| [9] | Bachmann KR, Dragoescu EA, Foster WC. Extranodal rosai-dorfman disease presenting as incidental bone tumor:a case report[J]. Am J Orthop(Belle Mead NJ), 2010, 39(11): e123–e125. |
| [10] | Hsu AR, Bhatia S, Kang RW, et al. Extranodal Rosai-Dorfman disease presenting as an isolated glenoid lesion in a high school athlete[J]. J Shoulder Elbow Surgery, 2012, 21(1): e6–e11. DOI:10.1016/j.jse.2011.05.017 |
| [11] | Walczak BE, Halperin DM, Bdeir RW. Orthopaedic case of the month a 50-year-old Woman with persistent knee pain[J]. Clin Orthop Relat Res, 2011, 469(12): 3527–3532. DOI:10.1007/s11999-011-2067-8 |
| [12] | Dean EM, Wittig JC, Vilalobos C, et al. A 16-year-old Boy with Multifocal, Painless Osseous Lesions[J]. Clin Orthop Relat Res, 2012, 470(9): 2640–2645. DOI:10.1007/s11999-012-2366-8 |
| [13] | Kang RW, Mcgill KC, Lin J, et al. Chronic ankle pain and swelling in a 25-year-old Woman:an unusual case[J]. Clin Orthop Relat Res, 2011, 469(5): 1517–1521. DOI:10.1007/s11999-011-1851-9 |
| [14] | Orvets ND, Mayerson JL, Wakely PE Jr. Extranodal Rosai-Dorfman disease as solitary lesion of the tibia in a 56-year-old woman[J]. Am J Orthop(Belle Mead NJ), 2013, 42(9): 420–422. |
| [15] | Baker JC, Kyriakos M, Mcdonald DJ. Primary Rosai-Dorfman disease of the femur[J]. Skeletal Radiol, 2017, 46(1): 129–135. DOI:10.1007/s00256-016-2515-3 |
| [16] |
周源, 汪栋, 乐美兆, 等.
胸骨Rosai-Dorfman病1例[J]. 中华胸心血管外科杂志, 2008, 24(6): 431.
DOI:10.3760/cma.j.issn.1001-4497.2008.06.034 Zhou Y, Wang D, Le MZ, et al. Sternal Rosai-Dorfman disease in 1 case[J]. Chin J Thorac Cardiovasc Surg, 2008, 24(6): 431. DOI:10.3760/cma.j.issn.1001-4497.2008.06.034 |
| [17] |
胡振彬. 脊柱骨肿瘤的临床、影像表现及病理对照研究[D]. 广州: 南方医科大学, 2016.
Hu ZB. The comparison of clinical, imaging and pathologic features in spinal tumors[D]. Guangzhou:Southern Medical University, 2016. http://cdmd.cnki.com.cn/Article/CDMD-12121-1016267766.htm |
| [18] |
王智园, 石灵春, 杨海峰, 等.
发生在指骨的Rosai-Dorfman病1例[J]. 实用医学杂志, 2010, 26(23): 4404.
DOI:10.3969/j.issn.1006-5725.2010.23.063 Wang ZY, Shi LC, Yang HF, et al. 1 case of Rosai-Dorfman disease occurred in the phalanx[J]. J Pract Med, 2010, 26(23): 4404. DOI:10.3969/j.issn.1006-5725.2010.23.063 |
| [19] |
刘春华, 徐杰, 黄惠梅, 等.
胫骨Rosai-Dorfman病一例报告[J]. 中国修复重建外科杂志, 2012, 26(6): 765–766.
Liu CH, Xu J, Huang HM, et al. A case report of tibial Rosai-Dorfman disease[J]. Chin J Reparative Reconstructive Surg, 2012, 26(6): 765–766. |
| [20] | Gupta P, Babyn P. Sinus histiocytosis with massive lymphadenopathy(Rosai-Dorfman disease):a clinicoradiological profile of three cases including two with skeletal disease[J]. Pediatr Radiol, 2008, 38(7): 821–822. DOI:10.1007/s00247-007-0701-0 |
| [21] | Paryani NN, Daugherty LC, O'connor MI, et al. Extranodal rosai-dorfman disease of the bone treated with surgery and radiotherapy[J]. Rare Tumors, 2014, 6(4): 5531. DOI:10.4081/rt.2014.5531 |
| [22] | Duijsens HM, Vanhoenacker FM, Ter BP, et al. Primary intraosseous manifestation of Rosai-Dorfman disease:2 case s and review of literature[J]. JBR-BTR, 2014, 97(2): 84–89. |
| [23] | Zaveri J, La Q, Yarmish G, et al. More than just Langerhans cell histiocytosis:a radiologic review of histiocytic disorders[J]. Radiographics, 2014, 34(7): 2008–2024. DOI:10.1148/rg.347130132 |
| [24] | Mannelli L, Monti S, Love JE, et al. Primary Rosai-Dorfman disease of the bone in a patient with history of breast cancer appearance on Tc-99m-MDP scintigraphy, CT, and x-ray[J]. Clin Nucl Med, 2015, 40(3): 247–249. DOI:10.1097/RLU.0000000000000595 |
 2017, Vol. 41
2017, Vol. 41


