胃部肿瘤定性主要依靠胃镜及活检病理结果,但胃镜对于肿瘤大小、局部侵犯范围、区域淋巴结转移及远处转移情况往往不能作出准确的判断,难以在治疗前全面评估肿瘤分期及指导诊疗。功能影像与解剖影像相结合的PET/CT是填补这一不足的重要的无创性检查手段,但由于设备昂贵、检查费用高,在临床上常常难以大规模地开展。我院采用18F-FDG SPECT/CT,为带有低剂量定位CT和SPECT的复合体,其在肿瘤的定位、定性诊断及疗效评价方面的性能优良[1-2],但图像分辨率不佳,对于病灶大小及侵犯范围的显示较模糊,对区域淋巴结及远处转移灶显示欠佳。我们将18F-FDG SPECT/CT与64排螺旋CT进行异机融合,以此弥补上述不足,更好地为患者提供诊断及治疗。
1 资料与方法 1.1 一般资料收集2015年1月至2016年12月在我院一周内分别行18F-FDG SPECT/CT和64排螺旋CT扫描的35例胃癌患者,其中,男性18例、女性17例,年龄35~86岁,平均年龄为(63.50±10.96)岁。入选患者符合以下3个条件:(1)经活检病理证实;(2)既往无其他恶性肿瘤病史;(3)患者系治疗前评估病情,治疗后评估疗效、监测有无复发或转移。35例患者共计56枚病灶,其中,28例患者可见胃部原发病灶,共计28枚(T组);12例患者存在区域淋巴结转移病灶,共计19枚(N组);7例患者存在肝脏等脏器转移病灶,共计9枚(M组)。
检查前均与患者谈话,所有患者同意并签署知情同意书。
1.2 显像方法检查前一周禁做胃肠道钡餐检查。CT扫描前5~10 min肌肉注射盐酸消旋山莨菪碱注射液(购自杭州民生药业有限公司)10~20 mg,开始扫描时即刻饮水500~1500 mL[3],采用美国GE公司生产的Lightspeed 64排VCT,从头扫描到股骨上段,扫描参数:120 kV,130 mAs,开启Care Dose 4D,螺距1.2,球管旋转时间0.5 s/圈,重建层厚0.75 mm,间隔0.5 mm。在工作站上的3D及Inspace软件中利用多平面重建、最大密度投影及容积再现等技术进行图像后处理。SPECT/CT显像仪器为美国GE公司生产的双探头符合线路Infinia VC Hawkeye 4型成像系统。患者安静休息10 min,控制空腹血糖<6.1 mmol/L或餐后血糖<7.8 mmol/L,将10 mg盐酸消旋山莨菪碱注入500 mL温水中混匀,患者饮用后,静脉注射185~296 MBq的18F-FDG后,静卧40~60 min,排尿后,再饮水500~1500 mL扩充胃肠道,之后进行显像。将图像传输至Xeleris 2工作站进行同机和异机CT图像与SPECT图像融合以及CT图像的多平面重建。
1.3 观察指标及图像质量分级观察指标主要包括病灶大小、数量及定位,边界是否清楚,融合图像是否有伪影。由3名经验丰富的主任医师对图像进行盲评打分,根据评分高低判断图像质量。采用3级法对图像质量进行分级:1级为可以清楚显示病灶大小及边界,且无伪影干扰;2级为可以显示病灶大小及边界,但边界不清;3级为可以显示病变,但无法准确判断病灶大小及边界[4]。
1.4 统计学方法采用SPSS 16.0软件对数据进行统计学分析。T、N、M 3组中异机融合与同机融合的图像质量分级对比采用卡方检验,以α=0.05为检验水准,P<0.05表示差异有统计学意义。
2 结果56枚病灶异机融合与同机融合的图像质量分级对比见表 1。在显示胃局部病灶的T组中,同机融合后图像质量为1、2、3级的病灶数量分别为8、14、6枚,异机融合分别为25、3、0枚,两者间差异有统计学意义(χ2=21.875,P<0.05);在显示转移淋巴结病灶的N组中,同机融合后图像质量为1、2、3级的病灶数量分别为7、5、7枚,异机融合分别为17、2、0枚,两者间差异有统计学意义(χ2=12.452,P<0.05);在显示远处脏器转移的M组中,同机融合后图像质量为1、2、3级的病灶数量分别为0、3、6枚,异机融合分别为8、1、0枚,两者间差异有统计学意义(χ2=15.000,P<0.05)。异机融合后病灶在代表图像质量优等的1级分类中的个数明显多于同机融合。异机融合后的图像质量明显优于同机融合,可提供更好的诊断依据(图 1、图 2)。
| 表1 56枚胃癌病灶在不同分组中的同机融合与异机融合图像质量的分级对比(个) Table 1 Comparison of image quality of 56 gastric cancer lesions among the three groups of T, N and M stages in the same and different machine fusions |

|
图 1 胃小弯侧胃癌患者18F-FDG SPECT/CT显像图 患者男性,45岁。图中,A:同机融合图像;B:异机融合图像。异机融合显示胃局部肿瘤的图像质量明显优于同机融合。 Figure 1 18F-FDG SPECT/CT images of the lesser curvature in the stomach of patients with gastric cancer |
|
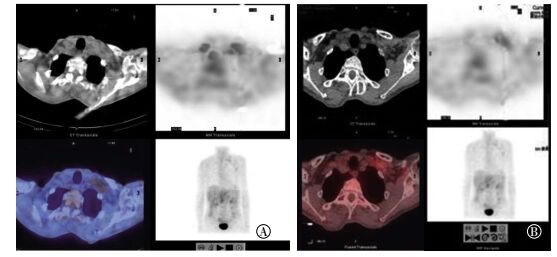
图 2 胃癌患者左锁骨后方肿大淋巴结18F-FDG SPECT/CT显像图 患者男性,55岁。图中,A:同机融合图像;B:异机融合图像。异机融合后图像对转移淋巴结病变的显示更清晰、明确。 Figure 2 18F-FDG SPECT/CT images of enlarged lymph nodes in patients with gastric cancer |
18F-FDG SPECT/CT图像虽然能基本满足临床诊断需要,但其在显示病灶形态、大小、密度方面不如64排CT图像,且图像伪影较重,特别是在胃癌原发病灶及转移病灶较小、转移淋巴结内部坏死、患者体内有金属植入物、骨转移灶和良性骨病的鉴别时常常难以准确定位、定性,极大地降低了诊断的准确率[5]。18F-FDG SPECT/CT图像常常仅能够提示病变性质,却难以精确定位和判断肿瘤分期,难以为临床提供充分的参考意见。64排螺旋CT扫描速度快,平扫图像空间分辨率及密度分辨率明显高于4排CT,能够精确定位及判断病灶大小、位置、密度,但却不能反映病变的代谢信息。
本研究进行18F-FDG SPECT/CT和64排螺旋CT图像异机融合,既以低成本实现了对病灶的精细定位,又能够反映病变的代谢特点,为病变的定位、定性提供有力帮助。18F-FDG SPECT/CT异机融合对转移性淋巴结及远处转移病灶的检出准确率非常高,这样更有利于治疗前分期,以及指导后续治疗方式,包括确定手术方式及放疗计划[6-7]。异机融合结合解剖与生物学信息,能较好地区分局部的肿瘤组织、水肿、坏死、瘢痕,亦能够鉴别肿瘤放疗后的组织坏死、炎症、纤维化及复发。本研究结果表明,异机融合弥补了SPECT/CT的许多不足之处,能够更好地服务于临床,为胃癌患者制定治疗方案、评价预后及监测复发提供准确的依据[8-9]。
本研究的不足之处包括以下方面:呼吸运动影响,在两次扫描之间患者不能做到呼吸幅度一致,致使后期异机融合不能完美匹配,影响诊断的准确率;辐射问题,患者行异机融合检查时必须接受两次CT扫描,增加额外辐射剂量。我们将在后续的研究中总结及改进以上问题。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 梁琰负责命题的提出、方法的设计;杜娟负责研究的实施、论文的撰写与修订;李展展、张永强、王昀璐、赵杰负责研究的实施及数据的收集。
| [1] |
何宗喜, 王文君, 顾华见, 等.
GE Infinia VC Hawkeye 4 SPECT/CT常见故障分析与处理[J]. 中国医疗设备, 2014, 29(3): 132–133.
DOI:10.3969/j.issn.1674-1633.2014.03.047 He ZX, Wang WJ, Gu HJ, et al. Analysis and troubleshooting of GE Infinia VC Hawkeye 4 SPECT/CT[J]. China Med Devices, 2014, 29(3): 132–133. DOI:10.3969/j.issn.1674-1633.2014.03.047 |
| [2] |
闫瑾, 林祥通.
PET预测及评价肿瘤疗效的新进展[J]. 国际放射医学核医学杂志, 2006, 30(4): 214–217.
Yan J, Lin XT. The new advance of prediction and evaluation of tumor therapeutic effects by PET[J]. Int J Radiat Med Nucl Med, 2006, 30(4): 214–217. |
| [3] |
张雪峰.
胃癌患者CT扫描前的准备技术[J]. 实用医技杂志, 2007, 14(19): 2550–2551.
Zhang XF. Preparation technique of CT scanning in patients with gastric cancer[J]. J Pract Med Tech, 2007, 14(19): 2550–2551. |
| [4] |
苏雪娟, 鲍红梅, 刘帆, 等.
经济型PET/CT与双源CT异机融合在肿瘤诊断中的应用[J]. 中国医学影像技术, 2012, 28(10): 1918–1921.
DOI:10.13929/j.1003-3289.2012.10.045 Su XJ, Bao HM, Liu F, et al. Application of fusion of coincidence PET/CT image and dual source CT image in diagnosis of tumors[J]. Chin J Med Imaging Technol, 2012, 28(10): 1918–1921. DOI:10.13929/j.1003-3289.2012.10.045 |
| [5] |
钱根年, 陈自谦, 赵春雷, 等.
影响PET/CT图像质量技术因素的探讨[J]. 中国医疗设备, 2011, 26(2): 12–14.
DOI:10.3969/j.issn.1674-1633.2011.02.004 Qian GN, Chen ZQ, Zhao CL, et al. Exploration of technology element of PET/CT imaging quality[J]. China Med Devices, 2011, 26(2): 12–14. DOI:10.3969/j.issn.1674-1633.2011.02.004 |
| [6] |
胡祥.
2014年第4版日本《胃癌治疗指南》更新要旨[J]. 中国实用外科杂志, 2015, 35(1): 16–19.
DOI:10.7504/CJPS.ISSN1005-2208.2015.01.05 Hu X. Japanese gastric cancer treatment guidelines-the 4th Edition 2014 update message[J]. Chin J Pract Surg, 2015, 35(1): 16–19. DOI:10.7504/CJPS.ISSN1005-2208.2015.01.05 |
| [7] |
陈峻青.
第4版日本《胃癌治疗指南》中7个"临床问题"解析[J]. 中国实用外科杂志, 2015, 35(4): 357–359, 435.
DOI:10.7504/CJPS.ISSN1005-2208.2015.04.04 Chen JQ. Explanation of the 7 clinical questions in Japanese gastric cancer treatment guidelines-the 4th edition 2014[J]. Chin J Pract Surg, 2015, 35(4): 357–359, 435. DOI:10.7504/CJPS.ISSN1005-2208.2015.04.04 |
| [8] | Charron M, Beyer T, Bohnen NN, et al. Image analysis in patients with cancer studied with a combined PET and CT scanner[J]. Clin Nucl Med, 2000, 25(11): 905–910. DOI:10.1097/00003072-200011000-00010 |
| [9] |
王昌军.
异机图像融合技术在临床中的应用[J]. 中国医疗设备, 2010, 25(4): 112–113, 81.
DOI:10.3969/j.issn.1674-1633.2010.04.050 Wang CJ. Image merger of different system in clinical[J]. China Med Devices, 2010, 25(4): 112–113, 81. DOI:10.3969/j.issn.1674-1633.2010.04.050 |
 2017, Vol. 41
2017, Vol. 41


