弥散加权成像(diffusion weighted imaging,DWI)作为目前唯一能监测活体组织内水分子扩散运动的无创性方法,在检出肝脏小病灶的应用中得到了充分的认可。钆塞酸二钠(gadolinium-ethoxibenzyl-diethylene triaminepentaacetic acid,Gd-EOB-DTPA)具有非特异性细胞外对比剂和肝胆特异性对比剂双重特性,其动态增强与延迟肝实质期扫描能提供病变形态、血供、细胞来源及肝功能等更多信息[1-2]。
我们对肝脏病变患者行Gd-EOB-DTPA增强前、后DWI检查,比较同一病灶不同时相表观弥散系数(apparent diffusion coefficient,ADC)值的变化情况,评估在肝脏增强扫描后行DWI的可行性。
1 资料与方法 1.1 一般资料收集2013年1月至2015年12月由我院收治的96例肝脏病变患者,均经临床或病理证实,另选30名例行体检的健康志愿者,共126例,其中,男性66例、女性60例,年龄36~70岁,平均(50.2±5.6)岁。96例肝脏病变患者中原发性肝癌25例、转移性肝癌20例、肝血管瘤28例、肝囊肿23例。所有受检者检查项目均经我院医学伦理会同意,并于检查前签署了知情同意书。
1.2 仪器与方法采用荷兰Philips公司Achieva 1.5T双梯度超导MR成像系统,梯度场强为66 mT/m和33 mT/m,梯度切换率为90 mT/(m·s)和180 mT/(m·s),SENSE Body线圈。
平扫包括:①轴位同相位T1快速场回波序列(T1-FFE-IP),重复时间(time of repeat,TR)137 ms、回波时间(time of echo,TE)4.6 ms、层数25、层厚6 mm、层间距1 mm、激励次数1、扫描时间26 s,二次闭气扫描;②轴位正反相位快速场回波序列(dual-FFE),TR 101 ms、TE 4.6和2.3 ms、层数25、层厚6 mm、层间距1 mm、激励次数1、扫描时间26 s,二次闭气扫描;③轴位呼吸门控多b值弥散加权序列(DWI-4b-RT)。
增强扫描采用闭气高分辨率各向同性容积激发序列(e-THRIVE-BH),TR 3.4 ms、TE 1.6 ms、层数25、层厚6 mm、层间距1 mm、激励次数1、扫描时间14 s。分别行动脉期、静脉期、3 min期、10 min期、20 min期、30 min期轴位扫描。在5 min期,行轴位呼吸门控T2加权精准频率反转恢复序列(T2W-SPAIR)扫描,TR 1128 ms、TE 85 ms、反转时间180 ms、层数25、层厚6 mm、层间距1 mm、激励次数1、扫描时间210 s;在15 min期,行轴位呼吸门控序列DWI-4b-RT扫描,接着行冠状位T2加权快速自旋回波闭气扫描序列(T2W-TSE-BH)扫描,TR 3.3 ms、TE 1.7 ms、层数18、层厚5 mm、层间距1 mm、激励次数1、扫描时间15 s;在25 min期,行轴位呼吸门控序列DWI-4b-RT扫描。
DWI-4b-RT为单次激发自旋回波-平面回波成像(SE-EPI)序列,TR 1137 ms、TE 59 ms、层数25、层厚6 mm、层间距1 mm、激励次数2,在频率编码、相位编码及层面选择3个方向上同时施加扩散敏感梯度场,b值取0、50、300、600 s/mm2,扫描时间196 s。
平扫DWI后,采用美国Medrad公司AVA 500 DCOV高压注射器由肘静脉向患者注射0.025 mmol/kg剂量的Gd-EOB-DTPA,再用20 ml生理盐水冲管。在高压注射器注射后约20~25 s,启动动脉期轴位e-THRIVE-BH。
1.3 图像后处理在Philips EWS工作站上,通过ADC分析函数,把b值为50、300、600 s/mm2的DWI像与b值为0的DWI像相减,生成该b值在平扫期、15 min期及25 min期的ADC图。在ADC图上,健康志愿者取不同区域5个ROI进行ADC值测量,取平均值作为正常肝脏的ADC值;原发性肝癌、转移性肝癌、肝血管瘤、肝囊肿患者取最具代表性的病灶勾画ROI,测量并作为该疾病的ADC值。
1.4 统计学分析采用SPSS 17.0统计学软件进行分析,同一b值下同一病灶在平扫期、15 min期、25 min期的ADC值符合正态性分布及方差齐性要求,进一步行t检验。P<0.05表示差异具有统计学意义。
2 结果在DWI像上,30名健康志愿者肝实质为等信号,胆管及血管为低信号。25例原发性肝癌患者大多数病灶表现为混杂信号,b值增大,病灶信号强度稍有降低,但仍高于肝实质(图 1)。20例转移性肝癌患者中原发灶有10例肺癌、4例鼻咽癌、4例前列腺癌、2例乳腺癌,其中11例肝脏病灶中心为低信号,b值越大,信号强度越低(图 2)。28例肝血管瘤患者病灶表现为均匀等或稍高信号,b值越大,病灶信号强度越低(图 3)。23例肝囊肿患者b值越大,病灶信号强度下降越明显(图 4)。
|
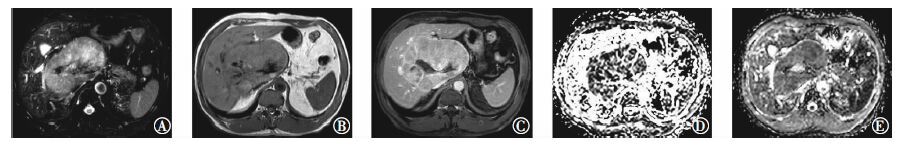
图 1 原发性肝癌患者(女性,56岁)的T2加权像、T1加权像和ADC图。图中,T2加权像(A)、平扫T1加权像(B)、静脉期T1加权像(C)可见肝门部并累及肝尾叶S8段大小约13.2 cm×8.1 cm巨大肿块,T1加权像呈低信号,T2加权像呈稍高信号,动脉期明显不均匀强化,静脉期持续强化,延迟期呈低信号;D、E为25 min期在b=50、600 s/mm2下的ADC图,ADC值分别为1.26×10-3 mm2/s和1.18×10-3 mm2/s;ADC:表观弥散系数。 Figure 1 The T2 weighted images,T1 weighted images and apparent diffusion coefficient images of primary liver cancer patient |
|
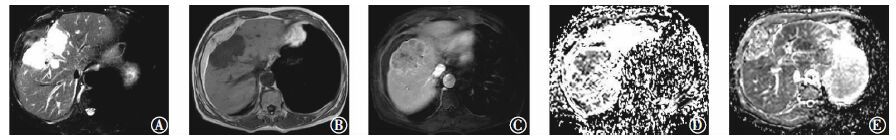
图 2 转移性肝癌患者(男性,47岁)的T2加权像、T1加权像和ADC图。图中,T2加权像(A)、平扫T1加权像(B)、3 min期T1加权像(C)可见右肝内侧S8段大小约4.90 cm×7.56 cm肿块,T1加权像呈低信号、T2加权像呈高信号,肿块强化不均匀,呈边缘环状强化;D、E为25 min期在b=50、600 s/mm2下的ADC图,ADC值分别为1.41×10-3 mm2/s和1.31×10-3 mm2/s;ADC:表观弥散系数。 Figure 2 The T2 weighted images,T1 weighted images and apparent diffusion coefficient images of metastatic liver cancer patient |
|
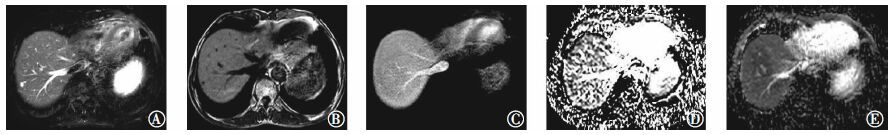
图 3 肝血管瘤患者(男性,51岁)的T2加权像、T1加权像和ADC图。图中,T2加权像(A)、平扫T1加权像(B)、10 min期T1加权像(C)可见肝右叶前S7段直径约1.1 cm的结节,边界清楚,T1加权像呈低信号、T2加权像呈高信号,信号均匀,动脉期结节边缘强化,静脉期、5 min期结节强化明显,10 min期、20 min期及30 min期强化逐渐减低;D、E为15 min期在b=50、600 s/mm2下的ADC图,ADC值分别为2.12×10-3 mm2/s和1.96×10-3 mm2/s;ADC:表观弥散系数。 Figure 3 The T2 weighted images,T1 weighted images and apparent diffusion coefficient images of hepatic hemangioma patient |
|
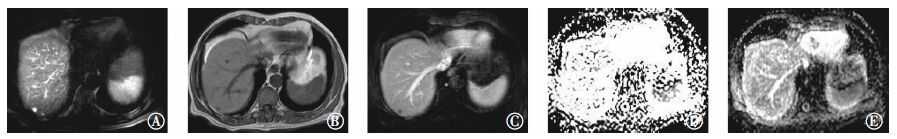
图 4 肝囊肿患者(女性,44岁)的T2加权像、T1加权像和ADC图。图中,T2加权像(A)、平扫T1加权像(B)、20 min期T1加权像(C)可见肝右叶后S7段直径约1.0 cm的结节,T1加权像呈低信号、T2加权像呈高信号,增强扫描后,结节未见明显强化;D、E为15 min期在b=50、600 s/mm2下的ADC图,ADC值分别为2.61×10-3 mm2/s和2.45×10-3 mm2/s;ADC:表观弥散系数。 Figure 4 The T2 weighted images,T1 weighted images and apparent diffusion coefficient images of hepatic cyst patient |
正常肝脏ADC图,肝实质为等信号,胆管和血管为高信号。原发性肝癌、转移性肝癌、肝血管瘤、肝囊肿在ADC图的信号强度与DWI像上的表现正好相反。同一性质病灶在同一b值下,ADC值为平扫期>25 min期>15 min期,但差异无统计学意义(t=0.25~1.29,均P>0.05);同一性质病灶在同一时相下,ADC值随b值增大而减小(b=50时>b=300时>b=600时),但差异亦无统计学意义(t=0.34~1.21,均P>0.05)。原发性肝癌、转移性肝癌的ADC值明显低于肝血管瘤、肝囊肿和正常肝脏,且差异具有统计学意义(t=5.28~10.24,均P<0.05),肝血管瘤、肝囊肿的ADC值低于正常肝脏,但差异无统计学意义(t=0.41~1.09,均P>0.05)(表 1)。
从表 1数据中发现,同一b值时,ADC最大降幅[即:(平扫期ADC值-15 min期ADC值)/平扫期ADC值]在正常肝脏中小于5.9%,在原发性肝癌中小于7.3%,在转移性肝癌中小于9.0%,在肝血管瘤中小于5.6%,在肝囊肿中小于5.2%。
| 表1 不同b值下各类肝脏疾病在不同时相的ADC值(×10-3 mm2/s) Table 1 Apparent diffusion coefficient values of various liver diseases under different b values at different time(×10-3 mm2/s) |
DWI的扩散敏感度常用b值来表示,在高b值情况下,扩散速度快慢的差异能够得到最佳地显示,指定b值的DWI像与b值为0时的DWI像相减,便是该b值下组织的ADC图。扩散速度快的组织具有较高的ADC值,在DWI像上表现为较低的信号,据此可以对不同病变进行鉴别。
Kenis等[3]和Golfieri等[4]的研究结果显示,在对肝转移瘤的检出上,DWI的灵敏度显著高于T2加权像,与动态对比增强相比无显著差异。Hardie等[5]和Lee等[6]的研究结果显示,在对直径≤1.0 cm的转移瘤的检出率上,DWI高于动态对比增强,但在对直径>1.0 cm的转移瘤的检出率上,二者无明显差异。荣凡令等[7]发现,在b=150 s/mm2时,肝血管瘤、肝囊肿信号强度很高,明显高于肝细胞癌和肝转移瘤,在b=800 s/mm2 时,信号明显下降,但仍高于正常肝脏组织。
在体内,Gd-EOB-DTPA一半由肾脏排泄,一半由肝胆道系统排泄,产生的肝脏强化是双期的,在静脉团注早期,产生类似Gd-DTPA动态增强效果。5 min后,肝脏T1信号强度呈现快速上升趋势,此后肝细胞对造影剂的摄取和滞留,使肝脏T1信号仍持续上升,但速度已减慢,约20 min后达到肝脏强化高峰,大约持续2 h,最后胆汁开始排泄,肝脏T1信号缓慢下降,胆道系统出现强化。
关于静脉注射Gd-EOB-DTPA对DWI的影响,国内外研究存在争论,多数研究结果显示静脉注射Gd-EOB-DTPA不会影响ADC值的测量,可以在增强扫描后行DWI扫描[3-5]。Purysko等[8]通过对63例肝脏肿瘤患者行多时相多b值DWI,发现Gd-EOB-DTPA对增强前后的ADC值没有影响,在增强后行DWI是可行的。Katsube等[9]在注射Gd-EOB-DTPA后,行肝脏5 min期、15 min期、25 min期DWI,发现增强后各期的ADC值与平扫期对比差异不大,认为对比剂的顺磁性效应对肝脏的扩散运动影响有限。Gulani等[10]通过观察平扫以及静脉注射Gd-EOB-DTPA后1~13 min肝脏、肾脏、脾脏DWI的信号强度及ADC值的变化,发现增强扫描后肝脏、肾脏的DWI信号强度及ADC值显著降低。
我们对肝脏行DWI后,发现原发性肝癌、转移性肝癌的ADC值最低,远低于肝血管瘤、肝囊肿及正常肝脏;肝血管瘤和肝囊肿的ADC值低于正常肝脏,但差异不大。同一病灶在相同的b值下,各个时相的ADC值不尽相同,平扫期ADC值最大,15 min期最小,25 min期居中,ADC值在注射Gd-EOB-DTPA后不断下降,15 min后再缓慢恢复,大约25 min后基本上与平扫期ADC值一致。b值越小,ADC值下降的幅度越大;b值越大,降幅越小。从总体降幅上看,正常肝脏<5.9%,原发性肝癌<7.3%,转移性肝癌<9.0%,肝血管瘤<5.6%,肝囊肿<5.2%。原因可能在于Gd-EOB-DTPA为小分子,对细胞外间隙的影响不明显,另外还有可能是Gd-EOB-DTPA的黏滞度与血浆的黏滞度接近,对水分子的扩散产生不了明显的影响。
肝脏DWI的信噪比较低,在与肺、含气肠道等气体交界面上有明显的磁敏感伪影。ADC 值的大小与b 值有关,低b值时,信噪比较高,DWI图像清晰,但受部分微循环血流灌注的影响,测得的ADC 值偏高;高b 值时,图像信噪比较低,磁敏感伪影较大,但可忽略血流灌注的影响,测得的ADC 值较接近肝脏的扩散系数值,更能反映组织的扩散特性[11]。要想获得清晰而又受血流灌注影响小的DWI像,须根据机器及参数选择合适的b 值,通过查阅资料,结合所分析的患者资料,我们认为选择b=600 s/mm2比较合适,既能获得清晰的图像,又能很好地反映组织的扩散特性。
静脉注射Gd-EOB-DTPA后,肝脏平扫与增强后的ADC值无明显差异,说明增强后行DWI获得的效果与平扫DWI一致。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 李伟负责设计研究命题、数据的获取与分析、论文的撰写与修订;龙晚生负责数据的获取、提供与分析,论点的提供;崔恩铭负责研究过程的实施,数据的获取、提供与分析;罗学毛、黄列彬、蒋基荣负责数据的获取、提供。
| [1] | Goshima S, Kanematsu M, Watanabe H, et al. Gd-EOB-DTPA-enhanced MR imaging:prediction of hepatic fibrosis stages using liver contrast enhancement index and liver-to-spleen volumetric ratio[J]. J Magn Reson Imaging, 2012, 36(5): 1148–1153. DOI:10.1002/jmri.23758 |
| [2] | Kudo M. Will Gd-EOB-MRI change the diagnostic algorithm in hepatocellular carcinoma?[J]. Oncology, 2010, 78(Suppl 1): S87–S93. DOI:10.1159/000315235 |
| [3] | Kenis C, Deckers F, De Foer B, et al. Diagnosis of liver metastases:can diffusion-weighted imaging(DWI) be used as a stand alone sequence?[J]. Eur J Radiol, 2012, 81(5): 1016–1023. DOI:10.1016/j.ejrad.2011.02.019 |
| [4] | Golfieri R, Renzulli M, Lucidi V, et al. Contribution of the hepatobiliary phase of Gd-EOB-DTPA-enhanced MRI to Dynamic MRI in the detection of hypovascular small(≤2 cm) HCC in cirrhosis[J]. Eur Radiol, 2011, 21(6): 1233–1242. DOI:10.1007/s00330-010-2030-1 |
| [5] | Hardie AD, Naik M, Hecht EM, et al. Diagnosis of liver metastases:value of diffusion-weighted MRI compared with gadolinium-enhanced MRI[J]. Eur Radiol, 2010, 20(6): 1431–1441. DOI:10.1007/s00330-009-1695-9 |
| [6] | Lee SA, Lee CH, Jung WY, et al. Paradoxical high signal intensity of hepatocellular carcinoma in the hepatobiliary phase of Gd-EOB-DTPA enhanced MRI:initial experience[J]. Magn Reson Imaging, 2011, 29(1): 83–90. DOI:10.1016/j.mri.2010.07.019 |
| [7] |
荣凡令, 徐青, 徐田勇.
低b值DWI在肝左叶小病灶中的应用价值[J]. 中国中西医结合影像学杂志, 2015, 13(1): 4–6.
Rong FL, Xu Q, Xu TY. Application value of lower b-value DWI to small lesions in the left liver lobe[J]. Chin Imaging J Integr Tradit West Med, 2015, 13(1): 4–6. DOI:10.3969/j.issn.1672-0512.2015.01.002 |
| [8] | Purysko AS, Remer EM, Veniero JC. Focal liver lesion detection and characterization with GD-EOB-DTPA[J]. Clin Radiol, 2011, 66(7): 673–684. DOI:10.1016/j.crad.2011.01.014 |
| [9] | Katsube T, Okada M, Kumano S, et al. Estimation of liver function using T1 mapping on Gd-EOB-DTPA-enhanced magnetic resonance imaging[J]. Invest Radiol, 2011, 46(4): 277–283. DOI:10.1097/RLI.0b013e318200f67d |
| [10] | Gulani V, Willatt JM, Blaimer M, et al. Effect of contrast media on single-shot echo planar imaging:implications for abdominal diffusion imaging[J]. J Magn Reson Imaging, 2009, 30(5): 1203–1208. DOI:10.1002/jmri.21945 |
| [11] | Kinner S, Umutlu L, Blex S, et al.Diffusion weighted MR imaging in patients with HCC and liver cirrhosis after administration of different Gadolinium contrast agents:is it still reliable?[J/OL].Eur J Radiol, 2012, 81(4):e625-e628[2016-08-25].http://www.sciencedirect.com/science/article/pii/S0720048-X12000228.DOI:10.1016/j.ejrad.2011.12.042. |
 2017, Vol. 41
2017, Vol. 41


