2. 内蒙古自治区第六地质矿产勘查开发院, 内蒙古 海拉尔 021008
2. Inner Mongolia Sixth Institute of Geology and Mineral Exploration, Hailar 021008, Inner Mongolia China
油页岩是一种含有可燃性固体有机质的沉积岩,由有机质和无机矿物质组成,低温干馏可获得类似原油的油页岩油,因此有“人造石油”之称[1].油页岩作为一种重要的非常规能源,因其储量巨大而引起全世界关注,被认为是石油和天然气的重要补充和替代能源[2-3].油页岩中含有的大量黏土矿物(蒙脱石、高岭石、伊利石等)不但对油页岩热解具有催化作用[4-5],还因其独有的结构特性(比表面积大、孔隙率高等)对金属离子具有良好的交换性和选择吸附性[6-10].前人[11-14]在研究过渡金属盐对页岩油干馏提取的催化作用时发现,钴盐对油页岩干馏具有一定的催化作用.为深入开展工作,本文针对油页岩对Co2+的吸附性能和吸附动力学方面进行研究,希望有助于进一步探索金属盐催化剂在油页岩热解中的催化作用及反应机理.
1 实验部分 1.1 主要试剂与仪器实验所用油页岩样品来自吉林省桦甸矿区,样品经粉碎、过筛、收集不同粒度范围的油页岩样品为实验备用.药品六水合氯化钴为分析纯试剂;实验用水为去离子水.
实验用仪器包括BB200WC型碎样机(德国RETSCH公司);PHS-3CT型数字pH计;电子分析天平;DZG-6210型电热真空干燥箱;iCAP 6000型电感耦合等离子体发射光谱仪(美国Thermo公司).
1.2 吸附实验准确量取一定初始浓度的Co2+金属离子溶液于250 mL烧杯中,加入一定质量的油页岩样品.静置至吸附平衡后,用电感耦合等离子体发射光谱仪(ICP-OES)测定清液中剩余Co2+的浓度.油页岩Co2+的吸附率(R,%)和吸附量(qe,10-6)用如下公式计算[15-16]:
| $ R=\frac{C_{0}-C_{\rm e}}{C_{0}} \times 100 $ | (1) |
| $ q_{\mathrm{e}}=\frac{\left(C_{0}-C_{\mathrm{e}}\right) V}{m} $ | (2) |
公式中:R为油页岩对溶液中Co2+的吸附率,qe为饱和吸附量,即达到吸附平衡时样品的吸附容量(10-6),C0为溶液的初始浓度即吸附前Co2+的浓度(mg/L),Ce为吸附达到平衡后溶液中剩余的Co2+离子的浓度即吸附后Co2+的浓度(mg/L),V为所取Co2+溶液的体积(mL),m是油页岩样品的质量(g).
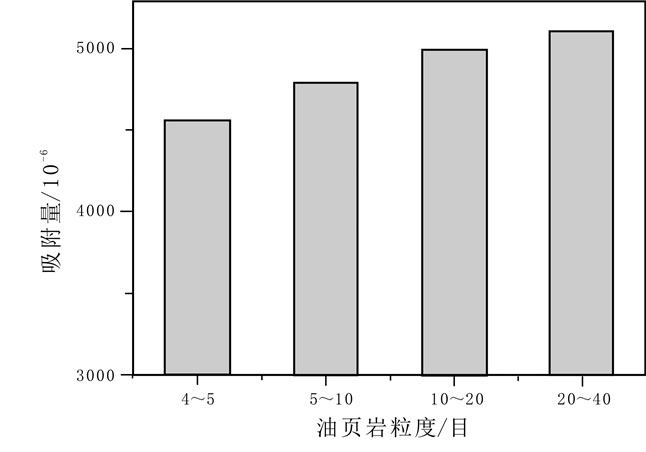
2 结果与讨论 2.1 样品粒度对Co2+吸附的影响准确量取初始浓度为245.0 mg/L的Co2+离子溶液50 mL于一组250 mL烧杯中,在室温20 ℃,自然pH条件下,分别加入1.0 g不同粒度的油页岩样品,静态吸附30 h,测溶液中Co2+含量,研究样品粒度对Co2+的吸附影响.结果表明(图 1),随着油页岩样品粒径的减小,油页岩对Co2+的吸附量呈逐渐增大的趋势.分析实验结果可知,油页岩对Co2+的吸附量随着样品粒径的减小而增大,主要原因是样品粒度减小,端面破键增多,阳离子交换能力略有增加.同时,粒度减小,比表面积增大,物理吸附也明显增强,总体结果是随粒度减小,吸附量增加.考虑到油页岩样品保存及应用对样品粒度的要求,在本文其他实验中,均选用5~10目粒级的油页岩样品.
|
图 1 油页岩粒度对吸附Co2+效果的影响 Fig.1 Effect of oil shale grain size on the Co2+ adsorption |
在室温20 ℃,自然pH条件下,在一组250 mL烧杯中分别加入Co2+初始浓度为82.1、125.8、187.5、240.5、302.5和345.9 mg/L的溶液50 mL,再分别加入1.0 g油页岩,静态吸附36 h,检测溶液中残余Co2+浓度,实验结果(表 1)表明,Co2+初始浓度直接影响油页岩对Co2+的吸附量和吸附率.随着溶液中Co2+初始浓度的增加,油页岩对Co2+离子的平衡吸附量和吸附总量逐渐增加.在Co2+的初始浓度小于240 mg/L时,吸附总量由2870×10-6增加到5140×10-6,吸附量增加的幅度较大,而浓度大于240 mg/L时,吸附总量为5160×10-6、5264×10-6,其增加幅度明显减小.油页岩对Co2+离子的吸附率表现出相反的变化规律.随着Co2+离子初始浓度的增加,油页岩对其吸附率明显降低.
|
|
表 1 初始浓度对油页岩吸附Co2+离子的影响 Table 1 Effect of Co2+ initial concentration on the adsorbability of oil shale |
在一组250 mL烧杯中加入Co2+初始浓度为289.4 mg/L的溶液50 mL,调节溶液pH为3.0~8.0,再分别加入1.0 g油页岩,静态吸附48 h后,检测溶液中残余Co2+含量.研究溶液pH值对油页岩吸附Co2+的影响.实验结果(图 2)表明,油页岩对Co2+离子的吸附量和吸附率均随溶液pH值的增大而增大.在较强的酸性条件下(pH为3和4时),不利于油页岩对Co2+的吸附,其吸附效果较差.因为在酸性环境下,溶液中的H+浓度较大,H+与Co2+均为正离子,两者发生吸附竞争,但H+半径远小于Co2+半径且H+的扩散速率较大,H+优先吸附到颗粒表面上. H+吸附于油页岩颗粒表面后,中和颗粒表面的OH-,降低了颗粒对Co2+的亲和力,致使油页岩对Co2+吸附量降低[17-18].在中性条件下(pH=7),油页岩对Co2+达到很好的吸附效果.当溶液pH值为8时,溶液中有絮状沉淀生成,根据化合物的沉淀溶解平衡常数溶度积Ksp值可以计算出在此浓度下溶液中的Co2+离子在pH值为7.68时生成氢氧化钴.因此溶液pH值过高,达到临界pH值后,其吸附量和吸附率是油页岩实际对Co2+吸附和生成氢氧化钴沉淀共同作用的结果.因此在实际应用油页岩对金属离子的吸附性能时,要选取适当的pH范围.

|
图 2 溶液pH值对油页岩吸附Co2+离子的影响 Fig.2 Effect of pH value of Co2+ solution on the adsorbability of oil shale 1—吸附总量(adsorption amount);2—吸附率(adsorption rate) |
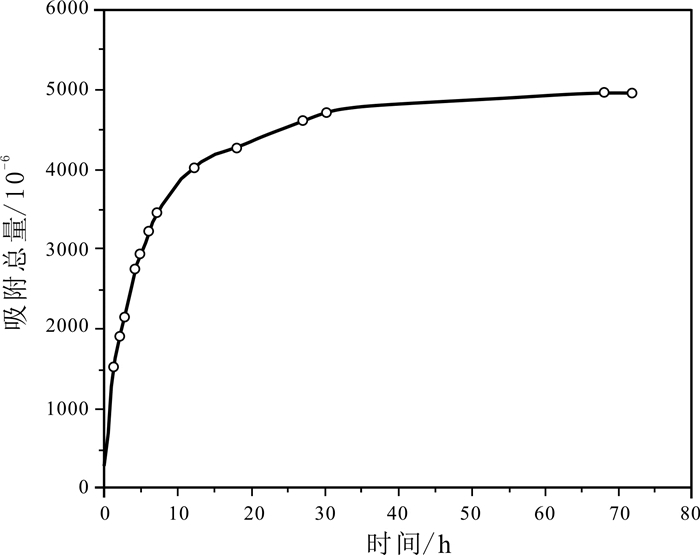
在室温20 ℃,自然pH条件下,在一组250 mL烧杯中加入Co2+初始浓度为490.1 mg/L的溶液50 mL和1.0 g油页岩样品,进行静态吸附实验,测定不同吸附时间油页岩对Co2+的吸附量.吸附速率反映了单位时间内吸附剂在液相中吸附量的大小,在曲线上,各点的斜率代表了瞬间吸附速率(dqt/dt).由图 3可见,随着吸附时间的增加,油页岩对Co2+的吸附量越来越大,30 h后达到吸附最大值.且吸附速率开始时较大,随着吸附时间的增加,吸附速率变小,这是由于吸附开始时,溶液中Co2+离子浓度较大,且油页岩吸附位点较多,吸附速率也就较大,吸附时间的延长使溶液中Co2+浓度减小,且油页岩中的吸附位点被大量占据,导致吸附速率的下降.
|
图 3 油页岩对Co2+的吸附曲线 Fig.3 Adsorption curve for oil shale on Co2+ |
为了研究油页岩对Co2+的吸附动力学特性,对图 3中的数据进行动力学模型拟合,以确定吸附反应级数和吸附机理.经常使用的动力学模型有:准一级动力学模型、准二级动力学模型和粒子内扩散模型.准一级动力学方程[19]为:
| $ \ln \left(q_{\rm e}-q_{t}\right)=\ln q_{\rm e}-K_{1} t $ | (3) |
其中:K1为准一级动力学速率常数.
准二级动力学方程[20]为:
| $ t / q_{t}=1 /\left(K_{2} q_{\rm e}^{2}\right)+t / q_{\rm e} $ | (4) |
其中:K2为准二级动力学速率常数.
粒子内扩散模型[21]为:
| $ q_{t}=K_{i} \; t^{0.5} $ | (5) |
其中:Ki为粒子内扩散速率常数.
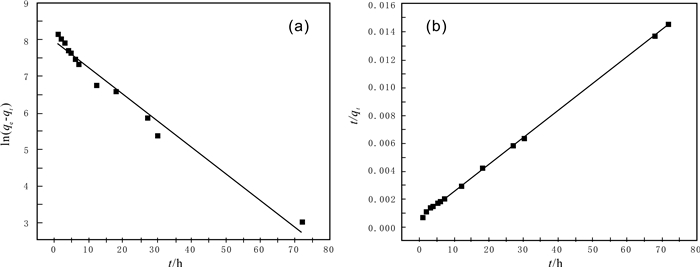
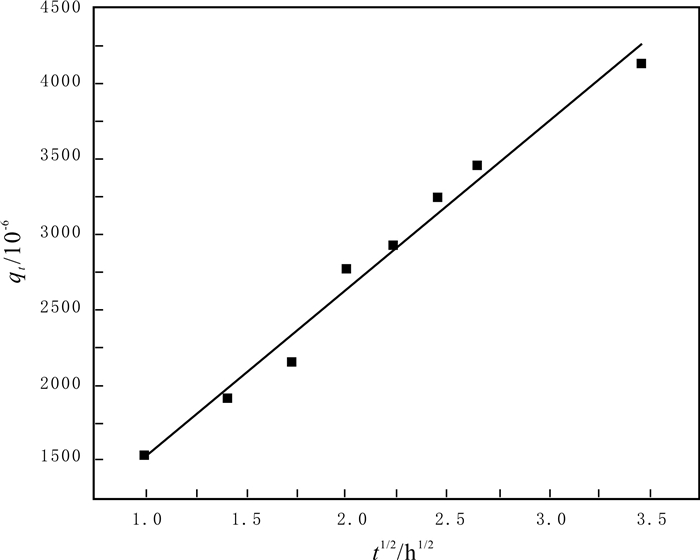
油页岩对Co2+吸附的准一级和准二级动力学拟合曲线见图 4,粒子内扩散模型拟合曲线见图 5,吸附动力学参数见表 2.由图 4中直线的线性关系和表 2中的参数值可以看到,准二级动力学拟合得到直线的相关系数为0.9986,大于准一级动力学的相关系数0.9749;由准二级动力学模型计算得到的理论平衡吸附量qe,cal为5220×10-6与实验值较为接近,而准一级动力学得到的理论计算值与实验值相差较大.说明准二级动力学对平衡数据拟合的较好,油页岩对Co2+的吸附符合准二级动力学过程.影响准二级动力学吸附作用的重要因素是化学键的形成,说明该吸附过程主要为化学吸附.从粒子内扩散机理数据可以看出,拟合后的相关系数为0.9776,拟合较好,符合粒子内扩散机理,但该粒子内扩散拟合曲线未通过原点,说明吸附过程比较复杂,粒子内扩散不是吸附过程唯一的速率控制步骤[22].综合准二级动力学拟合的结果来看,油页岩对Co2+的吸附可能是表面吸附和粒子内扩散共同作用.
|
图 4 油页岩对Co2+吸附的准一级(a)和准二级(b)动力学拟合曲线 Fig.4 Pseudo-first-order and pseudo-second-order kinetic fitting curves of oil shale adsorption on Co2+ |
|
图 5 油页岩对Co2+吸附的粒子内扩散模型拟合曲线 Fig.5 Intraparticle diffusion model fitting curve of oil shale adsorption on Co2+ |
|
|
表 2 油页岩对Co2+的吸附动力学常数 Table 2 Kinetic constants of oil shale adsorption on Co2+ |
(1)油页岩对Co2+具有良好的吸附性能,油页岩粒度、Co2+溶液初始浓度、溶液pH值、吸附时间等影响油页岩对Co2+的吸附性能.
(2)油页岩样品粒度为4~5、5~10、10~20和20~40目时,油页岩对Co2+的最大吸附量随样品粒径的减小而增大;在室温20 ℃,自然pH条件下,油页岩对Co2+的吸附总量随着Co2+初始浓度的增加而增加,而吸附率逐渐下降;溶液初始pH值在3~8范围内,油页岩对Co2+的吸附量和吸附率随着pH值的增大呈上升趋势;随着吸附时间的增加,油页岩对Co2+的吸附量先急剧上升,然后缓慢上升至吸附平衡,30 h后达到吸附最大值.
(3)通过吸附动力学研究发现,油页岩对Co2+的吸附过程符合准二级动力学过程和粒子内扩散机理.
| [1] |
钱家麟, 王剑秋, 李术元. 世界油页岩资源利用和发展趋势[J]. 吉林大学学报(地球科学版), 2006, 36(6): 877-887. |
| [2] |
Wilson K, Yang H, Seo C W, et al. Select metal adsorption by activated carbon made from peanut shells[J]. Bioresource Technology, 2006, 97(18): 2266-2270. DOI:10.1016/j.biortech.2005.10.043 |
| [3] |
钱家麟, 尹亮. 油页岩:石油的补充能源[M]. 北京: 中国石化出版社, 2008.
|
| [4] |
Fan C, Yan J W, Huang Y R, et al. XRD and TG-FTIR study of the effect of mineral matrix on the pyrolysis and combustion of organic matter in shale char[J]. Fuel, 2015, 139: 502-510. DOI:10.1016/j.fuel.2014.09.021 |
| [5] |
王擎, 张宏喜, 迟铭书, 等. 矿物质对桦甸油页岩热解产物影响特性[J]. 燃料化学学报, 2016, 44(3): 328-334. |
| [6] |
Xu D, Tan X L, Chen C L, et al. Adsorption of Pb (Ⅱ) from aqueous solution to MX-80 bentonite:Effect of pH, ionic strength, foreign ions and temperature[J]. Applied Clay Science, 2008, 41(1/2): 37-46. |
| [7] |
曹积飞, 杨秋荣, 李英杰, 等. 粘土矿物对重金属有害元素吸附性研究[J]. 环境科学与技术, 2008, 31(1): 42-44. |
| [8] |
Veli S, Alyüz B. Adsorption of copper and zinc from aqueous solutions by using natural clay[J]. Journal of Hazardous Materials, 2007, 149(1): 226-233. DOI:10.1016/j.jhazmat.2007.04.109 |
| [9] |
Tahir S S, Rauf N. Thermodynamic studies of Ni (Ⅱ) adsorption onto bentonite from aqueous solution[J]. The Journal of Chemical Thermodynamics, 2003, 35(12): 2003-2009. DOI:10.1016/S0021-9614(03)00153-8 |
| [10] |
Al-Asheh S, Banat F. Adsorption of copper and zinc by oil shale[J]. Environmental Geology, 2001, 40(6): 693-698. DOI:10.1007/s002540000234 |
| [11] |
Jiang H F, Song L H, Cheng Z Q, et al. Influence of pyrolysis condition and transition metal salt on the product yield and characterization via Huadian oil shale pyrolysis[J]. Journal of Analytical and Applied Pyrolysis, 2015, 112: 230-236. DOI:10.1016/j.jaap.2015.01.020 |
| [12] |
李俊锋, 宋丽华, 张永强, 等.一种用于油页岩提取页岩油的催化剂及其使用方法: 中国, 103464179A[P]. 2013-09-24.
|
| [13] |
宋丽华.过渡金属盐对油页岩热解催化作用研究[D].长春: 吉林大学, 2016: 1-127. http://cdmd.cnki.com.cn/Article/CDMD-10183-1017016042.htm
|
| [14] |
张永强.提高油页岩中页岩油提取率方法研究[D].长春: 吉林大学, 2014: 1-51. http://cdmd.cnki.com.cn/Article/CDMD-10183-1014268371.htm
|
| [15] |
Ahmad M A, Alrozi R. Removal of malachite green dye from aqueous solution using rambutan peel-based activated carbon:Equilibrium, kinetic and thermodynamic studies[J]. Chemical Engineering Journal, 2011, 171(2): 510-516. DOI:10.1016/j.cej.2011.04.018 |
| [16] |
Pei Y Y, Liu J Y. Adsorption of Pb2+ in wastewater using adsorbent derived from grapefruit peel[J]. Advanced Materials Research, 2011, 391-392: 968-972. DOI:10.4028/www.scientific.net/AMR.391-392.968 |
| [17] |
Abu-El-Sha'r W Y, Gharaibeh S H, Al-Kofahi M M. Removal of selected heavy metals from aqueous solutions using a solid by-product from the Jordanian oil shale refining[J]. Environmental Geology, 1999, 39(2): 113-116. DOI:10.1007/s002540050441 |
| [18] |
Ngah W S W, Hanafiah M A K M. Removal of heavy metal ions from wastewater by chemically modified plant wastes as adsorbents:A review[J]. Bioresource Technology, 2008, 99(10): 3935-3948. DOI:10.1016/j.biortech.2007.06.011 |
| [19] |
Chiou M S, Li H Y. Adsorption behavior of reactive dye in aqueous solution on chemical cross-linked chitosan beads[J]. Chemosphere, 2003, 50(8): 1095-1105. DOI:10.1016/S0045-6535(02)00636-7 |
| [20] |
Wang Y, Mu Y, Zhao Q B, et al. Isotherms, kinetics and thermodynamics of dye biosorption by anaerobic sludge[J]. Separation and Purification Technology, 2006, 50(1): 1-7. DOI:10.1016/j.seppur.2005.10.012 |
| [21] |
Ngah W S W, Fatinathan S. Adsorption of Cu (Ⅱ) ions in aqueous solution using chitosan beads, chitosan-GLA beads and chitosan-alginate beads[J]. Chemical Engineering Journal, 2008, 143(1/3): 62-72. |
| [22] |
孙小莉, 曾庆轩, 冯长根. 多胺型阴离子交换纤维吸附铬(Ⅵ)的动力学[J]. 物理化学学报, 2009, 25(10): 1951-1957. |
 2020, Vol. 29
2020, Vol. 29

