文章信息
- 南文争, 燕绍九, 彭思侃, 王晨, 王继贤
- NAN Wen-zheng, YAN Shao-jiu, PENG Si-kan, WANG Chen, WANG Ji-xian
- 石墨烯的液相剥离制备及在磷酸铁锂正极中的应用
- Preparation of graphene based on liquid phase exfoliation and its application on LiFePO4 electrode for lithium ion battery
- 材料工程, 2020, 48(11): 108-115
- Journal of Materials Engineering, 2020, 48(11): 108-115.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.001162
-
文章历史
- 收稿日期: 2019-12-13
- 修订日期: 2020-07-24
锂离子电池因具有高电压、高容量以及环境友好等特点,被视为目前最高效的电化学储能系统之一,其应用领域也在迅速拓展[1]。目前广泛应用的锂离子正极材料一般为导电性能不佳的过渡金属氧化物或过渡金属磷酸盐,包括LiCoO2(电导率为10-3S/cm)、LiMn2O4(电导率为10-4S/cm)、Li(NixMnyCo1-x-y)O2(电导率为10-7~10-4 S/cm)和LiFePO4(电导率只有10-9 S/cm)等[2]。因此,在锂离子电池制作中需加入导电剂来改善正极材料的导电性能,以减小电极中活性物质颗粒间、活性物质与集流体间的接触电阻,提高电子的移动速率。故导电剂是影响正极材料电化学性能的重要因素之一。目前锂离子电池常用导电剂有导电炭黑、碳纳米管、导电石墨等[3]。石墨烯是sp2杂化碳原子组成的单原子层厚度的新型纳米材料,具有独特的二维柔性结构及优异电子导电性[4-5],把其作为正极导电剂用于锂离子电池,有望得到比传统导电剂更优异的电化学性能[6],是石墨烯应用研究的一个热点方向。
目前,关于石墨烯作为正极导电剂在锂离子电池中应用的报道较多。如Su等[7]采用真空低温法[8]制备出石墨烯,并按2%(质量分数,下同)比例添加于磷酸铁锂电极。结果表明,由于高效导电网络的搭建,电极的倍率、循环性能明显优于添加20%导电炭黑(SP)的电极。Lei等[9]进一步研究表明,虽然石墨烯具有优异的电子导电性,但会阻碍Li+的传输,因此以石墨烯作为导电添加剂,极片的厚度将明显影响电极倍率特性。Liu等[10]将3种不同片径范围(1~2 μm,3~5 μm,10~15 μm)的石墨烯应用于磷酸铁锂电极中,结果表明,用石墨烯替代等量SP,可显著提高电极的低倍率放电容量。但石墨烯片径越大对Li+的阻碍作用越明显,相应电极表现出来的倍率性越差。Wei等[11]制备出两种不同石墨烯包覆状态的石墨烯/磷酸铁锂复合材料,结果表明,5 C放电倍率下,石墨烯半包覆状态的复合材料放电比容量(约80 mAh/g)远高于全包覆态(约40 mAh/g)。综上所述,石墨烯作为导电剂用于锂离子电池正极具有极大应用前景。但在具体应用中,不仅要考虑电极的电子传导性,也要考虑其离子传导性。因此,已有不少研究者通过石墨烯活化等方法,得到表面多孔的石墨烯,以减弱其对Li+的空间位阻效应。如Ha等[12]用KOH活化处理氧化石墨烯并热还原得到表面多孔的石墨烯。应用于正极中,与使用未活化处理的石墨烯电极相比,其倍率性能大幅提高。这是因为,在添加不带孔石墨烯的电极中,由于空间位阻效应,Li+绕过石墨烯纳米片曲折传输,传输路径延长,导致电极高倍率充放电时,Li+不能及时到达电化学反应位点,极化增大。因此,为了实现电子、离子传导的均衡性,制备出表面多孔且结晶度良好的石墨烯具有重要意义。
上述报道方法虽能显著提高电极电化学性能,但制备出的石墨烯普遍存在缺陷多、层数厚、纯度低等问题。此外,为减小石墨烯对Li+空间位阻的影响,需要对制备的石墨烯再进行改性处理,从而增加了工艺复杂性,难以实现工程化应用。本工作提出一种简易、低成本石墨烯制备方法,以高纯天然鳞片石墨为原料,通过氧化插层、高温膨胀得到前驱体,经高压均质装置进行液相剥离,得到高结晶度、低缺陷且表面带有纳米孔洞的石墨烯。作为导电添加剂应用于磷酸铁锂电极中,可显著提高电极功率特性。此外,本工作从电子传导和离子传输两方面影响机制对石墨烯的作用进行讨论。
1 实验材料与方法 1.1 实验材料液相剥离法制备石墨烯:将天然鳞片石墨(NFG)、硫酸(H2SO4)、重铬酸钾(K2Cr2O7)按质量比为1:3:0.15均匀混合,于100 ℃水浴中充分反应。随后将反应液加去离子水洗涤、过滤,50 ℃烘干。将烘干粉末置于马弗炉中,1000 ℃下膨化处理5 s,制得石墨烯前驱体。将石墨烯前驱体投入N-甲基吡咯烷酮(NMP)溶剂中,低速搅拌30 min,充分混合、浸润。然后将悬浮液通过高压均质装置(北京航空材料研究院自主开发)进行剥离,压力为70 MPa,循环6次,得到石墨烯溶液。最后将溶液冷冻干燥,制得石墨烯粉体(GR)。
实验所用天然鳞片石墨购于青岛聚和三杰石墨新材料有限公司,所用磷酸铁锂正极材料购于天津斯特兰能源科技有限公司,所用SP购于瑞士特密高公司,所用电解液购于东莞杉杉电池材料有限公司,所用化学试剂硫酸、重铬酸钾均为分析纯级,购于国药集团化学试剂有限公司。
1.2 扣式电池的组装将磷酸铁锂粉末、聚偏氟乙烯粉末(PVDF)、导电添加剂按质量比8:1:1均匀研磨。投入适量NMP中,利用搅拌机高速混合分散1 h,制得正极浆料。将浆料均匀涂覆于16 μm厚铝箔上,120 ℃真空干燥12 h制得正极极片。分别以SP,GR+SP(质量比SP:GR=4:1)为导电添加剂,按上述方法制备两种正极片,标记为SP-LFP,GR-LFP。对所有正极片辊压,控制压实密度为2.1 g/cm3,并将极片裁成直径为14 mm的圆片,制得工作电极。以锂片为对电极,聚丙烯Celgard2500为隔膜,在手套箱中装配成CR2016型扣式电池。手套箱内水、氧浓度均≤0.1×10-6。
1.3 材料微观组织表征和电化学性能测试采用场发射扫描电子显微镜(SEM)、透射电子显微镜(TEM)、原子力显微镜(AFM)观察材料形貌,利用X射线衍射仪(XRD)、拉曼光谱(Raman)对材料微观结构进行表征。用蓝电充放电测试仪对新组装好的扣式电池工作电极进行电化学测试,测试电压范围为2.5~4.1 V(vs Li/Li+);伏安循环测试电压扫描范围为2.3~4.3 V(vs Li/Li+),扫描速率分别为0.2, 0.5, 1.0, 2.0, 5.0 mV/s;阻抗谱测试频率范围为100 kHz~10 mHz,振幅为5 mV。所有电化学测试均在室温25 ℃下完成。
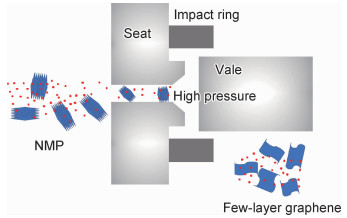
2 结果与分析 2.1 形貌分析图 1(a), (b), (c)分别为天然鳞片石墨、石墨烯前驱体、石墨烯纳米片的扫描电镜照片。从图 1(a)中可以看出,天然鳞片石墨呈片状,石墨层间排列紧密。经氧化插层、高温膨化后形成“蠕虫”状的石墨烯前驱体(图 1(b))。这是由于,插层化合物高温汽化,石墨片层沿c轴方向发生了大的扩展。从图 1(b)中的放大图可看出,前驱体片层间出现大的孔隙,石墨片具有褶皱弯曲结构特点,说明层间的分子间作用力(范德华力)很小。在外力高压作用下,液相分子容易嵌入片层间隙中,通过流体剪切、空穴效应、对流冲击等作用剥离出少层石墨烯[13-14](图 2)。制备的石墨烯片径在5 μm左右,具有典型的褶皱弯曲结构特点,呈半透明状(图 1(c))。

|
图 1 天然鳞片石墨(a)、石墨烯前驱体(b)及石墨烯(c)的扫描电镜照片 Fig. 1 SEM images of natural flake graphite(a), graphene precursor(b) and graphene(c) |
|
图 2 高压均质液相剥离法制备石墨烯示意图 Fig. 2 Schematic illustration for the preparation of graphene in NMP through high pressure homogenization |
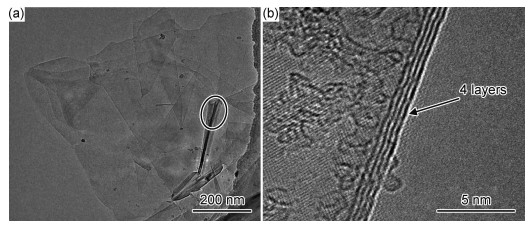
图 3为所制备石墨烯的透射电镜照片。从图 3(a)中可以看出,石墨烯纳米片成半透明状,说明石墨烯厚度非常薄。高分辨透射照片(图 3(a)标记处放大)显示,石墨烯厚度在4层左右(图 3(b))。
|
图 3 石墨烯的低倍(a)及高倍(b)透射电镜照片 Fig. 3 TEM images of graphene for low magnification(a) and high magnification(b) |
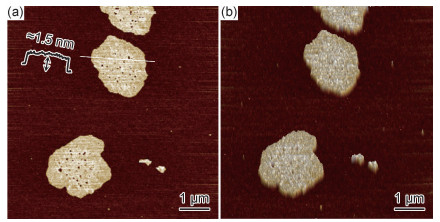
图 4为石墨烯的原子力显微镜照片。从图 4(a)中可以看出,石墨烯表面带有斑点。对厚度进行检测,结果显示为1.5 nm,这同透射结果一致。此外,三维图表明石墨烯表面斑点为纳米孔洞(图 4(b))。其产生原因包括:(1)天然鳞片石墨在氧化插层、高温气化过程中形成的微缺陷[15-17];(2)高压均质过程,石墨片层充分剥离,得到的石墨烯片层非常薄,孔洞缺陷容易呈现;(3)高压均质过程,液相粒子作用于石墨烯表面而形成的孔洞微缺陷[18]。
|
图 4 石墨烯材料的二维(a)及三维(b)原子力显微镜照片 Fig. 4 2D(a) and 3D(b) AFM images of graphene |
图 5为两种添加不同导电剂的正极片扫描电子显微镜照片。图 5(a), (b)分别为SP-LFP极片的表面及横截面扫描照片。可以看出,电极中磷酸铁锂颗粒大小不均,粒径均在2 μm以下。SP为零维纳米材料,均匀填充于磷酸铁锂颗粒间隙中(图 5(a)),且附着于磷酸铁锂颗粒表面(图 5(b)),两者以“点-点”模式接触。图 5(c), (d)分别为GR-LFP极片表面及横截面的扫描照片。可以看出,石墨烯良好分散,贴附于磷酸铁锂颗粒表面(图 5(c)),且穿插于极片中(图 5(d))。石墨烯、SP及磷酸铁锂颗粒间以“点-面”模式接触。因此,在GR-LFP电极中,石墨烯与SP协同构成了更高效的三维导电网络。

|
图 5 极片的扫描电子显微镜照片 (a)SP-LFP电极表面;(b)SP-LFP电极纵面;(c)GR-LFP电极表面;(d)GR-LFP电极纵面 Fig. 5 SEM images of SP-LFP and GR-LFP cathode (a)surface of SP-LFP cathode; (b)cross section of SP-LFP cathode; (c)surface of GR-LFP cathode; (d)cross section of GR-LFP cathode |
图 6(a)为原料鳞片石墨、石墨烯的XRD图谱。在26°处均发现尖锐的(002)衍射峰,代表典型石墨晶体结构,说明制备的石墨烯具有高的石墨化程度。同时衍射峰中没有观察到杂峰,说明材料不含杂质。图 6(b)为天然鳞片石墨、石墨烯及SP的拉曼光谱。分析发现,3种样品在1350 cm-1和1590 cm-1处均存在强吸收谱带。1350 cm-1处峰为D峰,源于材料sp2碳原子的呼吸振动,而1590 cm-1源于sp2碳原子对的伸缩振动。峰强比ID/IG反映了sp2杂化原子的比例。其值越小,缺陷越低[19-20]。可以看出,虽然本实验制备的石墨烯表面含有纳米孔洞缺陷,但仍然具有低缺陷特点。

|
图 6 材料的XRD图谱(a)及拉曼光谱(b) Fig. 6 XRD patterns(a) and Raman spectra(b) of materials |
上述结果表明,本实验制备的石墨烯结晶度高、缺陷低,品质高于一般氧化还原法制备的石墨烯[12, 21-22]。作为导电添加剂用于正极,可极大改善电极导电性。
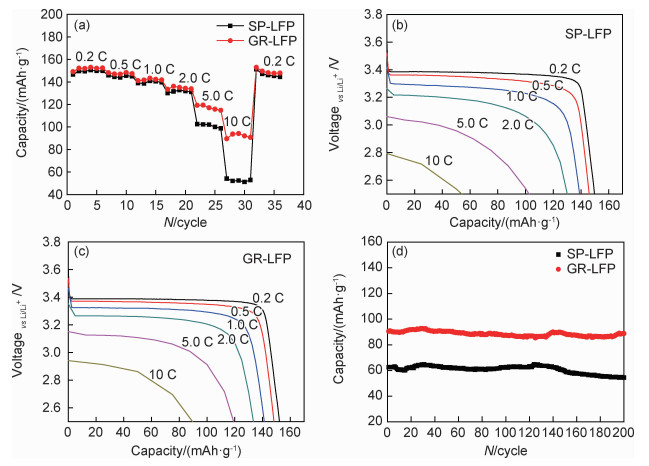
2.3 电化学性能表征 2.3.1 充放电测试将两种正极片组装成扣式电池,进行充放电测试。图 7(a)为两种样品的倍率循环性能,每周循环充电倍率均为0.2 C,放电倍率依次为0.2 C, 0.5 C, 1.0 C, 2.0 C, 5.0 C, 10 C。在0.2 C, 0.5 C, 1.0 C, 2.0 C放电倍率下,两种电极放电比容量接近。随着放电倍率继续提高,性能差异明显:在10 C放电倍率下,GR-LFP电极克容量达90 mAh/g,而SP-LFP电极比容量不足60 mAh/g。当放电倍率回到0.2 C时,各电极均恢复到初始状态,说明造成容量差异的原因不是由于电池的损坏,而是由于高倍率下电极发生了严重极化。图 7(b), (c)分别为对应的两种电极的倍率放电曲线,可以看出,添加石墨烯的电极,高倍率下放电平台更高,说明电化学极化更小。因此,添加了石墨烯的电极具有更优异的倍率特性。
|
图 7 两种磷酸铁锂电极的电化学性能对比 (a)倍率循环性能;(b)SP-LFP电极倍率放电性能;(c)GR-LFP电极倍率放电性能;(d)循环性能 Fig. 7 Electrochemical properties of LiFePO4 cathode with different conductive additives (a)rate performance; (b)discharge profiles for SP-LFP cathode; (c)discharge profiles for GR-LFP cathode; (d)cycling performance |
图 7(d)为两种电极5 C充放循环曲线。由于磷酸铁锂材料优异的结构稳定性,200周次循环后,两种电极放电比容量均未发生明显衰减。但明显看出,添加石墨烯的电极循环中保持高的放电比容量,达90 mAh/g,而只添加SP的电极克容量较低,不足70 mAh/g。
GR-LFP电极比SP-LFP电极倍率性能优异,原因可归结为:(1)同SP相比,石墨烯的石墨化程度更高,层间π电子可自由移动,电子导电性更优异。(2)SP颗粒与石墨烯纳米片协同构建“点-面”高效导电网络[23]。因此,石墨烯替换等量SP,作为二元导电剂添加于正极,能显著提高电子传输速度,减小极化。(3)高倍率充放电不仅需要高电子导电性,也需要高的离子传输速度。因此,石墨烯作为导电添加剂,其导电性不是唯一考虑的因素[24]。石墨烯片径一般大于磷酸铁锂粒径(磷酸铁锂一次颗粒为纳米颗粒),对离子的阻碍作用不能忽略。本实验制备的石墨烯表面有纳米孔洞,Li+在充放电过程中能及时到达或脱离反应位点,减小反应极化。
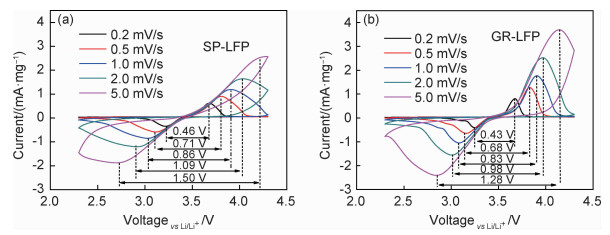
2.3.2 循环伏安测试为进一步分析两电极倍率性能差异,采用循环伏安测试分析电极充放电过程。图 8为两种样品在扫描速率分别为0.2, 0.5, 1.0, 2.0, 5.0 mV/s下的循环伏安曲线。分析发现,每种扫描速率下,两种样品均出现一对氧化还原峰,该氧化还原峰代表充放电过程中Li+的嵌入/脱出反应,伴随Fe2+/Fe3+的氧化还原。其相变过程可表示为LiFePO4⇌FePO4+Li++e-[21, 25]。氧化还原峰电位差越大,表示极化越大[22]。
|
图 8 SP-LFP电极(a)及GR-LFP电极(b)的伏安测试曲线 Fig. 8 CV curves of SP-LFP cathode(a) and GR-LFP cathode(b) |
从图 8中可以看出,随着扫描速率的增加,各电极氧化还原峰电位差增大。0.2 mV/s扫描速率下,SP-LFP,GR-LFP氧化还原峰电位分别为3.67 V/3.21 V,3.67 V/3.24 V,电位差GR-LFP (0.43 V)<SP-LFP (0.46 V),两者相差不大;5 mV/s扫描速率下,氧化还原峰电位分别为4.14 V/2.86 V,2.72 V/4.22 V,电位差GR-LFP(1.28 V)<SP-LFP(1.50 V),两者相差明显。说明随着电流强度的提高,电化学极化增大,但GR-LFP的极化更小。此外,在5.0 mV/s高扫描速率下,SP-LFP的氧化还原峰已不明显,且峰强较低,说明其极化严重。而GR-LFP具有尖锐的氧化还原峰,且峰强较高,说明该电极在高倍率下仍具有高的电化学反应可逆性,电化学活性高。
2.3.3 阻抗测试图 9为两种电池100 kHz到10 mHz的交流阻抗谱图。两种图谱都是由高频区的半圆弧和低频区的斜线构成。其中半圆弧在实轴高频区的截距值(接近坐标0处)代表电解液及电极内部阻抗Rs,中高频处的圆弧直径代表了电极材料与电解液界面间电荷转移的信息,即电荷转移阻抗Rct[26-28]。而低频区的斜线部分是Li+从电极材料表面扩散至电极材料晶格过程中所引起的Warburg阻抗,用符号Zw表示。从图 9中可以看出,SP-LFP电极电荷转移阻抗Rct明显大于GR-LFP。这是因为,GR-LFP电极中,高结晶多孔石墨烯与SP协同搭建了良好的导电导离子网络,提高了电荷转移效率。因此,在磷酸铁锂电极中添加本实验方法制备的石墨烯,对于提高充放电过程中电子及离子的传导速度具有重要作用。

|
图 9 磷酸铁锂电极的交流阻抗谱 Fig. 9 EIS curves of LiFePO4 cathode |
(1) 以天然鳞片石墨为原料,通过氧化插层、高温膨胀制备石墨烯前驱体,最后经高压均质液相剥离得到石墨烯纳米片。制备的石墨烯具有典型的褶皱弯曲结构特征,层数薄、结晶度高、缺陷低,且表面有多个纳米孔洞。
(2) 石墨烯添加于磷酸铁锂电极中,电极倍率性能显著提高:10 C倍率放电,放电比容量达90 mAh/g;5 C充放循环200周次,容量保持率100%,放电比容量达90 mAh/g。
(3) 高结晶度多孔石墨烯能同SP协同搭建良好的导电导离子网络,可显著提高电子及离子传输速率,减小反应极化,提高电极倍率性能。
| [1] |
ZHANG B, YU Y, LIU Y, et al. Percolation threshold of graphene nanosheets as conductive additives in Li4Ti5O12 anodes of Li-ion batteries[J]. Nanoscale, 2013, 5(5): 2100. DOI:10.1039/c2nr33099g |
| [2] |
BETTGE M, LI Y, SANKARAN B, et al. Improving high-capacity Li1.2Ni0.15Mn0.55Co0.1O2-based lithium-ion cells by modifiying the positive electrode with alumina[J]. Journal of Power Sources, 2013, 233: 346-357. DOI:10.1016/j.jpowsour.2013.01.082 |
| [3] |
YU L, YE S, MA X, et al. In-situ synthesizing superior high-rate LiFePO4/C nanorods embedded in graphene matrix[J]. Electrochimica Acta, 2014, 117(4): 105-112. |
| [4] |
燕绍九, 陈翔, 洪起虎, 等. 石墨烯增强铝基纳米复合材料研究进展[J]. 航空材料学报, 2016, 36(3): 57-70. YAN S J, CHEN X, HONG Q H, et al. Graphene reinforced aluminum matrix nanocomposites[J]. Journal of Aeronautical Materials, 2016, 36(3): 57-70. |
| [5] |
王晨, 燕绍九, 南文争, 等. 表面活性剂对高浓度石墨烯水分散液制备的影响[J]. 材料工程, 2019, 47(7): 50-56. WANG C, YAN S J, NAN W Z, et al. Effect of surfactants on preparation of high concentration graphene aqueous dispersion[J]. Journal of Materials Engineering, 2019, 47(7): 50-56. |
| [6] |
CHEN T, PAN L, LIU X, et al. A comparative study on electrochemical performances of the electrodes with different nanocarbon conductive additives for lithium ion batteries[J]. Materials Chemistry and Physics, 2013, 142(1): 345-349. DOI:10.1016/j.matchemphys.2013.07.027 |
| [7] |
SU F Y, YOU C H, HE Y B, et al. Flexible and planar graphene conductive additives for lithium-ion batteries[J]. Journal of Materials Chemistry, 2010, 20: 9644-9650. DOI:10.1039/c0jm01633k |
| [8] |
LV W, TANG D M, HE Y B, et al. Low-temperature exfoliated graphenes:vacuum-promoted exfoliation and electrochemical energy storage[J]. ACS Nano, 2009, 3(11): 3730-3736. DOI:10.1021/nn900933u |
| [9] |
LEI K, LV W, SU F Y, et al. Electrode thickness control:precondition for quite different functions of graphene conductive additives in LiFePO4 electrode[J]. Carbon, 2015, 92: 311-317. DOI:10.1016/j.carbon.2015.04.064 |
| [10] |
LIU T, SUN S M, ZANG Z, et al. Effects of graphene with different sizes as conductive additives on the electrochemical performance of a LiFePO4 cathode[J]. RSC Advances, 2017, 7(34): 20882-20887. DOI:10.1039/C7RA02155K |
| [11] |
WEI W, LV W, WU M B, et al. The effect of graphene wrapping on the performance of LiFePO4 for a lithium ion battery[J]. Carbon, 2013, 57: 5305363. |
| [12] |
HA J, PARK S K, YU S H, et al. A chemically activated graphene-encapsulated LiFePO4 composite for high-performance lithium ion batteries[J]. Nanoscale, 2013, 5(18): 8647. DOI:10.1039/c3nr02738d |
| [13] |
LIU T F, ZHAO L, ZHU J S, et al. The composite electrode of LiFePO4 cathode materials modified with exfoliated graphene from expanded graphite for high power Li-ion batteries[J]. Journal of Materials Chemistry:A, 2014, 2(8): 2822-2829. DOI:10.1039/C3TA14713D |
| [14] |
CAI M, THORPE D, ADAMSON D H, et al. Methods of graphite exfoliation[J]. Journal of Materials Chemistry, 2012, 22(48): 24992-25002. DOI:10.1039/c2jm34517j |
| [15] |
DIMIEV A, KOSYNKIN D V, ALEMANY L B, et al. Pristine graphite oxide[J]. Journal of the American Chemical Society, 2012, 134(5): 2815-2822. DOI:10.1021/ja211531y |
| [16] |
ELGLER S, ENZELELBERGER H M, GRIMM S, et al. Wet chemical synthesis of graphene[J]. Advanced Materials, 2013, 25(26): 3583-3587. DOI:10.1002/adma.201300155 |
| [17] |
EIGLER S, DOTZER C, HIESCH A, et al. Visualization of defect densities in reduced graphene oxide[J]. Carbon, 2012, 50(10): 3666-3673. DOI:10.1016/j.carbon.2012.03.039 |
| [18] |
SHANG J, XUE F, DING E, et al. Facile fabrication of few-layer graphene and graphite nanosheets by high pressure homogenization[J]. Chemical Communications, 2015, 51(87): 15811-15814. DOI:10.1039/C5CC06151B |
| [19] |
WU G, ZHOU Y, SHAO Z, et al. Carbon nanotube and graphene nanosheet co-modified LiFePO4 nanoplate composite cathode material by a facile polyol process[J]. Applied Surface Science, 2013, 283: 999-1005. DOI:10.1016/j.apsusc.2013.07.059 |
| [20] |
YANG J, WANG J, TANG Y, et al. LiFePO4-graphene as a superior cathode material for rechargeable lithium batteries:impact of stacked graphene and unfolded graphene[J]. Energy & Environmental Science, 2013, 6(5): 1521-1528. |
| [21] |
TANG R, YUN Q B, LV W, et al. How a very trace amount of graphene additive works for constructing an efficient conductive network in LiCoO2-based lithium-ion batteries[J]. Carbon, 2016, 103: 356-362. DOI:10.1016/j.carbon.2016.03.032 |
| [22] |
SHI Y, WEN L, PEI S, et al. Choice for graphene as conductive additive for cathode of lithium-ion batteries[J]. Journal of Energy Chemistry, 2019, 30(3): 27-34. |
| [23] |
ZHANG Y Z, CHEN L, OU J K., et al. Improving the performance of a LiFePO4cathode based on electrochemically cleaved grapphite oxides with high hydrophilicity and good conductivity[J]. Jounal of Material Chemistry A, 2013, 1: 7933-7941. DOI:10.1039/c3ta10736a |
| [24] |
ZHU X J, HU J, WU W, et al. LiFePO4/reduced graphene oxide hybrid cathode for lithium ion battery with outstanding rate performance[J]. Journal of Materials Chemistry:A, 2014, 2(21): 7812-7818. DOI:10.1039/C4TA00580E |
| [25] |
HUI B, HUANG F, TANG Y, et al. Study of LiFePO4 cathode modified by graphene sheets for high-performance lithium ion batteries[J]. Electrochimica Acta, 2013, 88(224): 414-420. |
| [26] |
FATHOLLAHI F, JAVANBAKHT M, OMIDVAR H, et al. Improved electrochemical properties of LiFePO4/graphene cathode nanocomposite prepared by one-step hydrothermal method[J]. Journal of Alloys and Compounds, 2015, 627: 146-152. DOI:10.1016/j.jallcom.2014.12.025 |
| [27] |
TANG Y F, HUANG F Q, BI H, et al. Highly conductive three-dimensional graphene for enhancing the rate performance of LiFePO4[J]. Journal of Power Sources, 2012, 203: 130-134. DOI:10.1016/j.jpowsour.2011.12.011 |
| [28] |
LEI X L, ZHANG H Y, CHEN Y M, et al. A three-dimensional LiFePO4/carbon nanotubes/graphene composite as a cathode material for lithium-ion batteries with superior high-rate performance[J]. Journal of Alloys and Compounds, 2015, 626: 280-286. DOI:10.1016/j.jallcom.2014.09.169 |
 2020, Vol. 48
2020, Vol. 48


