文章信息
- 吴胜财, 罗弦, 龙永富, 张露, 徐本军, 黄润
- WU Sheng-cai, LUO Xian, LONG Yong-fu, ZHANG Lu, XU Ben-jun, HUANG Run
- 二氧化硅掺杂对二氧化钛晶型转变机理的影响
- Effects of silicon doping on phase transformation mechanism of titanium dioxide
- 材料工程, 2020, 48(11): 99-107
- Journal of Materials Engineering, 2020, 48(11): 99-107.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000996
-
文章历史
- 收稿日期: 2019-10-31
- 修订日期: 2020-06-13
TiO2具有良好的化学稳定性,被广泛应用于涂料和光催化等领域[1-3]。TiO2主要有3种晶型:金红石(rutile)、锐钛矿(anatase)和板钛矿(brookite),其中板钛矿比较稀少[4]。在3种晶型中,金红石是热力学稳定相,而锐钛矿是亚稳定相,锐钛矿向金红石的相变(A→R相变)是不可逆的相变过程[5]。金红石和锐钛矿因其性质不同而有不同的用途。金红石比锐钛矿稳定而致密,有较高的硬度、密度、介电常数和折射率。因此,金红石广泛应用于涂料、建筑行业中。但是锐钛矿比金红石的光催化活性强,在水和空气净化中具有重要意义[6-8]。因此,如何调控二氧化钛晶型使之应用于不同的领域具有非常现实的意义。在通常情况下,纯锐钛矿二氧化钛转化为金红石二氧化钛的温度是610~915 ℃,要使锐钛矿二氧化钛完全转变为金红石型二氧化钛,煅烧温度要高于1000 ℃。影响A→R相变的主要因素有烧结温度、掺杂离子、烧结气氛[9-10]。研究表明,烧结温度的提高会促进二氧化钛从锐钛型到金红石型的转变,从热力学的角度出发,烧结温度的升高会提高钛原子和氧原子的扩散速率,使得相变过程中更快地重构金红石型,促进相变的发生[5]。掺杂离子的存在对A→R相变有显著的影响,掺杂离子可以阻碍或促进向金红石的转变。在置换固溶体形成的情况下,掺杂离子可以进入锐钛矿晶格,影响氧空位的水平,从而促进或抑制向金红石的转变。在形成间隙固溶体的情况下,将产生晶格畸变抑制相变的发生。如果超过杂质或掺杂物的溶解度,则杂质或掺杂物的析出可通过异质成核促进相变。Cui等[11]发现,Eu3+掺杂对二氧化钛从锐钛矿到金红石转变有促进作用。金丽娜等[12]发现,Zn2+对二氧化钛相变有抑制作用。辛柏福等[13]研究表明,Ag掺杂对二氧化钛相变有促进作用。烧结气氛对A→R相变的作用是不同气氛在二氧化钛晶体中所造成的氧缺陷和间隙钛的方式引起的。因为二氧化钛的锐钛型到金红石型的相变涉及6个钛氧键中2个键的断裂,一方面,氧缺陷的存在降低了相变能,从而有利于相变的进行;另一方面,产生了间隙钛后,会使晶格发生畸变产生应变能,对相变过程中氧原子和钛原子的扩散有阻碍作用[5]。因此,增加二氧化钛晶格中氧缺陷浓度的反应气氛则能够促进相变的进行。反之,增加二氧化钛晶格中间隙钛浓度的气氛能抑制相变。马利静等[14]研究了不同气氛对二氧化钛相变的影响,发现惰性气体会抑制A→R相变,而富氧气氛下会促进A→R相变。国内外学者对二氧化硅掺杂进行了相关研究。Liu等[15]发现,二氧化硅的掺杂会增加二氧化钛的晶粒尺寸,减小比表面积,进而提高二氧化钛的热稳定性,抑制二氧化钛从锐钛矿向金红石的转变。Zheng等[16]发现,二氧化硅的加入会提高二氧化钛晶体的热稳定性,从而阻碍二氧化钛从锐钛矿向金红石的转变。Cheng等[17]发现,二氧化硅会抑制二氧化钛从锐钛矿向金红石转变,但是会细化晶粒。常见的固体氧化物对二氧化钛相变的影响机理有:①低价阳离子置换Ti4+从而产生多余氧空位,为Ti4+和O2-重排成金红石二氧化钛提供空位,并减少Ti—O的断裂,从而促进A→R转变;掺杂离子置换晶格中Ti原子机制,产生晶格畸变,抑制A→R转变。②掺杂离子嵌入二氧化钛机制以及在晶界表面扎堆产生畸变能抑制A→R转变[18]。此外,如果超过了杂质或掺杂剂在二氧化钛中的溶解度极限,那么其沉淀可促进异相成核,减小形核能,从而促进A→R转变[19-22]。
本工作针对物理混合SiO2不同掺杂量(0%,2.5%,5%,7.5%,10%,12.5%)的样品,通过高温原位XRD,TEM,XPS测试及对高温原位XRD谱图进行Rietveld全谱拟合得到不同温度原位条件下二氧化钛不同晶型的含量、晶胞常数及晶粒大小,分析相变过程中二氧化钛不同晶型量、晶粒大小、化学态的变化规律,得到硅对锐钛矿到金红石二氧化钛转变的规律及对机理的影响。
1 实验材料与方法 1.1 原料制备将HCl溶液(AR)缓慢加入NaSiO3(AR)溶液中,当pH=6时得到白色非晶原硅酸沉淀。把沉淀多次过滤、洗涤至滤液不与饱和AgNO3溶液产生沉淀为止,过滤得到的原硅酸放入鼓风干燥箱烘干,然后研磨成粉末。将TiCl4(AR)溶液缓慢加入H2SO4(AR),制成TiOSO4溶液,将TiOSO4溶液静置48 h。然后把NaOH(AR)溶液缓慢加入TiOSO4,直至出现白色胶状偏钛酸。过滤、洗涤得到白色偏钛酸,放入鼓风干燥箱中烘干后研磨成粉末。把制备的原硅酸与偏钛酸按不同SiO2/TiO2质量比在玛瑙研钵中研磨混合均匀,制成样品。
1.2 分析方法使用综合热分析仪进行样品的热重-差热测试,测试条件为:温度26~1100 ℃,升温速率10 ℃/min;用高温原位XRD测试样品高温过程中相变情况,测试条件为:连续扫描,Cu靶,电压40 kV,电流40 mA,步长0.026°,起始角5°,结束角90°,每步停留时间49 s,温度26~1100 ℃,升温速率10 ℃/min;使用X射线光电子能谱仪测试样品中各元素的化学键及化学态,X光源采用单色化的AlKα源(Mono Al Kα),能量1486.6 eV,6 mA×12 kV。全谱扫描:通能为100 eV,步长1 eV,窄谱扫描:通能30 eV,步长0.1 eV。
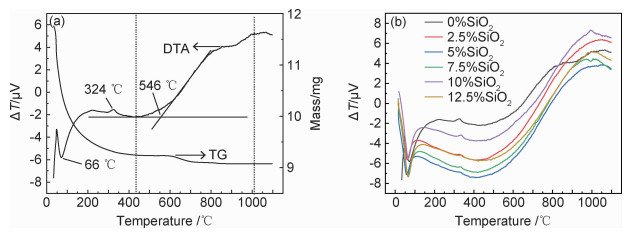
2 结果与讨论 2.1 热重-差热分析图 1是无SiO2掺杂的二氧化钛TG-DTA曲线及不同SiO2掺杂量的二氧化钛DTA曲线。由图 1(a)可知,无SiO2掺杂的二氧化钛在66 ℃左右的失重是样品中结晶水的脱除造成的,330 ℃左右的放热峰是部分非晶型向锐钛矿的转变,650 ℃的失重是脱硫反应[19]。由于在制备二氧化钛的过程中,偏钛酸容易吸附SO42-,所以在650 ℃会发生脱硫反应。在420~1000 ℃存在向上的放热台阶是锐钛矿向金红石的转变。利用基线外推法求相变点,即取曲线开始偏离基线那点的切线与曲线最大斜率切线的交点为相变点。所得不同SiO2掺杂量的二氧化钛A→R相变点如表 1所示。当SiO2掺杂量在0%~7.5%时,A→R的相变温度由546 ℃提高到603 ℃。当SiO2掺杂量为7.5%~12.5%时,A→R的相变温度由603 ℃降至550 ℃。
|
图 1 无SiO2掺杂的二氧化钛TG-DTA曲线(a)和不同SiO2掺杂量的二氧化钛DTA曲线(b) Fig. 1 TG-DTA curves of titanium dioxide without SiO2 doping(a) and DTA curves of titanium dioxide with different doping amounts of SiO2(b) |
| Mass fraction of SiO2/% | Phase transition temperature/℃ |
| 0 | 546 |
| 2.5 | 584 |
| 5 | 593 |
| 7.5 | 603 |
| 10 | 588 |
| 12.5 | 550 |
不同SiO2掺杂量下,二氧化钛高温原位XRD衍射谱图如图 2所示。可知,A→R相变是一个渐变的过程,金红石的晶面在相变过程中依次出现。SiO2掺杂量为0%~12.5%的二氧化钛A→R相变的相变点如表 2所示。

|
图 2 不同掺杂试样的高温原位XRD谱图 (a)0%SiO2; (b)2.5%SiO2; (c)5%SiO2; (d)7.5%SiO2; (e)10%SiO2; (f)12.5%SiO2 Fig. 2 High temperature in-situ XRD patterns of different doped samples (a)0%SiO2; (b)2.5%SiO2; (c)5%SiO2; (d)7.5%SiO2; (e)10%SiO2; (f)12.5%SiO2 |
| Mass fraction of SiO2/% | Phase transition temperature/℃ |
| 0 | 600 |
| 2.5 | 610 |
| 5 | 590 |
| 7.5 | 630 |
| 10 | 600 |
| 12.5 | 530 |
由表 2可知,随着SiO2掺杂量的提高,A→R相变温度先增加后减小,这与DTA测试的结果基本相符。图 2中没有发现SiO2衍射峰,因为SiO2为非晶态。用High Score Pluse软件分别对SiO2掺杂量为0%~12.5%的二氧化钛衍射谱图进行500,650,700 ℃ Rietveld全谱拟合,Rietveld全谱拟合法精修后得到的锐钛型二氧化钛的晶格相关参数如表 3所示,其中,a,b,c为晶格常数,α,β,λ为夹角,Rwp为重均因子,Rp为权重因子,Rexp为因子期望值,GoF为拟合优度。
| T/℃ | Mass fraction of SiO2/% | a/nm | b/nm | c/nm | Mass fraction of anatase/% | α, β, γ/(°) | Rwp | Rp | Rexp | GoF |
| 500 | 0 | 0.38035 | 0.38035 | 0.95701 | 100.0 | 90 | 9.97 | 7.75 | 7.46 | 1.78 |
| 2.5 | 0.38034 | 0.38034 | 0.95702 | 97.5 | 90 | 9.55 | 7.54 | 7.61 | 1.57 | |
| 5 | 0.38029 | 0.38029 | 0.95657 | 95.0 | 90 | 9.89 | 7.91 | 7.61 | 1.69 | |
| 7.5 | 0.38032 | 0.38032 | 0.95662 | 92.5 | 90 | 9.29 | 7.30 | 7.5 | 1.53 | |
| 10 | 0.38029 | 0.38029 | 0.95685 | 90.0 | 90 | 8.12 | 6.35 | 7.28 | 1.24 | |
| 12.5 | 0.37954 | 0.37954 | 0.95675 | 87.5 | 90 | 7.14 | 5.27 | 6.43 | 1.23 | |
| 650 | 0 | 0.38040 | 0.38040 | 0.95974 | 83.6 | 90 | 9.04 | 6.77 | 7.50 | 1.45 |
| 2.5 | 0.38029 | 0.38029 | 0.95933 | 83.8 | 90 | 10.80 | 8.54 | 7.65 | 1.99 | |
| 5 | 0.38036 | 0.38036 | 0.95956 | 80.9 | 90 | 10.36 | 7.76 | 7.68 | 1.81 | |
| 7.5 | 0.38044 | 0.38044 | 0.95957 | 82.0 | 90 | 9.88 | 7.62 | 7.51 | 1.73 | |
| 10 | 0.38036 | 0.38036 | 0.95966 | 69.9 | 90 | 9.51 | 7.27 | 7.31 | 1.69 | |
| 12.5 | 0.38005 | 0.38005 | 0.95954 | 56.9 | 90 | 7.35 | 5.70 | 6.51 | 1.27 | |
| 700 | 0 | 0.38046 | 0.38046 | 0.96178 | 71.2 | 90 | 9.82 | 7.37 | 7.54 | 1.69 |
| 2.5 | 0.38038 | 0.38038 | 0.95973 | 78.3 | 90 | 10.51 | 8.05 | 7.83 | 1.79 | |
| 5 | 0.38053 | 0.38053 | 0.95985 | 68.6 | 90 | 13.29 | 9.24 | 7.77 | 2.92 | |
| 7.5 | 0.38048 | 0.38048 | 0.96035 | 71.9 | 90 | 10.01 | 7.75 | 7.53 | 1.76 | |
| 10 | 0.38043 | 0.38043 | 0.96024 | 56.3 | 90 | 8.55 | 6.77 | 7.35 | 1.35 | |
| 12.5 | 0.38019 | 0.38019 | 0.96039 | 45.3 | 90 | 7.88 | 6.07 | 6.54 | 1.45 |
由表 3可知,500,650,700 ℃时,SiO2掺杂量为2.5%~12.5%的锐钛矿晶格常数a,b,c相比于无SiO2掺杂的均稍有减小。氧化物对二氧化钛的A→R相变,存在掺杂离子进入二氧化钛晶格或替换二氧化钛晶格节点中的Ti4+的情况[18]。由于Si4+半径(0.040 nm)远小于Ti4+半径(0.061 nm),所以当Si4+替代了锐钛矿晶格中Ti4+后形成了置换固溶体,锐钛矿的晶格常数a,b,c会稍减小。表 4是650,700 ℃时Rietveld精修后的金红石晶格参数。同样,掺杂了SiO2后的金红石的晶格常数a,b,c相比于未掺杂SiO2的稍有减小,再次说明Si4+替代了锐钛矿晶格中Ti4+的情况。在二氧化钛A→R相变过程中,涉及6个钛氧键中2个钛氧键的断裂[5],说明二氧化钛A→R相变过程中存在着锐钛矿Ti—O键断裂和Ti4+,O2-扩散结晶成金红石。当Si4+进入二氧化钛晶格形成置换固溶体后,将产生畸变能,阻碍Ti4+的扩散,结晶形成金红石,所以从高温原位XRD图中发现,当SiO2掺杂量为0%~7.5%时,A→R相变的相变温度随着SiO2掺杂量的增加而提高。
| T/℃ | Mass fraction of SiO2/% | a/nm | b/nm | c/nm | Mass fraction of rutile/% | α, β, γ/(°) | Rwp | Rp | Rexp | GoF |
| 650 | 0 | 0.46253 | 0.46253 | 0.29845 | 16.4 | 90 | 9.04 | 6.77 | 7.50 | 1.45 |
| 2.5 | 0.46239 | 0.46239 | 0.29834 | 13.7 | 90 | 10.80 | 8.54 | 7.65 | 1.99 | |
| 5 | 0.46242 | 0.46242 | 0.29839 | 14.1 | 90 | 10.36 | 7.76 | 7.68 | 1.81 | |
| 7.5 | 0.46260 | 0.46260 | 0.29846 | 10.5 | 90 | 9.88 | 7.62 | 7.51 | 1.73 | |
| 10 | 0.46259 | 0.46259 | 0.29844 | 20.1 | 90 | 9.51 | 7.27 | 7.31 | 1.69 | |
| 12.5 | 0.46210 | 0.46210 | 0.29825 | 30.6 | 90 | 7.35 | 5.70 | 6.51 | 1.27 | |
| 700 | 0 | 0.46270 | 0.46270 | 0.29858 | 28.8 | 90 | 9.82 | 7.37 | 7.54 | 1.69 |
| 2.5 | 0.46253 | 0.46253 | 0.29843 | 19.2 | 90 | 10.51 | 8.05 | 7.83 | 1.79 | |
| 5 | 0.46262 | 0.46262 | 0.29854 | 26.4 | 90 | 13.29 | 9.24 | 7.77 | 2.92 | |
| 7.5 | 0.46279 | 0.46279 | 0.29863 | 20.6 | 90 | 10.01 | 7.75 | 7.53 | 1.76 | |
| 10 | 0.46273 | 0.46273 | 0.29861 | 33.7 | 90 | 8.55 | 6.77 | 7.35 | 1.35 | |
| 12.5 | 0.46227 | 0.46227 | 0.29840 | 42.2 | 90 | 7.88 | 6.07 | 6.54 | 1.45 |
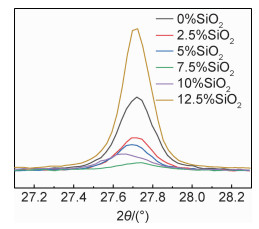
图 3为650 ℃不同SiO2掺杂量的金红石(110)晶面的XRD衍射峰。
|
图 3 650 ℃不同SiO2掺杂量的金红石(110)晶面的XRD衍射峰 Fig. 3 XRD peaks of rutile (110) crystal surface with different silicon contents at 650 ℃ |
由图 3可知,SiO2含量为0% ~7.5%时,随着SiO2掺杂量的增加,半峰宽不断增加。同时,金红石(110)晶面的XRD衍射峰发生偏移,其原因是掺杂SiO2后的金红石型二氧化钛产生了轻微的晶格畸变。用Scherrer公式[20]计算金红石型的晶粒尺寸:
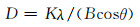
|
(1) |
式中:D是晶粒尺寸,nm;K为常数,K=0.89;λ为X射线波长, λ=0.15405 nm;B为最强衍射峰的半峰宽,nm;θ为布拉格衍射角, (°)。
表 5为650 ℃不同SiO2掺杂量的金红石晶粒尺寸。可知,当SiO2掺杂量为0% ~7.5%时,金红石型的晶粒尺寸呈减小的趋势。这是因为在加热过程中,Si4+进入二氧化钛晶格,形成置换固溶体后产生畸变能,阻碍了金红石的长大,细化了金红石的晶粒。当SiO2含量达到7.5%后,金红石的晶粒尺寸随着SiO2掺杂量的增加而增加。在二氧化钛中掺杂SiO2后,Si4+进入二氧化钛晶格有一定的溶解度,超过一定含量的掺杂物会充当金红石的晶核促进A→R相变,尤其是和二氧化钛有着相似晶型结构的掺杂物促进效果更显著,而SiO2和二氧化钛同属于四方晶系[21-24]。因此,当SiO2达到一定含量后,不能再形成置换固溶体,多余的SiO2充当金红石的晶核,避免金红石自主形核的过程,从而减少形核能,促进A→R相变。当SiO2掺杂量大于7.5%后,随着SiO2掺杂量的增加,金红石晶粒开始变大。掺杂量增加到12.5%时,晶粒急剧增大。
| Mass fraction of SiO2/% | FWHM/(°) | Crystal size/nm |
| 0 | 0.1703 | 68.2 |
| 2.5 | 0.1758 | 64.9 |
| 5 | 0.1759 | 64.9 |
| 7.5 | 0.2937 | 33.5 |
| 10 | 0.2375 | 43.5 |
| 12.5 | 0.1392 | 91.8 |
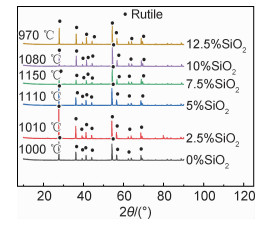
图 4为不同SiO2掺杂量下A→R相变终止时的XRD谱图。当SiO2掺杂量为0%~12.5%时,A→R相变的终止温度分别为1000,1010,1110,1150,1080,970 ℃。随着SiO2掺杂量的提高,A→R相变的终止温度呈现先增加后减小的趋势。
|
图 4 不同SiO2掺杂量下A→R相变终止时的XRD谱图 Fig. 4 XRD patterns of A→R phase transition termination at different SiO2 doping |
可知,SiO2对A→R相变的影响存在两种机制:一方面,Si4+进入二氧化钛晶格形成置换固溶体,产生的畸变能阻碍了A→R相变;另一方面,SiO2会充当金红石的晶核,减少形核能,促进A→R相变。在SiO2掺杂量低时,前一种为主导因素,含量高时以后一种为主导因素。所以,在DTA和XRD图上,掺杂SiO2后二氧化钛的A→R相变表现为先抑制后促进,同时其相变终止温度同样出现了先增加后减小的趋势。
2.3 TEM分析将SiO2掺杂量分别为0%,5%,7.5%,12.5%的二氧化钛煅烧至700 ℃,样品冷却后进行TEM测试,如图 5所示。

|
图 5 700 ℃时不同SiO2掺杂量的二氧化钛晶粒尺寸的TEM图 (a)0%;(b)5%;(c)7.5%;(d)12.5% Fig. 5 TEM images of the grain size of titanium dioxide with different silicon dioxide contents at 700 ℃ (a)0%;(b)5%;(c)7.5%;(d)12.5% |
对晶粒大小进行统计可以得出,随着二氧化硅掺杂量由0%提高到12.5%,二氧化钛的晶粒尺寸依次为61.4,54.3,40.8,172.4 nm。晶粒尺寸先减小后增大,TEM测试结果完全符合XRD的分析趋势,进一步说明了Rietveld全谱拟合法计算所得晶粒尺寸的可靠性及晶粒尺寸对二氧化钛A→R相变的影响。
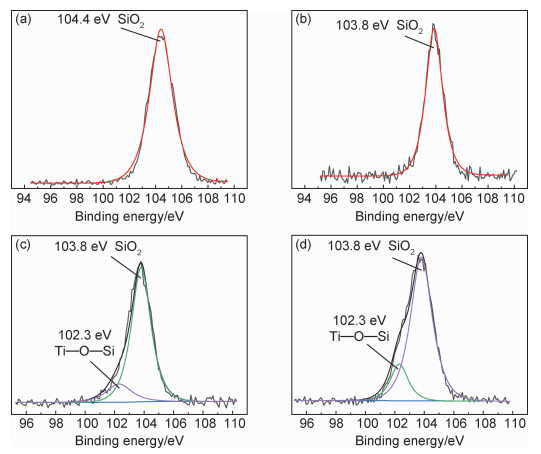
2.4 XPS分析将SiO2掺杂量为7.5%的二氧化钛分别煅烧至500,700,890 ℃,然后用X射线光电子能谱仪测试,所有测试谱图均经过C1s=284.78 eV校正。图 6是SiO2掺杂量为7.5%的二氧化钛在26,500,700,890 ℃的Si2p谱图。图 6(a)中Si2p的104.4 eV峰属于SiO2中的Si4+[25],由于样品的电荷效应,所以和标准SiO2的Si2p峰的位置103.3 eV有偏差[26]。图 6(b)中Si2p的103.8 eV峰属于SiO2,对比103.3 eV可知存在着结合能的化学位移,而两个峰型都比较对称,峰宽较窄,这是由于在加热的过程中,SiO2和TiO2的相互作用所致。与图 6(a),(b)相比,图 6(c),(d)的峰型明显不对称。对分峰拟合后可知,102.3 eV的轨道峰属于Ti—O—Si键[26]。说明在锐钛矿向金红石的转变过程中,由于SiO2的掺杂形成新的化学键Ti—O—Si,证明Si4+取代了TiO2晶格中Ti4+。
|
图 6 SiO2掺杂量为7.5%的二氧化钛不同温度的Si2p轨道峰 (a)26 ℃;(b)500 ℃;(c)700 ℃;(d)890 ℃ Fig. 6 Si2p orbital peaks of titanium dioxide with 7.5%SiO2 doping at different temperatures (a)26 ℃; (b)500 ℃; (c)700 ℃; (d)890 ℃ |
图 7为SiO2掺杂量为7.5%,0%的二氧化钛在26,500,700,890 ℃的O1s分峰拟合后对比图,所有谱图均经过C1s=284.78 eV校正。529.9 eV对应于TiO2中的O2-[27],533.5 eV对应于H2O中的O2-[26],532.89 eV对应于SiO2中的O2-[28],531.57 eV对应于羟基(—OH)[29],这是由于二氧化钛表面氧缺陷引起的羟基吸附[30],531.69 eV对应于Ti—O—Si键[31]。从图 7可知,在500 ℃后的煅烧过程中,SiO2掺杂量为7.5%的二氧化钛和未掺杂SiO2的二氧化钛相比,出现了新的化学键Ti—O—Si,这进一步说明SiO2掺杂量为7.5%的二氧化钛在A→R相变过程中存在着Si4+取代TiO2晶格中的Ti4+的情况。

|
图 7 SiO2掺杂量为7.5%(1)和0%(2)的二氧化钛不同温度的O1s轨道峰 (a)26 ℃;(b)500 ℃;(c)700 ℃;(d)890 ℃ Fig. 7 O1s orbital peaks of titanium dioxide with 7.5%SiO2(1) and 0%SiO2(2) doping at different temperatures (a)26 ℃; (b)500 ℃; (c)700 ℃; (d)890 ℃ |
分析掺杂SiO2后二氧化钛在A→R相变过程中Si2p和O1s轨道峰的变化,发现掺杂SiO2后出现了新的化学键Ti—O—Si,证明有部分Si4+替换二氧化钛晶格中的Ti4+,使之部分形成置换固溶体,产生畸变能,阻碍二氧化钛的A→R相变。
3 结论(1) 不同SiO2掺杂量下,A→R相变终止温度会随着SiO2掺杂量的提高而呈现先增加后减小的趋势。
(2) SiO2掺杂后,影响二氧化钛的A→R相变过程机理为畸变能和晶核形成共同控制。当SiO2掺杂量≥7.5%时为抑制相变作用,此时Si4+会置换二氧化钛晶格中的Ti4+,产生畸变抑制二氧化钛的A→R型转变;当SiO2掺杂量<7.5%时,多余的SiO2会充当金红石型二氧化钛的晶核,从而促进二氧化钛的A→R型转变。
| [1] |
RABHI S, BELKACEMI H, BOUOUDINA M, et al. Effect of Ag doping of TiO2 nanoparticles on anatase-rutile phase transformation and excellent photodegradation of amlodipine besylate[J]. Materials Letters, 2019, 236: 640-643. DOI:10.1016/j.matlet.2018.11.006 |
| [2] |
ERDOGAN N, PARK J, CHOI W, et al. Alkaline hydrothermal synthesis, characterization, and photocatalytic activity of TiO2 nanostructures:the effect of initial TiO2 phase[J]. Journal of Nanoscience and Nanotechnology, 2019, 19(3): 1511-1519. DOI:10.1166/jnn.2019.16171 |
| [3] |
KONDAMAREDDY K K, NEENA D, LU D, et al. Ultra-trace(parts per million-ppm) W6+ dopant ions induced anatase to rutile transition(ART) of phase pure anatase TiO2 nanoparticles for highly efficient visible light-active photocatalytic degradation of organic pollutants[J]. Applied Surface Science, 2018, 456: 676-693. |
| [4] |
PIGEOT-RÉMY S, GREGORI D, HAZIME R, et al. Size and shape effect on the photocatalytic efficiency of TiO2 brookite[J]. Journal of Materials Science, 2019, 54(2): 1213-1225. DOI:10.1007/s10853-018-2924-x |
| [5] |
姜贵民, 严继康, 杨钢, 等. TiO2晶型转变(A→R)的影响因素[J]. 材料导报, 2016, 30(19): 95-100. JIANG G M, YAN J K, YANG G, et al. Influencing factors of TiO2 crystal transformation (A→R)[J]. Materials Review, 2016, 30(19): 95-100. |
| [6] |
朱晓东, 王尘茜, 雷佳浩, 等. 锐钛矿型银掺杂二氧化钛紫外光及模拟太阳光光催化性能[J]. 材料工程, 2020, 48(2): 59-64. ZHU X D, WANG C X, LEI J H, et al. Photocatalytic activity of Ag-doped TiO2 with anatase structure under UV light and simulated sunlight[J]. Journal of Materials Engineering, 2020, 48(2): 59-64. |
| [7] |
RAMOS-CORELLA K J, SOTELO-LERMA M, GIL-SALIDO A A, et al. Controlling crystalline phase of TiO2 thin films to evaluate its biocompatibility[J]. Materials Technology, 2019, 34(8): 455-462. DOI:10.1080/10667857.2019.1576821 |
| [8] |
RANA S, RAWAT J, MISRA R D K. Anti-microbial active composite nanoparticles with magnetic core and photocatalytic shell:TiO2-NiFe2O4 biomaterial system[J]. Acta Biomaterialia, 2005, 1(6): 691-703. DOI:10.1016/j.actbio.2005.07.007 |
| [9] |
刘明, 严继康, 杨钢, 等. 铜掺杂纳米二氧化钛颗粒的相变研究[J]. 材料工程, 2019, 47(4): 105-112. LIU M, YAN J K, YANG G, et al. Phase transition process of Cu-doped TiO2 nanoparticles[J]. Journal of Materials Engineering, 2019, 47(4): 105-112. |
| [10] |
余尚银. 材料物理化学[M]. 西安: 西安交通大学出版社, 1994. YU S Y. Physical chemistry of materials[M]. Xi'an: Xi'an Jiaotong University Press, 1994. |
| [11] |
CUI L, CHANG M, CHEN J, et al. Judd-Ofelt analysis, photoluminescence and photocatalytic properties of core-shell SiO2@TiO2:Eu3+ nanospheres with different diameters[J]. Journal of Physics and Chemistry of Solids, 2018, 123: 162-171. DOI:10.1016/j.jpcs.2018.07.020 |
| [12] |
金丽娜, 史志铭, 闫龙. Zn2+掺杂对TiO2相变温度和晶粒尺寸的影响[J]. 人工晶体学报, 2007, 36(3): 631-633. JIN L N, SHI Z M, YAN L. Effect of Zn2+ doping on phase transition temperature and grain size of TiO2[J]. Journal of Artificial Crystals, 2007, 36(3): 631-633. |
| [13] |
辛柏福, 任志宇, 玄立春, 等. Ag同步掺杂与沉积对TiO2相变的影响[J]. 黑龙江大学自然科学学报, 2004, 21(1): 100-103. XIN B F, REN Z Y, XUAN L C, et al. The effect of Ag doping and deposition on the phase transition of TiO2[J]. Journal of Natural Science of Heilongjiang University, 2004, 21(1): 100-103. |
| [14] |
马利静, 郭烈锦. 采用原位变温X射线衍射技术研究不同气氛下TiO2的相变机理[J]. 光谱学与光谱分析, 2011, 31(4): 1133-1137. MA L J, GUO L J. Study on the phase transformation mechanism of TiO2 in different atmospheres by in-situ variable tempe-rature X-ray diffraction[J]. Spectroscopy and Spectral Analysis, 2011, 31(4): 1133-1137. |
| [15] |
LIU X, WU X, XU T, et al. Effects of silica additive on the NH3-SCR activity and thermal stability of a V2O5/WO3-TiO2 catalyst[J]. Chinese Journal of Catalysis, 2016, 37(8): 1340-1346. DOI:10.1016/S1872-2067(15)61109-3 |
| [16] |
ZHENG K, YANG G, SHEN W, et al. Preparation and denitration performance of VW/TiO2-SiO2 nanotube catalysts[J]. Water, Air, & Soil Pollution, 2018, 229(4): 109. |
| [17] |
CHENG W, LI C, MA X, et al. Effect of SiO2-doping on photogenerated cathodic protection of nano-TiO2 films on 304 stainless steel[J]. Materials & Design, 2017, 126: 155-161. |
| [18] |
杨建, 薛向欣, 王文忠, 等. 氧化物添加剂对TiO2相变和晶粒生长的影响机制[J]. 功能材料, 2005, 36(7): 978-980. YANG J, XUE X X, WANG W Z, et al. The influence mechanism of oxide additives on the phase transformation and grain growth of TiO2[J]. Functional Materials, 2005, 36(7): 978-980. |
| [19] |
雷立新.回转窑煅烧钛白热能利用分析[D].成都: 四川大学, 2005. LEI L X.Analysis of white heat energy utilization of titanium calcined in rotary kiln[D].Chengdu: Sichuan University, 2005. |
| [20] |
HAQUE B M, CHANDRA D B, JIBAN P, et al. Influence of Fe2+/Fe3+ ions in tuning the optical band gap of SnO2 nanoparticles synthesized by TSP method:surface morphology, structural and optical studies[J]. Materials Science in Semiconductor Processing, 2019, 89: 223-233. DOI:10.1016/j.mssp.2018.09.023 |
| [21] |
塔娜, 史志铭, 王晓欢, 等. 锡掺杂二氧化钛相变过程和微结构分析[J]. 人工晶体学报, 2014, 43(1): 163-167. TA N, SHI Z M, WANG X H, et al. Phase transformation and microstructure analysis of tin doped titanium dioxide[J]. Journal of Artificial Crystals, 2014, 43(1): 163-167. |
| [22] |
HANAOR D A H, SORRELL C C. Review of the anatase to rutile phase transformation[J]. Journal of Materials Science, 2011, 46(4): 855-874. DOI:10.1007/s10853-010-5113-0 |
| [23] |
郭俊怀, 沈星灿, 武丽艳, 等. 金红石型TiO2的快速晶型转变[J]. 应用化学, 2003, 20(7): 647-650. GUO J H, SHEN X C, WU L Y, et al. The accelerated crystal phase transition for rutile titania[J]. Chinese Journal of Applied Chemistry, 2003, 20(7): 647-650. |
| [24] |
吴玉程, 陈挺松, 解挺, 等. 掺W纳米TiO2材料改性与光催化性能研究[J]. 功能材料, 2005, 36(1): 121-123. WU Y C, CHEN T S, XIE T, et al. W doping modification and photocatalystic capacity of nanostructured titania[J]. Journal of Functional Materials, 2005, 36(1): 121-123. |
| [25] |
CONGER C P, SUZER S. Response of polyelectrolyte layers to the SiO2 substrate charging as probed by XPS[J]. Langmuir, 2009, 25(3): 1757-1760. |
| [26] |
LUNG C Y K, HEINONEN M, KUKK E, et al. Surface modification of titanium with thermally treated polydimethylsiloxane coating and the effect on resin to titanium adhesion[J]. Surface and Interface Analysis, 2015, 47(1): 105-112. DOI:10.1002/sia.5681 |
| [27] |
ZHU X, HAN S, FENG W, et al. The effect of heat treatment on the anatase-rutile phase transformation and photocatalytic activity of Sn-doped TiO2 nanomaterials[J]. RSC Advances, 2018, 8(26): 14249-14257. DOI:10.1039/C8RA00766G |
| [28] |
李晓坤, 马冬冬, 郑燕萍, 等. TiO2/SiO2复合载体上高分散Au催化剂的CO氧化性能[J]. 物理化学学报, 2015, 31(9): 1753-1760. LI X K, MA D D, ZHENG Y P, et al. CO oxidation performance of highly dispersed Au catalyst on TiO2/SiO2 composite support[J]. Journal of Physical Chemistry, 2015, 31(9): 1753-1760. |
| [29] |
STAMBOLOVA I, BLASKOV V, KAN E N, et al. Effect of titanium dopant on the surface features and on the photocatalytic characteristics of ZnO films[J]. Materials Science in Semiconductor Processing, 2014, 25: 244-250. DOI:10.1016/j.mssp.2013.12.020 |
| [30] |
李亚东.二氧化钛表面及界面性质的第一性原理研究[D].上海: 中国科学院上海应用物理研究所, 2017. LI Y D.First principles study on the surface and interface pro-perties of titanium dioxide[D].Shanghai: Shanghai Institute of Applied Physics, Chinese Academy of Sciences, 2017. |
| [31] |
樊国栋, 张国贤, 冯昕钰, 等. Ce-TiO2-SiO2的制备及其光降解罗丹明B的动力学[J]. 化工进展, 2017, 36(8): 3125-3133. FAN G D, ZHANG G X, FENG X Y, et al. Preparation of Ce-TiO2-SiO2 and kinetics of photodegradation of Rhodamine B[J]. Chemical Progress, 2017, 36(8): 3125-3133. |
 2020, Vol. 48
2020, Vol. 48


