文章信息
- 许文龙, 陈爽, 张津红, 刘会娥, 朱佳梦, 刁帅, 于安然
- XU Wen-long, CHEN Shuang, ZHANG Jin-hong, LIU Hui-e, ZHU Jia-meng, DIAO Shuai, YU An-ran
- 羧甲基纤维素-石墨烯复合气凝胶的制备及吸附研究
- Preparation and adsorption of carboxymethyl cellulose graphene composite aerogels
- 材料工程, 2020, 48(9): 77-85
- Journal of Materials Engineering, 2020, 48(9): 77-85.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000819
-
文章历史
- 收稿日期: 2019-09-06
- 修订日期: 2020-03-22
2. 天津滨海新区大港油田, 天津 300280
2. Dagang Oilfield, BinhaiNew Area, Tianjin 300280, China
水污染及其相关环境问题已成为一个非常棘手的问题,受到了全球的广泛关注,其中染料废水存在毒性大、难降解、稳定性强等特点[1]。目前,对于染料废水的处理国内外研究人员已经做了很多研究工作[2-5],这些方法在一定程度上可以解决染料废水问题,但同时也存在成本高、效率低、易造成二次污染等问题。吸附法具有成本低、效率高、操作简单等优点被广泛应用。传统的吸附剂虽然生产成本较低,但其吸附量较低,吸附速率缓慢[6-7]。因此,制备一种高吸附效率的吸附材料是染料废水处理领域的关键[8]。
石墨烯气凝胶表面具有许多的含氧官能团,可通过静电作用和π-π共轭吸附染料;大的比表面积可提供丰富的吸附位点,为其吸附染料提供了基础[9]。黄扬帆等[10]以氧化石墨为原料,利用乳液模板法制备的emGA-2吸附MB在510 min时趋于平衡,吸附效果良好。Ai等[8]将石墨烯和碳纳米管复合材料用于MB吸附,在碱性条件下去除率高达97%,吸附量可达81.97 mg·L-1。纤维素来源广泛、价格低廉、易降解且无毒环保,在水处理方面的应用吸引了越来越多的关注;同时,纤维素的长碳链多羟基结构含有大量的氢键,可作为很好的支架材料[11]。
本研究在石墨烯的基础上,添加适量价格低廉的羧甲基纤维素,以二维石墨烯片层为基底,一维羧甲基纤维素为填充材料制备了羧甲基纤维素/石墨烯复合气凝胶。并以亚甲基蓝为典型污染物,研究羧甲基纤维素/石墨烯复合气凝胶在含亚甲基蓝水溶液中的扩散和吸附过程。
1 实验材料与方法 1.1 实验材料氧化石墨(自制);羧甲基纤维素IV(AR),购自上海麦克林生物科技有限公司;L-抗坏血酸、亚甲基蓝(MB)购自国药集团化学试剂有限公司且为分析纯。
1.2 羧甲基纤维素/石墨烯复合气凝胶的制备以改进的Hummers法[12]制备粉末状氧化石墨(GO),分别配制一定浓度的GO和羧甲基纤维素(CMC)均相溶液,取两种溶液按质量比GO:CMC=10:1加入搅拌均匀,再按质量比GO:L-抗坏血酸=1:3加入适量L-抗坏血酸。将上述混合溶液装入水热釜中,95 ℃下反应6 h,得到羧甲基纤维素/石墨烯复合水凝胶。经去离子水洗涤至无黄色,冷冻干燥得到羧甲基纤维素/石墨烯复合气凝胶,命名为CMC/GA。
1.3 CMC/GA对MB的吸附配制一定浓度的MB溶液100 mL于锥形瓶中,将称重过的CMC/GA放入MB溶液中,在磁力搅拌器上进行搅拌直至吸附平衡。前期取样间隔为15 min,吸附后期取样间隔为30 min,测定MB的吸光度并计算浓度。MB的吸附量由下式计算。
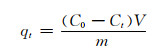
|
(1) |
式中:qt为t时刻的吸附量,mg·g-1;C0和Ct分别为溶液的初始浓度和t时刻的浓度,mg·L-1;m为气凝胶的质量,g;V为溶液的体积,L。
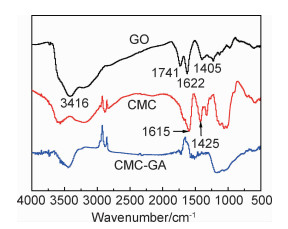
2 结果与分析 2.1 CMC/GA的表征 2.1.1 CMC/GA的官能团类型图 1为GO,CMC和CMC/GA的FT-IR谱图。如图 1所示,GO的FT-IR谱图中出现以下特征峰:3416 cm-1(O—H伸缩振动)、1741 cm-1 (C=O伸缩振动)、1622 cm-1 (C=C伸缩振动)等,与文献中GO红外光谱一致[13]。在CMC的谱图中出现以下特征峰:3345 cm-1(O—H伸缩振动)、1615 cm-1(—COOH伸缩振动)、1425 cm-1(葡萄糖基六元环上O—H的面内弯曲振动)、1100 cm-1(葡萄糖基六元环上C2, C3的C—O伸缩振动),与文献数据吻合[14]。CMC/GA综合了GO与CMC的特征峰,说明GO与CMC很好地复合在一起;经过水热还原后,CMC/GA在1405,1425,1741 cm-1处的吸收峰显著减弱甚至消失,说明GO与CMC的大部分含氧官能团被还原。
|
图 1 GO,CMC和CMC/GA的红外光谱图 Fig. 1 Infrared spectra of GO, CMC and CMC/GA |
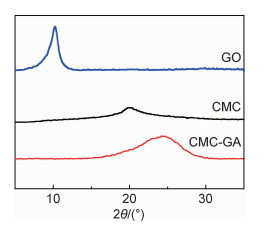
图 2为GO,CMC和CMC/GA的XRD谱图。如图 2所示,GO在2θ=10.9°(片层间距d=0.81 nm)处有一强的特征衍射峰;研究表明[15]石墨的特征衍射峰在2θ=26.4°处(片层间距d=0.34 nm),这表明石墨经过氧化后其片层间距增加,形成了氧化石墨片层。CMC在2θ=19.9°处(片层间距d=4.5 nm)有一特征峰;CMC/GA在2θ=24.2°(片层间距d=0.367 nm)附近有一宽峰。在加入L-抗坏血酸还原后,由于GO和CMC的羟基、羧基、羰基等含氧官能团逐渐减少,石墨烯片层发生重新堆叠、聚集,片层间距缩小,晶体结构的完整性下降,无序度增加,因此谱图中GO和CMC的特征峰消失。说明CMC与GO很好地复合在一起,这与FT-IR的结果是一致的。
|
图 2 GO,CMC和CMC/GA的XRD谱图 Fig. 2 XRD patterns of GO, CMC, CMC/GA |
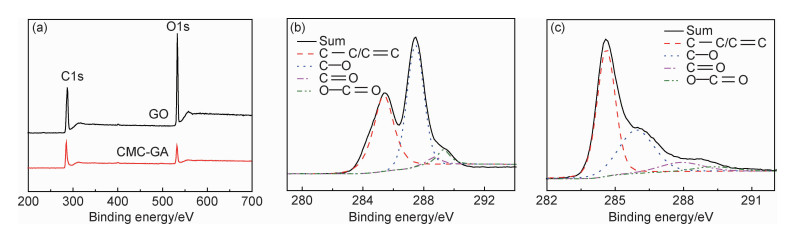
通过XPS对GO和CMC/GA进行元素组成分析,如图 3所示。图 3(a)GO的全谱图中C/O值为1.87,说明所制备的GO含有大量含氧官能团。对C1s谱图分峰处理后,由图 3(b), (c)可知C的类型主要有C—C/C=C(285.0 eV), C—O(286.6 eV), C=O(288.0 eV), O—C=O(289.0 eV),其中含量最多的是C=O[16-17]。对比CMC和GO的C1s谱图可知,CMC/GA的C1s谱图中C—O, C=O, O—C=O含量明显减少,其中C/O值为3.58。说明经过水热还原反应后,L-抗坏血酸上的氢质子与含氧官能团结合生成水,起到了还原的效果[18]。这与FT-IR所得结论类似。
|
图 3 GO和CMC/GA的XPS谱图 (a)总谱图;(b)GO的C1s谱图;(c)CMC/GA的C1s谱图 Fig. 3 XPS spectra of GO and CMC/GA (a)survey spectra; (b)C1s spectra of GO; (c)C1s spectra of CMC/GA |
利用SEM观察CMC/GA的微观形貌结构,结果如图 4所示。由图 4可知,CMC/GA具有丰富的孔隙结构,石墨烯片层之间相互连通,呈现三维网络结构,其孔径尺寸在几微米到上百微米不等。从图 4中还可以看出CMC/GA表面存在大量褶皱和折叠的区域,这些褶皱和三维网状结构不仅增加了气凝胶的比表面积和吸附位点,同时也有助于气凝胶形成超轻和可压缩回弹的性质。

|
图 4 CMC/GA的扫描电镜图 Fig. 4 SEM images of CMC/GA |
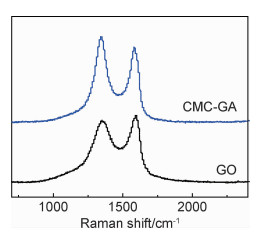
图 5为GO和CMC/GA的Raman光谱图。图中GO和CMC/GA在1350 cm-1和1590 cm-1附近分别有一强峰,前者为D峰,与石墨烯结构的晶格缺陷以及碳原子sp2杂化有关;后者为G峰,是由sp2碳原子的面内振动引起的。ID/IG是衡量石墨烯结构破坏情况的常用方法,ID/IG的比值越大说明石墨烯样品的缺陷程度越大;计算可知GO和CMC/GA的D峰和G峰的比值(ID/IG)分别是0.93和1.14,说明经过水热还原后石墨烯片层产生了更多的缺陷位点,缺陷位点的增加使得材料的表面能更加不均匀,从而增强了材料的吸附性能[18-19]。
|
图 5 GO和CMC/GA的拉曼光谱图 Fig. 5 Raman spectra of GO and CMC/GA |
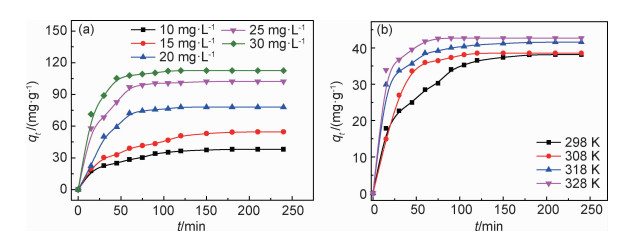
图 6为不同初始浓度和不同温度MB的qt-t关系图。由图 6(a)可以看出MB的初始浓度越大,平衡吸附量越大。MB初始浓度为10,15,20,25,30mg·L-1时,平衡吸附量分别为38.143,54.675,78.064,102.306,112.600 mg·L-1。这是因为当MB初始浓度高时,溶液含有的MB分子多,此时吸附驱动力大大增加,在相同时间内更多的MB分子被CMC/GA吸附;随着时间的增加,溶液浓度逐渐降低,CMC/GA的吸附位点减少,吸附阻力加大,使吸附速率减小逐渐趋于平衡。
|
图 6 MB的qt -t关系图 (a)不同初始浓度;(b)不同温度 Fig. 6 qt -t relation curves of MB (a)different initial concentrations; (b)different temperatures |
如图 6(b)所示,温度升高,CMC/GA的吸附速率增大,平衡吸附量也增加。这是因为温度升高加剧了溶液中MB分子的运动,MB分子与CMC/GA表面吸附位点结合的概率变大,更多的MB分子被吸附在CMC/GA表面,导致吸附量增大。随着吸附时间的增加,CMC/GA对MB的吸附速率先增大后变小,然后逐渐趋于平衡。原因是在吸附初始阶段,CMC/GA的吸附位点多且MB的浓度高,吸附驱动力大;但随着吸附的不断进行,CMC/GA表面的吸附位点逐渐减少,MB浓度较小,吸附阻力增大,进而使吸附速率降低。从图 6(b)中也可以看出CMC/GA对MB的吸附速率非常快,在100 min左右就开始趋于吸附平衡。这主要有两方面的原因:一是CMC/GA的孔道结构丰富,吸附位点多;另一主要原因是加入的CMC是阴离子型醚类纤维素,MB为阳离子染料,CMC与MB之间存在一定的静电作用,从而使吸附速率大大加快。
调研不同研究者所制备吸附材料对MB的吸附能力,汇总于表 1。可发现不同吸附材料对MB的吸附存在较大差别,本工作中CMC/GA对MB的平衡吸附量为112.600 mg·L-1,要高于马尾松球果[6]、改性稻壳[20]、石墨烯-碳纳米管复合材料[8]、纳米二氧化硅[21]等吸附材料;与石墨烯磁性复合材料[23]、椰壳炭[24]、叶蜡石[25]等相比,CMC/GA对MB表现出更强的吸附能力。
为更好地了解CMC/GA对水中MB的吸附,建立一个合适的吸附平衡曲线模型有助于理解CMC/GA的吸附机制。常用的吸附平衡曲线模型有Langmuir模型和Freundlich模型两种。
Langmuir模型[26]是从动力学理论中推导出的单分子层吸附模型,模型假设吸附为单分子层吸附,其表达式如下式所示:
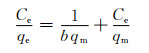
|
(2) |
式中:Ce是平衡浓度,mg·L-1;qe是平衡吸附量,mg·g-1;b是Langmuir模型常数,L·mg-1;qm是极限吸附量,mg·g-1。
Freundlich模型[27]是Henry吸附式的扩展,模型假设为非均匀表面上的吸附,其表达式如式(3)所示:
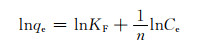
|
(3) |
式中:KF和1/n是Freundlich模型常数,1/n与吸附剂和吸附对象之间的亲和力有关,当0 < 1/n < 1时,吸附过程有利进行[28]。
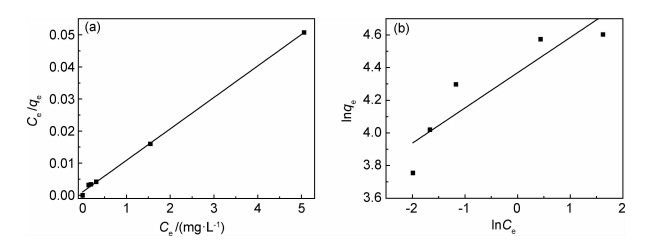
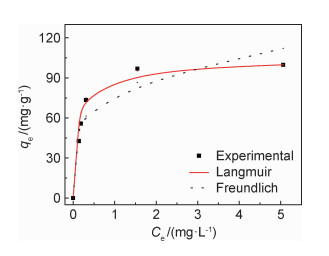
图 7为CMC/GA吸附MB的Langmuir和Freundlich吸附平衡拟合曲线。将图 7所得数据汇总于表 2可知,Langmuir模型的判定系数RL2为0.9986,极限吸附量qm为102.041 mg·g-1。Freundlich模型的判定系数RF2为0.7662,RF2远小于RL2。将实验数据点与两模型的拟合线绘制在图 8中,可清晰地看到实验数据点比较吻合地分布在Langmuir模型拟合线附近。因此,CMC/GA吸附MB过程符合Langmuir模型,表明CMC/GA对MB的吸附是单分子层,增加CMC/GA的比表面积将有利于MB的吸附。
|
图 7 Langmuir(a)和Freundlich(b)拟合曲线 Fig. 7 Fitting curve of Langmuir model(a) and Freundlich model(b) |
| Langmuir | Freundlich | |||||
| b/ (L·mg-1) | qm/ (mg·g-1) | RL2 | KF/ (L·g-1) | 1/n | RF2 | |
| 8.991 | 102.041 | 0.9986 | 78.958 | 0.2159 | 0.7662 | |
|
图 8 CMC/GA吸附MB的吸附等温线 Fig. 8 Adsorption isotherm curves for the adsorption of MB onto CMC/GA |
Langmuir模型的吸附特征可用常数RL来分析[21],其表达式如下式所示:
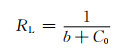
|
(4) |
若0 < RL < 1,吸附是有利的;若RL大于1,则不利于吸附;若RL=0,则说明吸附过程不可逆[21]。经计算得,CMC/GA吸附MB的RL在3.694×10-3~1.100×10-2之间,说明有利于吸附。
2.4 吸附动力学吸附速率是评价材料吸附过程的重要指标,可用准一级动力学(PFO)[29]和准二级动力学(PSO)[30]模型来研究,PFO和PSO表达式如下式所示:
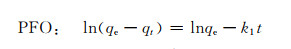
|
(5) |
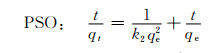
|
(6) |
式中:k1,PFO速率常数,L·min-1;k2,PSO速率常数,g·mg-1·min-1。
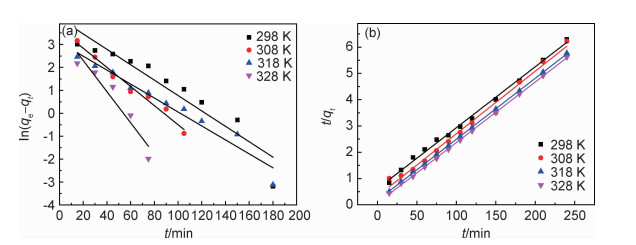
不同温度下CMC/GA吸附MB的PFO和PSO拟合曲线,如图 9所示;速率常数k1,k2和理论平衡吸附量qe, cal可根据PFO和PSO的直线斜率和截距得到,数据结果汇总于表 2。如图 9所示,在298, 308, 318, 328 K 4个温度下PSO模型的判定系数(R22)均远远大于PFO模型的判定系数(R12);同时,采取PSO方程计算出的平衡吸附量qe, cal2与实验得出的吸附量qe, exp更为接近;以上均能说明在不同温度下CMC,GA吸附MB符合PSO模型。不同温度下CMC/GA吸附MB的PFO和PSO模型参数汇总于表 3,由表 3可知,随着吸附温度的升高,k2也变大,也能说明温度对CMC/GA吸附MB有促进作用,温度越高,越利于吸附的进行。
|
图 9 不同温度下CMC/GA吸附MB的PFO(a)和PSO(b)拟合图 Fig. 9 Fitting charts of PFO(a) and PSO(b) for MB adsorbed by CMC/GA at different temperatures |
| T/K | qe, exp/(mg·g-1) | k1/(L·min-1) | qe, cal1/(mg·g-1) | R12 | k2/(g·mg-1·min-1) | qe, cal2/(mg·g-1) | R22 |
| 298 | 38.143 | 0.03360 | 62.368 | 0.8867 | 1.230×10-3 | 41.459 | 0.9962 |
| 308 | 38.542 | 0.04172 | 39.314 | 0.9743 | 2.354×10-3 | 41.186 | 0.9884 |
| 318 | 41.575 | 0.03045 | 22.208 | 0.9513 | 4.144×10-3 | 42.608 | 0.9998 |
| 328 | 42.698 | 0.06803 | 39.127 | 0.8883 | 1.107×10-2 | 43.215 | 0.9996 |
为进一步探究CMC/GA对MB的吸附机制,对CMC/GA吸附过程的活化能进行计算。利用Arrhenius公式求取吸附活化能[31],其表达式如下式所示:

|
(7) |
式中:k为吸附速率常数,g·mg-1·min-1;A为指前因子,g·mg-1·min-1;Ea为吸附活化能,J·mol-1;R为理想气体常数,8.314 J·mol-1·K-1;T为温度,K。
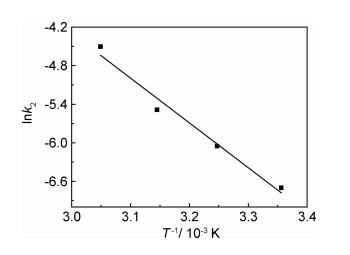
根据吸附速率常数k2,分别以T-1和lnk2为横、纵坐标作图,结果如图 10所示。可得CMC/GA吸附过程的活化能为Ea=57.951 kJ·mol-1。研究表明[32],吸附活化能在5~40 kJ·mol-1之间属于物理吸附,在40~800 kJ·mol-1之间属于化学吸附。说明CMC/GA吸附MB溶液的过程主要为化学吸附,温度越高,吸附速率越快。这是因为CMC为阴离子型纤维素,CMC/GA表面官能团与阳离子型染料MB分子的吸附主要为静电作用。
|
图 10 lnk2-T-1关系图 Fig. 10 Relationship curve of lnk2-T-1 |
CMC/GA吸附不同浓度MB的PFO和PSO模型参数汇总于表 4,由表 4可知,10,15,20,25,30 mg·L-1不同浓度下PSO模型的判定系数(R22)均远远大于PFO模型的判定系数(R12);同时,利用PSO方程计算出的平衡吸附量qe, cal2与实验得出的吸附量qe, exp更为接近;说明CMC/GA吸附不同浓度的MB溶液均符合PSO模型。
| C0/(mg·L-1) | qe, exp/(mg·g-1) | qe, cal1/(mg·g-1) | k1/(L·min-1) | R12 | qe, cal2/(mg·g-1) | k2/(g·mg-1·min-1) | R22 |
| 10 | 38.143 | 62.445 | 0.03362 | 0.8863 | 41.459 | 1.203×10-3 | 0.9893 |
| 15 | 54.675 | 77.643 | 0.02689 | 0.9100 | 60.976 | 5.989×10-4 | 0.9816 |
| 20 | 78.064 | 94.039 | 0.04064 | 0.9699 | 84.962 | 7.448×10-4 | 0.9824 |
| 25 | 102.306 | 80.609 | 0.03842 | 0.9418 | 106.724 | 1.137×10-3 | 0.9966 |
| 30 | 112.60 | 83.236 | 0.04626 | 0.9373 | 115.473 | 1.857×10-3 | 0.9989 |
为了进一步研究CMC/GA吸附MB的内部扩散情况,常用Weber-Morris[33]内扩散(IPD)模型来分析CMC/GA对MB的内扩散吸附机制,IPD模型的表达式如下式所示:
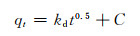
|
(8) |
式中:kd为内部扩散速率常数,mg·g-1·min-0.5;C为截距,mg·g-1。
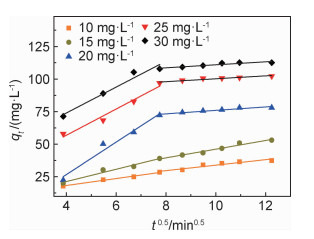
从图 11可明显看出IPD模型拟合直线分为两段,说明CMC/GA对不同浓度MB的吸附均分为两个阶段。第一阶段为大孔扩散,由SEM图可知CMC/GA具有丰富的孔道结构,在吸附开始阶段,MB经过大孔快速扩散至CMC/GA的吸附位点从而被吸附。第二阶段吸附为微孔扩散,MB分子扩散到CMC/GA的内部微孔,相比于第一段,一方面孔道尺寸变小,另一方面随着接触时间增加边界层阻力变大,因此吸附过程斜率明显变缓。
|
图 11 不同初始浓度MB的IPD线性拟合 Fig. 11 Linear relation of IPD model for different initial concentrations MB |
由表 5可知,IPD模型的曲线拟合不过原点说明CMC/GA对MB的吸附过程涉及颗粒的内扩散,但不是唯一的速率限制步骤。通过比较第一段kd1和第二段kd2可发现,不同吸附浓度下的吸附速率随吸附时间的增加是逐渐减小的,即大孔扩散速率大于微孔扩散速率。
| C0/(mg·L-1) | Step Ⅰ | Step Ⅱ | |||||
| C1/(mg·g-1) | kd1/(mg·g-1·min-0.5) | R12 | C2/(mg·g-1) | kd2/(mg·g-1·min-0.5) | R22 | ||
| 10 | 7.465 | 2.699 | 0.9918 | 32.895 | 0.358 | 0.7626 | |
| 15 | 5.953 | 4.072 | 0.9788 | 42.586 | 0.823 | 0.7784 | |
| 20 | -23.197 | 12.467 | 0.9602 | 62.651 | 1.330 | 0.8895 | |
| 25 | 16.627 | 10.060 | 0.9583 | 89.096 | 1.112 | 0.8771 | |
| 30 | 34.207 | 9.939 | 0.9434 | 99.446 | 1.149 | 0.8483 | |
(1) 温度和MB溶液的初始浓度对CMC/GA的吸附有重要的影响,温度升高、MB溶液的初始浓度的增加,有利于CMC/GA对MB的吸附,其平衡吸附量增加且达到吸附平衡时的时间减少。
(2)探究CMC/GA对MB的吸附动力学,发现不同温度和不同初始浓度MB溶液的动力学吸附模型为准二级动力学模型;吸附等温线符合Langmuir模型,根据不同温度下的动力学数据计算吸附体系的活化能为Ea=57.951 kJ·mol-1,说明CMC/GA对MB的吸附的单分子层且为化学吸附。
(3)CMC/GA对MB吸附速率非常快,在100 min左右就趋于吸附平衡。研究CMC/GA吸附MB的内扩散过程,发现CMC/GA对不同浓度MB的吸附过程均分为CMC/GA表面的大孔扩散和内部的微孔扩散两个阶段,且大孔扩散速率大于微孔扩散速率。
| [1] |
BAO N, LI Y, WEI Z, et al. Adsorption of dyes on hierarchical mesoporous TiO2 fibers and its enhanced photocatalytic properties[J]. Journal of Physical Chemistry C, 2011, 115(13): 5708-5719. DOI:10.1021/jp1100939 |
| [2] |
WEI G, MIAO Y, ZHANG C, et al. Ni-doped graphene/carbon cryogels and their applications as versatile sorbents for water purification[J]. ACS Applied Materials & Interfaces, 2013, 5(15): 7584-7591. |
| [3] |
WANG C, SHI Z H, PENG L, et al. Preparation of carbon foam-loaded nano-TiO2 photocatalyst and its degradation on methyl orange[J]. Surfaces & Interfaces, 2017, 7: 116-124. |
| [4] |
KHALID N R, AHMED E, HONG Z L, et al. Graphene modified Nd/TiO2, photocatalyst for methyl orange degradation under visible light irradiation[J]. Ceramics International, 2013, 39(4): 3569-3575. DOI:10.1016/j.ceramint.2012.10.183 |
| [5] |
刘湘粤, 张宇, 王晨, 等. 亚铁盐制备高结晶度MIL-100 (Fe)纳米材料及其光降解有机染料性能[J]. 材料工程, 2018, 46(10): 127-134. LIU X Y, ZHANG Y, WANG C, et al. Highly crystalline MIL-100 (Fe) nanoparticles prepared from ferrous salts and applications in photodegradation of organic dyes[J]. Journal of Materials Engineering, 2018, 46(10): 127-134. |
| [6] |
SEN T K, AFROZE S, ANG H M. Equilibrium, kinetics and mechanism of removal of methylene blue from aqueous solution by adsorption onto pine cone biomass of pinus radiata[J]. Water Air & Soil Pollution, 2010, 218(1/4): 499-515. |
| [7] |
WENG C H, LIN Y T, TZENG T W. Removal of methylene blue from aqueous solution by adsorption onto pineapple leaf powder[J]. Journal of Hazardous Materials, 2009, 170(1): 417-424. DOI:10.1016/j.jhazmat.2009.04.080 |
| [8] |
AI L, JIANG J. Removal of methylene blue from aqueous solution with self-assembled cylindrical graphene-carbon nanotube hybrid[J]. Chemical Engineering Journal, 2012, 192(2): 156-163. |
| [9] |
ZHAO J, REN W, CHENG H M. Graphene sponge for efficient and repeatable adsorption and desorption of water contaminations[J]. Journal of Materials Chemistry, 2012, 22(38): 20197-20202. DOI:10.1039/c2jm34128j |
| [10] |
黄扬帆, 刘会娥, 马雁冰, 等. 乳液法制备石墨烯气凝胶及其吸附水中亚甲基蓝[J]. 化工进展, 2018, 37(8): 3092-3099. HUANG Y F, LIU H E, MA Y B, et al. Fabrication of graphene aerogels by emulsion method and their adsorption of methylene blue[J]. Chemical Industry and Engineering Progress, 2018, 37(8): 3092-3099. |
| [11] |
ZHOU G, LI F, CHENG H M. Progress in flexible lithium batteries and future prospects[J]. Energy Environ Sci, 2014, 7(4): 1307-1338. DOI:10.1039/C3EE43182G |
| [12] |
DONG G S, YEO H, KU B C, et al. A facile synthesis method for highly water-dispersible reduced graphene oxide based on covalently linked pyridinium salt[J]. Carbon, 2017, 121: 17-24. DOI:10.1016/j.carbon.2017.05.064 |
| [13] |
PENG L, XU Z, LIU Z, et al. An iron-based green approach to 1-h production of single-layer graphene oxide[J]. Nature Communications, 2015, 6: 5716-5716. DOI:10.1038/ncomms6716 |
| [14] |
WAN C, LI J. Graphene oxide/cellulose aerogels nanocomposite: preparation, pyrolysis, and application for electromagnetic interference shielding[J]. Carbohydrate Polymers, 2016, 150: 172-179. DOI:10.1016/j.carbpol.2016.05.051 |
| [15] |
CHEN J, CHI F, HUANG L, et al. Synthesis of graphene oxide sheets with controlled sizes from sieved graphite flakes[J]. Carbon, 2016, 110: 34-40. DOI:10.1016/j.carbon.2016.08.096 |
| [16] |
HAN Z, TANG Z, LI P, et al. Ammonia solution strengthened three-dimensional macro-porous graphene aerogel[J]. Nanoscale, 2013, 5(12): 5462-5467. DOI:10.1039/c3nr00971h |
| [17] |
LI Y, CHEN J, HUANG L, et al. "Pottery" of porous graphene materials[J]. Advanced Electronic Materials, 2015, 1(5): 1-7. |
| [18] |
SUI Z, ZHANG X, LEI Y, et al. Easy and green synthesis of reduced graphite oxide-based hydrogels[J]. Carbon, 2011, 49(13): 4314-4321. DOI:10.1016/j.carbon.2011.06.006 |
| [19] |
ZHANG Y, TAO B, XING W, et al. Sandwich-like nitrogen-doped porous carbon/graphene nanoflakes with high-rate capacitive performance[J]. Nanoscale, 2016, 8(15): 7889-7898. DOI:10.1039/C5NR05151G |
| [20] |
夏天明, 王营茹, 范鹏程, 等. 改性稻壳吸附亚甲基蓝模拟废水试验研究[J]. 工业水处理, 2013, 33(3): 47-50. XIA T M, WANG Y R, FAN P C, et al. Study on the adsorption of modified rice hull for methylene blue in simulated wastewater[J]. Industrial Water Treatment, 2013, 33(3): 47-50. |
| [21] |
FERENCZI S, DEVENYI T. SnO2 quantum dots decorated silica nanoparticles for fast removal of cationic dye (methylene blue) from wastewater[J]. Chemical Engineering Journal, 2015, 281(4): 482-490. |
| [22] |
BO Y, CHEN Z, LU C, et al. Fabrication of polyaniline hydrogel: synthesis, characterization and adsorption of methylene blue[J]. Applied Surface Science, 2015, 356: 39-47. DOI:10.1016/j.apsusc.2015.08.024 |
| [23] |
ZHANG C, CHEN Z. Removal of methylene blue from aqueous solution by a solvothermal-synthesized graphene/magnetite composite[J]. Journal of Hazardous Materials, 2011, 192(3): 1515-1524. DOI:10.1016/j.jhazmat.2011.06.068 |
| [24] |
KAVITHA D, NAMASIVAYAM C. Experimental and kinetic studies on methylene blue adsorption by coir pith carbon[J]. Bioresour Technol, 2007, 98(1): 14-21. DOI:10.1016/j.biortech.2005.12.008 |
| [25] |
SHENG J W, XIE Y N, ZHOU Y. Adsorption of methylene blue from aqueous solution on pyrophyllite[J]. Applied Clay Science, 2009, 46(4): 422-424. DOI:10.1016/j.clay.2009.10.006 |
| [26] |
YU D S, LV T T, CHEN G H, et al. Characteristics of ammonia adsorption and kinetics by nitrifying sludge immobilized pellets[J]. Environmental Science, 2019, 40(2): 774-782. |
| [27] |
葛梦妮, 张建峰, 曹惠杨, 等. 剥离时间对二维Ti3C2吸附染料污染物性能的影响[J]. 材料工程, 2018, 46(7): 144-150. GE M N, ZHANG J F, CAO H Y, et al. Effect of etching time on the adsorption performance of two-dimensional Ti3C2 for organic dyes[J]. Journal of Materials Engineering, 2018, 46(7): 144-150. |
| [28] |
VASILIU S, BUNIA I, RACOVITA S, et al. Adsorption of cefotaxime sodium salt on polymer coated ion exchange resin microparticles: kinetics, equilibrium and thermodynamic studies[J]. Carbohydrate Polymers, 2011, 85(2): 376-387. DOI:10.1016/j.carbpol.2011.02.039 |
| [29] |
王艳春, 曾效舒, 敖志强, 等. 热还原石墨烯的制备及其对重金属Pb2+的吸附性[J]. 材料工程, 2017, 45(10): 6-11. WANG Y C, ZENG X S, AO Z Q, et al. Preparation of graphene via thermal reduction and its adsorption capacity for heavy metal Pb2+[J]. Journal of Materials Engineering, 2017, 45(10): 6-11. |
| [30] |
MOHAMMAD M, MAITRA S, AHMAD N, et al. Metal ion removal from aqueous solution using physic seed hull[J]. Journal of Hazardous Materials, 2010, 179(1/3): 363-372. |
| [31] |
WU C H. Adsorption of reactive dye onto carbon nanotubes: equilibrium, kinetics and thermodynamics[J]. Journal of Hazardous Materials, 2007, 144(1): 93-100. |
| [32] |
ELLATIF M A, IBRAHIM A M, ELKADY M. Adsorption equilibrium, kinetics and thermodynamics of methylene blue from aqueous solutions using biopolymer oak sawdust composite[J]. The Journal of American Science, 2010, 6(6): 267-283. |
| [33] |
AHMED, MUTHANNA J. Adsorption of quinolone, tetracycline, and penicillin antibiotics from aqueous solution using activated carbons: review[J]. Environ Toxicol Pharmacol, 2017, 50: 1-10. DOI:10.1016/j.etap.2017.01.004 |
 2020, Vol. 48
2020, Vol. 48


