文章信息
- 刘媛媛, 李舒婷, 彭军, 安胜利
- LIU Yuan-yuan, LI Shu-ting, PENG Jun, AN Sheng-li
- Gd2O3掺杂量对Ce1-xGdxO2-δ电解质导电性能的影响
- Influence of Gd2O3 doping contents on conductivity of Ce1-xGdxO2-δ electrolyte
- 材料工程, 2020, 48(6): 118-124
- Journal of Materials Engineering, 2020, 48(6): 118-124.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000322
-
文章历史
- 收稿日期: 2019-04-06
- 修订日期: 2020-01-16
2. 内蒙古先进陶瓷材料与器件重点实验室, 内蒙古 包头 014010;
3. 内蒙古科技大学 化学与化工学院, 内蒙古 包头 014010
2. Inner Mongolia Key Laboratory of Advanced Ceramic Materials and Devices, Baotou 014010, Inner Mongolia, China;
3. College of Chemistry and Chemical Engineering, Inner Mongolia University of Science and Technology, Baotou 014010, Inner Mongolia, China
SOFC作为一种新型洁净的能量转换装置,以其能量转换效率高、环境友好、燃料适应性强(可直接利用生物质气)等突出优点,而受到广泛关注[1-3]。固体电解质作为SOFC的核心组分,是其能够以不受卡诺循环限制的非热机方式直接高效发电的根源[4-5]。在SOFC中,电解质层主要起隔断阴阳极之间的气体扩散和电子传导,以及将生成于阴极侧的氧离子在氧分压的驱动下传输到阳极的作用。目前研究和使用比较多的电解质材料包括掺杂氧化锆、掺杂氧化铈、锶和锰掺杂的镓酸镧以及一些新型材料[6-7]。其中,掺杂CeO2被认为是最有前景的中低温SOFC电解质材料[8-10],当掺杂离子半径与主离子半径(Ce4+)最为接近时,获得最高的氧离子电导率[11-14]。对于Ce4+而言,Gd3+及Sm3+与其具有较为相近的离子半径,在各种Gd及Sm掺杂浓度下,在500~700 ℃具有较高的离子电导率[15-16]。在低于700 ℃时,掺杂CeO2的电导率约高于YSZ电解质材料1~2个数量级,一定程度上和Ce4+半径(0.087 nm)大于Zr4+半径(0.082 nm)有关,大的离子半径会导致氧离子在较为开放的空间结构中更容易迁移[17]。然而,CeO2基电解质材料也存在稳定性问题,在低氧分压下(当氧分压小于10-14 Pa)Ce4+会被还原成Ce3+,产生电子泄露现象,且影响SOFC电解质体积,这种现象主要产生3种结果:(1)还原过程造成点阵体积膨胀,影响电解质力学性能;(2)电子电导的引入导致阴阳极之间的电子泄露,降低SOFC电化学性能;(3)混合离子电子导体特性降低CeO2基材料中的离子迁移数及SOFC电池的开路电压(OCV),最终减小CeO2基材料应用于SOFC电解质的效率[18-20]。
本工作以不同含量Gd2O3的Ce1-xGdxO2-δ为研究对象,应用交流阻抗谱法(AC impedance)和Hebb-Wagner极化法,分析在空气气氛下,不同Gd2O3掺杂量对GDC固体电解质总电导率及电子电导率的影响,研究总电导率、电子电导率与Gd2O3掺杂量、温度、氧分压之间的变化规律,为固体电解质组装的SOFC提供实验基础。
1 实验 1.1 GDC粉体的合成采用溶胶-凝胶法合成了不同掺杂比例的Ce1-xGdxO2-δ(x=0.05,0.10,0.15,0.20,0.25,摩尔分数)固体电解质粉体[21]。按照化学计量比称取适量的Gd2O3和Ce(NO3)3·6H2O,其中Gd2O3溶于适量的稀硝酸中,Ce(NO3)3·6H2O溶于去离子水中。将两种溶液完全溶解后混合,并向其中加入柠檬酸、EDTA氨水溶液和硝酸铵,金属氧化物(阳离子): EDTA:柠檬酸:硝酸铵的摩尔比为1:1:1.2:1.5。待溶液充分混合后置于水浴锅中,用氨水调节溶液pH值至中性,80 ℃水浴加热至形成白色凝胶,将凝胶置于电阻炉上加热,生成浅黄色前驱体。将该前驱体置于马弗炉中800 ℃焙烧,得到实验所需粉体。将所得粉体置于φ16 mm模具中,利用台式电动压片机压制成片。在1450 ℃下烧结5 h,得到致密性良好的GDC电解质片。
1.2 样品物相和微观组织表征采用PW1700型X射线衍射仪对GDC粉体进行物相分析,衍射靶为Cu靶,工作电压40 kV,工作电流40 mA,扫描速率2 (°)/min,衍射角10°~90°;采用JSM6510型SEM电镜表征GDC电解质片的表面和断面微观组织。
1.3 GDC电解质电导率测定采用IVIUMSTAT电化学工作站测试5种不同掺杂量GDC的交流阻抗谱图和极化曲线,实验在空气中进行,测试频率0.1~106 Hz,测量温度450~750 ℃,温度间隔50 ℃。根据得到的交流阻抗谱,由式(1)计算GDC电解质的总电导率值。
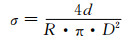
|
(1) |
式中:σ为电解质总电导率,S·cm-1; R为对应温度下的阻抗,Ω;D为电解质片的直径,cm;d为电解质片的厚度,cm。
1.4 离子阻塞电极的制备及电子电导率测定在Ce1-xGdxO2-δ电解质片表面涂铂浆,焙烧形成铂电极,用高温密封材料将粘有银丝的一侧密封于φ16 mm×3 mm的刚玉坩埚中,组装成阻塞电极测量电池:(-) O2(阻塞电极), Pt | Ce1-xGdxO2-δ(GDC) | Pt, O2(air) (+)。待测量电池的两个电极分别通过银丝连接到电化学测试仪器上,采用Hebb-Wagner极化法测量Ce1-xGdxO2-δ电解质的电子电导率。
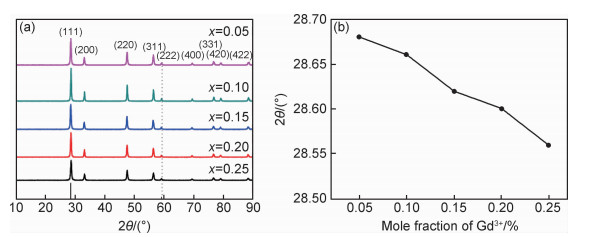
2 结果与讨论 2.1 GDC粉体物相分析图 1为不同掺杂量GDC的XRD谱图及特征峰衍射角。采用溶胶-凝胶法制备的5种不同Gd3+掺杂量的GDC粉体在800 ℃烧结2 h,去除未完全反应的有机物之后测得的XRD谱图如图 1(a)所示,可以看出,5种不同Gd3+掺杂量的GDC衍射峰相对强度与角度均与立方萤石结构的CeO2的标准卡JCPDS 89-8436相一致,XRD谱图中没有新的衍射峰出现,说明已经形成了具有单一立方萤石结构的GDC。图 1(b)为GDC粉体(111)晶面衍射峰位置随Gd3+掺杂量的变化,可以看到,随着Gd2O3含量的增加,GDC的衍射峰向低角度偏移,说明晶格常数增大,这是因为Gd3+的半径比Ce4+的半径大,Gd3+进入晶格中取代部分Ce4+,导致晶格膨胀,这与之前报道的研究结果一致[22]。
|
图 1 不同掺杂量GDC的XRD谱图(a)及特征峰衍射角变化(b) Fig. 1 XRD patterns of different doping amounts GDC(a) and the variation of characteristic peak diffraction angle(b) |
通过形貌的表征可以判断电解质片晶体的生长情况,便于考察不同成分GDC晶体的生长差异。5种不同Gd3+掺杂量(x=0.05,0.10,0.15,0.20,0.25)GDC电解质烧结体的表面和断面形貌如图 2所示。可知,GDC固体电解质的表面晶粒生长较好,分布均匀,且致密性较佳;断面晶粒度相对比较均匀、致密,虽有微孔,但均为闭口。

|
图 2 不同Gd3+掺杂量GDC固体电解质的表面(1)和断面(2)SEM图 (a)x=0.05;(b)x=0.10;(c)x=0.15;(d)x=0.20;(e)x=0.25 Fig. 2 SEM images of surface(1) and cross section(2) for different Gd3+ doping GDC electrolytes (a)x=0.05;(b)x=0.10;(c)x=0.15;(d)x=0.20;(e)x=0.25 |
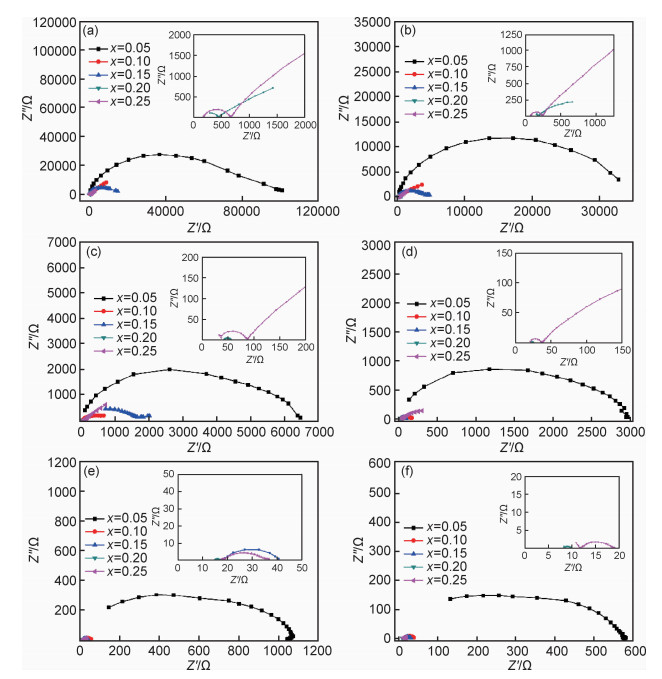
空气气氛下,450~750 ℃时Ce1-xGdxO2-δ固体电解质的交流阻抗谱图如图 3所示。
|
图 3 空气气氛下不同测试温度时GDC电解质的交流阻抗谱 (a)500 ℃; (b)550 ℃; (c)600 ℃; (d)650 ℃; (e)700 ℃; (f)750 ℃ Fig. 3 Impedance spectra of GDC electrolytes at different text temperatures in air (a)500 ℃; (b)550 ℃; (c)600 ℃; (d)650 ℃; (e)700 ℃; (f)750 ℃ |
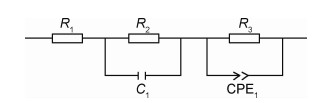
对氧离子固体电解质,理想的阻抗图谱均由晶粒、晶界、极化3个半圆构成,这是因为晶粒过程、晶界过程和电极反应过程具有的时间常数不同,因此在不同的频率范围内阻抗谱中出现不同的圆弧[15-16]。从图 3中可以看出,在高温时,仅有一个完整的圆弧,对应于晶界电阻,高频端与实轴的交点即为晶粒电阻,在低于700 ℃时,交流阻抗谱上出现2个明显的半圆弧,是因为低温下极化反应速率较慢,极化电阻较大,而高温下,该反应的过程迅速,极化电阻很小,因而在交流阻抗谱上无对应的圆弧出现[23]。根据GDC的交流阻抗谱可知,掺杂量为0.20的总电导率最大,用Z-view进行数据拟合,其等效电路为R1(R2C1)(R3Q1)(图 4),其中R1,R2,R3分别代表晶粒电阻、晶界电阻和极化电阻,Q代表一个常相位角元件(CPE),分析得到待测样品的总电阻值,根据式(1)计算得到总电导率。
|
图 4 固体电解质的等效电路图 Fig. 4 Equivalent circuit of solid electrolytes |
图 5为不同Gd2O3含量GDC电解质的总电导率和温度关系曲线。对比5种不同Gd2O3含量的GDC总电导率可以发现,掺杂量为0.20时,总电导率最大,为8.59×10-2 S · cm-1(750 ℃)。这是因为,随着Gd2O3掺杂量增加,GDC中氧空位浓度越来越高,氧离子迁移能力不断增强,同时氧空位间的库仑作用也不断增大。当Gd的掺杂量为0.20时,氧离子总电导率最大,是由于当Gd掺杂量继续增加时,晶格内氧空位浓度过高,各种缺陷间的相互作用成为主导因素,氧空位移动受到束缚,所以更大的掺杂量反而使离子导电能力下降[18]。

|
图 5 不同掺杂量GDC电解质的总电导率与温度的关系 Fig. 5 Relationship between total conductivity of different doping GDC electrolytes and temperature |
纯的CeO2离子总电导率很低(σ600 ℃约为10-5 S·cm-1),掺杂Gd3+之后电解质Ce1-xGdxO2-δ的离子总电导率有非常明显的提升,因为三价离子Gd3+的掺杂增加了氧空位[20]: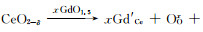
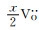
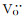
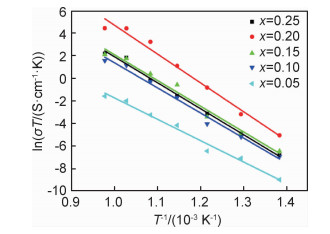
图 6为450~750 ℃下不同掺杂量GDC总电导率与温度的Arrhenius线性关系。可以看出,GDC电解质的总电导率σ与温度T的关系符合Arrhenius方程。
|
图 6 不同掺杂量GDC总电导率与温度的Arrhenius线性关系 Fig. 6 Arrhenius linear relationship between total conductivity of different doping GDC and temperature |
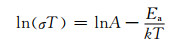
|
(2) |
式中:k为玻尔兹曼常数,k=8.617 ×10-5 eV/K;A为指前因子,是与结构有关而与温度无关的物理量;Ea为活化能,eV。
根据式(2),由图 6中直线斜率可求得活化能Ea的值。从图 6可知,GDC固体电解质的总电导率与温度呈现出良好的线性关系,并且随着温度的升高而增大。表 1列出了Ce1-xGdxO2-δ总电导率的活化能,可以看到,x=0.05的活化能最低,而x=0.20的活化能最高,说明Gd3+的掺杂量会直接影响氧空位的产生数量,所以迁移速率会随着氧空位的增多(即掺杂量的增加)而增大,但随着掺杂量增大,过多的氧空位会缔合,且GDC的晶格常数增大,导致晶体弹性应变加强,使得氧空位缔合能力增加,减少了自由氧空位的数量,从而增大了GDC的活化能[12]。
| x | Ea/eV |
| 0.05 | 0.8263 |
| 0.10 | 0.9112 |
| 0.15 | 0.9591 |
| 0.20 | 0.9945 |
| 0.25 | 0.9242 |
从表 1的活化能数据可以看出,5个组分GDC电解质的活化能均小于1 eV,都属于快离子导体,x=0.20组分的GDC活化能相对较大,说明在该成分下氧离子通道最多,导电所需经过能垒增大。活化能越高,温度升高时反应速率增加得越快,反应速率对温度越敏感[14]。
2.4 GDC电子电导率 2.4.1 极化电压的选择选取掺杂量为0.20的GDC阻塞电极电池为样品,对其施加外电压。极化电压的范围为0.2~0.7 V,以0.1 V为间隔,在450~750 ℃范围内测试电池在每个电压点的输出电流,得到不同温度下Ce0.8Gd0.2O1.9的Hebb-Wagner极化曲线,如图 7所示。

|
图 7 不同温度下Ce0.8Gd0.2O1.9的Hebb-Wagner极化曲线 Fig. 7 Hebb-Wagner polarization curves of Ce0.8Gd0.2O1.9 at different temperatures |
从图 7可以看出,当电压在0.2~0.6 V时,电流随电压增长缓慢,说明离子阻塞电极中密封的氧气都可以被抽出。而当极化电压大于0.6 V时,电流增大迅速,此时样品不稳定。所以,极化电压为0.6 V是外加电压的最佳选择。
2.4.2 电子电导率分析Hebb-Wagner极化法的原理采用不对称电池设计,一端是离子阻塞电极, 另一端为可逆电极。当对其施加合适的外加电压时,氧离子将在外电压的作用下迁移至外侧,阻塞电极侧氧气变为氧原子。若要2p轨道电子全充满,需不断从外电路获得电子生成O2-,进入电解质中的氧空位。其缺陷反应方程式为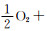

当由电位梯度产生的离子流和由浓度梯度产生的化学扩散离子流相等时,离子流降为0,此时电流只由电子或电子空穴产生[19]。电子电导率σe为:
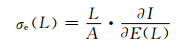
|
(3) |
式中:L,A,I和E分别为电解质的厚度,截面面积,稳态电流和极化电压。
图 8为不同Gd2O3掺杂量的GDC电解质的电子电导率和氧分压的关系曲线。可以看出,不论哪个组分,随着氧分压的降低,电子电导率也随之下降,在5个组分中,掺杂量为0.10的GDC的电子电导率在所取氧分压范围内,电子电导率均最大,为6.47×10-4 S·cm-1(750 ℃),相比于其他组分,掺杂量为0.25的GDC的电子电导率最小。实验结果说明,Gd3+的掺杂量抑制了电子电导的产生,在组装SOFC时常用的掺杂量0.20的GDC电解质也具有较小的电子电导率,这使得氧离子导电能力更强。

|
图 8 不同掺杂量GDC的电子电导率与氧分压的关系 Fig. 8 Relationship between PO2 of different doping GDC and electronic conductivity |
图 9为450~750 ℃下不同掺杂量GDC电子电导率与温度的Arrhenius关系图。可以看出,GDC固体电解质的电子电导率随掺杂量的增加而降低,这是因为Gd3+的掺杂限制了Ce4+的还原过程。但掺杂量为0.05时的电子电导率并不是最大的,这是因为Gd3+的掺杂限制了电子电导的产生,同时因为掺杂量太低没有产生足够的氧空位。GDC固体电解质中电子电导的产生是由于发生Ce4+向Ce3+的转变,其电子电导率随温度的升高而增大,升温过程导致电子动能增加,热运动增强,能量增大,移动速率增加所导致。

|
图 9 不同掺杂量GDC电子电导率与温度的Arrhenius线性关系 Fig. 9 Arrhenius linear relationship between electronic conductivity of different doping GDC and temperature |
通过图 9中的Arrhenius曲线,计算得出450~750 ℃时Ce1-xGdxO2-δ的电子电导率活化能,见表 2。可以看出活化能值较大,表明在此温度范围内GDC电解质的电子导电能力不强。
| x | Ea/eV |
| 0.05 | 1.453 |
| 0.10 | 1.221 |
| 0.15 | 1.250 |
| 0.20 | 1.190 |
| 0.25 | 0.9687 |
(1) 应用溶胶-凝胶法合成了GDC粉体,XRD表征其晶体结构为立方萤石结构。在1450 ℃下烧结5 h后,获得致密的GDC固体电解质。
(2) 利用交流阻抗方法测量了GDC电解质在450~750 ℃的总电导率,750 ℃时总电导率为σ(x=0.20)>σ(x=0.25)>σ(x=0.15)>σ(x=0.10)>σ(x=0.05)。x=0.20、温度为750 ℃时,总电导率最大,可达8.59×10-2 S·cm-1。
(3) 设计的离子阻塞电极可以成功阻塞氧离子。在450~750 ℃下,GDC固体电解质的电子电导率为10-7~10-4 S·cm-1。x=0.10、温度为750 ℃时,电子电导率最大,达6.47×10-4 S·cm-1。
(4) 掺杂量为0.20时,GDC电解质具有最高的总电导率和相对较小的电子电导率。
| [1] |
MINH N Q. Ceramic fuel-cells[J]. Journal of the American Ceramic Society, 1993, 76: 563-588. DOI:10.1111/j.1151-2916.1993.tb03645.x |
| [2] |
石井弘毅.图说燃料电池的原理与应用[M].白彦华, 杨晓辉, 译.北京: 科学出版社, 2003. ISHII H. Illustrated the principle and application of fuel cell[M]. Translated by BAI Y H, YANG X H.Beijing: Science Press, 2003. |
| [3] |
毛宗强.燃料电池[M].北京: 化学工业出版社, 2005. MAO Z Q. Fuel cell[M]. Beijing: Chemical Industry Press, 2005. |
| [4] |
STEELE B C, HEINZEL A. Materials for fuel-cell technologies[J]. Nature, 2001, 414(6861): 345-352. DOI:10.1038/35104620 |
| [5] |
MINH N Q, TAKAHASHI T. Science and technology of ceramic fuel cells[M]. Amsterdam: Elsevier, 1990.140.
|
| [6] |
韩敏芳, 张永亮. 固体氧化物燃料电池中的陶瓷材料[J]. 硅酸盐学报, 2017(45): 1548-1554. HAN M F, ZHANG Y L. Ceramic materials for solid oxide fuel cell[J]. Journal of the Chinese Ceramic Society, 2017(45): 1548-1554. |
| [7] |
LAKSHMI V V, BAURI R, GANDHI A S, et al. Synthesis and characterization of nanocrystalline ScSZ electrolyte for SOFCs[J]. International Journal of Hydrogen Energy, 2011, 36(22): 14936-14942. DOI:10.1016/j.ijhydene.2011.02.139 |
| [8] |
薛守庆. 纳米二氧化铈的化学制备方法及应用研究[J]. 化工技术与开发, 2014(8): 38-40. XUE S Q. Study progress of chemical preparation of nanometer CeO2[J]. Technology & Development of Chemical Industry, 2014(8): 38-40. DOI:10.3969/j.issn.1671-9905.2014.08.013 |
| [9] |
郭瑞华, 张捷宇, 周国治, 等. 固体氧化物燃料电池电解质Gd0.1BaxCe0.9-xO2-σ的制备及性能分析研究[J]. 化工新型材料, 2017, 45(7): 120-122. GUO R H, ZHANG J Y, ZHOU G Z, et al. Preparation and performance analysis of solid oxide fuel cell electrolyte Gd0.1BaxCe0.9-xO2-σ[J]. New Chemical Materials, 2017, 45(7): 120-122. |
| [10] |
WUT W, JIA G X, WANG X X, et al. Transitional area of Ce4+ to Ce3+ in SmxCayCe1-x-yO2-δ with various doping and oxygen vacancy concentrations: a GGA+U study[J]. Chinese J Struct Chem, 2018, 37(2): 198-209. |
| [11] |
吴铜伟, 贾桂霄, 包金小, 等. CaO或BaO与Sm2O3共掺杂CeO2体系电子结构和氧离子迁移的DFT+U研究[J]. 无机化学学报, 2016, 32(8): 1363-1369. WU T W, JIA G X, BAO J X, et al. Electronic structure and oxygen ion migration of the CaO or Bao and Sm2O3Co-doped CeO2system:a DFT + U study[J]. Chinese Journal of Inorganic Chemistry, 2016, 32(8): 1363-1369. |
| [12] |
YAHIRO H, EGUCHI Y, EGUCHI K, et al. Oxygen ion conductivity of the ceria-samarium oxide system with fluorite structure[J]. Journal of Applied Electrochemistry, 1988, 18(4): 527-531. DOI:10.1007/BF01022246 |
| [13] |
苑亚杰, 张梦霏, 李天君, 等. Ce0.8Sm0.1Nd0.1O2-σ/La10Si6O27复合电解质材料的电学性能研究[J]. 稀有金属材料与工程, 2018, 47(1): 339-343. YUAN Y J, ZHANG M F, LI T J, et al. Electrical properties of Ce0.8Sm0.1Nd0.1O2-σ/La10Si6O27composite electrolyte[J]. Rare Metal Materials and Engineering, 2018, 47(1): 339-343. |
| [14] |
ZHANG T S, MA J, CHENG H, et al. Ionic conductivity of high-purity Gd-doped ceria solid solutions[J]. Materials Research Bulletin, 2006, 41(3): 563-568. DOI:10.1016/j.materresbull.2005.09.008 |
| [15] |
MOGENSEN M, SAMMES N M, TOMPSETT G A. Physical, chemical and electrochemical properties of pure and doped ceria[J]. Solid State Ionics, 2000, 129: 63-94. DOI:10.1016/S0167-2738(99)00318-5 |
| [16] |
STEELE B C H. Appraisal of Ce1-yGdyO2-y/2 electrolytes for IT-SOFC operation at 500 ℃[J]. Solid State Ionics, 2000, 129: 95-110. DOI:10.1016/S0167-2738(99)00319-7 |
| [17] |
LEE K T, YOON H S, WACHSMAN E D. The evolution of low temperature solid oxide fuel cells[J]. Journal of Materials Research, 2012, 27: 2063-2078. DOI:10.1557/jmr.2012.194 |
| [18] |
SHIMONOSONO T, HIRATA Y, EHIRA Y, et al. Electronic conductivity measurement of Sm- and La-doped ceria ceramics by Hebb-Wagner method[J]. Journal of Solid State Ionics, 2004, 174(1/4): 27-33. |
| [19] |
WANG S R, TAKEHISA K, MASAYUKI D, et al. Electrical and ionic conductivity of Gd-doped ceria[J]. Journal of the Electrochemical Society, 2000, 147(10): 3606-3609. DOI:10.1149/1.1393946 |
| [20] |
QIAN J, TAO Z, XIAO J, et al. Performance improvement of ceria-based solid oxide fuel cells with yttria-stabilized zirconia as an electronic blocking layer by pulsed laser deposition[J]. International Journal of Hydrogen Energy, 2013, 38: 2407-2412. DOI:10.1016/j.ijhydene.2012.11.112 |
| [21] |
程亮, 罗凌虹, 徐序, 等. 燃烧法制备不同钆含量的GDC纳米粉体及其电导性[J]. 硅酸盐学报, 2018(3): 354-360. CHENG L, LUO L H, XU X, et al. Preparation of GDC nano-powder with different gadolinium contents by combustion method and its electrical conductivity[J]. Journal of the Chinese Ceramic Society, 2018(3): 354-360. |
| [22] |
宋希文, 赵永旺, 彭军, 等. Gd2O3掺杂CeO2-δ固体电解质的电化学性能研究[J]. 功能材料, 2004, 35(增刊1): 988-990. SONG X W, ZHAO Y W, PENG J, et al. Electrochemical performance of Gd2O3 doped CeO2-δelectrolyte[J]. Journal of Functional Materials, 2004, 35(Suppl 1): 988-990. |
| [23] |
史美伦.交流阻抗谱原理及应用[M].北京: 国防工业出版社, 2001. SHE M L. AC impedance spectroscopy principles and applications[M]. Beijing: National Defense Industry Press, 2001. |
| [24] |
王立帆, 刘媛媛, 彭军, 等. Ce0.8Sm0.2O1.9固体电解质的电子电导性研究[J]. 中国稀土学报, 2018, 36(1): 107-113. WANG L F, LIU Y Y, PENG J, et al. Study on the electronic conductivity of Ce0.8Sm0.2O1.9 solid electrolyte[J]. Journal of the Chinese Rare Earth Society, 2018, 36(1): 107-113. |
 2020, Vol. 48
2020, Vol. 48


