文章信息
- 张小广, 邓慧宇, 陈庆春, 邦宇, 晏乐安, 那兵
- ZHANG Xiao-guang, DENG Hui-yu, CHEN Qing-chun, BANG Yu, YAN Le-an, NA Bing
- 5-异氰酸酯异肽酰氯/ZnO/超支化聚酰胺纳滤膜的制备及性能
- Preparation and characterization of 5-isocyanato-isophthaloyl chloride/ZnO/hyperbranched polyamide nanofiltration membranes
- 材料工程, 2020, 48(5): 91-99
- Journal of Materials Engineering, 2020, 48(5): 91-99.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000725
-
文章历史
- 收稿日期: 2019-08-01
- 修订日期: 2019-12-12
2. 东华理工大学 核资源与环境国家重点实验室, 南昌 330013
2. State Key Laboratory of Nuclear Resources and Environment, East China University of Technology, Nanchang 330013, China
膜污染是降低膜使用寿命的关键因素之一,主要有无机、结垢、有机和生物污染等几种类型。其中,有机和生物污染对膜性能的影响尤为严重。增强膜的亲水性可提高膜的抗有机污染,而提高膜的抗生物污染则通常是在膜表面或本体中引入抑菌物质,如纳米银、碳纳米管、石墨烯、二氧化钛、季铵盐、卤胺、辣素碱、茶多酚及壳聚糖等[1-3]。事实上,多数抑菌剂不仅具有抑菌效果,而且能增强膜的亲水性,如二氧化钛、季铵盐、壳聚糖等。ZnO是一种Ⅱ-Ⅵ宽带隙半导体材料,激子束缚能较高(60 meV),具有非迁移性荧光性,可见光透过率80%以上,通过引入缺陷能级可获得较低的电阻率(10-3~10-4 Ω·cm),目前,已广泛应用于光学材料[4]、光电材料[5]、气敏元件[6]、透明电极[7-8]、太阳能电池材料等领域。
近年来,人们发现ZnO具有与TiO2类似的抑菌性。当其粒度处于纳米级时,由于量子尺寸效应,导带和价带能级变成分立能级,能隙变宽。光照下,价带上的电子被激发到导带上,形成空穴,将吸附在ZnO粒子表面的—OH和H2O分子氧化成羟基自由基,这些自由基可将小分子有机物细菌分解成二氧化碳而具有抑菌性。研究表明[9-10],无光催化作用时,Zn2+的存在同样赋予ZnO抑菌特性。因此,采用ZnO及其衍生物以改善膜性能引起人们的广泛关注。Hayati等[11]直接将纳米ZnO与待处理的刚果红染料溶液混合,然后用哌嗪聚酰胺纳滤膜分离,发现ZnO的存在能减少刚果红在分离过程中对膜孔的堵塞,从而提高膜通量。Juholin等[12]采用原子层沉积法在NF270,NF90商品纳滤膜上沉积ZnO,发现表面负载20 nm厚ZnO层后,虽然两种膜的疏水性及粗糙度均增大,但是在处理采矿废水时,膜的通量恢复率明显比未改性膜高。Stefan等[13]和Zangeneh等[14]则分别将纳米ZnO和(C,N,S三摻杂)L-蛋氨酸-TiO2-ZnO与聚醚砜(PES)共混,然后相转化成膜,发现氧化锌或改性氧化锌的加入不仅能够提高通量,降低膜污染,而且能够提高待分离物质的截留率。此外,还有研究者采用辐照接枝将ZnO或改性产品引入膜中[15-16]。与上述方法相比,界面聚合是一种方便快捷的制备有机-无机杂化分离膜的方法,碳纳米管,Al(OH)3,MOFs[17-19]等多种无机纳米粒子都曾通过这种方法引入分离膜中。Revathy等[20]和Al-hobaib等[21]分别用氧化石墨烯/ZnO复合物和铝掺杂的ZnO改性聚酰胺反渗透膜,取得较好效果。一般,参与界面聚合的反应物不同,膜形貌及性能会发生明显变化[22]。因此,探讨氧化锌等在其他界面聚合体系的应用效果有利于更充分、更有效地发挥其优势,优化膜性能。
本工作通过超支化聚酰胺(HBPA)与5-异氰酸酯异肽酰氯(ICIC),在聚丙烯腈(PAN)超滤膜表面的界面聚合反应,将纳米氧化锌引入表面分离层中构建纳滤膜,着重分析ZnO加入量对膜分离性能及抑菌性的影响,同时考察ZnO存在下,单体含量及反应时间对膜分离性能的影响。
1 实验 1.1 试剂5-氨基-间苯二甲酸,分析纯,阿拉丁;草酰氯、二乙烯三胺、丙烯酸甲酯、氯化钠、硫酸钠、氯化镁和硫酸镁等试剂均为分析纯,购自国药集团化学试剂有限公司;牛肉膏、蛋白胨和琼脂等生物试剂购自北京奥博星生物技术有限公司;纳米氧化锌,< 100 nm,上海普本化工新材料科技有限公司。
1.2 实验步骤及方案 1.2.1 超支化聚酰胺的制备本实验参考文献[23]制备端氨基超支化聚酰胺。将52 mL二乙烯三胺置于250 mL三口瓶中,冰水浴中N2保护下,缓慢滴加43 mL丙烯酸甲酯和100 mL甲醇的混合溶液,室温反应4 h,得到淡黄色透明AB2型单体。然后转移至旋转蒸发仪中,减压蒸馏去除甲醇,升温至95 ℃继续反应4 h,得到的黏稠淡黄色物质即为超支化聚酰胺(HBPA)。
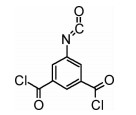
1.2.2 5-异氰酸酯异肽酰氯的制备参考文献[24]制备5-异氰酸酯异肽酰氯,其结构式如图 1所示。在装有回流冷凝器、搅拌器、温度计、氯化氢吸收装置的四口烧瓶中依次加入20 g 5-氨基间苯二甲酸,80 mL氯苯,100 mL草酰氯、0.75 mL N-甲基咪唑。搅拌、升温至75 ℃,反应8~12 h,然后升温至100~110 ℃继续反应2~4 h,蒸馏回收过量草酰氯和氯苯,采用毛细管蒸馏法继续升温至140 ℃蒸馏,取馏分,为粗产品,四氯化碳重结晶后得5-异氰酸酯异肽酰氯精制产品。
|
图 1 5-异氰酸酯异肽酰氯结构式 Fig. 1 Structure of ICIC |
将碱处理后的PAN超滤膜固定在模具中,倒入100 mL含量为0.6%(质量分数,下同)的超支化聚酰胺水溶液(含0.5%的十二烷基硫酸钠),静置30 min,将水溶液倒出,膜晾干;接着倒入80 mL含量为0.5%的5-异氰酸异肽酰氯溶液,反应10 min后放入烘箱中60 ℃热处理10 min,冷却、洗涤,保存于去离子水中。
将纳米氧化锌预先分散在ICIC溶液中,采用同样步骤得到不同ZnO含量的分离膜。依次改变单体的含量和反应时间,制备方案如表 1所示。
| Membrane | w(HBPA)/% | w(ICIC)/% | ZnO content/g | Reaction time/min |
| NF1 | 0.4 | 0.2 | 0 | 10 |
| NF2 | 0.4 | 0.2 | 0.01 | 10 |
| NF3 | 0.4 | 0.2 | 0.02 | 10 |
| NF4 | 0.4 | 0.2 | 0.03 | 10 |
| NF5 | 0.4 | 0.2 | 0.05 | 10 |
| NF6 | 0.6 | 0.2 | 0.02 | 10 |
| NF7 | 0.8 | 0.2 | 0.02 | 10 |
| NF8 | 1.0 | 0.2 | 0.02 | 10 |
| NF9 | 0.8 | 0.05 | 0.02 | 10 |
| NF10 | 0.8 | 0.1 | 0.02 | 10 |
| NF11 | 0.8 | 0.4 | 0.02 | 10 |
| NF12 | 0.8 | 0.1 | 0.02 | 0.25 |
| NF13 | 0.8 | 0.1 | 0.02 | 1 |
| NF14 | 0.8 | 0.1 | 0.02 | 3 |
| NF15 | 0.8 | 0.1 | 0.02 | 20 |
(1) 通量
将膜放置在错流式SF-20膜评价仪中,去离子水为进料液,0.8 MPa压力下预压30~40 min,待膜的透过性能稳定后,在0.6 MPa下记录收集10 mL渗透液所需时间,根据式(1)计算膜的通量。
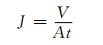
|
(1) |
式中:J为膜的通量,L·m-2·h-1;V为t时间段渗透液的体积,L;A为膜的有效面积,m2,本实验中为2.375×10-3 m2。将去离子水换成含量均为1 g/L的NaCl,MgCl2,Na2SO4和MgSO4,根据式(1)计算膜的溶液通量。
(2) 截留率
分别测量NaCl,MgCl2,Na2SO4和MgSO4的进料液和渗透液含量,根据式(2)计算截留率R,操作压力为0.6 MPa。
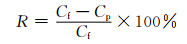
|
(2) |
式中:Cf为料液含量;Cp为渗透液含量。
1.2.5 抑菌性能测试参照文献[25]测试膜的抑菌性。配制牛肉膏蛋白胨液体培养基,调节pH值后于高压灭菌锅中灭菌处理,接种大肠杆菌,37 ℃恒温摇床150 r/min培养24 h,取出,将大肠杆菌含量稀释成105~106 CFU/mL溶液备用。
将膜裁剪为1 cm×2 cm,灭菌后放入到装有备用稀释菌液的试管中,37 ℃恒温培养箱培养24 h;取出的膜样品用15 mL液体培养基振荡冲洗,随后将冲洗液稀释至一定倍数,取200 μL接种于牛肉膏蛋白胨固体培养基中,涂布均匀,37 ℃恒温培养箱中培养24 h,计算菌落数。抑菌率S如式(3)所示。
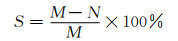
|
(3) |
式中M和N分别为改性前后膜上的菌落数。
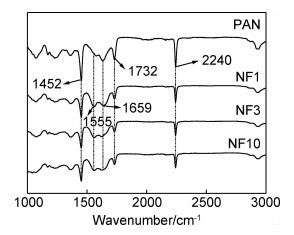
2 结果与讨论 2.1 ATR-FTIR分析采用Nicolet-380红外光谱仪分析膜表面组成。图 2为PAN基膜,NF1,NF3和NF10膜的红外光谱图。2240,1452 cm-1分别为PAN基膜表面—CN和—CH2的伸缩振动吸收峰。PAN基膜的支撑层是聚酯无纺布,因此在1732 cm-1处出现酯羰基的特征吸收峰。发生界面聚合后,由于聚酰胺分离层的形成,上述峰的强度均有所减弱。此外,PAN基膜实验前保存在去离子水中,会发生部分水解,因此在1659 cm-1和1555 cm-1处分别出现酰胺Ⅰ带和酰胺Ⅱ带的吸收峰,但界面聚合后,酰胺键的吸收峰明显增强。需要指出的是,虽然水相单体HBPA也含有酰胺键,但是它溶于水,界面聚合后经过水洗、水中保存后,膜表面吸附的HBPA量不多,认为此处酰胺键吸收峰的增强主要归结于HBPA与ICIC反应生成了聚酰胺。
|
图 2 PAN基膜,NF1,NF3和NF10膜的红外光谱图 Fig. 2 ATR-FTIR spectra of PAN substrate membrane, NF1, NF3 and NF10 membranes |
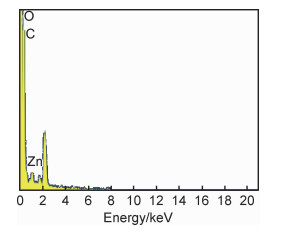
采用NNS-450场发射扫描电镜观察膜的表面及断面形貌,如图 3所示。NF10膜的表面元素组成如图 4所示。由图 3可知,PAN基膜表面平整,较为光滑,小孔均匀分布。界面聚合后,NF1膜表面有环状囊泡形成。张林课题组[26]以多孔聚砜膜为基膜,通过在水相中加入水溶性大分子,使水相哌嗪的扩散速率远低于油相中均苯三甲酰氯的扩散速率,从而得到了粒状、管带状囊泡图灵结构的聚酰胺。本工作环状结构的形成,可能与HBPA及ICIC的扩散速率差、产物在界面的表面张力变化有关。加入0.02 g ZnO的NF10表面,环状囊泡结构减少,且有粒状物的形成。EDS分析(图 4)显示含有锌元素,初步证实氧化锌成功引入到膜表面。由于聚酰胺分离层非常薄,所以界面聚合前后膜断面形貌未发生明显变化。

|
图 3 膜的表面(1)和断面(2)形貌(a)PAN基膜;(b)NF1;(c)NF10 Fig. 3 Surface(1) and cross section(2) morphologies of the membranes (a)PAN substrate membrane; (b)NF1;(c)NF10 |
|
图 4 NF10膜的能谱分析 Fig. 4 EDS analysis of the NF10 membrane |
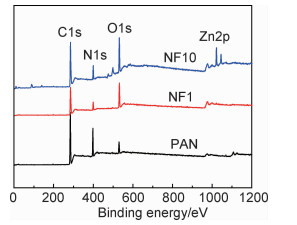
采用PHI 5000C ESCA系统分析PAN基膜,NF1和NF10膜的X射线光电子能谱,如图 5所示。可知,PAN基膜及NF1膜在285,398,531 eV附近分别出现C1s,N1s和O1s特征吸收峰,加入ZnO的NF10膜表面在1022 eV附近出现Zn2p的特征吸收峰,再次证实ZnO成功引入到膜表面。
|
图 5 PAN基膜,NF1和NF10膜的X射线光电子能谱图 Fig. 5 XPS spectra of PAN substrate membrane, NF1 and NF10 membranes |
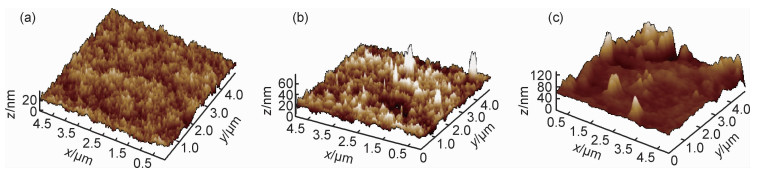
采用Solver next原子力显微镜观察PAN基膜,NF1和NF10膜表面的粗糙度,如图 6所示。结果表明,PAN基膜表面光滑,平均粗糙度为3.5 nm;界面聚合后,膜的表面粗糙度有所增大,未加ZnO的NF1膜表面平均粗糙度为4.21 nm,分离性能较佳的NF10膜平均粗糙度为7.9 nm。
|
图 6 PAN基膜,NF1和NF10膜的AFM图 Fig. 6 AFM images of PAN substrate membrane(a), NF1(b) and NF10 membranes(c) |
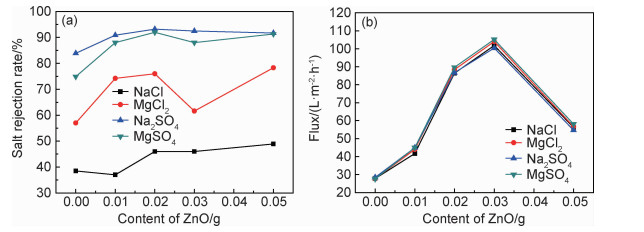
图 7为ZnO用量对膜脱盐率和通量的影响(w(HBPA)=0.4%, w(ICIC)=0.2%,反应时间为10 min)。由图 7(a)可知,ZnO的加入不影响膜的脱盐顺序,膜对NaCl,MgCl2,Na2SO4和MgSO4四种盐的脱除率顺序始终为Na2SO4>MgSO4>MgCl2>NaCl,呈现典型的荷负电特征。同时,加入ZnO的膜脱盐率明显比加入前大,只是增加幅度随用量不同发生变化。未加ZnO的膜对Na2SO4的截留率为83.9%,分别加入0.01,0.02,0.03,0.05 g ZnO后,Na2SO4截留率分别为90.9%,93.2%,92.5%和91.7%。与此类似,不加ZnO的膜对MgCl2截留率为57%,加入0.01 g和0.02 g的ZnO后,截留率分别为74.2%和76%,继续增大ZnO用量至0.05 g,截留率为78.3%。众所周知,纳滤膜基于孔径筛分与电荷排斥效应实现对不同物质的选择性分离。ZnO的加入增大Na2SO4的截留率,可能与ZnO有利于增大膜表面的负电荷有关。
|
图 7 ZnO用量对膜分离性能的影响(a)脱盐率; (b)通量 Fig. 7 Effect of ZnO content on the membrane separation performances (a)salt rejection rate; (b)flux |
膜通量随着ZnO用量的增加呈现先增加后下降的趋势,如图 7(b)所示。可知,未加ZnO的膜通量约为28 L·m-2·h-1,当ZnO用量为0.01 g时,通量增加到43 L·m-2·h-1左右,ZnO用量增加至0.03 g后,通量达到102 L·m-2·h-1左右,但继续增大用量到0.05 g后,通量下降至57 L·m-2·h-1左右。
究其原因,ZnO的加入会提高膜表面粗糙度,对于亲水性材料而言,粗糙度越大亲水性越好,未加ZnO的膜接触角为48°,加入0.01 g和0.03 g的膜接触角分别为33.2°和22.7°,可见ZnO的添加增强了膜的亲水性,有利于通量的增大。此外,ZnO的存在对于HBPA与ICIC的界面聚合具有空间位阻作用,使生成的聚酰胺分离层结构疏松,用量越大,聚酰胺分离层结构越疏松,因此通量随之增大。但加入量太大时,过多的ZnO会堵塞膜孔,导致通量减小。
膜的脱盐率是膜分离性能考察的主要指标之一,当ZnO用量为0.02 g时,膜对NaCl,MgCl2,Na2SO4和MgSO4四种盐的脱除率最大,所以后续实验均采用此用量,调节其他反应条件以进一步优化膜性能。
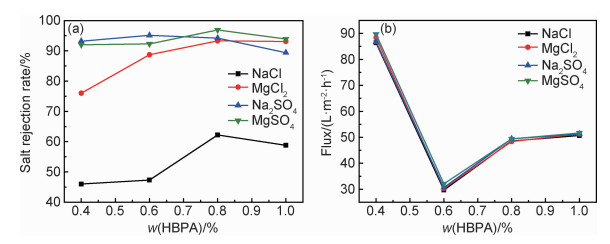
2.4.2 HBPA含量对膜分离性能的影响图 8为HBPA含量对膜脱盐率和通量的影响(w(ICIC)=0.2%,ZnO用量为0.02 g,反应时间为10 min)。由图 8(a)可知,随着HBPA含量的增加,纳滤膜对MgCl2的截留率增大,对其他三种盐截留率基本呈现先增大再减小的趋势。当HBPA为0.4%时,膜对MgCl2的截留率为76%,增加到0.6%后,截留率提高到88.7%,继续升高HBPA至0.8%,截留率为93.3%,但增加到1.0%时,截留率不再变化。其他三种盐以Na2SO4为例,当HBPA为0.4%,0.6%,0.8%和1.0%时,截留率分别为93.2%,95.1%,94.2%和89.4%。当HBPA为0.4%和0.6%时,截留率为Na2SO4>MgCl2;HBPA为0.8%和1.0%时,MgCl2>Na2SO4。
|
图 8 HBPA含量对膜分离性能的影响 (a)脱盐率; (b)通量 Fig. 8 Effect of HBPA concentration on the membrane separation performances (a)salt rejection rate; (b)flux |
随着HBPA含量的增加,通量先减小再增大,如图 8(b)所示。HBPA为0.4%时,制备的膜通量约为87 L·m-2·h-1,0.6%时降低至31 L·m-2·h-1左右,增加至0.8%后,提高到49 L·m-2·h-1左右,1.0%时约为51 L·m-2·h-1。
究其原因,界面聚合发生在两相之间,反应速率受单体扩散速率的影响,含量增加单体扩散速率增大,反应加快,形成的聚酰胺层越发致密,此时透膜阻力变大,孔径筛分效应增强,表现为截留率增加,通量降低。含量超过0.6%,过量未反应的官能团导致聚酰胺分离层结构疏松,透膜阻力降低,表现为通量增大,截留率降低。但需要注意,此时,过量未反应的HBPA能引入更多的—NH2,使膜表面正电荷数目增加,有利于高价阳离子无机盐的脱除。两种效应作用下,最终MgCl2截留率逐渐高于Na2SO4。
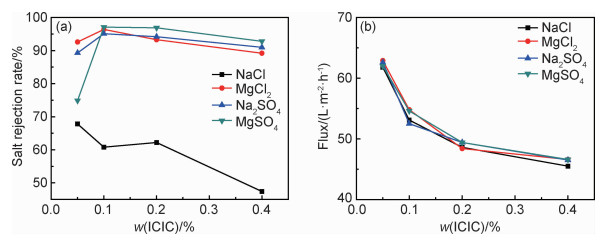
2.4.3 ICIC含量对膜分离性能的影响图 9为ICIC含量对膜脱盐率和通量的影响(w(HBPA)=0.8%, ZnO用量为0.02 g, 反应时间为10 min)。图 9(a)显示,改变ICIC的含量,除了NaCl,其他三种盐的截留率都随着ICIC含量的增加先增大后减小。ICIC为0.05%时,Na2SO4截留率为89.3%,0.1%时截留率上升到95.1%,0.4%时截留率下降至91%。需要指出的是,当ICIC含量超过一定值时,膜对各种盐的优先脱除顺序也发生了变化。如,ICIC为0.05%和0.1%时,截留率为MgCl2>Na2SO4;ICIC增加为0.2%和0.4%时,Na2SO4>MgCl2。
|
图 9 ICIC含量对膜分离性能的影响 (a)脱盐率; (b)通量 Fig. 9 Effect of ICIC concentration on the membrane separation performances (a)salt rejection rate; (b)flux |
究其原因,界面聚合时ICIC含量增加使聚酰胺层更加致密,孔径筛分效应增强,截留率提高,后期含量继续增大脱盐率有所下降,可能与此时膜表面电荷量减少有关。此外,ICIC含量较低时,HBPA含量相对高,未发生反应的—NH2使膜表面的正电荷数目较多,因此对高价阳离子盐MgCl2的截留率大于高价阴离子盐Na2SO4。当ICIC含量增大后,未参与聚合反应的ICIC与水反应生成—COOH,羧基电离引入带负电的羧酸根离子,膜表面负电荷量增多,所以膜对Na2SO4的截留率逐渐大于MgCl2。
通量则随着ICIC含量的增加逐渐降低(图 9(b)),0.05%增大到0.4%时,通量由63 L·m-2·h-1逐渐降低至46 L·m-2·h-1左右。这主要是由于,在本实验含量调节范围内,增加ICIC的质量分数,聚酰胺分离层结构趋于逐渐致密,透膜阻力增大,导致通量降低。
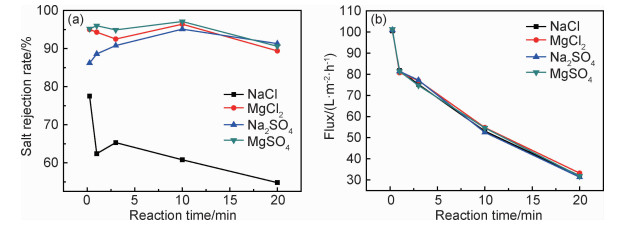
2.5 反应时间对膜分离性能的影响图 10为反应时间对膜脱盐率和通量的影响(w(HBPA)=0.8%, w(ICIC)=0.1%, ZnO用量为0.02 g)。由图 10(a)可知,界面聚合反应时间少于10 min时,MgCl2的截留率大于Na2SO4,随着反应时间的延长,Na2SO4的截留率逐渐升高,与MgCl2截留率之间的差距逐渐减小。反应15 s制备的膜对MgCl2和Na2SO4截留率分别为95%和86.2%;延长反应时间到1 min,MgCl2和Na2SO4截留率分别为94.3%和88.6%;继续延长反应时间至10 min,MgCl2和Na2SO4截留率分别为96.4%和95.1%;反应20 min后,MgCl2和Na2SO4截留率分别降低为89.4%和91.3%。
|
图 10 反应时间对膜分离性能的影响 (a)脱盐率; (b)通量 Fig. 10 Effect of reaction time on the membrane separation performances (a)salt rejection rate; (b)flux |
究其原因,当反应时间为15 s时,HBPA与ICIC未充分反应,HBPA中未参与聚合反应的—NH2引入的正电荷量较多,静电排斥效应对盐的脱除起着主导,所以MgCl2的截留率比Na2SO4高。随着界面聚合反应时间的延长,HBPA反应充分,膜致密度逐渐增大,孔径筛分效应逐渐占主导作用,而Mg2+与SO42-的水合离子半径近似,因此膜对MgCl2和Na2SO4的截留率差异逐渐减小。
从图 10(b)的通量变化可以看出,随着时间的增加,膜的通量一直处于下降的状态。15 s反应时间制备的膜通量可达100 L·m-2·h-1,反应时间延长至1 min,通量约为81 L·m-2·h-1,继续反应至10 min和20 min,通量约为52 L·m-2·h-1和31 L·m-2·h-1。这可能是由于反应时间越长,聚酰胺分离层致密度和厚度均增加,透膜阻力增大,从而使通量降低。
由此可见,优化制备条件为:HBPA含量为0.8%, ICIC含量为0.1%,ZnO用量为0.02 g,反应时间为10 min,制备的纳滤膜对NaCl,MgCl2,Na2SO4和MgSO4的截留率分别为60.8%,96.4%,95.1%,96.7%,通量分别达到53,54.7,53.7 L·m-2·h-1和54.7 L·m-2·h-1。
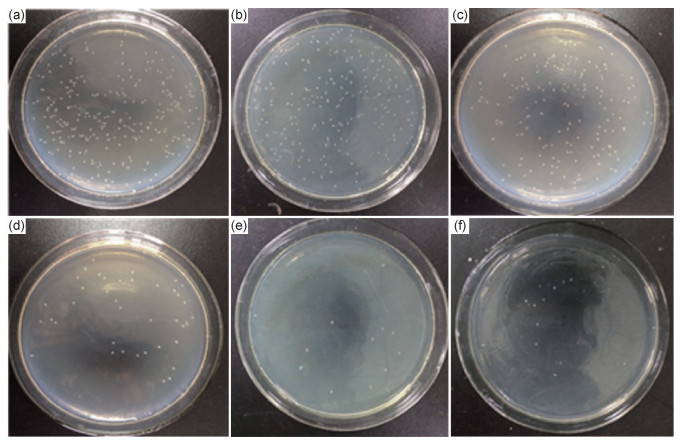
2.6 膜的抑菌性能测试图 11为PAN基膜,NF1,NF2,NF3,NF4和NF5膜的抑菌效果图。可知,随着ZnO加入量的增加,膜的抑菌效果增强。与PAN基膜相比,不加ZnO的NF1膜抑菌率为11.2%,ZnO加入量为0.01,0.02,0.03 g和0.05 g的NF2,NF3,NF4和NF5膜的抑菌率分别为35.6%,94.2%,95%,95.9%。ZnO用量大于0.02 g的膜的抑菌效果明显比目前多数聚酰胺商品纳滤膜好。
|
图 11 膜的抑菌效果图 (a)PAN基膜;(b)NF1;(c)NF2;(d)NF3;(e)NF4;(f)NF5 Fig. 11 Antibiosis performance of the membranes (a)PAN substrate membrane; (b)NF1;(c)NF2;(d)NF3;(e)NF4;(f)NF5 |
(1) ZnO的加入,不仅能够提高膜的无机盐脱除率,同时能够增大膜通量,增强抑菌性。
(2) HBPA含量的增加会改变无机盐脱除顺序及通量。
(3) ICIC含量的增加及时间的延长会使膜通量下降。
(4) 优化条件下制备的纳滤膜对MgCl2,Na2SO4和MgSO4截留率分别为96.4%,95.1%,96.7%,通量分别为54.7,53.7,54.7 L·m-2·h-1,有望在重金属废水处理、硬水软化等行业得到应用。
| [1] |
ZHAO K Y, ZHANG X X, WEI J F, et al. Calcium alginate hydrogel filtration membrane with excellent anti-fouling property and controlled separation performance[J]. Journal of Membrane Science, 2015, 492: 536-546. DOI:10.1016/j.memsci.2015.05.075 |
| [2] |
ZHANG X X, LIN B B, ZHAO K Y, et al. A free-standing calcium alginate/polyacrylamide hydrogel nanofiltration membrane with high anti-fouling performance:preparation and characterization[J]. Desalination, 2015, 365: 234-241. DOI:10.1016/j.desal.2015.03.015 |
| [3] |
GUO J, ZHAO K Y, ZHANG X X, et al. Preparation and characterization of carboxyl multi-walled carbon nanotubes/calcium alginate composite hydrogel nano-filtration membrane[J]. Materials Letters, 2015, 157: 112-115. DOI:10.1016/j.matlet.2015.05.080 |
| [4] |
VIKTORIYA K, MYKOLA S, MIKHAIL M, et al. The violet luminescence band in ZnO and ZnO-Ag thin films[J]. Journal of Luminescence, 2019, 213: 519-524. DOI:10.1016/j.jlumin.2019.04.045 |
| [5] |
SALEM M, AKIR S, MASSOUDI I, et al. Photoelectrochemical and optical properties tuning of graphene-ZnO nanocomposites[J]. Journal of Alloys and Compounds, 2018, 767: 982-987. DOI:10.1016/j.jallcom.2018.07.202 |
| [6] |
JIAO W L, ZHANG L. Fabrication of new C/ZnO/ZnO composite material and their enhanced gas sensing properties[J]. Materials Science in Semiconductor Processing, 2018, 86: 63-68. DOI:10.1016/j.mssp.2018.05.021 |
| [7] |
LIN J, HUANG B, DAI Y F, et al. Chiral ZnO nanoparticles for detection of dopamine[J]. Materials Science and Engineering:C, 2018, 93: 739-745. DOI:10.1016/j.msec.2018.08.036 |
| [8] |
SON D B, JOON M B, LEE A, et al. Polarity effects of ZnO on charge recombination at CsPbBr3 nanoparticles/ZnO interfaces[J]. Applied Surface Science, 2019, 483: 165-169. DOI:10.1016/j.apsusc.2019.03.300 |
| [9] |
KAARIAINEN M L, WEISS C K, RITZ S, et al. Zinc release from atomic layer deposited zinc oxide thin films and its antibacterial effect on Escherichia coli[J]. Applied Surface Science, 2013, 287: 375-380. DOI:10.1016/j.apsusc.2013.09.162 |
| [10] |
SUDHEESH K P T, LAKAHMANANV K, RAJ M, et al. Eva-luation of wound healing potential of β-chitin hydrogel/nano zinc oxide composite bandage[J]. Pharmaceutical Research, 2013, 30: 523-537. DOI:10.1007/s11095-012-0898-y |
| [11] |
HAYATI H N H, MOHAMMAD A W, HASSAN K A A. Influence of zinc oxide nanoparticles in the nanofiltration of hazardous Congo red dyes[J]. Chemical Engineering Journal, 2015, 260: 907-915. DOI:10.1016/j.cej.2014.08.068 |
| [12] |
JUHOLIN P, KAARIAINEN M L, RIIHIMAKI M, et al. Comparison of ALD coated nanofiltration membranes to unmodifiedcommercial membranes in mine wastewater treatment[J]. Separation and Purification Technology, 2018, 92: 69-77. |
| [13] |
STEFAN B, ARCADIO S, PATRICIA L, et al. A new outlook on membrane enhancement with nanoparticles:the alternative of ZnO[J]. Journal of Membrane Science, 2012, 389: 155-161. DOI:10.1016/j.memsci.2011.10.025 |
| [14] |
ZANGENEH H, ZINATIZADEH A A, ZINDINI S, et al. Preparation ultrafine L-Methionine (C, N, S triple doped)-TiO2-ZnO nanoparticles and their photocatalytic performance for fouling alleviation in PES nanocomposite membrane[J]. Composites Part B, 2019, 76(107158): 1-11. |
| [15] |
EI-ARNAOUTY M B, ABDEL G A M, EID M, et al. Nano-modi- fication of polyamide thin film composite reverse osmosis membranes by radiation grafting[J]. Journal of Radiation Research and Applied Sciences, 2018, 11: 204-216. DOI:10.1016/j.jrras.2018.01.005 |
| [16] |
HEBA I. Development of thin-film composite membranes via radical grafting with methacrylic acid/ZnO doped TiO2 nanocomposites[J]. Reactive and Functional Polymers, 2018, 131: 400-413. DOI:10.1016/j.reactfunctpolym.2018.08.018 |
| [17] |
LI H B, SHI W Y, ZHANG Y F, et al. Improved performance of poly (piperazineamide) composite nanofiltration membranes by adding aluminum hydroxide nanospheres[J]. Separation and Purification Technology, 2016, 166: 240-251. DOI:10.1016/j.seppur.2016.04.024 |
| [18] |
ZHAO F Y, JI Y L, WEN X D, et al. High-flux positively charged nanocomposite nanofiltration membranes filled with poly(dopamine) modified multi-walled carbon nanotubes[J]. ACS Applied Materials & Interfaces, 2016, 8(10): 6693-6700. |
| [19] |
MANSOR E S, JAMIL T S, ABDALLAH H, et al. Highly thin film nanocomposite membrane based metal organic complexes for brackish water desalination[J]. Journal of Enviromental Chemical Engineering, 2018, 6(4): 5459-5469. DOI:10.1016/j.jece.2018.08.034 |
| [20] |
REVATHY R, VINISHA B, MATHAVA K, et al. Effect of ZnO morphology on GO-ZnO modified polyamide reverse osmosis membranes for desalination[J]. Desalination, 2019, 467: 245-256. DOI:10.1016/j.desal.2019.06.018 |
| [21] |
AL-HOBAIB A S, GHOUL J E, GHILOUFI I, et al. Synthesis and characterization of polyamide thin-film nanocomposite membrane reached by aluminum doped ZnO nanoparticles[J]. Materials Science in Semiconductor Processing, 2016, 42: 111-114. DOI:10.1016/j.mssp.2015.07.058 |
| [22] |
VERISSIMO S, PEINEMANN K V, BORDADO J. Influence of the diamine structure on the nanofiltration performance, surface morphology and surface charge of the composite polyamide membranes[J]. Journal of Membrane Science, 2006, 279: 266-275. DOI:10.1016/j.memsci.2005.12.014 |
| [23] |
张峰, 陈宇岳, 张德锁, 等. 端氨基超支化聚合物及其季铵盐的制备与性能[J]. 高分子材料科学与工程, 2009, 25(8): 141-144. ZHANG F, CHEN Y Y, ZHANG D S, et al. Preparation and properties of amino-terminated hyperbranched polymers and its quaternary ammonium salt[J]. Polymer Materials Science and Engineering, 2009, 25(8): 141-144. |
| [24] |
刘立芬, 徐德志, 陈焕林, 等. 5-异氰酸酯-异肽酰氯的合成[J]. 化工进展, 2013, 32(1): 184-187. LIU L F, XU D Z, CHEN H L, et al. Synthesis of 5-isocyanato-isophthaloyl chloride[J]. Chemical Industry and Engineering Progress, 2013, 32(1): 184-187. |
| [25] |
陈培培, 徐佳, 蒋钰烨, 等. 新型抑菌Cu2+固载超滤膜的制备及性能表征[J]. 高等学校化学学报, 2013, 34(3): 739-745. CHEN P P, XU J, JIANG Y Y, et al. Preparation and characte-rization of a novel anti-biofouling ultrafiltration membrane with Cu2+ immobilization[J]. Chemical Journal of Chinese Universities, 2013, 34(3): 739-745. |
| [26] |
TAN Z, CHEN S F, PENG X S, et al. Polyamide membranes with nanoscale Turing structures for water purification[J]. Science, 2018, 360(6388): 518-521. DOI:10.1126/science.aar6308 |
 2020, Vol. 48
2020, Vol. 48


