文章信息
- 温敬运, 邱晓宇, 李明飞, 彭锋, 边静, 孙润仓
- WEN Jing-yun, QIU Xiao-yu, LI Ming-fei, PENG Feng, BIAN Jing, SUN Run-cang
- 半纤维素基水凝胶制备及应用研究进展
- Research progress in preparation and application of hemicellulose-based hydrogels
- 材料工程, 2020, 48(2): 1-10
- Journal of Materials Engineering, 2020, 48(2): 1-10.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000500
-
文章历史
- 收稿日期: 2019-05-27
- 修订日期: 2019-10-23
2. 大连工业大学 生物质科学与工程中心 辽宁省制浆造纸工程高校重点实验室, 辽宁 大连 116034
2. Liaoning Key Laboratory Pulp and Paper Engineering, Center for Lignocellulose Science and Engineering, Dalian Polytechnic University, Dalian 116034, Liaoning, China
水凝胶是由亲水聚合物形成的具有三维网络结构的功能高分子材料[1]。高度交联的聚合物网络使水凝胶具有优异的保水性和良好的力学、化学和生物学性能[2]。水凝胶根据交联方式主要包括化学交联水凝胶和物理交联水凝胶两大类。化学交联水凝胶是在交联剂的作用下,通过自由基的原位聚合,在分子间形成共价键合成水凝胶网络,具有较好的结构稳定性。物理交联水凝胶主要由结晶、范德华力、氢键[3]和静电作用[4]等可逆的非共价作用力形成,可避免由于化学试剂使用带来的不利影响。水凝胶根据合成原料可分为合成聚合物水凝胶和天然聚合物水凝胶。合成聚合物水凝胶的结构及化学成分可控、强度可调,但生物可降解性较差,不适于在生物细胞或组织中应用;天然聚合物水凝胶具有良好的生物相容性、生物可降解性及环境友好性等特性[5-7],在农业[8]、生物医药材料[9]、废水处理[10]、生物传感器[11]等领域得到广泛的应用。
半纤维素作为一种天然高分子聚合物,是木质纤维素细胞壁中含量仅次于纤维素的重要基质多糖,具有低分子量和多分枝性等特点,平均聚合度仅为80~200[12]。半纤维素的结构单元类型主要由几种不同的五碳糖(D-木糖、L-阿拉伯糖)、六碳糖(D-葡萄糖、D-甘露糖、D-半乳糖、L-鼠李糖和L-岩藻糖)和糖醛酸(D-葡萄糖醛酸、4-O-甲基-D-葡萄糖醛酸和D-半乳糖醛酸)组成[13]。原料不同,半纤维素的结构组成不同。阔叶木半纤维素主要是4-O-甲基葡萄糖醛酸木聚糖,针叶木半纤维素中最多的是半乳糖葡萄糖甘露聚糖和阿拉伯糖半乳聚糖,禾本科植物的半纤维素主要是阿拉伯糖木聚糖。这些结构赋予了半纤维素羟基、乙酰基及羧基等官能团,可通过交联或进一步改性形成具有不同功能的半纤维素基水凝胶,拓展半纤维素在材料领域的应用。本文主要综述了半纤维素基水凝胶的制备方法和机理,及半纤维素基水凝胶在生物医药、伤口敷料、废水处理和3D打印等领域的应用现状和前景,以期为新型功能性半纤维素材料的研究提供参考。
1 半纤维素基水凝胶的制备 1.1 化学交联水凝胶化学交联法制备的水凝胶可在分子间形成共价键,使聚合物之间作用更加紧密,具有更为理想的结构稳定性和力学强度。自由基聚合是化学交联法制备水凝胶最为常用的方法,是在光、热、辐射或引发剂的作用下致使小分子单体产生自由基,经共聚或缩聚反应形成高聚物的过程[14]。该方法对单体的适用范围广,反应条件温和。在化学交联中,分子间共价键的形成通常需要交联剂的加入,常用的交联剂有丙烯酸、聚乙二醇、聚乙烯醇、戊二醛、丙烯酰胺、环氧氯丙烷及漆酶等。此外,在自由基聚合过程中,常常需要半纤维素的改性反应和紫外光辐射、微波辐射、酶及辉光放电电解等离子体等引发体系的参与。
1.1.1 改性交联半纤维素的分子量和聚合度较低,且低分枝度的半纤维素在水中的溶解性较差,限制了其在水凝胶领域的应用。因此,利用半纤维素分子链上含有大量活泼的羟基,对其进行改性,赋予半纤维素新的官能团,改善半纤维素的分子量、溶解性、热稳定性等理化性能,可以解决半纤维素水凝胶强度不够和功能性不足的问题,拓展半纤维素基水凝胶的发展。常见的半纤维素改性方法可分为氧化、醚化、酯化、接枝共聚等,部分改性方法如表 1所示[15-23]。
| Material | Origin | Modifier | Modified polymer | Reference |
| AcGGM | Spruce | GMA | AcGGM-MA | [15] |
| Hemicellulose | Phyllostachys pubescens | ETA | Quaternized hemicellulose | [16] |
| Hemicellulose | Spruce | HEMA-Im | HEMA-modified AcGGM | [17] |
| GGM | - | Laccase/TEMPO system | Oxidized hemicellulose | [18] |
| AcGGM | Spruce | TBL | Thiolated hemicellulose | [19] |
| Hemicellulose | Spruce | HEMA-monomer | HEMA-hemicellulose | [20] |
| Hemicellulose | Wood and grasses | DTPA | DTPA-modified hemicellulose | [21] |
| Hemicellulose | Corncob | MA,Acetic anhydride | AHC,Post-acetylated xylan | [22-23] |
| Abbreviations:O-acetyl galactoglucomannan(AcGGM);Glycidyl methacrylate(GMA);Maleic anhydride(MA);2,3-epoxypropyltrimethyl ammonium chloride(ETA);2-[(1-imidazolyl)formyloxy]ethyl methacrylate(HEMA-Im);Galactoglucomannan(GGM);γ-thiobutyrolactone(TBL);Diethylene triamine pentaacetic acid(DTPA);Acylated hemicellulose(AHC) | ||||
因半纤维素的相对分子质量和聚合度较低,成胶后分子结构之间作用力较弱,水凝胶的机械强度较低。通过改性反应,能增大半纤维素分子量,进而增强半纤维素基水凝胶的力学性能。Qi等[16]将季铵基团通过醚化反应引入到半纤维素中得到季铵化半纤维素(QH),然后将QH与环氧氯丙烷反应交联得到分子链扩展的半纤维素(CQH),接着加入丙烯酸单体,在交联剂N, N′-亚甲基双丙烯酰胺和引发剂过硫酸铵(APS)和四甲基乙二胺(TEMDA)作用下形成水凝胶。由于半纤维素链的延展,分子量增大,该水凝胶最大压缩应力达到750 kPa,优于纯半纤维素水凝胶的38.6 kPa,强度明显提高。利用细胞壁中木质素与半纤维素能通过酯键和醚键相互连接的机理[24],Oinonen等[25]将云杉半乳葡甘聚糖与木质素混合,通过漆酶催化木质素芳香基团进行单电子氧化,产生自由基,实现半乳葡甘聚糖与木质素的连接,提高了半乳葡甘聚糖的分子量,从而改善了半乳葡甘聚糖基水凝胶的力学性能。
半纤维素也可作为多种功能聚合物的载体,经化学改性后制备新型半纤维基水凝胶。Roos等[17]利用2-[(1-咪唑基)甲酰氧基甲基]丙烯酸乙酯(HEMA-Im)对O-乙酰基-半乳葡甘露聚糖(AcGGM)改性。研究发现,随着改性AcGGM中HEMA取代度的增加,牛血清白蛋白的释放效率降低,达到药物缓释的目的。Ayoub等[21]在次亚磷酸钠(SHP)催化下,用二乙烯三胺五乙酸(DTPA)改性半纤维素,得到半纤维素-DTPA; 然后将半纤维素-DTPA与壳聚糖交联形成水凝胶,冷冻干燥后形成半纤维素基吸附剂。DTPA中含有大量的羧基基团,能与重金属离子产生强螯合作用,对Pb2+,Cu2+和Ni2+的吸收效率分别能达到2.90,0.95 mg/g和1.37 mg/g。Dax等[23]利用甲基丙烯酸缩水甘油酯为甲基丙烯酸酯来源,4-二甲氨基吡啶(DMAP)为催化剂,二甲基亚砜(DMSO)为溶剂,在50 ℃对半乳葡甘露聚糖(GGM)改性,得到GGM-甲基丙烯酸酯衍生物。改性后的GGM-甲基丙烯酸酯衍生物在过硫酸铵引发下合成水凝胶。该水凝胶对废水中As5+和Cr6+的吸附能力有较大的提高,并随pH和溶胀性能发生变化。
半纤维素的化学改性通常是多步骤的,反应过程繁琐且耗时,而一锅法改性反应通过一个步骤便能发生多种反应,明显缩短了反应时间。研究发现γ-硫代丁内酯(TBL)作为合成大分子的功能单体,可通过一锅法反应实现对半纤维素的改性[26]。Maleki等[19]以活化的云杉半纤维素为原料,NaH为催化剂,与TBL发生亲核开环反应,一锅法合成了巯基改性的半纤维素;巯基改性的半纤维素进一步在过硫酸钾/亚硫酸钠自由基引发体系下,通过硫醇-迈克尔加成点击反应或硫醇-烯点击反应,实现了半纤维素基水凝胶的制备。巯基改性简化了传统半纤维素改性的操作步骤,并通过不同的自由基合成体系为半纤维素基水凝胶的制备提供了更多选择。
1.1.2 引发交联引发交联是聚合物链间形成共价键的一种有效方法,常用的引发体系包括:紫外光辐射、酶、微波辐射和辉光放电电解等离子体(GDEP)等,部分半纤维素基水凝胶的引发体系如表 2所示[27-33]。该方法合成的水凝胶纯度高,能减少有毒试剂的使用,对制备智能响应性的半纤维素基水凝胶有很大促进作用。
| Material | Initiator | Cross-link | Solvent | Reference |
| Hemicellulose-MA | UV light | N-isopropylacrylamide | LiCl/DMF | [27] |
| Derivatized xylan | UV light | N, N′-diallylaldardiamides | Distilled water | [28] |
| Hemicellulose-TA conjugate | HRP and H2O2 | HRP and H2O2 | PBS | [29-30] |
| Xylan | Microwave and KPS | PVP | Distilled water | [31] |
| Hemicellulose | GDEP | MBA | Distilled water | [32-33] |
| Abbreviations:Hemicelluloses-MA:a derivative of hemicellulose by grafting maleic anhydride;Lithium chlori(LiCl);Dimethyl formamide(DMF);Tyramine(TA);Horseradish peroxidase(HRP);Hydrogen peroxide(H2O2);pH buffer solutions (PBS); Sodium persulphate(KPS);Polyvinylpyrrolidone(PVP);Glow discharge electrolysis plasma(GDEP);N, N′-methylene double acrylamide(MBA) | ||||
光引发剂在紫外光作用下能产生自由基,引发聚合反应,是分子间形成共价键的有效方法,在半纤维素基水凝胶中有一定的应用[34]。Yang等[27]利用半纤维素中的羟基与顺丁烯二酸酐发生酯化反应,以2,2-二甲氧基-基苯乙酮为光引发剂,N-异丙基丙烯酰胺为交联剂,在365 nm的紫外光波长下照射得到温度响应的半纤维素基水凝胶。Pohjanlehto等[28]利用丁基和烯丙基缩水甘油醚对木聚糖改性,然后在光引发剂过硫酸钾作用下,紫外光照射3~4 min便可制备木聚糖基水凝胶。该体系操作简单,反应时间短,可在常温下进行,制备效率高。
酶引发的自由基聚合反应条件简单,能减少化学引发剂和有机溶剂的使用,制备的水凝胶有较好的生物相容性。Markstedt等[29]通过TEMPO氧化将羧基引入O-乙酰基-半乳葡甘聚糖(AcGGM)中,用N-羟基琥珀酰亚胺(NHS)/1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDAC)活化羧基,选择过氧化氢(H2O2)作为催化剂,在辣根过氧化物酶(HPR)的引发作用下,室温原位聚合约20 s完成交联反应。研究发现,细胞在AcGGM-TA水凝胶中培养48 h后,存活率为95%,表明该水凝胶具有很好的生物相容性。Kuzmenko等[30]也对HRP/H2O2的引发体系进行了研究。利用酪胺(TA)中的氨基与云杉木聚糖中的羧基发生耦合反应,形成木聚糖-TA;然后将木聚糖-TA溶于HRP和H2O2的PBS缓冲液中反应,室温下20 s形成水凝胶,通过扫描电镜和共聚焦显微镜观察,该凝胶体系保留了其向细胞分化的能力,可用于封装小鼠间充质干细胞。
微波辐射引发体系具有反应快速、无滞后效应和选择性好等优点[35],在半纤维素基水凝胶领域也有一定应用。Meena等[31]开发了一种微波辅助快速成胶的水凝胶系统。将木聚糖和卡拉胶均匀混合,在水溶性引发剂过硫酸钠的引发下,加入聚乙烯吡咯烷酮(PVP),微波辐射5~15 min即可得到半互穿网络水凝胶。实验表明,当没有过硫酸钠引发剂和微波辐射作用时,水凝胶中仅含有14%~18%(质量分数,下同)的PVP;而当过硫酸钠引发剂和微波辐射共同作用时,水凝胶中含有36%~42%的PVP,显著改善了PVP的掺入。该分析可以推测在过硫酸钠和微波共同作用下,PVP分子和木聚糖骨架之间能更好地发生化学交联。微波辐射缩短了反应时间,且随着PVP的加入,水凝胶的吸水能力和力学性能均得到增强。
目前,化学引发可产生副产物,光引发和微波辐射引发存在耗能高等问题,而辉光放电电解等离子体(GDEP)体系因在水溶液中进行,且条件温和,反应可控,提纯步骤简单,装置成本低廉,无二次污染,在半纤维素基水凝胶领域有更好的应用[32]。Zhang等[32]利用等离子电解过程产生的大量高活性粒子(如HO·,H·,H3O+,eaq-,HO2+和H2O2)为引发剂,丙烯酸和N-异丙基丙烯酰胺为单体,N, N′-亚甲基双丙烯酰胺为交联剂制备了具有pH和温度双重响应的半纤维素基智能水凝胶。实验发现,在500 V的放电电压下,自由基的数量较少,导致聚合不完全,网络呈现针状结构;而当放电电压增至600 V,活性颗粒和自由基的数量增加,反应完全聚合,网络结构呈现连续的网状结构。Zhang等[36]采用GDEP合成了芦苇半纤维素水凝胶,用于吸附水溶液中的重金属离子。采用Langmuir等温线模型对吸附过程进行分析,发现放电电压和放电时间对芦苇半纤维素基水凝胶的吸附均有重要影响。在620 V的放电电压下,对Pb2+,Cd2+和Zn2+的吸附容量分别为799,621 mg/g和365 mg/g,吸附性能较好;而当放电电压大于和小于620 V时,吸附性能均下降。其原因可能为:当放电电压小于620 V时,产生的自由基较少,导致聚合物的网络结构不稳定致使金属离子吸附能力较低;当放电电压超过620 V时,较多的自由基产生更密集的网络,减少了水凝胶的活性位点的数量,因此吸附能力亦降低。
1.2 物理交联水凝胶化学交联水凝胶因制备过程中需要加入引发剂、交联剂等,这些试剂大多具有一定的细胞毒性,致使水凝胶生物相容性欠佳。而物理水凝胶不仅可以避免交联剂使用带来的不利影响,而且可以形成可逆的非共价作用力网络,赋予水凝胶良好的自修复性能。
1.2.1 非共价作用力Qi等[3]用木聚糖、蒙脱土(MMT)与聚丙烯酸钠物理交联,成功制备了自修复、可生物降解的木聚糖基水凝胶。用1-甲基胍盐酸盐改性木聚糖引入氨基,改性后的木聚糖上的氨基与聚丙烯酸盐的氧阴离子形成强的氢键和静电作用力,快速形成凝胶网络结构。实验表明,断裂的木聚糖基水凝胶在几分钟内便能自愈修复,主要可归因于复合水凝胶中氢键和静电吸附等大量可逆非共价键的作用。Guan等[37]将季铵化半纤维素与蒙脱土均质混合,在静电作用过程中,蒙脱土剥离形成带负电荷的表面,季铵化半纤维素的表面带正电荷,通过正负电荷之间的强静电作用形成半纤维素/蒙脱土复合物。进一步发现,蒙脱土不仅起到物理交联点的作用,而且能增强凝胶材料的热力学性能。
半纤维素和壳聚糖也能通过非共价作用力合成水凝胶。Gabrielii等[4]将杨木木聚糖与壳聚糖混合,通过木聚糖的酸性基团和壳聚糖氨基之间的静电和氢键作用形成半纤维素/壳聚糖复合水凝胶。半纤维素是无定形物质,自身不能形成网络结构;而加入壳聚糖后,木聚糖与壳聚糖之间能形成微晶结构并作为物理交联点,微晶连接起来进行聚合物的结晶排列,形成共结晶网络结构。当壳聚糖含量达到5%~20%时,共结晶结构形成网状结构,制得半纤维素/壳聚糖复合水凝胶。
1.2.2 反复冷冻-解冻技术反复冷冻-解冻技术(冻融技术)能促进氢键作用力的产生,从而简单有效地制备具有高机械强度和高弹性的水凝胶。其制备机理为:室温下,聚合物分子在溶液中自由运动,分子间接触时间较短。而在冷冻过程中,聚合物和溶剂之间发生一定程度的相分离,在冰晶区域的分子运动减弱,分子间接触时间增加,促进氢键的形成,形成水凝胶网络结构。随着冻融的进行,冰晶周围聚合物浓度变大,尺寸逐渐增大。恢复室温后,冰晶溶解,在原位置形成孔,其三维网络结构依然稳定,从而形成多孔水凝胶[38]。Guan等[39]将毛竹半纤维素与甲壳素纳米晶须溶解于水中,加入聚乙烯醇(PVA)均匀混合,混合溶液在―20 ℃冷冻10 h,常温下解冻1 h,反复数次制备出高强度的水凝胶。随着冻融次数的增加,分子间交联程度增加,氢键作用力增强,水凝胶网络结构变得紧密[40]。该水凝胶有较为均匀的多孔结构,并且随着甲壳素纳米晶须含量的增加,孔径逐渐变小。水凝胶的抗压强度最高达到10.5 MPa,热力学性能也明显增加。
1.3 复合水凝胶单一的半纤维素基水凝胶强度较低,且不能满足某一特定用途,如废液中污染物的选择性吸附和生物医药中抗菌、抗氧化等。而将半纤维素与另一种或多种功能性天然有机或无机聚合物复合,可以获得具有多种组分优点的新型智能半纤维素基复合水凝胶,拓展半纤维素水凝胶在不同领域的应用。
半纤维素/天然聚合物复合水凝胶是在单一半纤维素水凝胶的基础上引入天然聚合物。其中,纳米纤维素和壳聚糖与半纤维素形成复合水凝胶最为常见[41-42]。Karaaslan等[20]将经甲基丙烯酸羟乙酯(HEMA)改性的半纤维素,沉积在表面改性的纳米纤维素晶须上,得到更多的交联位点,通过HEMA的原位自由基聚合反应,形成纳米纤维素增强的半纤维素水凝胶网络结构。实验发现,随着纳米纤维素含量的增加,半纤维素复合水凝胶在韧性、黏弹性、自恢复性能方面都得到增强。Ayoub等[21]尝试用半纤维素与壳聚糖混合,制备具有吸附性能的半纤维素/壳聚糖复合水凝胶。首先用SHP为催化剂,通过DTPA对半纤维素改性以增加半纤维素的羧基含量;然后加入壳聚糖反应聚合2.5 h形成凝胶,用于金属离子的吸附。壳聚糖的加入改善了网状结构的完整性,提高了水凝胶的润涨性能、力学稳定性,改善了对铅、铜、镍等重金属离子的吸附性能。半纤维素也能与羧甲基壳聚糖衍生物分子链上的氨基发生席夫碱反应,制得半纤维素/壳聚糖吸附材料[43]。羧甲基壳聚糖的引入提高了复合水凝胶的力学稳定性,拓展了半纤维素基水凝胶的应用。
氧化石墨烯(GO)、黏土和TiO2等无机聚合物常作为功能材料与半纤维素复合制备水凝胶。Kong等[44]用富含环氧化物、羧基等活性含氧官能团的GO与半纤维素通过自由基聚合制备了具有强韧性和高弹性的半纤维素基复合水凝胶。首先对半纤维素进行羧甲基改性,接着在N2条件下将丙烯酰胺(AM)和羧甲基半纤维素(CMH)混合,以过硫酸铵为引发剂,N, N′-亚甲基双丙烯酰胺为交联剂,经自由基聚合反应,将聚丙烯酰胺(PAM)接枝到CMH链上,GO纳米片中的含氧官能团通过氢键与PAM网络相互作用,获得GO/PAM/CMH复合水凝胶;然后通过CMH的羧基和Al3+的配位作用形成GO/PAM/Al-CMH纳米复合水凝胶。力学性能测试发现,该水凝胶的最大抗压强度和杨氏模量达到1.12 MPa和13.27 MPa,较纯PAM水凝胶(0.017 MPa和0.072 MPa)分别增加约6488%和18330%。
黏土纳米片有较高的比表面积,与半纤维素复合制备水凝胶,在离子吸附领域有一定的应用前景[45]。Cheng等[46]将半纤维素与黏土纳米片混合,经剧烈搅拌使黏土纳米片均匀分散在半纤维素溶液中,然后加入聚乙二醇二缩水甘油醚(PEGDE),通过半纤维素羟基的去质子化和PEGDE的开环反应,形成具有高效吸附性能的复合水凝胶。研究表明,添加和未添加黏土纳米片的复合水凝胶对亚甲基蓝的最大吸附量分别为148.8 mg/g和95.6 mg/g,表明黏土纳米片的层状结构为水凝胶提供高的比表面积,明显提高离子吸附能力。半纤维素和黏土纳米片的羟基之间形成强的氢键作用,95%应变下水凝胶的压缩模量和抗压强度分别为36.9 kPa和304.5 kPa,远远高于未添加黏土纳米片的1.9 kPa和116.5 kPa。
2 半纤维素水凝胶的应用半纤维素基水凝胶凭借良好的生物相容性、生物可降解性、大的比表面积和三维多孔结构,在生物医药和废水吸附净化等领域具有较为广阔的应用前景。
2.1 药物控释药物控释的主要目的是延长药物作用时间、减少给药次数、降低药物毒性。半纤维素基智能水凝胶有大的比表面积和良好的生物相容性,并且能对pH[21, 47]、温度[48]、光[49]、磁场[50]、盐[7]和有机溶剂[7]等外部条件变化产生智能响应,可作为药物载体,控制药物的吸收输送速率,实现药物控制释放的目的。部分半纤维素基水凝胶的智能响应体系如表 3所示[7, 21, 48, 50-51]。
| Release type | Cross-link | Release medium | Reference |
| Salt, pH and organic solvent | MBA | PBS | [7] |
| pH | DCC and DMAP | PBS(5.0 and 7.4) | [21] |
| Temperature and pH | MBA | NIH3T3 cells and FBS | [48] |
| Magnetic | Epichlorohydrin | BSA | [50] |
| Antibacterial | Schiff-base reaction | Sterile water | [51] |
| Abbreviations:pH buffer solutions(PBS);N, N′-dicyclohexylcarbod-iimide(DCC);4-dimethylaminopyridine(DMAP);Bovine serum albumin(BSA);Mouse embryonic fibroblasts(NIH3T3 cells);Fetal bovine serum(FBS) | |||
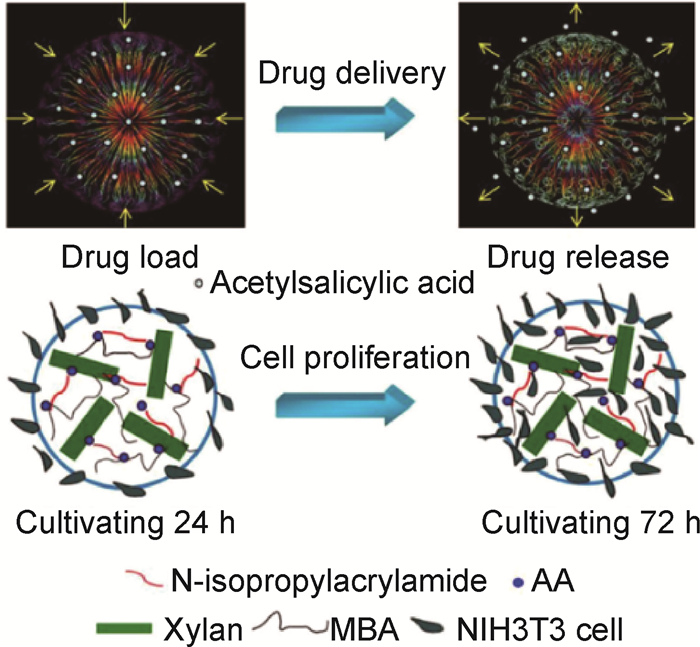
在功能聚合物中,聚N-异丙基丙烯酰胺(PNIPAm)、聚丙烯酸(PAA)和Fe3O4纳米颗粒常作为功能分子与半纤维素制备智能响应水凝胶用于药物控制释放。Gao等[48]将木聚糖与N-异丙基丙烯酰胺单体和丙烯酸在紫外光下交联,制备了温度/pH响应水凝胶,其药物递送行为和细胞增殖如图 1所示。通过细胞活性实验证明木聚糖水凝胶与小鼠胚胎成纤维细胞具有较好生物相容性。NIPAm和AA单体对水凝胶乙酰水杨酸载量有较大影响。NIPAm含量从0.02 g增加到0.1 g,载药量逐渐减少。随着AA/木聚糖质量比从6:1增加到12:1,载药量呈现先增加后降低的趋势。这是因为高的AA含量降低了水凝胶的接枝率,导致溶胀率降低,药物负荷减少。实验还模拟了胃液(pH值为1.5)和肠道(pH值为7.4)环境下该水凝胶中乙酰水杨酸的释放效率。在模拟肠道环境中,体外累积药物释放效率8 h可达到90.12%;而在模拟胃液中药物释放量仅为26.35%。胃液中释放量较低可能是由于在酸性溶液中药物与水凝胶之间形成氢键,使水凝胶网络变得更加紧密,抑制了药物的释放。该温度/pH响应水凝胶具有一定的药物控制释放性能,可作为潜在的口服药物载体。Zhao等[50]利用磁性Fe3O4纳米粒子与半纤维素合成磁响应水凝胶,以牛血清白蛋白(BSA)为模型药物,发现含15% Fe3O4纳米颗粒的水凝胶对牛血清蛋白的吸收能力达到146.5 mg/g,大于纯半纤维素基水凝胶的100.2 mg/g。该复合水凝胶中的Fe3O4纳米粒子能与多个BSA分子中的NH2基团结合,提高了对BSA分子的吸收能力。此外,磁响应水凝胶在5 d内牛血清蛋白的释放量为109 mg/g,在一定程度上实现了对BSA分子的缓释效果。
Edlund等[52]尝试将活化后的半纤维素与甲基丙烯酸-2-羟乙酯(HEMA)交联生成微球,并作为BSA和咖啡因的载体,对药物释放速率进行了研究。研究发现BSA和咖啡因的释放速率受半纤维素取代度的影响。取代度越高,半纤维素链上可交联基团越多,与BSA和咖啡因分子交联越紧密,扩散速率越慢。BSA和咖啡因分子的扩散速率还与分子大小有关。当取代度为36%时,大分子BSA延缓释放时间为500 min,而较小分子的咖啡因仅能延缓释放60 min,表明大分子BSA比小分子咖啡因更难释放。
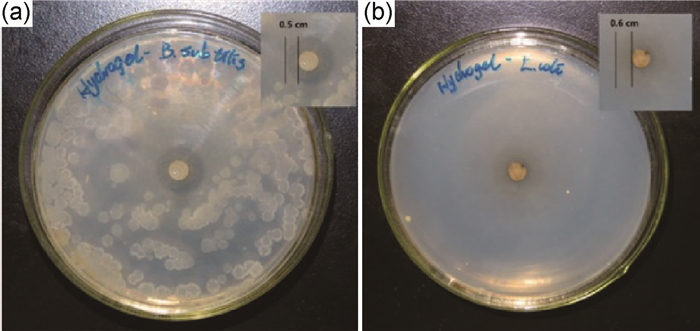
2.2 伤口敷料理想的伤口凝胶敷料应具备加快伤口愈合、保护伤口不受细菌感染、不易黏附皮肤、容易移除及允许气体交换等性质[53]。木聚糖具有独特的免疫防御、抑制细胞突变和抗氧化等性能,常与Ag纳米颗粒[54]、壳聚糖[55]等抗菌物质复合制备抗菌、抗氧化水凝胶,用于伤口敷料领域。Bao等[42]通过席夫碱反应将壳聚糖与半纤维素聚合,制备了复合水凝胶。抗菌和抗氧化性能研究发现,大肠杆菌和金黄色葡萄球菌受到抑制,抗菌活性增加。这是因为壳聚糖阳离子与细菌细胞表面的阴离子物质之间的相互作用,改变了细胞膜的通透性,从而阻断物质进入细胞,起到抗菌效果[56]。壳聚糖和木聚糖的糖胺缩合也使水凝胶具有较好的抗氧化活性[57]。Guan等[51]在添加壳聚糖的基础上引入Ag纳米颗粒,制得半纤维素(DHC)/壳聚糖/Ag复合水凝胶。从图 2可以看出,金黄色葡萄球菌和大肠杆菌的抑菌圈直径分别为0.5 cm和0.6 cm,表明该复合水凝胶对大肠杆菌和金黄色葡萄球菌均有一定的抑制效果。Ag纳米颗粒附着在细菌细胞膜表面,可扰乱细胞膜的正常生长,起到杀死细菌的效果。此外,Ag纳米粒子的颗粒越小,产生的接触面积越大,抗菌效果越好。
导电聚合物具有特殊的电学性质,电导率在7.6×10-8~1.1×10-3 S/cm范围内的刺激即可促进生物体内细胞的生长和分化,加快伤口愈合[58]。半纤维素与导电聚合物形成导电复合水凝胶,能作为伤口敷料。Zhao等[59-60]利用云杉半纤维素与具有良好溶解性的苯胺低聚物交联,制得半纤维素基导电水凝胶。随着苯胺低聚物含量的增加,水凝胶的电导率也逐渐增加(2.93×10-8~1.58×10-6 S/cm),但溶胀性能会呈下降趋势。因此,该半纤维素基导电复合水凝胶通过调节电导率的大小能促进伤口的愈合。
2.3 吸附工业废水中含有大量有毒的染料和重金属离子,对生态环境和人类的健康构成了巨大威胁,吸附是净化废水最有效的方法之一[61]。半纤维素基水凝胶有大量的孔结构,吸水性强,研究发现对重金属离子和有机染料等污染物有很好的吸附效果。
活性黑5(RB-5)和亚甲基蓝等有机染料在废水中广泛存在,半纤维素基水凝胶可以通过静电作用对这些染料进行吸附。Bankeeree等[62]制备了木聚糖/聚乙烯醇复合水凝胶,对RB-5进行吸附研究发现,在第一个脱色循环(6 h)内,RB-5的最大脱色效率达到(98.45±1.96)%,重复使用8次后,水凝胶对RB-5的脱色效率仍能达到(55.35±2.46)%。Sun等[63]引入CaCO3作为致孔剂,将半纤维素与丙烯酸混合制备了复合水凝胶,研究对亚甲基蓝的吸附能力。CaCO3的引入使水凝胶的孔隙增多,提高了比表面积,同时使水凝胶中-COOH基团暴露在水凝胶表面,为亚甲基蓝的附着提供大量的位点,大大提高了吸附效率。
半纤维素基水凝胶通过静电作用对重金属离子也有较好的吸附效果。Peng等[64]利用半纤维素与丙烯酸交联,引入电负性的羧基基团,通过静电作用实现对重金属离子的吸附。该水凝胶对Pd2+, Cd2+和Zn2+的最大吸附能力分别为859,495 mg/g和274 mg/g;重复使用对金属离子的吸附效率影响不大,当吸附解吸循环8次后,Pd2+, Cd2+和Zn2+的吸附量仍能达到774,441 mg/g和230 mg/g。此外,在凝胶体系中引入壳聚糖[65]、蒙脱土[40]、Fe3O4粒子[66]等吸附材料,也能提高其对重金属离子的吸附效率。
2.4 其他应用在细胞壁中,半纤维素作为一个填充的基质与纤维素和木质素作用支撑细胞壁结构。借助半纤维素和纤维素在细胞壁中的相互作用也能对凝胶材料的性能产生影响[67]。Markstedt等[68]利用酪胺功能化的半纤维素同纤维素纳米纤维(CNF)合成新型油墨,通过3D打印技术制备出水凝胶。为研究木聚糖引入对油墨稳定性的作用,对不同油墨进行了测试:纯CNF油墨能交联成形,但在打印后受到机械力的作用,打印的形状会坍塌;纯木聚糖制备的油墨很容易交叉连接,但不能打印成形;混合CNF和木聚糖的油墨有较好的打印效果。此外,油墨中酪胺取代度和CNF与木聚糖/酪胺的含量也能影响油墨的印刷性和稳定性,进而影响3D打印水凝胶的性能。该凝胶完全由生物组分构成,具有很好的生物相容性和溶胀性能,扩展了半纤维素的应用潜力。
3 结束语半纤维素基水凝胶凭借其良好的可加工性、可调的溶胀性能、高的比表面和对外界刺激(温度、pH、磁场等)的快速响应性等优点,在药物控释、伤口敷料和废水净化等领域具有广泛的应用前景。对这些半纤维素基水凝胶已经进行了大量的基础研究,包括原料的选择、交联剂的筛选以及物理和化学交联合成的机理等。但仍有很多问题亟待解决:
(1) 半纤维素基水凝胶的制备过程大多仍需有毒试剂的使用,并且反应能耗过高,如何设计绿色(安全溶剂、无毒交联剂)和低能耗的反应体系仍需要更多的探索。
(2) 由于半纤维素分子量较小,聚合度较低,制备的半纤维素基水凝胶的力学强度较差,仍需通过改性或引入其他聚合物高分子来改善水凝胶的力学性能。
(3) 如何设计具有pH、温度和磁场等多重响应性质的新型智能半纤维素基水凝胶,丰富半纤维素的应用还需深入研究。
(4) 半纤维素基水凝胶大多的研究还停留在实验室阶段,如何加快实现半纤维素基水凝胶在农业、环境保护、废水处理和生物医药等领域的规模应用,又是一大难题。相信随着对半纤维素基水凝胶研究的不断深入,这些挑战性问题都将得到解决。
| [1] |
尹大伟, 周英, 刘玉婷, 等. 水凝胶的最新研究进展[J]. 化工新型材料, 2012, 40(2): 21-23. YIN D W, ZHOU Y, LIU Y T, et al. The new research development of hydrogel[J]. New Chemical Materials, 2012, 40(2): 21-23. DOI:10.3969/j.issn.1006-3536.2012.02.007 |
| [2] |
AHMED E M. Hydrogel:preparation, characterization, and applications:a review[J]. Journal of Advanced Research, 2015, 6(2): 105-121. |
| [3] |
QI X M, GUAN Y, CHEN G G, et al. A non-covalent strategy for montmorillonite/xylose self-healing hydrogels[J]. RSC Advances, 2015, 5(51): 41006-41012. DOI:10.1039/C5RA04115E |
| [4] |
GABRIELII I, GATENHOLM P, GLASSER W G, et al. Separation, characterization and hydrogel-formation of hemicellulose from aspen wood[J]. Carbohydrate Polymers, 2000, 43(4): 367-374. DOI:10.1016/S0144-8617(00)00181-8 |
| [5] |
MARTÍNEZ-GÓMEZ F, GUERRERO J, MATSUHIRO B, et al. In vitro release of metformin hydrochloride from sodium alginate/polyvinyl alcohol hydrogels[J]. Carbohydrate Polymers, 2017, 155: 182-191. DOI:10.1016/j.carbpol.2016.08.079 |
| [6] |
AMIN M C I M, AHMAD N, HALIB N, et al. Synthesis and characterization of thermo-and pH-responsive bacterial cellulose/acrylic acid hydrogels for drug delivery[J]. Carbohydrate Polymers, 2012, 88(2): 465-473. DOI:10.1016/j.carbpol.2011.12.022 |
| [7] |
PENG X W, REN J L, ZHONG L X, et al. Xylan-rich hemicelluloses-graft-acrylic acid ionic hydrogels with rapid responses to pH, salt, and organic solvents[J]. Journal of Agricultural and Food Chemistry, 2011, 59(15): 8208-8215. DOI:10.1021/jf201589y |
| [8] |
LI X, PAN X. Hydrogels based on hemicellulose and lignin from lignocellulose biorefinery: a mini-review[J]. Journal of Biobased Materials and Bioenergy, 2010, 4(4): 289-297. DOI:10.1166/jbmb.2010.1107 |
| [9] |
JAYAKUMAR R, PRABAHARAN M, KUMAR P T S, et al. Biomaterials based on chitin and chitosan in wound dressing applications[J]. Biotechnology Advances, 2011, 29(3): 322-337. DOI:10.1016/j.biotechadv.2011.01.005 |
| [10] |
LI G X, DU Y M, TAO Y Z, et al. Iron(Ⅱ)cross-linked chitin-based gel bead:preparation, magnetic property and adsorption of methyl orange[J]. Carbohydrate Polymers, 2010, 82(3): 706-713. DOI:10.1016/j.carbpol.2010.05.040 |
| [11] |
LI T, LI L H, SUN H W, et al. Porous ionic membrane based flexible humidity sensor and its multifunctional applications[J]. Advanced Science, 2017, 4(5): 1600404. DOI:10.1002/advs.201600404 |
| [12] |
PENG F, PENG P, XU F, et al. Fractional purification and bioconversion of hemicelluloses[J]. Biotechnology Advances, 2012, 30(4): 879-903. DOI:10.1016/j.biotechadv.2012.01.018 |
| [13] |
SCHELLER H V, ULVSKOV P. Hemicelluloses[J]. Annual Review of Plant Biology, 2010, 61: 263-289. DOI:10.1146/annurev-arplant-042809-112315 |
| [14] |
程合丽, 冯清华, 陈洪雷, 等. 半纤维素基水凝胶制备方法研究进展[J]. 造纸科学与技术, 2015, 34(6): 40-45. CHENG H L, FENG Q H, CHEN H L, et al. Research progress in preparation methods of hemicellulose-based hydrogels[J]. Paper Science & Technology, 2015, 34(6): 40-45. |
| [15] |
ELGUETA E, SÁNCHEZ J, DAX D, et al. Functionalized galactoglucomannan-based hydrogels for the removal of metal cations from aqueous solutions[J]. Journal of Applied Polymer Science, 2016, 133(41): 1-8. |
| [16] |
QI X M, CHEN G G, GONG X D, et al. Enhanced mechanical performance of biocompatible hemicelluloses-based hydrogel via chain extension[J]. Scientific Reports, 2016, 6: 1-10. DOI:10.1038/s41598-016-0001-8 |
| [17] |
ROOS A A, EDLUND U, SJOBERG J, et al. Protein release from galactoglucomannan hydrogels:influence of substitutions and enzymatic hydrolysis by β-mannanase[J]. Biomacromolecules, 2008, 9(8): 2104-2110. DOI:10.1021/bm701399m |
| [18] |
PARIKKA K, NIKKILÄ I, PITKÄNEN L, et al. Laccase/TEMPO oxidation in the production of mechanically strong arabinoxylan and glucomannan aerogels[J]. Carbohydrate Polymers, 2017, 175: 377-386. DOI:10.1016/j.carbpol.2017.07.074 |
| [19] |
MALEKI L, EDLUND U, ALBERTSSON A C. Thiolated hemicellulose as a versatile platform for one-pot click-type hydrogel synthesis[J]. Biomacromolecules, 2015, 16(2): 667-674. DOI:10.1021/bm5018468 |
| [20] |
KARAASLAN M A, TSHABALALA M A, YELLE D J, et al. Nanoreinforced biocompatible hydrogels from wood hemicelluloses and cellulose whiskers[J]. Carbohydrate Polymers, 2011, 86(1): 192-201. DOI:10.1016/j.carbpol.2011.04.030 |
| [21] |
AYOUB A, VENDITTI R A, PAWLAK J J, et al. Novel hemicellulose-chitosan biosorbent for water desalination and heavy metal removal[J]. ACS Sustainable Chemistry & Engineering, 2013, 1(9): 1102-1109. |
| [22] |
LIU S J, CHEN F G, SONG X Y, et al. Preparation and characterization of temperature- and pH-sensitive hemicellulose-containing hydrogels[J]. International Journal of Polymer Analysis and Characterization, 2017, 22(3): 187-201. DOI:10.1080/1023666X.2016.1276257 |
| [23] |
DAX D, CHÁVEZ M S, XU C L, et al. Cationic hemicellulose-based hydrogels for arsenic and chromium removal from aqueous solutions[J]. Carbohydrate Polymers, 2014, 111: 797-805. DOI:10.1016/j.carbpol.2014.05.045 |
| [24] |
LAWOKO M, HENRIKSSON G, GELLERSTEDT G. Characterisation of lignin-carbohydrate complexes(LCCs) of spruce wood(Picea abies L.)isolated with two methods[J]. Holzforschung, 2006, 60(2): 156-161. DOI:10.1515/HF.2006.025 |
| [25] |
OINONEN P, ARESKOGH D, HENRIKSSON G. Enzyme catalyzed cross-linking of spruce galactoglucomannan improves its applicability in barrier films[J]. Carbohydrate Polymers, 2013, 95(2): 690-696. DOI:10.1016/j.carbpol.2013.03.016 |
| [26] |
OLSÉN P, UNDIN J, ODELIUS K, et al. Establishing α-bromo-γ-butyrolactone as a platform for synthesis of functional aliphatic polyesters-bridging the gap between ROP and SET-LRP[J]. Polymer Chemistry, 2014, 5(12): 3847-3854. DOI:10.1039/C4PY00148F |
| [27] |
YANG J Y, ZHOU X S, FANG J. Synthesis and characterization of temperature sensitive hemicellulose-based hydrogels[J]. Carbohydrate Polymers, 2011, 86(3): 1113-1117. DOI:10.1016/j.carbpol.2011.05.043 |
| [28] |
POHJANLEHTO H, SETÄLÄ H, KAMMIOVIRTA K, et al. The use of N, N'-diallylaldardiamides as cross-linkers in xylan derivatives-based hydrogels[J]. Carbohydrate Research, 2011, 346(17): 2736-275. |
| [29] |
MARKSTEDT K, XU W Y, LIU J L, et al. Synthesis of tunable hydrogels based on O-acetyl-galactoglucomannans from spruce[J]. Carbohydrate Polymers, 2017, 157: 1349-1357. DOI:10.1016/j.carbpol.2016.11.009 |
| [30] |
KUZMENKO V, HÄGG D, TORIZ G, et al. In situ forming spruce xylan-based hydrogel for cell immobilization[J]. Carbohydrate Polymers, 2014, 102: 862-868. DOI:10.1016/j.carbpol.2013.10.077 |
| [31] |
MEENA R, LEHNEN R, SAAKE B. Microwave-assisted synthesis of kC/xylan/PVP-based blend hydrogel materials:physicochemical and rheological studies[J]. Cellulose, 2014, 21(1): 553-568. DOI:10.1007/s10570-013-0155-5 |
| [32] |
ZHANG W M, ZHU S, BAI Y P, et al. Glow discharge electrolysis plasma initiated preparation of temperature/pH dual sensitivity reed hemicellulose-based hydrogels[J]. Carbohydrate Polymers, 2015, 122: 11-17. DOI:10.1016/j.carbpol.2015.01.007 |
| [33] |
WANG Y, FENG Q L, WEI N, et al. A simple method for the production of hydrogels based on hemicellulose in aqueous solution[J]. Polymer Science Series: B, 2016, 58(3): 351-360. DOI:10.1134/S1560090416030179 |
| [34] |
NGUYEN K T, WEST J L. Photopolymerizable hydrogels for tissue engineering applications[J]. Biomaterials, 2002, 23(22): 4307-4314. DOI:10.1016/S0142-9612(02)00175-8 |
| [35] |
WIESBROCK F, HOOGENBOOM R, SCHUBERT U S. Microwave-assisted polymer synthesis:state-of-the-art and future perspectives[J]. Macromolecular Rapid Communications, 2004, 25(20): 1739-1764. DOI:10.1002/marc.200400313 |
| [36] |
ZHANG W M, LIANG Z L, FENG Q L, et al. Reed hemicellulose-based hydrogel prepared by glow discharge eletrolysis plasma and its adsorption properties for heavy metal ions[J]. Fresenius Environ Bull, 2016, 25(6): 1791-1798. |
| [37] |
GUAN Y, ZHANG B, TAN X, et al. Organic-inorganic composite films based on modified hemicelluloses with clay nanoplatelets[J]. ACS Sustainable Chemistry & Engineering, 2014, 2(7): 1811-1818. |
| [38] |
HASSAN C M, WARD J H, PEPPAS N A. Modeling of crystal dissolution of poly (vinyl alcohol) gels produced by freezing/thawing processes[J]. Polymer, 2000, 41(18): 6729-6739. DOI:10.1016/S0032-3861(00)00031-8 |
| [39] |
GUAN Y, ZHANG B, BIAN J, et al. Nanoreinforced hemicellulose-based hydrogels prepared by freeze-thaw treatment[J]. Cellulose, 2014, 21(3): 1709-1721. DOI:10.1007/s10570-014-0211-9 |
| [40] |
GUAN Y, BIAN J, PENG F, et al. High strength of hemicelluloses based hydrogels by freeze/thaw technique[J]. Carbohydrate Polymers, 2014, 101: 272-280. DOI:10.1016/j.carbpol.2013.08.085 |
| [41] |
SAXENA A, ELDER T J, RAGAUSKAS A J. Moisture barrier properties of xylan composite films[J]. Carbohydrate Polymers, 2011, 84(4): 1371-1377. DOI:10.1016/j.carbpol.2011.01.039 |
| [42] |
BAO Y P, ZHANG H, LUAN Q, et al. Fabrication of cellulose nanowhiskers reinforced chitosan-xylan nanocomposite films with antibacterial and antioxidant activities[J]. Carbohydrate Polymers, 2018, 184: 66-73. DOI:10.1016/j.carbpol.2017.12.051 |
| [43] |
WU S P, HU J, WEI L T, et al. Construction of porous chitosan-xylan-TiO2 hybrid with highly efficient sorption capability on heavy metals[J]. Journal of Environmental Chemical Engineering, 2014, 2(3): 1568-1577. DOI:10.1016/j.jece.2014.07.001 |
| [44] |
KONG W Q, HUANG D Y, XU G B, et al. Graphene oxide/polyacrylamide/aluminum ion cross-linked carboxymethyl hemicellulose nanocomposite hydrogels with very tough and elastic properties[J]. Chemistry-an Asian Journal, 2016, 11(11): 1697-1704. DOI:10.1002/asia.201600138 |
| [45] |
ZHANG S, GUAN Y, FU G Q, et al. Organic/inorganic superabsorbent hydrogels based on xylan and montmorillonite[J]. Journal of Nanomaterials, 2014, 2014(2): 1-11. |
| [46] |
CHENG H L, FENG Q H, LIAO C A, et al. Removal of methylene blue with hemicellulose/clay hybrid hydrogels[J]. Chinese Journal of Polymer Science, 2016, 34(6): 709-719. DOI:10.1007/s10118-016-1788-2 |
| [47] |
KUMAR S U, KUMAR V, PRIYADARSHI R, et al. pH-responsive prodrug nanoparticles based on xylan-curcumin conjugate for the efficient delivery of curcumin in cancer therapy[J]. Carbohydrate Polymers, 2018, 188: 252-259. DOI:10.1016/j.carbpol.2018.02.006 |
| [48] |
GAO C D, REN J L, ZHAO C, et al. Xylan-based temperature/pH sensitive hydrogels for drug controlled release[J]. Carbohydrate Polymers, 2016, 151: 189-197. DOI:10.1016/j.carbpol.2016.05.075 |
| [49] |
CAO X F, PENG X W, ZHONG L X, et al. Multiresponsive hydrogels based on xylan-type hemicelluloses and photoisomerized azobenzene copolymer as drug delivery carrier[J]. Journal of Agricultural and Food Chemistry, 2014, 62(41): 10000-10007. DOI:10.1021/jf504040s |
| [50] |
ZHAO W F, ODELIUS K, EDLUND U, et al. In situ synthesis of magnetic field-responsive hemicellulose hydrogels for drug delivery[J]. Biomacromolecules, 2015, 16(8): 2522-2528. DOI:10.1021/acs.biomac.5b00801 |
| [51] |
GUAN Y, CHEN J H, QI X M, et al. Fabrication of biopolymer hydrogel containing Ag nanoparticles for antibacterial property[J]. Industrial & Engineering Chemistry Research, 2015, 54(30): 7393-7400. |
| [52] |
EDLUND U, ALBERTSSON A C. A microspheric system:hemicellulose-based hydrogels[J]. Journal of Bioactive and Compatible Polymers, 2008, 23(2): 171-186. DOI:10.1177/0883911507088400 |
| [53] |
SHEN X P, SHAMSHINA J L, BERTON P, et al. Hydrogels based on cellulose and chitin:fabrication, properties, and applications[J]. Green Chemistry, 2016, 18(1): 53-75. DOI:10.1039/C5GC02396C |
| [54] |
ADUBA JR D C, AN S S, SELDERS G S, et al. Fabrication, characterization, and in vitro evaluation of silver-containing arabinoxylan foams as antimicrobial wound dressing[J]. Journal of Biomedical Materials Research: Part A, 2016, 104(10): 2456-2465. DOI:10.1002/jbm.a.35783 |
| [55] |
BHATTARAI N, GUNN J, ZHANG M Q. Chitosan-based hydrogels for controlled, localized drug delivery[J]. Advanced Drug Delivery Reviews, 2010, 62(1): 83-99. DOI:10.1016/j.addr.2009.07.019 |
| [56] |
KRAJEWSKA B, WYDRO P, JANNCZYK A. Probing the modes of antibacterial activity of chitosan.Effects of pH and molecular weight on chitosan interactions with membrane lipids in langmuir films[J]. Biomacromolecules, 2011, 12(11): 4144-4152. DOI:10.1021/bm2012295 |
| [57] |
LI X X, SHI X W, JIN Y, et al. Controllable antioxidative xylan-chitosan Maillard reaction products used for lipid food storage[J]. Carbohydrate Polymers, 2013, 91(1): 428-433. DOI:10.1016/j.carbpol.2012.08.052 |
| [58] |
GUARINO V, ALVAREZ-PEREZ M A, BORRIELLO A, et al. Conductive PANi/PEGDA macroporous hydrogels for nerve regeneration[J]. Advanced Healthcare Materials, 2013, 2(1): 218-227. DOI:10.1002/adhm.201200152 |
| [59] |
ZHAO W F, GLAVAS L, ODELIUS K, et al. A robust pathway to electrically conductive hemicellulose hydrogels with high and controllable swelling behavior[J]. Polymer, 2014, 55(13): 2967-2976. DOI:10.1016/j.polymer.2014.05.003 |
| [60] |
ZHAO W F, GLAVAS L, ODELIUS K, et al. Facile and green approach towards electrically conductive hemicellulose hydrogels with tunable conductivity and swelling behavior[J]. Chemistry of Materials, 2014, 26(14): 4265-4273. DOI:10.1021/cm501852w |
| [61] |
DRAGAN E S, APOPEI D F. Synthesis and swelling behavior of pH-sensitive semi-interpenetrating polymer network composite hydrogels based on native and modified potatoes starch as potential sorbent for cationic dyes[J]. Chemical Engineering Journal, 2011, 178: 252-263. DOI:10.1016/j.cej.2011.10.066 |
| [62] |
BANKEEREE W, PRASONGSUK S, IMAI T, et al. A novel xylan-polyvinyl alcohol hydrogel bead with laccase entrapment for decolorization of reactive black 5[J]. BioResources, 2016, 11(3): 6984-7000. |
| [63] |
SUN X F, GAN Z, JING Z X, et al. Adsorption of methylene blue on hemicellulose-based stimuli-responsive porous hydrogel[J]. Journal of Applied Polymer Science, 2015, 132(10): 1-10. |
| [64] |
PENG X W, ZHONG L X, REN J L, et al. Highly effective adsorption of heavy metal ions from aqueous solutions by macroporous xylan-rich hemicelluloses-based hydrogel[J]. Journal of Agricultural and Food Chemistry, 2012, 60(15): 3909-3916. DOI:10.1021/jf300387q |
| [65] |
WU S P, DAI X Z, KAN J R, et al. Fabrication of carboxymethyl chitosan-hemicellulose resin for adsorptive removal of heavy metals from wastewater[J]. Chinese Chemical Letters, 2017, 28(3): 625-632. DOI:10.1016/j.cclet.2016.11.015 |
| [66] |
李亚婧, 孙晓锋, 叶青, 等. 新型半纤维素基磁性水凝胶的制备及性能[J]. 物理化学学报, 2014, 30(1): 111-120. LI Y J, SUN X F, YE Q, et al. Preparation and properties of a novel hemicellulose-based magnetic hydrogel[J]. Acta Physico-Chimica Sinica, 2014, 30(1): 111-120. |
| [67] |
PRAKOBNA K, KISONEN V, XU C L, et al. Strong reinforcing effects from galactoglucomannan hemicellulose on mechanical behavior of wet cellulose nanofiber gels[J]. Journal of Materials Science, 2015, 50(22): 7413-7423. DOI:10.1007/s10853-015-9299-z |
| [68] |
MARKSTEDT K, ESCALANTE A, TORIZ G, et al. Biomimetic inks based on cellulose nanofibrils and cross-linkable xylans for 3D printing[J]. ACS Applied Materials & Interfaces, 2017, 9(46): 40878-40886. |
 2020, Vol. 48
2020, Vol. 48