文章信息
- 余煜玺, 马锐, 王贯春, 张瑞谦, 彭小明
- YU Yu-xi, MA Rui, WANG Guan-chun, ZHANG Rui-qian, PENG Xiao-ming
- 高比表面积、低密度块状Al2O3气凝胶的制备及表征
- Preparation and characterization of Al2O3 bulk aerogel with high specific surface area and low density
- 材料工程, 2019, 47(12): 136-142
- Journal of Materials Engineering, 2019, 47(12): 136-142.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2017.000852
-
文章历史
- 收稿日期: 2017-07-04
- 修订日期: 2019-08-23
2. 中国核动力研究设计院 反应堆燃料及材料重点实验室, 成都 610000
2. Science and Technology on Reactor Fuel and Materials Laboratory, Nuclear Power Institute of China, Chengdu 610000, China
氧化铝气凝胶作为一种新型耐高温的纳米多孔材料,不仅具有一般气凝胶的各种优良特性,如高比表面积、低密度、高孔隙率等,而且具有耐高温(使用温度≥1000℃)和高温热稳定性[1-4],可广泛应用于高温隔热、高温催化及高温载体等领域[5-6]。
从Yoldas首次通过异丙醇铝(AIP)和仲丁醇铝(ASB)在酸催化作用下水解、缩聚制备得到氧化铝凝胶后[7-9],在其研究基础上,有很多研究者以有机铝醇盐和无机铝盐为铝源,通过溶胶-凝胶法来研究氧化铝干凝胶和气凝胶的制备。何飞等[10]以硝酸铝无机盐为铝源,采用常压干燥法制备氧化铝干凝胶,虽然制备成本低,但制备周期长,干凝胶收缩严重,容易开裂和形成粉末。Janosovits等[11]以铝醇盐为前驱体,在过量的水中水解铝醇盐得到氧化铝溶胶,来制备得到氧化铝凝胶。Poco等[12]以仲丁醇铝(ASB)为铝源,用少量水经溶胶-凝胶两步法制备得到稳定的Al2O3凝胶,再经乙醇超临界干燥制备得到多晶态块状的Al2O3气凝胶,其比表面积为376m2/g。高庆福等[13]以仲丁醇铝为铝源,经过水解缩聚得到块状氧化铝气凝胶,其比表面积为447m2/g,1200℃热处理后比表面积缩小至73m2/g。Zu等[14]同样采用仲丁醇铝为铝源,经过溶胶-凝胶过程和超临界过程得到氧化铝气凝胶,比表面积为690m2/g。
对比国内外研究者采用不同方法制备得到的氧化铝气凝胶,我们发现由于铝醇盐的高反应活性、凝胶过程的复杂反应以及干燥时易收缩开裂等影响因素,使得制备完整的高比表面积块状氧化铝气凝胶较为困难。本工作以仲丁醇铝为前驱体,乙酸为催化剂,乙酰乙酸乙酯为螯合剂,通过溶胶-凝胶过程和超临界干燥制备得到高比表面积、低密度的块状氧化铝气凝胶,研究工艺参数对Al2O3气凝胶的影响,并对其成分结构与热稳定性能进行表征分析。
1 实验材料与方法 1.1 样品的制备实验所用试剂:仲丁醇铝(ASB)、乙酰乙酸乙酯(Etac)、乙醇(EtOH)、乙酸(HAc)均来自国药集团化学试剂有限公司,为分析纯试剂。样品的制备和清洗所用水均为去离子水。
实验采用分步水解的方法配制氧化铝溶胶,首先按摩尔比例n(ASB):n(EtOH):n(Etac):n(H2O)=1:10:(0.05~0.2):0.6依次加入仲丁醇铝、乙酰乙酸乙酯、乙醇、乙酸并快速混合均匀,在60℃水浴中搅拌1h,待其冷却至室温,得到部分水解的铝溶胶,记作Al-1。然后按摩尔比例n(ASB):n(EtOH):n(H2O):n(HAc)= 1:(10~30):2.4:0.1依次加入乙醇、水和乙酸至Al-1中,快速搅拌均匀,得到充分水解的铝溶胶,记作Al-2。静置一段时间得到湿凝胶,将其置于乙醇中老化一段时间,每6h更换一次乙醇,置换4次。
将清洗后的氧化铝凝胶放入超临界釜中,冲扫氮气10min,并将釜内压力提高至1.0MPa。设置加热电压为150V,以1℃/min的速率升温至260℃,保温40min。然后以0.2MPa/min的速率进行卸压,卸压后冲扫氮气30min。自然冷却至室温,得到氧化铝气凝胶。
1.2 表征采用X’pert PRO型X射线衍射仪分析样品的结晶形态。采用SU70型扫描电子显微镜观察样品的微观形貌。采用TristarⅡ3020型比表面积及孔径分析仪测试样品的比表面积及孔径分布。采用Avatar 360型傅里叶红外光谱仪分析样品的化学键与官能团。采用DSC204 Cell型差示扫描量热仪分析样品的热稳定性,在空气气氛条件下,分析样品的热稳定性,测试温度范围从室温到1200℃,升温速率为10℃/min。将样品加工成规则形状,按密度公式计算样品的体积密度。
2 结果与分析氧化铝气凝胶制备的关键在于配置稳定且澄清的铝溶胶。由于铝醇盐中存在二聚物以及寡聚单元[15],使铝醇盐对水非常敏感,水解反应剧烈;同时,受铝醇盐前驱体及其水解产物的溶解度影响,制备铝溶胶过程中易形成沉淀。受以上两个因素的影响,难以制得稳定且澄清的溶胶体系。本实验通过采用分步水解和引入螯合剂的方式,利用两者的协同效应制得如图 1(a)所示的稳定且澄清的铝溶胶,经过水解缩聚反应和超临界干燥,最终得到如图 1(b)所示完整的氧化铝气凝胶块体。

|
图 1 氧化铝溶胶(a)和氧化铝气凝胶(b)的实物图 Fig. 1 Photos of alumina sol (a) and alumina aerogel (b) |
乙醇作为溶剂,可使反应物混合均匀,有利于得到均匀且完整的块体气凝胶;也可通过调节乙醇的比例来控制气凝胶的体积密度。实验中固定n(ASB):n(H2O):n(Etac):n(HAc)=1:3:0.1:0.1,研究乙醇量(EtOH/ASB=20,25,30,35和40)对氧化铝气凝胶的影响情况。
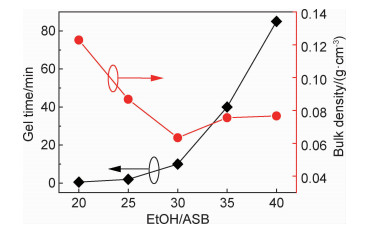
图 2描述了不同乙醇量对凝胶时间和气凝胶体积密度的影响,如图可见,随乙醇量的增加,凝胶时间逐渐增大。乙醇一方面作为溶剂,调节反应物的浓度来控制水解、缩聚反应速率,进而影响铝溶胶的凝胶时间;另一方面乙醇也作为铝醇盐的水解产物,其含量的增加抑制了水解反应,不利于Al—OH的产生,导致缩聚反应难度加大,凝胶时间被延长[16]。随着乙醇比例的增加,氧化铝气凝胶的密度先减小后增大,最后趋于稳定;当EtOH/ASB=30时,密度达到最小值0.0634g/cm3。乙醇量的增加,使得同体积的湿凝胶内,溶剂占据的体积增加,网络结构占据的体积减小,超临界干燥能保持湿凝胶的网络结构不变,因此,随着乙醇量的增加,密度会逐渐降低。但过高的乙醇含量将导致溶液中反应物浓度较低,缩聚反应进行困难。同时,过量的乙醇会分离水解形成的产物Al—OH,阻碍并破坏Al—O—Al键的形成,导致铝溶胶中簇与簇的分离,难以形成稳固的三维网络结构,凝胶骨架结构的强度较差,干燥过程中容易发生结构的部分坍塌和收缩,反而使气凝胶的密度变大[17]。
|
图 2 乙醇含量对氧化铝气凝胶制备过程的凝胶时间和体积密度的影响关系图 Fig. 2 Gel time and bulk density of alumina aerogels formed with different ethanol contents |
分别由BET和BJH算法计算得到气凝胶的比表面积和孔结构信息,气凝胶的结构主要是通过比表面积、平均孔径、孔体积和平均粒径这4个参数来进行分析,用平均粒径来体现气凝胶结构中颗粒的平均大小。表 1为不同乙醇量下制得的Al2O3气凝胶的孔结构信息,随着乙醇比例的增大,气凝胶的比表面积先增大后减少,但增减幅度较小,颗粒尺寸都在10nm左右;当EtOH/ASB<30时,气凝胶孔径都在20nm以上,当EtOH/ASB ≥30时,孔径降低至12nm左右,较少的乙醇量会导致凝胶速度过快,凝胶内部会由于缩聚不均匀出现一些不均匀的大孔,使气凝胶整体的孔径偏大。
| Sample | Specific surface area/ (m2·g-1) |
Average pore size/ nm |
Average particle size/nm |
Volume density/ (g·cm-3) |
| E-20 | 604.09 | 24.29 | 9.93 | 0.122 |
| E-25 | 658.66 | 27.26 | 9.10 | 0.086 |
| E-30 | 685.19 | 12.70 | 8.75 | 0.063 |
| E-35 | 658.20 | 12.28 | 9.11 | 0.075 |
| E-40 | 548.27 | 11.85 | 10.94 | 0.076 |
| Note: sample E-20 represents alumina aerogel sample with molar ratio EtOH/ASB=20. | ||||
仲丁醇铝具有很高的反应活性,水解反应特别剧烈,为稳定其水解反应,除了采用分步水解外,本实验引入乙酰乙酸乙酯作为螯合剂[18]。乙酰乙酸乙酯为酮式(CH3COHCHCOOC2H5)和烯醇式(CH3COCH2COOC2H5)的平衡混合物,烯醇异构体中存在的活性羟基容易和铝醇盐发生反应形成螯合物,其具体的螯合机理如图 3所示。首先,乙酰乙酸乙酯取代铝醇盐中的烷氧基团,然后,与铝原子螯合形成相对稳定的六元环状络合物,使得水分子难以直接发起亲核攻击,极大地延缓了仲丁醇铝的水解缩聚反应速率,阻止了沉淀的产生,进而提高铝溶胶的稳定性和均匀性。

|
图 3 乙酰乙酸乙酯螯合机理 Fig. 3 Chelating mechanism of ethyl acetoacetate |
本实验固定n(ASB):n(H2O):n(EtOH):n(HAc)=1:3:30:0.1,研究乙酰乙酸乙酯量(Etac/ASB=0.05,0.10,0.15和0.20)对氧化铝气凝胶的影响。
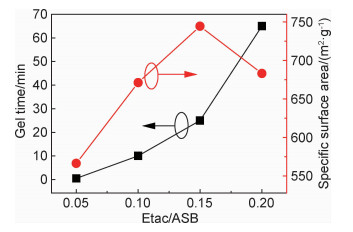
图 4为乙酰乙酸乙酯含量对Al2O3气凝胶的凝胶时间和比表面积的影响关系,由于乙酰乙酸乙酯对铝醇盐水解缩聚的阻碍作用,随着螯合剂含量的增加,阻碍作用增强,延长了凝胶时间。过量的乙酰乙酸乙酯使铝溶胶的缩聚反应极难发生,极弱的骨架强度难以形成稳定的凝胶体系,因此当Etac/ASB≥0.02时,铝溶胶长时间未出现凝胶状态。乙酰乙酸乙酯的比例控制在Etac/ASB=0.1~0.2可达到较好的效果;螯合剂的比例(Etac/ASB)从0.05增大到0.20,对应气凝胶的比表面积先增加后降低,当Etac/ASB=0.15时,比表面积达到最高744.52m2/g。
|
图 4 乙酰乙酸乙酯含量对氧化铝气凝胶的凝胶时间和比表面积的影响关系 Fig. 4 Gel time and specific surface areas of alumina aerogels formed at different Etac contents |
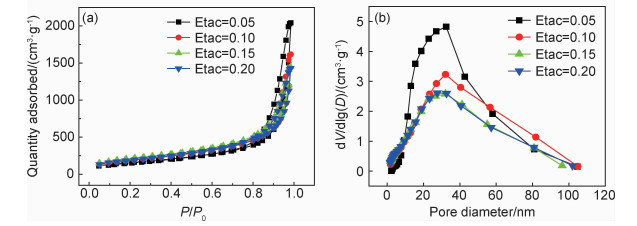
具体的气凝胶孔结构信息如表 2所示,随着乙酰乙酸乙酯量的增加,孔体积和孔径都在较小的范围内波动,可见螯合剂乙酰乙酸乙酯的加入对气凝胶内部孔结构的影响较小。氧化铝气凝胶的等温吸附脱附曲线和孔径分布(图 5)与二氧化硅气凝胶的差别不大,属于IUPAC分类法中的第IV类等温线,即制备出的氧化铝气凝胶具有典型的介孔(2nm≤孔径≤50nm)结构[19]。氧化铝气凝胶的吸附-脱附等温线前半段上升缓慢,后半段发生了急剧上升,并在一定的相对压力时达到吸附饱和,吸附等温线又呈直线平缓上升,当相对压力(P/P0)为0.936时,在脱附曲线上发生吸附量急剧变化,表明此时是孔径分布集中的范围,其孔径大小集中分布在20~40nm,进一步可看出氧化铝气凝胶具有介孔结构。
| Sample | Specific surface area/ (m2·g-1) |
Average pore size/ nm |
Average particle size/nm | Volume density/ (g·cm-3) |
| A-0.05 | 566.29 | 23.05 | 3.159 | 10.59 |
| A-0.10 | 671.19 | 15.26 | 2.501 | 8.93 |
| A-0.15 | 744.52 | 12.76 | 2.239 | 8.05 |
| A-0.20 | 683.12 | 13.31 | 2.213 | 8.78 |
| Note: sample A-0.05 represents alumina aerogel sample with molar ratio of Etac/ASB=0.05. | ||||
|
图 5 不同乙酰乙酸乙酯含量制备得到的氧化铝气凝胶的等温吸附-脱附曲线(a)和孔径分布图(b) Fig. 5 N2 adsorption-desorption isotherms (a) and pore size distributions (b) of alumina aerogels at different Etac contents |
为了分析氧化铝气凝胶的热稳定性以及在热处理过程发生的各种物理化学变化情况,对在n(ASB):n(H2O):n(EtOH):n(Etac):n(HAc)=1:3:30:0.15:0.1的比例条件下得到的高比表面积氧化铝气凝胶进行热重分析。
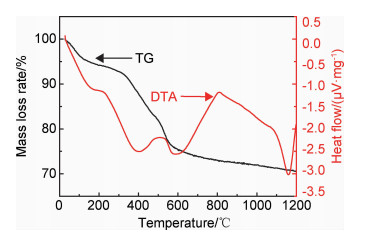
从热重-差热曲线(图 6)可以看出,Al2O3气凝胶从室温到1200℃存在两次比较明显的失重阶段,第一次失重是在≤100℃时,失重率为3.73 %,主要是气凝胶中物理吸附水以及少量醇溶剂的去除。第二次失重是在300~600℃之间,失重率为18.82%,主要是水合氧化铝中结构水的脱除,其反应式为:2AlOOH=Al2O3+H2O[20],由于H2O的排出,形成吸热反应,因此DTA曲线在该区域出现一个吸热峰。在800~1000℃时发生一系列的晶型转变而出现吸热峰,在1170℃时由于α-Al2O3的晶型转变而出现放热峰。随着温度升高至1200℃,氧化铝气凝胶中有机基团已完全分解,没有出现明显的失重和放热峰,表明Al2O3气凝胶在该温度范围内结构与形态不发生明显变化,具有良好的热稳定性。
|
图 6 氧化铝气凝胶的热重-差热曲线 Fig. 6 TG-DTA curves of alumina aerogels |
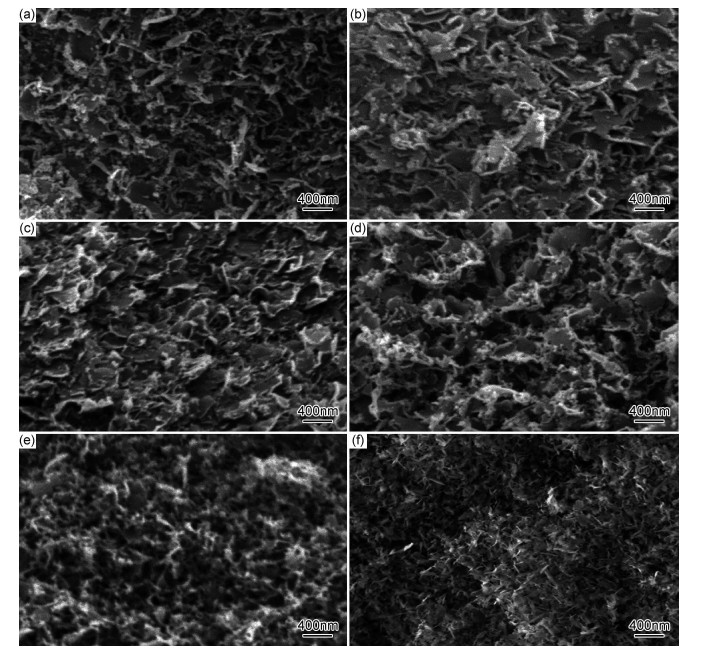
图 7为不同热处理温度下得到的Al2O3气凝胶的扫描电镜图,该Al2O3气凝胶具有叶片状颗粒堆积形成的纳米多孔网络结构,与以往球状颗粒形成的多孔结构不同,产生这种差异是由于仲丁醇铝与少量水反应主要形成勃姆石相,勃姆石单体通过氢键与其他单体连接起来形成层片状,随机堆积形成多孔结构的氧化铝气凝胶[13]。随着热处理温度的升高,其网络多孔结构进一步加强;叶片状厚度增加,相互连接后导致叶片状多孔结构减弱,但依旧保持良好的网络多孔结构,1200℃热处理后比表面积仍有153.45m2/g。
|
图 7 氧化铝气凝胶未热处理及在不同温度热处理2h后的SEM图 (a)未热处理;(b)400℃;(c)600℃;(d)800℃;(e)1000℃;(f)1200℃ Fig. 7 SEM images of alumina aerogels without heat treatment and treated at different temperatures for 2h (a)without heat treatment; (b)400℃; (c)600℃; (d)800℃; (e)1000℃ (f)1200℃ |
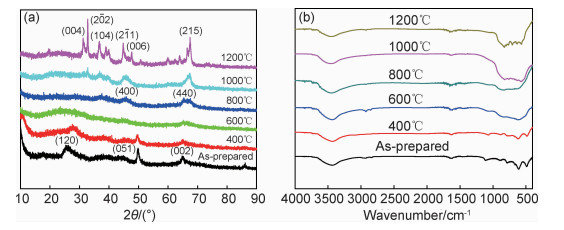
图 8(a)为不同热处理温度后气凝胶的X射线衍射图谱,由图可见,27°,50°和65°处的衍射峰对应于勃姆石结构,经400℃热处理后勃姆石结构慢慢分解,600℃热处理后几乎看不到勃姆石的晶型特征峰。800~1000℃在45°和67°处逐渐出现γ-Al2O3晶型的特征峰,其对应晶面指数分别是(400)和(440)。1000℃时γ-Al2O3开始转变为α-Al2O3,当达到1200℃时,氧化铝气凝胶则出现明显的α-Al2O3晶型的特征峰[21],说明在1200℃温度下转变成了稳定的α-Al2O3。
|
图 8 不同温度热处理后氧化铝气凝胶的XRD图谱(a)和红外光谱图(b) Fig. 8 XRD patterns (a) and FT-IR curves (b) of alumina aerogels after heat treatment at different temperatures |
由不同温度热处理后的氧化铝气凝胶的红外光谱图(图 8(b))可知,随着热处理温度的升高,波长在2951,2841,1466cm-1对应于C—H基团峰逐渐消失,说明氧化铝气凝胶结构上存在含碳的有机物残余,并随着温度的升高而分解。热处理温度从400℃升至1200℃,波长1109,896,781,609cm-1和495cm-1对应的AlO—H拟勃姆石峰[14]逐渐减弱,直至消失,说明随着温度的升高,氧化铝气凝胶晶型发生转变,勃姆石结构逐渐分解并消失,与XRD图谱分析的结果相同。
表 3为不同温度热处理后氧化铝气凝胶的孔结构信息。由表 3可知,随着热处理温度的升高,气凝胶的结构受到一定的破坏,胶粒之间发生团簇长大,颗粒平均大小从8nm增大至39nm,从而导致比表面积从744.52m2/g逐渐降低至153.45m2/g。1000, 1200℃热处理后比表面积分别为221.09, 153.45m2/g,相对于同类型的氧化铝气凝胶,该氧化铝气凝胶在热处理后保持更高的比表面积,周洁洁等[22]制备的氧化铝气凝胶在1000℃热处理后比表面积为174m2/g,高庆福等[13]制备的氧化铝气凝胶在1200℃热处理后比表面积为73m2/g。不同温度热处理后的气凝胶孔径主要分布在10~30nm之间,还是属于介孔范围,说明热处理后的氧化铝气凝胶中绝大部分的孔径都小于常温下空气的分子平均自由程(69nm[23]),因此在不同温度处理后的气凝胶也可以有效地抑制气态热传导和对流传热,从而达到保温绝热的效果[24]。
| Sample | Specific surface area/ (m2·g-1) |
Average pore size/ nm |
Average particle size/nm | Volume density/ (g·cm-3) |
| As-prepared | 744.52 | 12.76 | 8.05 | 0.078 |
| A-400 | 579.44 | 11.40 | 10.35 | 0.085 |
| A-600 | 461.75 | 12.02 | 12.99 | 0.089 |
| A-800 | 417.10 | 11.29 | 14.38 | 0.108 |
| A-1000 | 221.09 | 16.50 | 27.13 | 0.224 |
| A-1200 | 153.44 | 17.61 | 39.10 | 0.404 |
| Note: sample A-400 indicates that alumina aerogel sample was heat treated at 400℃ for 2 hours. | ||||
(1) 通过分步水解和添加螯合剂(乙酰乙酸乙酯)的方式,稳定铝醇盐的水解和缩聚过程,制备得到高比表面积、低密度的块状氧化铝气凝胶。螯合剂的引入对氧化铝气凝胶的结构影响很小。
(2) 采用此制备方法,实验所得最优物料配比为n(ASB):n(EtOH):n(Etac):n(H2O):n(HAc)=1:30:0.15:3:0.1,制备得到的氧化铝气凝胶比表面积高达744.52m2/g,在1200℃下热处理后仍有较高的比表面积153.45m2/g。氧化铝气凝胶密度可低至0.063g/cm3。
(3) 超临界制备出来的氧化铝气凝胶为多晶勃姆石相,由大量叶片状结构组成,经不同温度热处理后,叶片状多孔结构未发生明显变化,氧化铝气凝胶具有高温稳定性。
| [1] |
McHALE J M, AUROUX A, PERROTTA A J, et al. Surface energies and thermodynamic stability in nanocrystalline alumina[J]. Science, 1997, 277(5327): 788-791. DOI:10.1126/science.277.5327.788 |
| [2] |
KEYSAR S, SHTER G E, HAZAN Y D, et al. Heat treatment of alumina aerogels[J]. Chemistry of Materials, 1997, 9(11): 2464-2467. DOI:10.1021/cm970208s |
| [3] |
余煜玺, 马锐. SiC微/纳米纤维毡增强SiO2气凝胶复合材料的制备和表征[J]. 材料工程, 2018, 46(11): 45-50. YU Y X, MA R. Preparation and characterization of silicon carbide micro/nano fibrous mat reinforced silica aerogel composites[J]. Journal of Materials Engineering, 2018, 46(11): 45-50. DOI:10.11868/j.issn.1001-4381.2017.001493 |
| [4] |
刘洪丽, 邓青沂, 褚鹏. 超临界干燥制备PSNB气凝胶及其超疏水性能研究[J]. 材料工程, 2018, 46(2): 22-26. LIU H L, DENG Q Y, CHU P. Preparation and hydrophobic properties of polyborosilazane aerogels via CO2 supercritical drying[J]. Journal of Materials Engineering, 2018, 46(2): 22-26. DOI:10.3969/j.issn.1673-1433.2018.02.007 |
| [5] |
HIRASHIMA H, KOJIMA C, IMAI H. Application of alumina aerogels as catalysts[J]. Journal of Sol-Gel Science and Technology, 1997, 8(1/3): 843-846. |
| [6] |
ZU G, SHEN J, ZOU L, et al. Nanoengineering super heat-resistant, strong alumina aerogels[J]. Chemistry of Materials, 2013, 25(23): 4757-4764. DOI:10.1021/cm402900y |
| [7] |
YOLDAS B E. Hydrolysis of aluminium alkoxides and bayerite conversion[J]. Journal of Applied Chemistry & Biotechnology, 2007, 23(11): 803-809. |
| [8] |
YOLDAS B E. Alumina gels that form porous transparent Al2O3[J]. Journal of Materials Science, 1975, 10(11): 1856-1860. DOI:10.1007/BF00754473 |
| [9] |
YOLDAS B E, PARTLOW D P. Formation of mullite and other alumina-based ceramics via hydrolytic polycondensation of alkoxides and resultant ultra-and microstructural effects[J]. Journal of Materials Science, 1988, 23(5): 1895-1900. DOI:10.1007/BF01115736 |
| [10] |
何飞, 赫晓东, 李垚. 无机盐和有机醇盐制备Al2O3干凝胶[J]. 硅酸盐学报, 2006, 34(9): 1093-1097. HE F, HE X D, LI Y. Al2O3 xerogels synthesized by inorganic salt and organic alkoxide[J]. Journal of the Chinese Ceramic Society, 2006, 34(9): 1093-1097. DOI:10.3321/j.issn:0454-5648.2006.09.014 |
| [11] |
JANOSOVITS U, ZIEGLER G, SCHARF U, et al. Structural characterization of intermediate species during synthesis of Al2O3 aerogels[J]. Journal of Non-Crystalline Solids, 1997, 210(1): 1-13. DOI:10.1016/S0022-3093(96)00573-X |
| [12] |
POCO J F, SATCHER JR J H, HRUBESH L W. Synthesis of high porosity monolithic alumina aerogels[J]. Journal of Non-Crystalline Solids, 2001, 285(1/3): 57-63. |
| [13] |
高庆福, 张长瑞, 冯坚, 等. 低密度、块状氧化铝气凝胶制备[J]. 无机化学学报, 2008, 24(9): 1456-1460. GAO Q F, ZHANG C R, FENG J, et al. Preparation of low density monolithic alumina aerogels[J]. Chinese Journal of Inorganic Chemistry, 2008, 24(9): 1456-1460. DOI:10.3321/j.issn:1001-4861.2008.09.016 |
| [14] |
ZU G, SHEN J, WEI X, et al. Preparation and characterization of monolithic alumina aerogels[J]. Journal of Non-Crystalline Solids, 2011, 357(15): 2903-2906. DOI:10.1016/j.jnoncrysol.2011.03.031 |
| [15] |
HIMMEL B, GERBER T, BURGER H, et al. Structural characterization of SiO2-Al2O3 aerogels[J]. Journal of Non-Crystalline Solids, 1995, 185(1/2): 56-66. |
| [16] |
HEGDE N D, RAO A V. Physical properties of methy-ltrimethoxysilane based elastic silica aerogels prepared by the two-stage sol-gel process[J]. Journal of Materials Science, 2007, 42(16): 6965-6971. DOI:10.1007/s10853-006-1409-5 |
| [17] |
HEGDE N D, RAO A V. Effect of processing temperature on gelation and physical properties of low density TEOS based silica aerogels[J]. Journal of Sol-Gel Science and Technology, 2006, 38(1): 55-61. DOI:10.1007/s10971-006-5348-z |
| [18] |
XU L, JIANG Y G, FENG J Z, et al. Influence of ethyl acetoacetate on the structure and thermal stability of alumina aerogel[J]. Materials Science Forum, 2015, 816: 157-162. DOI:10.4028/www.scientific.net/MSF.816.157 |
| [19] |
SING K S W. Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity (recommendations 1984)[J]. Pure & Applied Chemistry, 1985, 57(4): 603-619. |
| [20] |
WANG J A, BOKHIMI X, MORALES A, et al. Aluminum local environment and defects in the crystalline structure of sol-gel alumina catalyst[J]. The Journal of Physical Chemistry B, 1999, 103(2): 299-303. DOI:10.1021/jp983130r |
| [21] |
BODAGHI M, MIRHABIBI A R, ZOLFONUN H, et al. Investigation of phase transition of γ-alumina to α-alumina via mechanical milling method[J]. Phase Transitions, 2008, 81(6): 571-580. DOI:10.1080/01411590802008012 |
| [22] |
周洁洁, 陈晓红, 胡子君, 等. 热处理对块状氧化铝气凝胶微观结构的影响[J]. 宇航材料工艺, 2010, 40(2): 51-54. ZHOU J J, CHEN X H, HU Z J, et al. Effect of heat treatment on microstructure of monolithic alumina aerogels[J]. Aerospace Materials and Technology, 2010, 40(2): 51-54. DOI:10.3969/j.issn.1007-2330.2010.02.014 |
| [23] |
余煜玺, 朱孟伟. 高球形度、高比表面积SiO2/TiO2气凝胶小球的制备和表征[J]. 材料工程, 2017, 45(2): 7-11. YU Y X, ZHU M W. Preparation and characterization of highly spherical silica-titania aerogel beads with high surface area[J]. Journal of Materials Engineering, 2017, 45(2): 7-11. DOI:10.3969/j.issn.1673-1433.2017.02.003 |
| [24] |
段远源, 林杰, 王晓东, 等. 二氧化硅气凝胶的气相热导率模型分析[J]. 化工学报, 2012, 63(增刊1): 54-58. DUAN Y Y, LIN J, WANG X D, et al. Analysis of gaseous thermal conductivity models of silica aerogels[J]. Journal of Chemical Industry and Engineering, 2012, 63(Suppl 1): 54-58. |
 2019, Vol. 47
2019, Vol. 47


