文章信息
- 舒华金, 吴春萱, 杨康, 刘廷武, 李晨, 曹传亮
- SHU Hua-jin, WU Chun-xuan, YANG Kang, LIU Ting-wu, LI Chen, CAO Chuan-liang
- 快速膨胀海藻酸钠/二氧化硅纤维复合支架的制备及其快速止血功能的应用
- Preparation of rapid expansion alginate/silica fiber composite scaffold and application of rapid hemostatic function
- 材料工程, 2019, 47(12): 124-129
- Journal of Materials Engineering, 2019, 47(12): 124-129.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000699
-
文章历史
- 收稿日期: 2019-07-26
- 修订日期: 2019-10-15
2. 南昌大学第二临床医学院, 南昌 330006;
3. 南昌大学 药学院, 南昌 330031;
4. 南昌大学第二附属医院, 南昌 330006;
5. 南昌大学 机电工程学院, 南昌 330031
2. The Second Clinical Medical School, Nanchang University, Nanchang 330006, China;
3. College of Pharmacy, Nanchang University, Nanchang 330031, China;
4. The Second Affiliated Hospital of Nanchang University, Nanchang 330006, China;
5. School of Mechanical and Electronic Engineering, Nanchang University, Nanchang 330031, China
在交通事故、坠楼、医院手术和战场等情况下,失血过多是导致死亡最为主要的原因,因此迅速而高效地止血能够挽救无数人的生命[1-2]。人体凝血过程分为两步:初级止血过程和凝血级联反应过程,其中凝血级联反应过程主要是将血液转化为纤维蛋白,从而实现止血。因此,止血是早期伤口愈合的第一步,具有非常重要的意义。然而,在没有止血装置和药剂的帮助下,尤其是在紧急情况下,靠自身凝血作用并不能实现及时止血。在过去的几十年里,最为常用的止血方式是传统的止血绷带和纱布,这些止血材料在表浅伤口和低出血量的伤口中表现出了一定的优势,但面对深部创口,传统止血材料由于难以触及和较低的吸水性往往难以起效。针对这种情况,已开发出一些可填充在深部出血点并引发凝血过程的沸石[3-4]、止血粉[5-6]、胶原蛋白[7-8]和壳聚糖海绵[9-10]等。但是面对大出血时,沸石不仅容易进入毛细血管导致血栓形成,并且它们还具有吸水性和产热的倾向,会对皮肤产生伤害;止血粉表现出弱的黏附性,容易被血液带走;激发凝血过程的胶原或壳聚糖止血海绵在面对出血时往往需要一定时间来募集纤维蛋白和凝血因子,而且这种有机大分子物质通常表现出强的免疫排斥反应。因此,临床上亟须开发新型生物相容性好且具有快速止血能力的海绵支架材料[11]。
静电纺丝是制备多孔支架的一种绿色和常用的方法[12-13],采用静电纺丝法制备二氧化硅纳米纤维支架因其优异的生物相容性和有利于细胞生长等特点被广泛报道,但该方法制备的二氧化硅纳米纤维丝脆性较大,不能具备良好膨胀性能,限制了其应用于止血海绵支架。海藻酸盐敷料是一种已经被广泛用于伤口愈合[14]、伤口止血[9]的支架材料,表现出优异的生物相容性和止血凝血性能,但是纯海藻酸钠敷料没有坚韧的骨架作为支撑,强度低,仍未能应用于深部大伤口止血。近年,丁斌教授团队报道了利用静电纺丝技术与梯度冷冻法来制备高度多孔性支架的文章,具有孔率高、质量轻、韧性大等优势,但并未研究其膨胀性及快速止血海绵的应用[15]。
本研究开发出一种具有高亲水性和膨胀性,良好生物相容性的二氧化硅纳米纤维,并使用海藻酸钠(ALG)包覆在纳米纤维上,以提高快速膨胀性能及促凝效果,对海藻酸钠/二氧化硅纤维复合三维支架(ALG/SiO2止血海绵)的形貌和结构进行了表征。为制备出一种具有高膨胀性能快速止血性的复合伤口敷料,关键点是优化合成材料的配方,因此,本课题组将制备得到的ALG/SiO2止血海绵进行了钙离子交联,最终得到钙离子交联的海藻酸盐包裹纳米SiO2纤维的止血海绵(ALG/SiO2/Ca2+止血海绵),而后对海绵的膨胀性及细胞毒性进行了研究,并采用兔股动脉出血实验评估了该止血海绵的深部止血性能。
1 实验材料与方法 1.1 试剂正硅酸乙酯(TEOS)、聚乙烯醇(PVA)、磷酸、海藻酸钠(ALG)、氯化钙、氯化钠、淀粉和葡萄糖均购自上海麦克林生物化学有限公司。胰酶和培养基(1640)购自北京索普迪奥科技有限公司。
1.2 止血海绵的制备将10.7mL的正硅酸乙酯(TEOS)与0.042mL的磷酸溶液和10mL的超纯水混合,在室温下搅拌反应12h后加入20mL 10%(质量分数,下同)的聚乙烯醇(PVA)溶液,进一步搅拌12h,室温陈化,制得纺丝液。然后在纺丝电压为25kV和流速为1mL/h的条件下通过自制的静电纺丝装置进行静电纺丝,得到PVA/TEOS纳米纤维,将其在800℃下进行煅烧,制备出纯的SiO2纳米纤维。将0.9g的SiO2纳米纤维添加到300mL 1.5%的海藻酸钠溶液中,并在12000r/min的转速下高速剪切30min,将所得的分散体在干冰/丙酮浴中梯度冻结后,冷冻干燥12h获得海藻酸纳包裹SiO2纤维支架(也即ALG/SiO2止血海绵)。最后将ALG/SiO2止血海绵浸泡在0.3mol/L CaCl2溶液中10min,取出后冷冻干燥48h,最终得到ALG/SiO2/Ca2+止血海绵。
1.3 材料的表征利用SU8000型扫描电子显微镜对制备的SiO2纳米纤维、经海藻酸钠和氯化钙交联后的海绵进行表征,并通过EDS对所得纤维和海绵的元素含量与分布进行测定。设计了海绵的吸水膨胀实验,将海绵在水中压缩,其中V1为浸入水后海绵的体积,V0为海绵的原始体积。体积膨胀率(%)=V1/V0×100%。
1.4 细胞毒性实验采用CCK-8法评估材料的细胞毒性。在37℃ SPX-250型培养箱中用无血清细胞培养基浸泡24h,得到ALG/SiO2/Ca2+止血海绵浸提液。从培养箱中取出已经培养到一定细胞密度的L929细胞培养瓶,以每孔3×103 Cells/L的浓度接种L929细胞到96孔板后,震荡混匀并放入培养箱中,在培养箱中培养24h后,每孔加入100μL PBS洗涤细胞及100μL不同浓度的浸提液,放入培养箱中继续培养。每两天更换一次培养基,在第1天,第3天,第7天提前2h加入10μL CCK-8试剂,最后用酶标仪(吸光度:450nm)测其OD值。
1.5 死活细胞染色从培养箱中取出已经培养到一定细胞密度的L929细胞培养瓶,以每孔4×103 Cells/L的浓度接种L929细胞到24孔板后,震荡混匀并放入培养箱中,在培养箱中培养24h后,每孔加入100μL PBS洗涤细胞,再加入100μL不同浓度的浸提液,放入培养箱中继续培养。分别在培养的第1天,第3天,第7天时加入死活细胞染液,然后放入37℃培养箱孵育30min,最后在荧光显微镜下观察。
1.6 体内止血实验选取6只新西兰大白兔(南昌大学动物中心),分为ALG/SiO2/Ca2+止血海绵组和加压纱布组,每组3只。手术中在左侧股三角区域腹股沟内1/3与外2/3交点处摸到股动脉,触及股动脉搏动后,沿动脉行走方向做长约2cm的切口,游离股动脉,剪断。然后立即将止血材料压进创口内部,并记录相应时刻止血效果图片。
2 结果与分析 2.1 SiO2纤维和ALG/SiO2/Ca2+海绵的微观结构分析图 1(a)是SiO2纳米纤维的扫描电子显微镜照片,显示了平均直径约为200nm均匀分布的SiO2纳米纤维,说明煅烧后的纳米纤维表面较光滑,粗细较均匀。在SiO2纳米纤维的静电纺丝过程中可以通过控制电压、PVA含量、流速和电导率得到不同直径的纳米纤维,在以往的研究中表明,提高电压、增大电导率、降低流速和减小黏度可以减小纳米纤维直径,增大电导率可以提高纳米纤维的孔隙率。图 1(b)是ALG/SiO2/Ca2+海绵的扫描电子显微镜照片,表明ALG/SiO2/Ca2+海绵具有高度疏松的多孔结构,有利于海绵的止血。由图 1可知ALG/SiO2/Ca2+海绵的离子交联过程并没有破坏支架的多孔结构,虽然观察到在海绵的制备过程中部分二氧化硅纳米纤维发生了断裂,但互相交联的海藻酸钠弥补了断裂的二氧化硅之间的连接。ALG/SiO2/Ca2+海绵的这种疏松的蜂窝状多孔结构用做止血海绵在快速止血方面是非常重要的,可以迅速吸收大量的伤口分泌物,从而使伤口处的血浆浓度增加,除此之外,高度亲水性的多孔结构还可以使伤口处保持湿润状态,有利于伤口的愈合。

|
图 1 SiO2纳米纤维(a)和ALG/SiO2/Ca2+海绵(b)的SEM图 Fig. 1 SEM images of SiO2 nanofiber (a) and ALG/SiO2/Ca2+ sponge (b) |
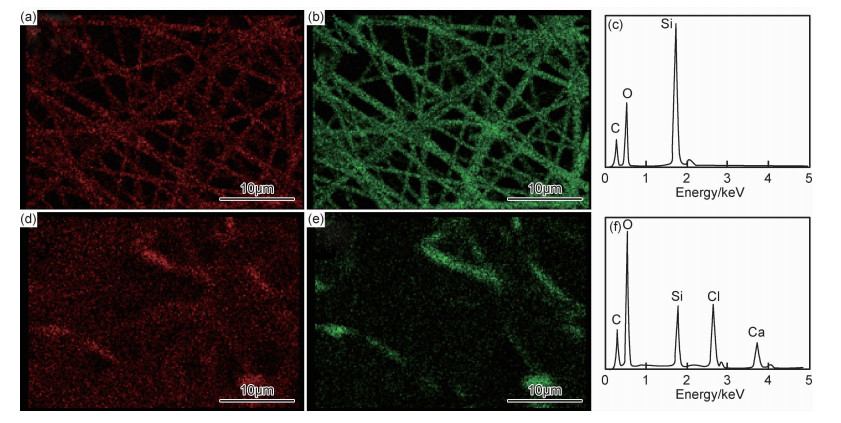
图 2是SiO2纳米纤维支架和ALG/SiO2/Ca2+复合支架的面扫描图和元素全分析能谱图,结果显示支架均以SiO2纳米纤维为主要骨架,其中SiO2纳米纤维支架O和Si元素分布完全相同,且与扫描电镜的形貌吻合,说明支架为纯的SiO2纳米纤维,元素全分析显示除了O和Si的峰外,仅有少量的C元素,进一步证实了支架为SiO2纳米纤维支架。ALG/SiO2/Ca2+海绵的元素分析光谱(图 2(f))显示O和Si元素分布也基本一致,说明了海藻酸钠均匀地包裹在SiO2纳米纤维表面,元素分析发现了C,O,Si,Cl和Ca的峰值,可推知Ca2+交联剂成功地被负载到ALG/SiO2/Ca2+止血海绵上。
|
图 2 SiO2纳米纤维(a), (b), (c)和ALG/SiO2/Ca2+海绵(d), (e), (f)的能量色散X射线图谱 Fig. 2 EDX images of SiO2 nanofiber (a), (b), (c) and ALG/SiO2/Ca2+ sponge (d), (e), (f) |
在深部止血过程中,海绵的吸水膨胀是海绵激发的一系列物理-生化止血过程的第一步,即通过膨胀带来的压力压迫血管,达到初步止血目的。因此,海绵的吸水膨胀特性对实现其止血功能具有重要意义。ALG/SiO2/Ca2+海绵的溶胀性能测试实验结果如图 3所示。图 3(a)直观展示了海绵的快速溶胀性,将压缩后的ALG/SiO2/Ca2+海绵支架,加入水后10s内完成膨胀过程,体积增大到原来的219%。尽管其溶胀的倍数仍有待进一步提升,但其溶胀速率非常快,10s内达到最大膨胀倍数,这对于快速止血与挽救生命来说是一个相当重要的指标。因为支架的快速膨胀性会对独立的出血血管产生一个瞬时压迫力,另外支架的高溶胀性也可以用于从血清中有效地吸收水分以浓聚凝血因子和红细胞以阻止血液的流出,从而在短时间内对伤口起到封闭作用以减少出血量。

|
图 3 ALG/SiO2/Ca2+海绵的溶胀性能测试结果 (a)体积膨胀示意图;(b)体积膨胀率随时间关系曲线 Fig. 3 Results of water absorption expansion test of ALG/ SiO2/Ca2+ sponge (a)schematic diagram of volume expansion; (b)curve of volume expansion ratio versus time |
生物医学材料首先的要求就是其对人体无毒害作用[16]。采用CCK-8法和死活细胞染色来测试ALG/SiO2/Ca2+海绵对L929细胞增殖的影响,结果见图 4。图 4(a)是ALG/SiO2/Ca2+海绵的细胞毒性测试结果,由图可知吸光度值之间没有显著的差异。如图 4(b)所示,在第1, 3, 7天,细胞的数量逐渐增多并且ALG/SiO2/Ca2+海绵的浸提液并没有对细胞产生任何的负面作用,说明ALG/SiO2/Ca2+海绵没有生物毒性,并且具有较好的细胞相容性。

|
图 4 ALG/SiO2/Ca2+海绵的细胞实验结果 (a)海绵浸提液对细胞增殖的影响;(b)海绵的死活细胞染色荧光显微镜图(control表示用细胞培养基(DMEM)培养的细胞作为对照组) Fig. 4 Cell experiment results of ALG/SiO2/Ca2+sponge (a)effect of sponge extract on cell proliferation; (b)fluorescence microscopy image of live/dead cell staining of ALG/SiO2/Ca2+ sponge (control indicates that cells cultured with cell culture medium (DMEM) is served as a control group) |
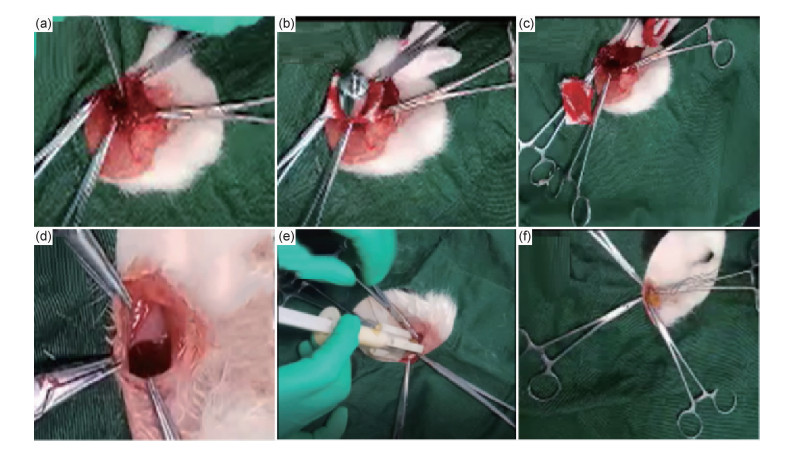
为了进一步贴近实际中可能的情况,如图 5所示,本课题组设计了家兔股动脉出血实验以模仿实际情况中可能出现的大出血。手术中在左侧股三角区域腹股沟内1/3与外2/3交点处摸到股动脉,触及股动脉搏动后,沿动脉行走方向做长约2cm的切口,游离股动脉,剪断。之后立即使用ALG/SiO2/Ca2+海绵进行止血,对照组采用传统的医用纱布进行止血,每组3只,以降低实验误差。实验组使用止血海绵的止血效果如图 5(d)~(f)所示,出血均可在10s内被遏制。然而,当用加压纱布法进行常规止血时(如图 5(a)~(c)所示),无法有效止血,出血时间超过120s。ALG/SiO2/Ca2+海绵之所以可以快速止血,是因为ALG/SiO2/Ca2+海绵能迅速从血液中吸收大量水分并且膨胀可以对出血血管产生一个瞬时压迫力从而防止血液外流。同时,溶胀的海绵可在短时间内封闭伤口,以减少出血量并降低感染风险。因此,ALG/SiO2/Ca2+海绵的溶胀膨胀特性对目前的止血支架具有重要意义。
|
图 5 加压纱布及ALG/SiO2/Ca2+海绵的体内止血实验 (a)构建加压纱布组的伤口模型;(b)加压纱布法止血(第10s);(c)加压纱布法止血(第120s);(d)构建ALG/SiO2/Ca2+海绵组的伤口模型;(e)ALG/SiO2/Ca2+海绵止血(第2s);(f)ALG/SiO2/Ca2+海绵组止血(第10s) Fig. 5 In vivo hemostasis experiment of ALG/SiO2/Ca2+ sponge (a)construct a wound model of a pressurized medical gauze group; (b)hemostatic result of pressurized medical gauze method (10th second); (c)hemostatic results of pressurized medical gauze method (120 seconds); (d)construct a wound model of a ALG/SiO2/Ca2+sponge; (e)hemostatic result of ALG/SiO2/Ca2+sponge (2nd second); (f)hemostatic result of a ALG/SiO2/Ca2+sponge (10th second) |
(1) 采用静电纺丝工艺加高温煅烧得到二氧化硅纳米纤维,并以它为骨架表面附着海藻酸钠,然后用钙离子交联,通过冷冻干燥技术,最终得到结构疏松多孔的ALG/SiO2/Ca2+海绵。
(2) ALG/SiO2/Ca2+海绵吸水膨胀性好,能在10s内达到最大体积,且具有良好的生物相容性,在深部创口中能迅速吸水膨胀,压迫血管,封闭伤口,促进血液的快速凝结,相比传统纱布止血效果明显。
(3) 基于ALG/SiO2/Ca2+海绵良好的止血效果,设想结合细胞种植或添加其他活性物质如各种生长因子等,可以进一步拓展其应用范围,为以后寻找新型止血敷料提供了新的思路。
| [1] |
李丽娟, 邢克飞, 刁天喜. 美军止血材料研究进展[J]. 中华创伤杂志, 2018, 34(3): 242-245. LI L J, XING K F, XI T X. Research progress in hemorrhage control products of U.S.army[J]. Chinese Journal of Trauma, 2018, 34(3): 242-245. |
| [2] |
BEHRENS A M, SIKORSKI M J, KOFINAS P. Hemostatic strategies for traumatic and surgical bleeding[J]. Journal of Biomedical Materials Research Part A, 2014, 102(11): 4182-4194. |
| [3] |
YU L S, SHANG X Q, CHEN H, et al. A tightly-bonded and flexible mesoporous zeolite-cotton hybrid hemostat[J]. Nature Communications, 2019(10): 1932. |
| [4] |
毕宏达, 李学拥, 王玉, 等. 沸石对猪致命性血管损伤模型的止血作用[J]. 西北国防医学杂志, 2006, 27(3): 164-166. BI H D, LI X Y, WANG Y, et al. Hemostatic effects of zeolite in a lethal vascular injury model in swine[J]. Medical Journal of National Defending Forces in Northwest China, 2006, 27(3): 164-166. |
| [5] |
XI C Y, ZHU L G, ZHUANG Y, et al. Experimental evaluation of tranexamic acid-loaded porous starch as a hemostatic powder[J]. Clinical and Applied Thrombosis/Hemostasis, 2017, 24(2): 279-286. |
| [6] |
杜宝堂, 李英俊, 史跃, 等. 微孔真空多聚糖止血粉有效性及安全性实验[J]. 医疗卫生装备, 2018, 39(9): 20-23. DU B T, LI Y J, SHI Y, et al. Effectiveness and biological safety of microporous vacuum polysaccharide hemostatic microspheres[J]. Chinese Medical Equipment Journal, 2018, 39(9): 20-23. |
| [7] |
SHEN W L, CHEN X, HU Y J, et al. Long-term effects of knitted silk-collagen sponge scaffold on anterior cruciate ligament reconstruction and osteoarthritis prevention[J]. Biomaterials, 2014, 35(28): 8154-8163. |
| [8] |
何越, 侯增淼, 李晓颖, 等. 重组胶原蛋白海绵的制备及性状表征[J]. 中国组织工程研究, 2019, 23(6): 912-916. HE Y, HOU Z M, LI X Y, et al. Preparation and properties of recombinant collagen sponge[J]. Chinese Journal of Tissue Engineering Research, 2019, 23(6): 912-916. |
| [9] |
WANG C, LUO W F, LI P W, et al. Preparation and evaluation of chitosan/alginate porous microspheres/bletilla striata polysaccharide composite hemostatic sponges[J]. Carbohydrate Polymers, 2017, 174: 432-442. |
| [10] |
邹圣灿, 林莎莎, 王宝群, 等. 壳聚糖止血海绵的制备及其性能[J]. 纺织导报, 2019(3): 74-77. ZOU S C, LIN S S, WANG B Q, et al. Preparation and properties of chitosan hemostatic sponges[J]. China Textile Leader, 2019(3): 74-77. |
| [11] |
汪向飞, 张晓丹, 周汉新. 生物医用可吸收止血材料的研究与临床应用[J]. 中国组织工程研究与临床康复, 2010, 14(21): 3973-3976. WANG X F, ZHANG X D, ZHOU H X. Research and clinical application of biomedical absorbable hemostatic materials[J]. Journal of Clinical Behabilitative Tissue Engineering Research, 2010, 14(21): 3973-3976. |
| [12] |
龚文正, 周晶晶, 阮诗伦, 等. 静电纺丝与静电喷雾技术共纺制备PPESK/PVDF复合锂电池隔膜[J]. 材料工程, 2018, 46(3): 1-6. GONG W Z, ZHOU J J, RUAN S L, et al. PPESK/PVDF lithium-ion battery composite separators fabricated by combination of electrospinning and electrospraying techniques[J]. Journal of Materials Engineering, 2018, 46(3): 1-6. |
| [13] |
龚文正, 常保宁, 阮诗伦, 等. 静电纺丝聚芳醚砜酮纤维膜穿刺强度研究[J]. 材料工程, 2019, 47(4): 32-38. GONG W Z, CHANG B N, RUAN S L, et al. Puncture strength research of electrospun PPESK fibrous membrane[J]. Journal of Materials Engineering, 2019, 47(4): 32-38. |
| [14] |
LIU X, NIELSEN L H, KŁODZIŃSKA S N, et al. Ciprofloxacin-loaded sodium alginate/poly (lactic-co-glycolic acid) electrospun fibrous mats for wound healing[J]. European Journal of Pharmaceutics and Biopharmaceutics, 2018, 123: 42-49. |
| [15] |
SI Y, WANG L H, WANG X Q, et al. Ultrahigh-water-content, superelastic, and shape-memory nanofiber-assembled hydrogels exhibiting pressure-responsive conductivity[J]. Adv Mater, 2017, 29: 1700339. |
| [16] |
马凤森, 喻炎, 章捷, 等. 生物材料细胞毒性评价研究进展[J]. 材料导报, 2018, 32(1): 76-85. MA F S, YU Y, ZHANG J, et al. A state-of-the-art review of cytotoxicity evaluation of biomaterials[J]. Materials Review, 2018, 32(1): 76-85. |
 2019, Vol. 47
2019, Vol. 47


