文章信息
- 郭莉, 张开来, 张鑫, 赵芳丽, 赵强, 杨晓, 王丹军, 付峰
- GUO Li, ZHANG Kai-lai, ZHANG Xin, ZHAO Fang-li, ZHAO Qiang, YANG Xiao, WANG Dan-jun, FU Feng
- g-C3N4量子点修饰球形Bi2WO6及其光催化活性增强机制
- g-C3N4 quantum dots decorated spherical Bi2WO6 photocatalyst and its enhanced photocatalytic activities mechanism
- 材料工程, 2019, 47(11): 128-134
- Journal of Materials Engineering, 2019, 47(11): 128-134.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2018.000459
-
文章历史
- 收稿日期: 2018-04-24
- 修订日期: 2019-06-20
2. 陕西省化学反应工程重点实验室, 陕西 延安 716000
2. Key Laboratory of Chemical Reaction Engineering of Shaanxi Province, Yan'an 716000, Shaanxi, China
自从1972年Fujishima等[1]首次报道了TiO2的光催化活性以来,半导体光催化在环境污染治理方面的应用引起了全世界范围的广泛关注[2]。然而,传统TiO2基催化材料只能在紫外光下被激发,限制了半导体催化技术的实际应用。因此,寻找高效的催化剂成为研究的一个热点。Bi2WO6作为一种结构最为简单的Aurivillius型氧化物,禁带宽度为2.7eV,可以吸收可见光而被激发,具有可见光响应活性。然而,Bi2WO6可见光利用率不高、光生电子-空穴对易于复合,限制了它在光催化方面的应用[3-9]。为了提高Bi2WO6基催化材料的活性,一方面,减小禁带宽度可以拓宽光谱响应范围[10-12];另一方面,通过掺杂使导带更负,价带更正,在热力学上有利于光催化反应体系中的氧化还原反应。然而,这两方面又是相互矛盾的,对于单组分Bi2WO6基催化材料而言,不可能同时满足上述两方面。
近年来,人们受自然界植物光合作用的启发而设计构筑的Z-型结构催化材料,可以同时满足上述两点要求。Z-型光催化材料包括含导电介质的离子型和固态型两大类,其中,无导电介质的固态型具有独特的能带结构和电荷传输方式,使得电子和空穴在空间上高度分离,表现出强氧化还原性。从原理上看,构筑无导电介质固态型Z-型光催化体系的关键是光催化体系Ⅰ(photocatalysis system Ⅰ, PSⅠ)和光催化体系Ⅱ(photocatalysis system Ⅱ, PSⅡ)的能带结构要匹配,PSⅡ的导带电势要与PSⅠ的价带电势低,且与PSⅠ的价带点势接近。光照条件下,PSⅠ和PSⅡ的电子分别被激发至导带上,而在价带上留下空穴。PSⅡ导带上的激发电子(eCB)与PSⅠ的价带空穴(hVB+)复合,这样的体系表现出PSⅠ导带的还原能力(PSⅠ-eCB)和PSⅡ的氧化能力(PSⅠ-hVB+)。
因此,从Z-型催化体系的结构特征出发,构筑新颖的Bi2WO6基Z-型催化材料成为提高Bi2WO6基催化材料催化活性的重要手段。类石墨结构氮化碳(g-C3N4)是一种窄带隙(Eg=2.7eV)层状结构半导体,具有一定的可见光响应活性[13-16]。Gui等[17]将Bi2WO6颗粒植入g-C3N4的层状结构中,提高了g-C3N4的催化活性。然而,催化剂的比表面积较小,所得复合不利于催化活性的提高。本课题组采用水热法制备了多孔分解结构的三维Bi2WO6,并采用贵金属沉积、元素掺杂、半导体表面修饰等方法,有效提高了Bi2WO6的催化活性[18-20]。本工作采用浸渍法将g-C3N4量子点沉积在三维结构的Bi2WO6表面,获得g-C3N4/Bi2WO6(简写为CN/BWO)异质结。以偶氮成分染料亚甲基蓝(MB)和对硝基苯酚(p-NPh)为模型污染物,考察g-C3N4量子点表面修饰对Bi2WO6光催化活性的影响,并对其活性增强机理进行了讨论。
1 实验材料与方法 1.1 试剂硝酸铋(Bi(NO3)3·5H2O,分析纯),钨酸钠(Na2WO4,分析纯),三聚氰胺(C3N3H3,分析纯),购于阿拉丁化学试剂有限公司;亚甲基蓝(C16H18ClN3S,分析纯),对硝基苯酚(C6H5NO3,分析纯)购于百灵威化学试剂公司,均为分析纯。实验用水为实验室自制Ⅰ级蒸馏水。
1.2 样品的制备Bi2WO6的制备:称取0.97014g的Bi(NO3)3·5H2O,溶于2.5mL浓度为4mol/L的HNO3溶液中,室温高速磁力搅拌至固体溶解;称取0.3299g的Na2WO4溶于20mL水中,然后将其逐滴加入上述Bi(NO3)3溶液中,继续搅拌1h,停止搅拌后将此混合溶液转入50mL水热反应釜中,密封放入电热恒温鼓风干燥箱中,在180℃水热反应4h。反应结束后,自然冷却至室温,将所得沉淀经水洗、醇洗、干燥,得到纯Bi2WO6。
g-C3N4/Bi2WO6的制备:称取5g三聚氰胺于马弗炉中,550℃下焙烧4h,得到g-C3N4,称重计算产率约为20%。将1.000g的三聚氰胺加入甲醇中,室温下用高速磁力搅拌器搅拌12h,然后加入一定计量比的Bi2WO6粉末,继续磁力搅拌6h,将混合物转入恒温干燥箱中70℃恒温至甲醇挥发完全,将得到的固体粉末移入马弗炉中550℃下焙烧4h,研磨得到γg-C3N4/Bi2WO6系列复合催化剂,其中γ为g-C3N4的沉积量(γ的质量分数分别为5%,10%,15%,20%,25%,30%)。
1.3 样品的表征样品的物相结构采用XRD-7000型全自动X射线粉末衍射仪(XRD)表征,CuKα(Ni滤玻片滤波,λ=0.15418nm),管电压40kV,管电流30mA,步长0.02°,扫描范围2θ=20°~80°,扫描速率1(°)·min-1;样品的形貌在JEOL-6701型场发射扫描电子显微镜(FE-SEM)上观察;透射电镜(TEM)图谱在JEM-2100型透射电镜上测试,加速电压200kV; 比表面积和孔径测试在V-Sorb2800P全自动比表面-孔径测试仪上进行;粉体UV-Vis吸收光谱(UV-Vis-DRS)采用UV-2550型紫外-可见分光光度计测定,扫描范围200~800nm, 标准BaSO4为参比。
1.4 光催化活性评价使用XPA系列光催化仪进行样品催化活性评价,光源为300W金卤灯,用滤光片过滤掉420nm以下的光。反应器中加入200mg催化剂、200mL浓度为10mg·L-1的亚甲基蓝(MB)或者对硝基苯酚(p-NPh)溶液,充分搅拌30min,达到吸附/脱附平衡后启动金卤灯进行光照,间隔10min取样离心分离出催化剂,取上清液测定紫外-可见吸收光谱在亚甲基蓝和对硝基苯酚最大吸收波长处的吸光度A,采用光度法确定浓度,以此评价催化剂的催化活性。
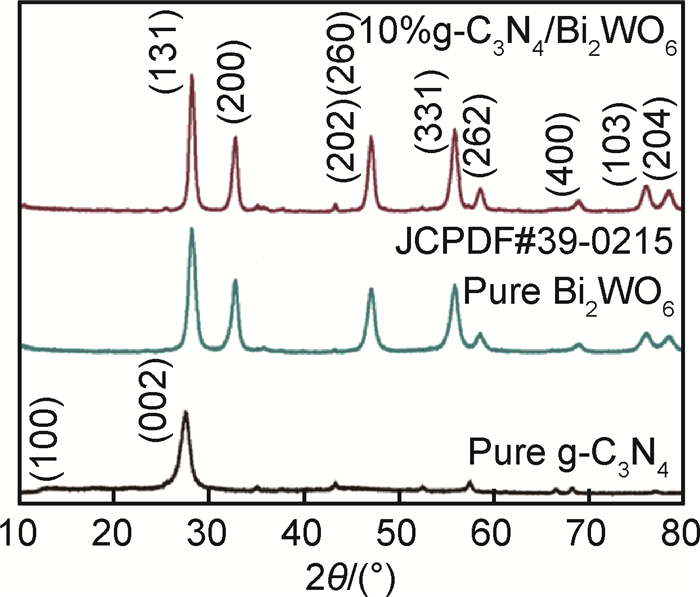
2 结果与讨论 2.1 样品的表征图 1为Bi2WO6, g-C3N4和10%g-C3N4/Bi2WO6的XRD谱图。可以看出,特征衍射峰较为尖锐,结晶度好,且各衍射峰位置与标准卡片完全吻合,没有出现任何杂质相,表明所得样品为纯正交晶系Bi2WO6[3-5]。还可以看出,纯g-C3N4在13.04°和27.47°处有明显的峰值,分别对应于平面结构和芳香结构的堆叠[14-15]。10%g-C3N4/Bi2WO6催化剂的衍射峰与纯Bi2WO6的衍射峰类似,而g-C3N4的衍射峰较弱,这是由于g-C3N4的含量较低所致。图 2是180℃水热反应4h所得Bi2WO6的FE-SEM照片和孔径分布。由图 2(a),(b)可以看出,纯Bi2WO6具有三维分级球形结构,半径约为5μm。由高分辨FE-SEM照片可以清晰看出,Bi2WO6微球是由厚度为20~30nm的纳米片组装而成。图 2(c)为纯Bi2WO6的氮气吸附-脱附和孔径分布曲线,可以看出,Bi2WO6孔径主要在10nm左右。此外,Bi2WO6在30~100nm范围内也出现孔径分布峰,这可能是由Bi2WO6纳米片相互交错形成的大孔所致。表明,在Bi2WO6的片层结构上有介孔存在,而在微球的表面上则有大孔存在。
|
图 1 Bi2WO6, g-C3N4和10%g-C3N4/Bi2WO6的XRD谱图 Fig. 1 XRD patterns of pure Bi2WO6, pure g-C3N4and 10%g-C3N4/Bi2WO6 |

|
图 2 Bi2WO6的FE-SEM照片(a), (b), 氮气吸附-脱附等温线以及BJH孔径分布曲线(c) Fig. 2 FE-SEM images(a), (b), nitrogen adsorption/desorption isotherms and BJH pore size distribution(c) of Bi2WO6 |
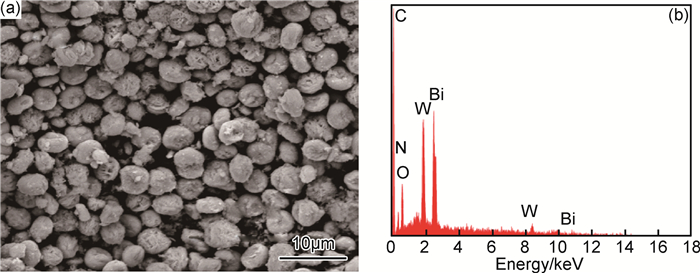
表 1为系列g-C3N4/Bi2WO6样品的组成与比表面积(SBET)。可知,纯Bi2WO6的比表面积约为46.5m2·g-1,而g-C3N4量子点(QDs)表面修饰对Bi2WO6比表面积的影响很小。图 3为5%g-C3N4/Bi2WO6异质结的FE-SEM和EDS能谱。由图 3(a)可以看出,5%g-C3N4/Bi2WO6的形貌和微观结构与纯Bi2WO6比较接近。EDS能谱(图 3(b))显示,所得5%g-C3N4/Bi2WO6和其他g-C3N4/Bi2WO6系列催化剂中g-C3N4的实际含量与理论沉积量接近(表 1)。图 4是g-C3N4和5%g-C3N4/Bi2WO6的TEM照片。由图 4(a)可以看出,g-C3N4量子点尺寸在5nm左右,且粒径比较均匀(图 4(a)中小图);由图 4(b)可以看出,g-C3N4量子点均匀沉积在Bi2WO6的表面。
| Sample | g-C3N4 theoretical content/% | g-C3N4 experimental content/% | SBET/(m2·g-1) |
| Pure Bi2WO6 | 0 | 0 | 46.5 |
| 5%g-C3N4/Bi2WO6 | 5 | 4.86 | 46.8 |
| 10%g-C3N4/Bi2WO6 | 10 | 9.42 | 47.2 |
| 20%g-C3N4/Bi2WO6 | 20 | 19.65 | 46.7 |
|
图 3 5%g-C3N4/Bi2WO6异质结的形貌(a)与EDS能谱(b) Fig. 3 Morphology(a) and EDS spectrum(b) of 5%g-C3N4/Bi2WO6 heterostructure |

|
图 4 g-C3N4(a)和5%g-C3N4/Bi2WO6(b)的TEM照片(插图为粒径分布图) Fig. 4 TEM images of g-C3N4(a) and 5%g-C3N4/Bi2WO6(b)(insert picture is particle size distribution) |
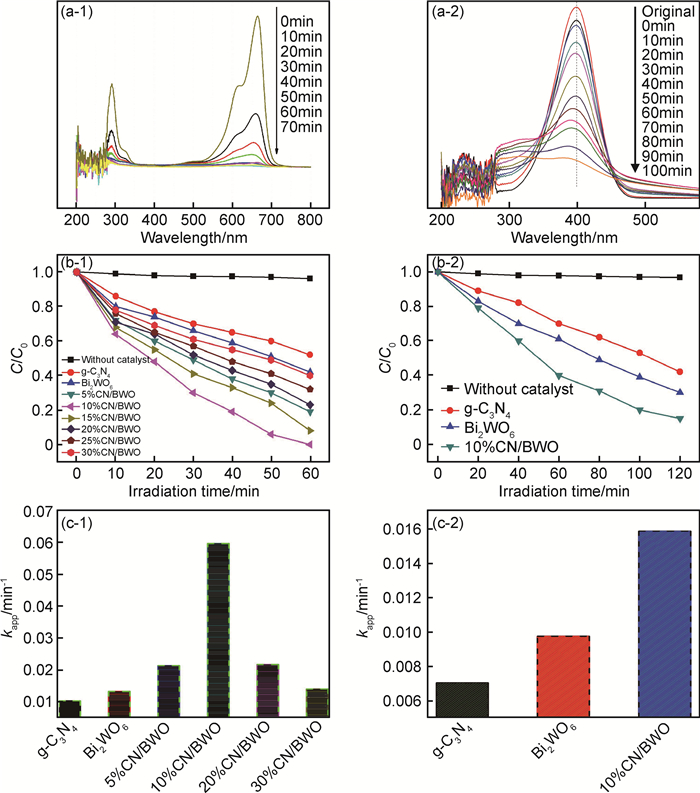
图 5为可见光照射下催化剂对MB和p-NPh的光催化降解活性。由图 5(a-1),(b-1)可见,g-C3N4/Bi2WO6异质结对MB的催化降解活性相对于纯g-C3N4和Bi2WO6显著提高,而且其光催化活性在g-C3N4的沉积量从5%到30%的范围内随着负载量的增加呈先增强后下降的趋势,g-C3N4的沉积量小于10%时,随着沉积量的增加g-C3N4/Bi2WO6异质结对MB的光催化活性增强。当g-C3N4的沉积量大于10%时,随着沉积量的增加活性反而下降。当g-C3N4沉积量为10%时,所得10%g-C3N4/Bi2WO6对MB的光催化降解活性最强,可见光照射60min,MB的光催化活性接近100%,其对降解MB的表观速率常数(kapp)分别是纯Bi2WO6和g-C3N4的4.5倍和5.8倍(图 5(c-1))。
|
图 5 纯g-C3N4,Bi2WO6和g-C3N4/Bi2WO6异质结对MB(1)和p-NPh(2)的催化降解活性 (a)吸收光谱随光照时间的变化;(b)浓度随光照时间的变化;(c)表观速率常数 Fig. 5 Photocatalytic activities of pure g-C3N4, Bi2WO6 and g-C3N4/Bi2WO6 heterostructures for MB(1) and p-NPh(2) (a)change in absorption spectra vs irradiation time; (b)concentration changing vs irradiation time; (c)apparent rate constant |
为了进一步探讨g-C3N4/Bi2WO6异质结催化材料的光催化活性,以硝基酚(p-NPh)作为模拟污染物,考察纯g-C3N4,Bi2WO6和10%g-C3N4/Bi2WO6异质结对p-NPh的降解活性比较。由图 5(a-2), (b-2), (c-2)可以看出,与纯g-C3N4和Bi2WO6相比,10%g-C3N4/Bi2WO6对p-NPh的降解活性显著提高,可见光照射120min,p-NPh的降解率约80%,其降解p-NPh的表观速率常数分别是纯Bi2WO6和g-C3N4的2.6倍和1.6倍。
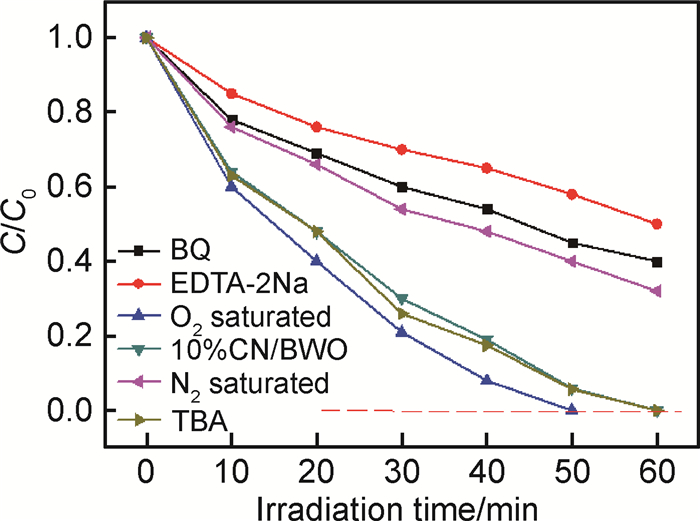
2.3 Z-型g-C3N4/Bi2WO6的光催化活性增强机理为了进一步了解g-C3N4/Bi2WO6异质结的活性增强机制,在光催化反应体系中加入自由基捕获剂来推测MB反应过程中活性物种的种类,结果见图 6。可见,当在反应体系中加入O2·-自由基捕获剂苯醌(BQ)时,MB的降解反应速率降低,说明O2·-是MB降解的主要活性物质。此外,当体系中加入空穴捕获剂EDTA-2Na时,MB的降解速率有所下降,表明空穴直接氧化也是MB光催化氧化分解的途径之一。然而,当向体系中添加羟基自由基捕获剂叔丁醇(TBA)时,次甲基蓝的降解率变化不显著,这表明·OH自由基不是MB光催化降解的主要活性物种。此外,为了验证O2在MB降解过程的作用,通过向反应体系中通N2和O2来考察MB降解活性的变化,由图 6可以看出,O2饱和时MB的降解速率明显加快,而N2饱和时MB的降解速率则显著降低。
|
图 6 捕获剂对g-C3N4/Bi2WO6活性的影响 Fig. 6 Effect of scavengers on the photocatalytic activity ofg-C3N4/Bi2WO6 |
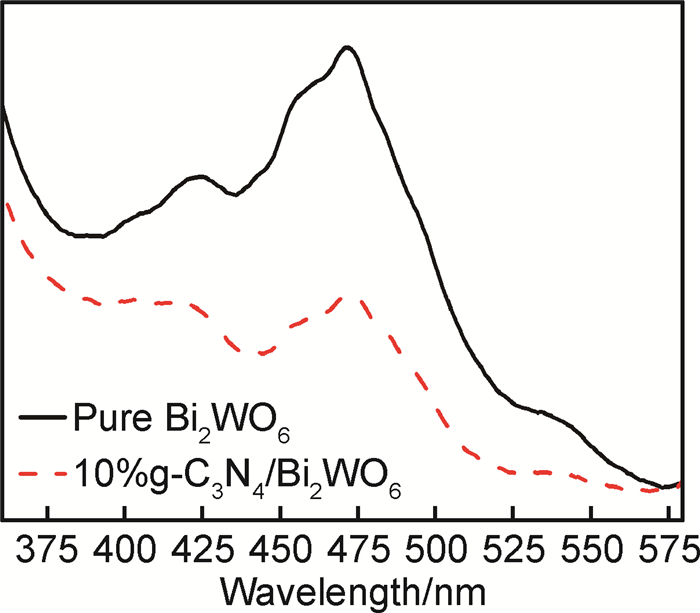
一般说来,O2·-可以通过两种途径产生:第一,敏化光催化。光照条件下,染料分子吸收光子能量后被激发至激发态,激发态的染料分子迅速将电子注入半导体催化剂的导带(CB)形成导带电子(eCB-),转移至导带的电子与吸附态的O2分子反应形成O2·-;由于MB的还原电位为0.532eV,大于O2·-的还原电位,表明激发态的MB*不能把电子转移给催化剂的导带进而被O2捕获形成O2·-[20],因此,敏化光催化不是MB催化降解的主要途径。第二,光照条件下,半导体的电子被激发至导带形成导带电子,同时在价带上留下空穴(hVB+),半导体被激发后产生的价带电子可以直接与吸附在半导体表面的氧分直接反应形成O2·-,O2·-和价带空穴共同作用可将MB彻底矿化分解。由于g-C3N4的导带和价带(VB)位置分别约为-0.82eV和1.87eV, 而Bi2WO6的CB和VB约为1.02eV和1.73eV[20]。此外,采用PL谱来进一步解释Z型结构g-C3N4/Bi2WO6的光催化反应机制[21]。当激发波长为300nm时,Bi2WO6在460~530nm之间的宽带发射峰,对应于423, 485nm和528nm处有3个发射峰,且纯Bi2WO6和g-C3N4/Bi2WO6的发射峰的位置一致(图 7),而后者的强度明显减弱,表明g-C3N4量子点表面沉积可显著延缓Bi2WO6光生电子/空穴对的复合。
|
图 7 纯Bi2WO6和10%g-C3N4/Bi2WO6的室温光致发光谱 Fig. 7 Room temperature photoluminescence(PL) spectra of pureBi2WO6 and 10%g-C3N4/Bi2WO6 |
可见光照下,g-C3N4和Bi2WO6价带电子均可被激发至导带,同时在价带上留下空穴;由于g-C3N4和Bi2WO6的能带结构能很好匹配,形成新颖的Z-型催化体系[20-22],g-C3N4导带上的激发电子与Bi2WO6的价带空穴复合,体系表现出Bi2WO6导带的还原能力和g-C3N4的价带空穴氧化能力,CN-eCB-被氧分子捕获形成O2·-,同时CN-hVB+可以直接氧化MB形成中间产物。O2·-和价带空穴与初级氧化产物反应,最终将MB和p-NPh矿化成CO2和H2O等小分子。同时,g-C3N4的VB空穴可氧化H2O产生O2和H+,而O2则可以与Bi2WO6的CB电子作用形成活性物种的O2·-,这样O2·-和h+的协同作用有利于催化剂活性的提高,图 8为g-C3N4/Bi2WO6异质结的光催化活性增强机理示意图。根据实验结果,MB在g-C3N4/Bi2WO6表面的降解过程为:
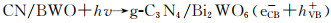
|
(1) |
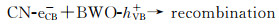
|
(2) |
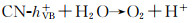
|
(3) |

|
(4) |
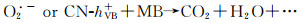
|
(5) |

|
图 8 g-C3N4/Bi2WO6异质结的光催化活性增强机理 Fig. 8 Photocatalytic activity enhanced mechanism ofg-C3N4/Bi2WO6 heterostructure |
(1) 采用浸渍-焙烧法将g-C3N4量子点均匀沉积在Bi2WO6的表面,成功构筑了Z-型结构g-C3N4/Bi2WO6催化材料。
(2) 与纯Bi2WO6和g-C3N4相比,g-C3N4/Bi2WO6对MB和p-NPh的降解活性显著提高,10%g-C3N4/Bi2WO6对降解MB的表观速率常数(kapp)分别是纯Bi2WO6和g-C3N4的4.5倍和5.8倍,降解p-NPh的kapp分别是纯Bi2WO6和g-C3N4的2.6倍和1.6倍。活性物种捕获实验表明,O2-和hVB+是MB催化降解的主要活性物种。
(3) g-C3N4和Bi2WO6形成新颖的Z-型催化体系,Bi2WO6导带上的激发电子与g-C3N4的价带空穴复合,表现出g-C3N4导带的还原能力和Bi2WO6的氧化能力,CN-eCB-被氧分子捕获形成O2·-,O2·-和hVB+与MB/p-NPh反应,最终将其矿化成CO2和H2O等小分子。
| [1] | FUJISHIMA A, HONDA K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238 (5358): 37–38. DOI: 10.1038/238037a0 |
| [2] |
周锋, 任向红, 刘建友, 等. 光催化降解水体有机污染物的研究进展[J].
材料工程, 2018, 46 (10): 9–19.
ZHOU F, REN X H, LIU J Y, et al. Development of photocatalytic degradation of organic pollutants in water[J]. Journal of Materials Engineering, 2018, 46 (10): 9–19. DOI: 10.11868/j.issn.1001-4381.2017.000972 |
| [3] | ZHANG C, ZHU Y. Synthesis of square Bi2WO6 nanoplates as high-activity visible-light-driven photocatalysts[J]. Chemistry of Materials, 2005, 17 (13): 3537–3545. DOI: 10.1021/cm0501517 |
| [4] | ZHANG L S, WANG W Z, CHEN Z G, et al. Fabrication of flower-like Bi2WO6 superstructures as high performance visible-light driven photocatalysts[J]. Journals of Materials Chemistry, 2007, 17 : 2526–2532. DOI: 10.1039/b616460a |
| [5] | WU L, BI J H, LI Z H, et al. Rapid preparation of Bi2WO6 photocatalyst with nanosheet morphology via microwave-assisted solvothermal synthesis[J]. Catalysis Today, 2008, 131 : 15–20. DOI: 10.1016/j.cattod.2007.10.089 |
| [6] | SHANG M, WANG W Z, SUN S M, et al. Bi2WO6 nanocrystals with high photocatalytic activities under visible light[J]. Journal of Physical Chemistry, 2008, 112 (28): 10407–10411. |
| [7] | SHANG M, WANG W Z, XU H L. New Bi2WO6 nanocages with high visible-light-driven photocatalytic activities prepared in refluxing EG[J]. Crystal Growth & Design, 2009, 9 (2): 991–996. |
| [8] | MA D K, HUANG S M, CHEN W X, et al. Self-assembled three-dimensional hierarchical umbilicate Bi2WO6 microspheres from nanoplates:controlled synthesis, photocatalytic activities, and wettability[J]. Journal of Physical Chemistry C, 2009, 113 (11): 4369–4374. DOI: 10.1021/jp810726d |
| [9] | ZHANG G K, LU F, LI M, et al. Synthesis of nanometer Bi2WO6 synthesized by sol-gel method and its visible-light photocatalytic activity for degradation of 4BS[J]. Journal of Physical Chemistry Solids, 2010, 71 (4): 579–582. DOI: 10.1016/j.jpcs.2009.12.041 |
| [10] | ROLAND M. Semiconductor composites:strategies for enhancing charge carrier separation to improve photocatalytic activity[J]. Advanced Functional Materials, 2014, 24 : 2421–2440. DOI: 10.1002/adfm.201303214 |
| [11] | QU Y Q, DUAN X F. Progress, challenge and perspective of heterogeneous photocatalysts[J]. Chemical Society Reviews, 2013, 42 : 2568–2580. DOI: 10.1039/C2CS35355E |
| [12] |
张相辉. La掺杂改性Bi2WO6纳米材料的制备及其光催化性能[J].
材料工程, 2018, 46 (11): 57–62.
ZHANG X H. Preparation and photocatalytic properties of La doped Bi2WO6 nanomaterials[J]. Journal of Materials Engineering, 2018, 46 (11): 57–62. DOI: 10.11868/j.issn.1001-4381.2017.000939 |
| [13] | WANG H L, ZHANG L S, CHEN Z G, et al. Semiconductor heterojunction photocatalysts:design, construction, and photocatalytic performances[J]. Chemical Society Reviews, 2014, 43 : 5234–5244. DOI: 10.1039/C4CS00126E |
| [14] | ZHANG J S, WANG B, WAGN X C. Chemical synthesis and applications of graphitic carbon nitride[J]. Acta Physico-Chimica Sinca, 2013, 29 (9): 1865–1876. |
| [15] | WANG X C, BLECHERT S. Polymeric graphitic carbon nitride for heterogeneous photocatalysis[J]. ACS Catalysis, 2012, 2 (8): 1596–1602. DOI: 10.1021/cs300240x |
| [16] | LI X N, HUANG R K, HU Y H, et al. A templated method to Bi2WO6 hollow microsphere and their conversion to double-shell Bi2O3/Bi2WO6 hollow microsphere with improved performance[J]. Inorganic Chemistry, 2012, 51 (11): 6245–6250. DOI: 10.1021/ic300454q |
| [17] | GUI M S, WANG P F, YUANG D, et al. Synthesis and visible-light photocatalytic activity of Bi2WO6/g-C3N4 composite photocatalysts[J]. Chinese Journal of Inorganic Chemistry, 2013, 29 (10): 2057–2064. |
| [18] | WANG D J, ZHEN Y Z, XUE G L, et al. Synthesis of mesoporous Bi2WO6 architectures and their gas sensitivity to ethanol[J]. Journal of Materials Chemistry C, 2013 (26): 4153–4162. |
| [19] | WANG D J, XUE G L, ZHEN Y Z, et al. Monodispersed Ag nanoparticles loaded on the surface of spherical Bi2WO6 nanoarchitectures with enhanced photocatalytic activities[J]. Journal of Materials Chemistry, 2012, 22 (11): 4751–4758. DOI: 10.1039/c2jm14448d |
| [20] | WANG D J, GUO L, ZHEN Y Z, et al. AgBr quantum dots decorated mesoporous Bi2WO6 architectures with enhanced photocatalytic activities for methylene blue[J]. Journal of Materials Chemistry A, 2014, 2 (30): 11716–11727. DOI: 10.1039/C4TA01444H |
| [21] | HIRAKAWA T, KAMAT P V. Charge separation and catalytic activity of Ag@TiO2 core-shell composite clusters under UV-irradiation[J]. Journal American Chemistry Society, 2005, 127 (11): 3928–3934. DOI: 10.1021/ja042925a |
| [22] | LI M L, ZHANG L X, FAN X Q, et al. Highly selective CO2 photoreduction to CO over g-C3N4/Bi2WO6 composite under visible light[J]. Journal of Materials Chemistry A, 2015, 3 (9): 5189–5196. DOI: 10.1039/C4TA06295G |
 2019, Vol. 47
2019, Vol. 47


