文章信息
- 张国芳, 孙涵丰, 许剑轶, 张羊换
- ZHANG Guo-fang, SUN Han-feng, XU Jian-yi, ZHANG Yang-huan
- 具可变价态稀土氧化物对Mg2Ni合金储氢性能的催化作用
- Catalytic effect of rare earth oxides with variable valences on hydrogen storage properties of Mg2Ni alloy
- 材料工程, 2019, 47(10): 90-96
- Journal of Materials Engineering, 2019, 47(10): 90-96.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2018.000266
-
文章历史
- 收稿日期: 2018-03-13
- 修订日期: 2019-04-28
Mg基储氢合金具有储氢容量高、价格低廉、资源丰富等特性,从而引起人们的极大关注,但其放氢温度过高、易被腐蚀及动力学性能差。为此,人们采取多种措施来改善Mg基合金的储氢性能,其中最常用的方法包括在合金中添加催化剂及对合金进行球磨处理等。高能球磨能破坏合金表面惰性氧化膜,细化合金颗粒,增大表面缺陷浓度,进而提高合金表面活性。在球磨过程中进一步添加催化剂,通常能够显著提高Mg基合金的储氢性能[1]。稀土元素特有的4f电子结构使其具备良好的催化特性。研究表明,将稀土氧化物应用于储氢材料中能够有效提高其储氢性能。张国芳等[2]分别将CeO2, La2O3及Eu2O3添加入Mg2Ni储氢材料中,发现催化剂可有效提高材料的放氢容量及速率,其中CeO2具有更好的催化性能。通过研究纳米CeO2及掺杂CeO2基固溶体对Mg2Ni储氢合金电化学及动力学性能的催化影响,证明掺杂CeO2固溶体可有效提高Mg基合金的最大放电容量及改善其动力学性能[3-4]。Xie等[5]报道CeO2催化剂可使复合材料MgH2-CeO2在空气中稳定存在,且具备较好的吸放氢性能。Zhang等[6]通过对比CeO2及MoS2催化剂对YMg11Ni合金储氢性能的影响,发现CeO2具有更佳的催化性能。
关于CeO2的催化机理方面,研究认为与Ce离子的易变价特性有关,但易变价特性对于催化效果的影响程度大小尚需进一步深入研究。17种稀土氧化物中,只有Ce,Pr及Tb离子可同时表现出+3或+4的可变价态。Ce离子在通常情况下是以+4价态稳定存在,但由于Ce4+的半径偏小,为了维持MO8型八配位氧化物稳定的萤石结构,晶格中部分Ce离子会还原为半径稍大的Ce3+价态,这种价态的变化会引起相应晶格氧的补偿,因此CeO2的易变价特性是其催化性能优异的重要原因;另一方面,对于Tb氧化物,单纯的二氧化物或三氧化物都无法稳定存在,一般是由一定比例的Tb3+/Tb4+组成为Tb4O7,这种变价性使其同样具有良好的催化性能而应用在诸多领域[7-8]。本工作分别选取具有可变价离子的CeO2,Tb4O7和具有稳定Nd3+价态的Nd2O3为催化剂,系统研究不同类型稀土氧化物对Mg2Ni合金电化学、气态储氢性能及动力学性能的影响,进而探索稀土氧化物对Mg基储氢合金的催化机理。
1 实验材料与方法铸态Mg2Ni合金锭采用中频感应炉熔炼制备,将合金锭粉碎过200目筛后待用。分别将纯度均为99.99%的稀土氧化物CeO2,Nd2O3及Tb4O7与Mg2Ni合金粉及Ni粉按照质量比为Mg2Ni:Ni:RExOy=1:1:0.05混合后球磨。球磨罐中的球料质量比为40:1,球磨转速350r/min,球磨时间20h,整个过程均在高纯Ar气中进行,为防止球磨时间过长发热,每球磨3h停止1h进行冷却。
样品的结构采用D8 Advanced X射线衍射仪(XRD)进行分析,CuKα靶,扫描速率4(°)/min。样品形貌及元素分析分别采用JEOL JEM-2100透射电镜(TEM)及QUANTA 400扫描电镜(SEM,EDS)进行测试。
样品的电化学储氢性能测试:将球磨样品与羰基镍粉按照质量比为1:4混合压片制备成合金电极,将其作为负极置于三电极电池管中进行测试,以Hg/HgO电极作为参比电极,以Ni(OH)2/NiOOH作为正极,6mol/L KOH溶液为电解液。采用Land电池测试系统,在40mA/g的恒定电流密度下进行充放电循环测试。材料的动力学性能在PARSTAT2273电化学工作站上进行测试。交流阻抗及动电位极化曲线均在50%放电深度下测试。交流阻抗的频率扫描范围为10kHz~5.0mHz,电位扰动幅度5mV;动电位极化曲线的扫描速率为5mV/s,测试所得阳极极化曲线的峰值电流密度为极限电流密度ⅠL。球磨样品的气态吸氢动力学性能在全自动Sieverts设备上进行,吸氢压力为3MPa,吸氢温度分别为100℃及250℃。
2 结果与分析 2.1 组织结构分析图 1为Mg2Ni-Ni-5%RExOy(CeO2,Nd2O3及Tb4O7)球磨样品的XRD谱图。为便于观察比较,含稀土氧化物催化剂球磨样品的XRD谱图峰强度增大了5倍。可知,与无稀土氧化物催化剂的Mg2Ni-Ni样品相比,添加RExOy样品的衍射峰都发生了宽化,衍射峰强度明显降低,几乎观察不到Mg2Ni合金峰,说明少量的稀土氧化物催化剂可以有效细化合金晶粒,降低合金的结晶度,进而提高比表面积,增加合金表面缺陷浓度。球磨Mg2Ni-Ni-5%RExOy样品中几乎观察不到稀土氧化物的衍射峰,这可能是由于催化剂含量低于XRD检测限的缘故。

|
图 1 Mg2Ni-Ni-5%RExOy样品的XRD谱图 Fig. 1 XRD patterns of Mg2Ni-Ni-5%RExOy samples |
图 2为Mg2Ni-Ni-5%RExOy样品的SEM图。可知,Mg2Ni-Ni-5%RExOy样品的颗粒形貌相近,大小相似,该结果与XRD结果相一致。Mg2Ni-Ni-5%CeO2及Mg2Ni-Ni-5%Nd2O3样品中存在一些粒度较小颗粒,而Mg2Ni-Ni-5%Tb4O7样品团聚较为明显,所有样品的平均粒度均小于10μm。样品的元素分析结果如表 1所示,成分均为Mg,Ni,O及相应的稀土元素。经过比较可知,样品中各元素测试含量与理论值很接近,而其中氧元素含量比理论值稍高,这是由于球磨及测试过程中Mg合金发生部分氧化所致。稀土氧化物催化剂在合金表面的分布情况采用面扫描进行测试,如图 3所示,球磨样品中的稀土元素分布均匀,说明球磨处理能够使稀土氧化物催化剂均匀分布。

|
图 2 Mg2Ni-Ni-5%RExOy样品的SEM图 (a)CeO2;(b)Nd2O3;(c)Tb4O7 Fig. 2 SEM images of Mg2Ni-Ni-5%RExOy samples (a)CeO2; (b)Nd2O3; (c)Tb4O7 |
| Sample | Mg2Ni-Ni-5%CeO2 | Mg2Ni-Ni-5%Nd2O3 | Mg2Ni-Ni-5%Tb4O7 | |||||||||||
| O | Mg | Ni | Ce | O | Mg | Ni | Nd | O | Mg | Ni | Tb | |||
| Experimental value | 3.1 | 44.85 | 51.74 | 0.51 | 2.54 | 49.24 | 47.75 | 0.47 | 2.64 | 35.39 | 61.25 | 0.72 | ||
| Theoretical value | 1.3 | 40.70 | 57.30 | 0.60 | 0.98 | 40.87 | 57.50 | 0.65 | 1.02 | 40.88 | 57.51 | 0.58 | ||

|
图 3 Mg2Ni-Ni-5%RExOy样品中稀土元素分布面扫描图 (a)Ce; (b)Nd; (c)Tb Fig. 3 EDS mapping images of the distribution of rare earth elements of Mg2Ni-Ni-5%RExOy samples 3(a)Ce; (b)Nd; (c)Tb |
对于合金电极来说,放电电压特性是衡量电池输出电量稳定性的重要衡量指标及最直接的决定因素,该性能可通过放电曲线的电压平台进行分析。金属氢化物负极的放电电压平台越长且越平坦,表明合金具有越好的放电性能[9]。图 4为Mg2Ni-Ni-5%RExOy样品的电化学性能。图 4(a)为Mg2Ni-Ni-5%RExOy样品在电流密度为40mA/g时的放电电压曲线。该过程对应于Mg基氢化物中的氢原子发生氧化脱氢反应,稀土氧化物对提高合金放电电压特性具有明显的催化作用,放电平台显著变长,与不含稀土氧化物Mg2Ni-Ni样品的放电容量(615.5mAh/g)相比,添加稀土氧化物样品的放电容量均有明显提高,其中添加CeO2样品的放电容量为722.3mAh/g,添加Nd2O3样品的放电容量为718.2mAh/g,而含Tb4O7球磨样品的放电容量最大,达到817.2mAh/g。根据XRD结果可知,添加催化剂球磨样品的晶粒减小,比表面积增大,因此可以允许更多氢原子扩散至合金内部及表面,使氢原子在合金内部的扩散路径变短,从而提高了合金的最大放电容量[10]。图 4(b)为球磨Mg2Ni-Ni-5%RExOy样品的循环稳定性曲线。可知,所有样品均在第一次循环即达到最大放电容量,表明样品具有很好的活化性能。样品的活化性能良好主要是由于经过球磨处理后Mg合金表面的氧化物层被破坏,露出了新鲜的合金表面,进而降低了氢原子进出合金的阻力;同时,通过XRD结果可知,在同样球磨条件下,添加稀土氧化物催化剂复合材料的峰强变小,峰宽变大,表明合金的比表面积增大,缺陷浓度提高,因此稀土氧化物催化剂的添加会进一步提高合金的活化性能。图 4(b)中的插图为样品经过20次恒定电流充放电循环后的容量保持率S20。可知,Mg2Ni-Ni-5%RExOy样品的循环保持率分别为29.5%(Mg2Ni-Ni),25.0%(Mg2Ni-Ni-5%CeO2),22.3%(Mg2Ni-Ni-5%Nd2O3),29.8%(Mg2Ni-Ni-5%Tb4O7)。催化剂的添加可以提高最大放电容量,但CeO2及Nd2O3催化剂对样品的循环稳定性没有促进作用,而Tb4O7催化剂不但可以有效提高合金的最大放电容量,还可较好地保持循环稳定性。由SEM结果可知,含CeO2及Nd2O3催化剂样品中小的合金颗粒较多,比表面积大,在充放电循环过程中更加容易被腐蚀,导致容量保持率低。而添加Tb4O7样品的颗粒有一定团聚,在某种程度上可阻止碱液对合金的腐蚀,因此保持率稍高。以上结果表明,添加Tb4O7催化剂对提高合金的电化学性能催化效果最佳。

|
图 4 Mg2Ni-Ni-5%RExOy样品的电化学性能 (a)放电电压曲线;(b)循环稳定性(插图为含不同催化剂样品的容量保持率S20) Fig. 4 Electrochemical properties of Mg2Ni-Ni-5%RExOy samples (a)discharge potential curves; (b)cycle stability(inset shows the capacity retaining rate S20of the samples with different catalysts) |
球磨样品的动力学性能分别通过交流阻抗(EIS)及动电位极化曲线进行考察。通过EIS图可完整反映合金电极的电化学过程,进而考察合金电极表面的电荷转移速率。EIS曲线主要包括三部分:高频区域的小容抗弧代表合金粉与集流体的接触电阻;中频区较大容抗弧表示合金表面的电荷转移电阻(Rct);低频区的直线部分对应于Warburg阻抗[11],该曲线精确地表征合金电极的电化学过程。通过比较圆弧半径的大小,可定性比较各频率区域电阻的大小。图 5为Mg2Ni-Ni-5%RExOy样品的动力学性能。由图 5(a)可知,无催化剂样品的高频区域容抗弧半径较大,而添加稀土氧化物催化剂样品的容抗弧普遍较小,表明催化剂可有效降低合金粉与集流体的接触电阻;通过拟合中频区圆弧半径[12],Rct由大到小依次为Mg2Ni-Ni(146.1mΩ)>Mg2Ni-Ni-5%Nd2O3(137.6mΩ)>Mg2Ni-Ni-5%Tb4O7(93.1mΩ)>Mg2Ni-Ni-5%CeO2(73.5mΩ)。结果表明,三种稀土氧化物均可有效提高电极表面电荷转移速率,其中CeO2及Tb4O7催化剂对提高合金电极表面活性具有最佳的催化作用。

|
图 5 Mg2Ni-Ni-5%RExOy样品的动力学性能 (a)交流阻抗谱图;(b)动电位极化曲线 Fig. 5 Kinetic properties of Mg2Ni-Ni-5%RExOy samples (a)electrochemical impedance spectra(EIS); (b)potentiodynamic polarization curves |
极限电流密度ⅠL是考察氢原子扩散过程的重要参数,其值可通过对合金电极测试动电位极化曲线得到,如图 5(b)所示。每条阳极极化曲线都存在一个明显的拐点,该拐点所对应的横坐标对应于极限电流密度的值,表示合金电极表面发生氧化反应后所形成的氧化物层阻碍了氢原子的进一步扩散[13],极限电流密度的大小表征了氢原子在合金体相内扩散能力的大小。可知,IL值由小到大的顺序依次为Mg2Ni-Ni≈Mg2Ni-Ni-5%Nd2O3<Mg2Ni-Ni-5%CeO2<Mg2Ni-Ni-5%Tb4O7。添加Nd2O3催化剂对极限电流密度IL的影响不明显,而添加Tb4O7及CeO2催化剂可明显提高合金体相内氢原子的扩散速率,其中Tb4O7的催化效果最佳。
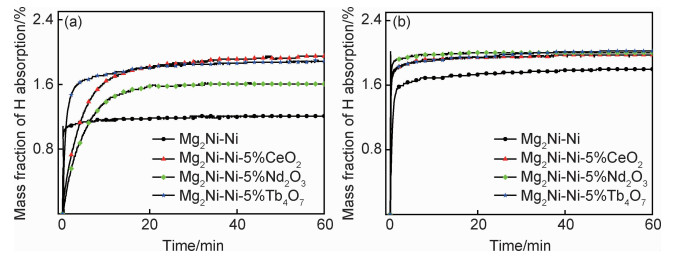
2.4 气态吸氢动力学图 6为Mg2Ni-Ni-5%RExOy样品在不同温度下的吸氢动力学曲线。由图 6(a)可知,在温度为100℃、H2压力为3MPa条件下,1h后吸氢量由大到小的顺序为Mg2Ni-Ni-5%CeO2(1.95%)>Mg2Ni-Ni- 5%Tb4O7(1.89%)>Mg2Ni-Ni-5%Nd2O3(1.62%)> Mg2Ni-Ni(1.21%),样品吸氢速率的顺序为Mg2Ni-Ni > Mg2Ni-Ni-5%Tb4O7>Mg2Ni-Ni-5%CeO2>Mg2Ni-Ni-5%Nd2O3。由图 6(b)可知,当温度升高至250℃时,所有样品的吸氢速率都有明显提升,在前5min的吸氢量即达到饱和吸氢量的90%。1h后样品吸氢量大小顺序为Mg2Ni-Ni-5%Tb4O7(2.02%)>Mg2Ni-Ni-5%Nd2O3(2.00%)> Mg2Ni-Ni-5%CeO2(1.97%)>Mg2Ni-Ni(1.80%)。以上结果表明,在不同温度下,添加稀土氧化物催化剂样品的吸氢量都有明显提升。值得注意的是,CeO2在较低温度下对合金具有良好的催化效果,随着温度的提升,吸氢量没有明显变化,而Nd2O3催化剂在较高温度下的催化效果较为明显。综合来说,含Tb4O7催化剂样品在两个温度下都具有较好的吸氢动力学及较高的吸氢量。
|
图 6 Mg2Ni-Ni-5%RExOy样品的吸氢动力学曲线 (a)100℃; (b)250℃ Fig. 6 Hydrogen absorption kinetic curves of Mg2Ni-Ni-5%RExOy samples (a)100℃; (b)250℃ |
稀土氧化物对合金储氢机制的催化作用可以从以下几个方面进行分析:首先,由样品XRD及SEM结果可知,添加稀土氧化物催化剂后球磨样品的结晶度变低,说明合金颗粒的比表面积变大,缺陷浓度增大,因此允许更多的氢原子进入合金之中,同时氢原子在合金内部的扩散路径变短,使得储氢容量得到提高;其次,添加不同稀土氧化物所得复合物的粒度大小相似,而样品的储氢容量及动力学性能有明显不同,因此样品的储氢性能除与样品的晶粒大小有关外,还应与不同催化剂所表现出的催化性能有关。三种稀土氧化物中,以Tb4O7及CeO2的催化效果较为突出,而Nd2O3的催化效果稍弱。对比三种稀土金属氧化物,其最为显著的区别在于稀土元素中4f电子数的不同。研究表明,催化剂的微观电子跃迁性能与催化性能有密切联系。如Oelerich等[14]提出具有可变价态的过渡金属氧化物具有更好的催化性能,金属原子的不同电子价态在合金吸放氢过程中起到重要的作用;具可变价态的过渡金属催化剂对MgH2的催化作用是由于催化剂与Mg—H键发生了电子交互作用[15];MgH2与CeO2催化剂发生的电子交换过程可促进Mg—H的解离及氢原子的再结合,而这种催化效果与CeO2中Ce离子的变价特性相关[16-18]。Cui等[19]通过研究Ti基材料(TiH2, TiO2和TiCl3)对Mg的催化作用,提出其催化机制是多价态的Ti(+2,+3及+4)离子可作为Mg2+及H-之间电子转移的中介及活性点,从而提高Mg的吸放氢速率。基于以上研究可知,催化剂的催化效果与其自身的电子结构有密切联系。如前所述,Tb4O7及CeO2中的稀土离子均具有易变价特性,特别是Tb4O7中的Tb离子本身即同时存在Tb3+及Tb4+两种价态,CeO2中的Ce4+离子很容易在反应中变为+3价,而Nd2O3中的Nd3+离子价态一直保持稳定。由电化学及动力学性能测试结果可知,含Tb4O7样品的最大放电容量及气态吸氢量最大,动力学性能也最佳,因此Tb4O7对储氢合金的综合催化性能最佳,添加CeO2催化剂样品的电化学及气态储氢量位列其次,而Nd2O3的催化效果则不够明显。由此可推测,这三种催化剂的催化性能与离子的变价特性密切相关,稀土离子的变价性越强,则催化性能越好。
3 结论(1) Mg2Ni-Ni-5%RExOy复合材料的电化学及动力学性能均有明显提高,其中Mg2Ni-Ni-5%Tb4O7的最大放电容量及循环稳定性都最佳。
(2) 三种稀土氧化物催化剂均可明显提高合金的气态吸氢量,其中Tb4O7对提高合金在低温时储氢动力学性能的催化效果最好。
(3) 稀土氧化物催化剂的催化能力与稀土离子的变价特性有密切联系,催化能力由大到小的顺序为Tb4O7>CeO2>Nd2O3。
| [1] |
张国芳, 翟亭亭, 胡锋, 等. 纳米CuO催化剂晶粒尺寸对Mg2Ni基复合材料储氢性能的影响[J].
材料工程, 2018, 46 (7): 151–156.
ZHANG G F, ZHAI T T, HU F, et al. Effect of different sizes of nano CuO catalysts on hydrogen storage properties of Mg2Ni based composites[J]. Journal of Materials Engineering, 2018, 46 (7): 151–156. |
| [2] |
张国芳, 张羊换, 许剑轶, 等. Ni-5%RExOy复合添加剂对Mg2Ni电化学储氢性能的影响[J].
材料工程, 2017, 45 (11): 72–77.
ZHANG G F, ZHANG Y H, XU J Y, et al. Effects of Ni-5%RExOy composite additives on electrochemical hydrogen storage performance of Mg2Ni[J]. Journal of Materials Engineering, 2017, 45 (11): 72–77. DOI: 10.11868/j.issn.1001-4381.2016.000345 |
| [3] | ZHANG G F, XU J Y, HOU Z H, et al. Research on micro-structure and catalysis properties of nanosized Ce1-x(Fe0.5Eu0.5)xO2-δ solid solutions[J]. Journal of Rare Earths, 2017, 35 (1): 63–70. DOI: 10.1016/S1002-0721(16)60175-8 |
| [4] |
张国芳, 张羊换, 许剑轶, 等. Mg2Ni-Ni-xCeO2复合材料储氢性能研究[J].
稀有金属, 2014, 38 (6): 1035–1042.
ZHANG G F, ZHANG Y H, XU J Y, et al. Hydrogen storage properties of Mg2Ni-Ni-xCeO2 composites[J]. Chinese Journal of Rare Metals, 2014, 38 (6): 1035–1042. |
| [5] | XIE L, LI J, ZHANG T, et al. Air-stable MgH2-CeO2 composite with facilitated dehydrogenation kinetics synthesized by high energy ball milling[J]. Materials Characterization, 2017, 133 : 94–101. DOI: 10.1016/j.matchar.2017.09.031 |
| [6] | ZHANG Y, HUANG G, YUAN Z, et al. A comparison study of hydrogen storage performances of as-milled YMg11Ni alloy catalyzed by CeO2 and MoS2[J]. Materials Science " Engineering B, 2017, 225 : 1–9. DOI: 10.1016/j.mseb.2017.08.006 |
| [7] | ISMAI E, MEHMET A, SEMRA D A, et al. Phase stability and electric conductivity of Eu2O3-Tb4O7 co-doped Bi2O3 electrolyte[J]. International Journal of Hydrogen Energy, 2015, 40 (30): 9485–9490. DOI: 10.1016/j.ijhydene.2015.05.098 |
| [8] | ZHANG Y, DENG J, ZHANG H, et al. Three-dimensionally ordered macroporous Pr6O11 and Tb4O7 with mesoporous walls:preparation, characterization, and catalytic activity for CO oxidation[J]. Catalysis Today, 2015, 245 : 28–36. DOI: 10.1016/j.cattod.2014.09.017 |
| [9] | ZHANG Y, YANG T, CAI Y, et al. Structures and electroche-mical performances of RE-Mg-Ni-Mn-based alloys prepared by casting and melt spinning[J]. Jounal of Rare Earths, 2016, 34 (12): 1241–1251. DOI: 10.1016/S1002-0721(16)60160-6 |
| [10] | DABAKI Y, BOUSSAMI S, KHALDI C, et al. The effect of ZnO addition on the electrochemical properties of the LaNi3.55Mn0.4Al0.3Co0.2Fe0.55 electrode used in nickel-metal hydride batteries[J]. Journal of Solid State Electrochemistry, 2017, 21 (4): 1–8. |
| [11] | KURIYAMA N, SAKAI T, MIYAMURA H, et al. Electro-chemical impedance and deterioration behavior of metal hydride electrodes[J]. Journal of Alloys and Compound, 1993, 202 (1/2): 183–197. |
| [12] | KURIYAMA N, SAKAI T, MIYAMURA H, et al. Electro-chemical impedance spectra and deterioration mechanism of metal hydride electrodes[J]. Journal of the Electrochemical Society, 1992, 139 : 72–73. DOI: 10.1149/1.2221180 |
| [13] | WU M S, WU H R, WANG Y Y, et al. Surface treatment for hydrogen storage alloy of nickel/metal hydride battery[J]. Journal of Alloys and Compoud, 2000, 302 (1/2): 248–257. |
| [14] | OELERICH W, KLASSEN T, BORMANN R. Metal oxides as catalysts for improved hydrogen sorption in nanocrystalline Mg-based materials[J]. Journal of Alloys and Compounds, 2001, 315 (1): 237–242. |
| [15] | TSUDA M, DINO W A, KASAI H, et al. Mg-H dissociation of magnesium hydride MgH2 catalyzed by 3d transition metals[J]. Thin Solid Films, 2006, 509 (1): 157–159. |
| [16] | JANOT R, DAROK X, ROUGIER A, et al. Hydrogen sorption properties for surface treated MgH2 and Mg2Ni alloys[J]. Journal of Alloys and Compoud, 2005, 404/406 (12): 293–296. |
| [17] | GULICOVSKI J, RASKOVIC-LOVRE Z, KURKO S, et al. Influence of vacant CeO2 nanostructured ceramics on MgH2 hydrogen desorption properties[J]. Ceramics International, 2012, 38 (2): 1181–1186. DOI: 10.1016/j.ceramint.2011.08.047 |
| [18] | MUSTAFA N S, ISMAIL M. Hydrogen sorption improvement of MgH2 catalyzed by CeO2 nanopowder[J]. Journal of Alloys and Compoud, 2017, 695 : 2532–2538. DOI: 10.1016/j.jallcom.2016.11.158 |
| [19] | CUI J, WANG H, LIU J, et al. Remarkable enhancement in dehydrogenation of MgH2 by a nano-coating of multi-valence Ti-based catalysts[J]. Journal of Materials Chemistry A, 2013, 1 (18): 5603–5611. DOI: 10.1039/c3ta01332d |
 2019, Vol. 47
2019, Vol. 47


