文章信息
- 亓淑艳, 王德朋, 赵亚栋, 胥焕岩
- QI Shu-yan, WANG De-peng, ZHAO Ya-dong, XU Huan-yan
- 电气石/ZnO复合材料光催化机制
- Photocatalytic mechanism of tourmaline/ZnO composites
- 材料工程, 2019, 47(9): 145-151
- Journal of Materials Engineering, 2019, 47(9): 145-151.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2018.000033
-
文章历史
- 收稿日期: 2018-01-08
- 修订日期: 2019-02-22
近几年来,ZnO作为一种重要的Ⅱ~Ⅵ族直接带隙n型半导体材料,在电学、光学和光子学领域表现出卓越的性能。室温下ZnO的禁带宽度为3.37eV,激子结合能为60meV[1-2],同时,ZnO不仅具有较强的自由激子跃迁发光特性[3],而且还具有极好的化学、力学、热稳定性和光催化性能, 其作为光催化剂具有活性高、价格低廉、环保等特点,所以在光催化污水处理方面备受青睐[4]。但是其也存在缺点,一是光催化效率低,另外,ZnO光电响应范围较窄,而且不同形貌和结构的ZnO使其光学性能发生改变,影响了光催化活性。Han等[5]采用不同的方法,合成了片状、六角柱状和六角金字塔状ZnO,催化结果表明,不同的显露晶面时其化学活性有很大差别,活性最大的晶面为Zn2+在末端的六角柱状ZnO。Wang[6]利用CTAB和PEG-400作为表面活性剂,采用水热法合成了5种不同形貌和晶型ZnO粉体,发现当使用PEG-400表面活性剂时制得的ZnO为颗粒状,尺寸减小,光吸收能力最强,表面氧缺陷浓度最高。国内外的许多学者在元素掺杂[7]、贵金属掺杂[8]、碳材料掺杂[9]、离子掺杂[10]、半导体复合[11]和矿物质复合[12]等方面开展了大量的研究工作。
电气石是由Al,Na,Ca,Mg和Fe等元素组成的天然环状硅酸盐矿物,化学成分复杂,通式可写为XY3ZS6i6O18(BO3)3W4(X=Na,Ca,K;Y=Mn,Fe,Mg,Al;Z=Al,Fe,Cr,Mg;W=OH,F,O)。由于具有许多优良的性能,被广泛应用在环保、保健、建筑材料、食品和农业领域等[13-14]。电气石具有很好的吸附性能,能够吸附水中的污染物和一些重金属离子,并且其本身的晶格组成能够释放负离子,对水和空气有净化作用,被誉为21世纪改善环境、促进人体健康的全新材料[15]。电气石最重要的特性是在其表面存在能够形成电偶极子的自发永久性磁极,因此在电气石颗粒表面存在强烈的电场,尤其对于小尺寸电气石颗粒更是如此。郭昀等[16]利用极性电气石(0001)晶面作为生长衬底,制备出了直立片状晶体交叉结构的纳米ZnO薄膜,结果表明,随着电气石含量增加,晶体沿c轴的固有电偶极矩越高,表面电场作用越强,ZnO纳米片的厚径比越小。Zhang等[17]利用溶胶凝胶法合成了TiO2复合材料,结果发现,加入电气石之后,复合材料比表面积明显高于纯TiO2,且电子和空穴复合的效率降低。本工作采用简单的一步水热法将电气石和ZnO进行复合,对其结构、形貌和光学等性能进行研究,并在模拟太阳光下,以酸性品红为目标污染物,探讨电气石对ZnO光催化性能的影响。
1 实验 1.1 电气石/ZnO复合材料的制备分别称取0.74g尿素、3.70g六水硝酸锌,倒入62mL蒸馏水中,超声振荡溶解后,分别加入质量为0.01,0.03,0.05,0.07,0.09,0.11,0.13g的电气石,记为1%,3%,5%,7%,9%,11%,13%,超声使其分散均匀。将配置好的溶液放入聚四氟乙烯内衬反应釜中,160℃烘箱中保温10h;将产物进行抽滤、洗涤(去离子水和无水乙醇洗涤3次);将滤饼放入60℃烘箱中干燥6h;将干燥后的样品放入500℃马弗炉中煅烧1h,冷却即得到不同电气石负载比例的ZnO纳米颗粒。
1.2 表征方法采用D/max-3B型X射线衍射仪对样品进行定性分析;采用FEISirion 200扫描电子显微镜对样品形貌进行扫描;PL光谱采用RF-5301PC荧光分光光度计进行测试;采用ST-08型比表面积测定仪进行样品比表面积的测定;采用USB-400型紫外可见漫反射光谱测定样品的光吸波长和反射波长,gxz500型500W氙灯作为光源。
1.3 光催化实验方法采用分光光度计测量不同时刻酸性品红溶液的吸光度,由式(1)计算得出不同时间内的脱色率D。

|
(1) |
式中:C0为酸性品红的初始吸光度;Ct为不同时刻酸性品红脱色后溶液的吸光度。
配制20mg/L的品红溶液,取100mL倒入烧杯中,在酸性品红的最大吸收波长545nm处测定C0。称0.2g样品,加入酸性品红溶液中,避光吸附0.5h,使其达到吸附-脱附平衡, 离心后测量吸光度Ct,共测2组。然后将溶液置于氙灯下进行光催化,每隔0.5h取出溶液进行离心测量吸光度,共测6组。
1.4 羟基自由基(·OH)的测定应用荧光技术(PL)、以对苯二甲酸为分子探针检测光催化剂在光激发条件下表面是否产生羟基自由基(·OH)。首先,配制对苯二甲酸(TA)溶液(其中NaOH的浓度为2mmol·L-1,TA的浓度为0.5mmol·L-1),然后利用TA对光催化剂进行羟基自由基活性测试。·OH是光催化反应过程中产生的具有强氧化性的物质。活性羟基能够与TA反应生成羟基对苯二甲酸(TAOH)。在激发波长为315nm的光照射下,TAOH中会发出波长为420nm左右的荧光。因此在催化过程中产生的·OH数量可以依据TAOH的荧光强度来表征。实验方法与光催化测试相同,其中酸性品红溶液用TA溶液代替,每隔1h取样,进行荧光强度测试。
2 结果与表征 2.1 XRD分析图 1为不同含量的电气石/ZnO复合材料的XRD谱图。可以看出,每种样品中都含有电气石的特征衍射峰,ZnO样品的XRD谱图出现的各衍射峰与标准卡片PDF 79-207的衍射峰一致,表明ZnO样品为纤锌矿结构,并且属于六方晶系。随着电气石含量的增加,复合样品的晶体结构没有改变,但衍射峰强度逐渐变低,结晶度逐渐变差。在电气石含量低时未发现电气石的衍射峰,是由于两方面的原因:其一是电气石的含量少;其二是电气石附着在ZnO表面。这与Song等[18]和Liu[19]研究的结果相一致。

|
图 1 不同含量的电气石/ZnO复合材料XRD谱图 Fig. 1 XRD patterns of tourmaline/ZnO composites withdifferent contents |
图 2为7%含量的电气石/ZnO复合材料的能谱图及SEM图。可以看出,复合材料中含有Zn,O,Al,Si,Ag,Ba,Pr,Nd,Fe元素。因此,可以进一步确定样品中含有ZnO及含多种元素的天然电气石。

|
图 2 7%电气石/ZnO复合材料的能谱图(a)及SEM图(b) Fig. 2 EDS spectrum(a) and SEM image(b) of 7% tourmaline/ZnO |
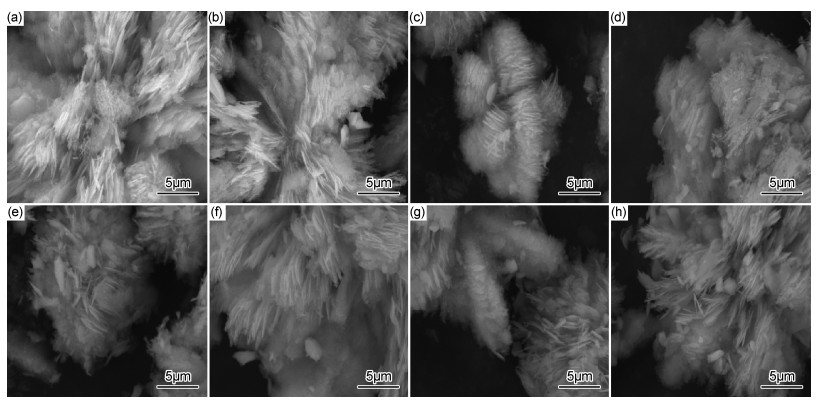
图 3为不同含量电气石/ZnO复合材料的SEM图。ZnO形貌为花束形状,直径约为10~20μm,花瓣是由薄片组成,片层厚度约为50nm。从复合后的电气石/ZnO材料可以看出,ZnO的表面长有电气石。并且随着电气石含量的增加, ZnO花束的形状变得不太规则,直径的大小和薄片的厚度也变得不固定,周围出现单片散落的花瓣,说明电气石影响ZnO晶粒的生长。这一点和Wang[6]的研究相似,不同形貌及复杂结构使得ZnO的表面形态发生变化,进而影响其光催化活性。
|
图 3 不同含量的电气石/ZnO复合材料SEM图 (a)1%;(b)3%;(c)5%;(d)7%;(e)9%;(f)11%;(g)13%;(h)15% Fig. 3 SEM images of tourmaline/ZnO composites with different contents (a)1%;(b)3%;(c)5%;(d)7%;(e)9%;(f)11%;(g)13%;(h)15% |
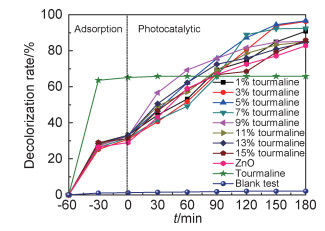
图 4为电气石/ZnO复合材料吸附及光催化曲线。发现在吸附过程中,0.1g电气石有较好的吸附效果,30min时染料的脱色率达到63.61%,而电气石/ZnO复合材料对染料的吸附脱色率均要高于纯ZnO。
|
图 4 不同含量电气石/ZnO复合材料的吸附及光催化曲线 Fig. 4 Adsorption and photocatalytic curves of tourmaline/ZnO composites with different contents |
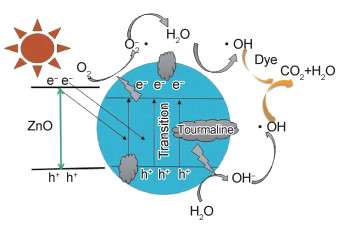
可以看出,在光催化过程中电气石本身并没有光催化性能,且酸性品红在无光、无催化剂的情况下,240min内自身脱色率仅有2%。ZnO光催化降解酸性品红最大脱色率为80.8%,而复合电气石后,酸性品红的脱色率均得到了明显的提高。当电气石含量为5%时,染料在240min内脱色率达到最大值96.62%。产生这种结果的原因是:(1)由于电气石良好的吸附性能,增加了染料在催化剂表面的吸附,使得染料与催化剂充分接触;(2)电气石具有自发永久电极性,能有效地抑制ZnO电子-空穴对复合,提高空穴浓度,有利于羟基自由基(·OH)浓度的增加;(3)电气石中的金属离子在ZnO的导带和价带间形成了杂质能级,使复合材料从价带到导带的荷移跃迁吸收带发生红移,降低了ZnO的带隙能。当电气石含量超过5%时,过多的电气石覆盖在ZnO表面,导致电气石/ZnO光利用率下降,复合材料的光催化能力降低,其原理图如图 5所示。电气石的加入降低了ZnO的禁带宽度,使其更容易在可见光下激发产生电子-空穴对,而水中的OH-与空穴(h+)作用产生具有强氧化性的·OH,水中的O2与电子作用形成超氧负离子(O2-·),进而与H2O形成·OH,最终·OH将酸性品红降解为CO2和H2O[20]。
|
图 5 电气石/ZnO复合材料光催化机理图 Fig. 5 Photocatalytic schematic diagram of tourmaline/ZnO composites |
主要化学反应为:
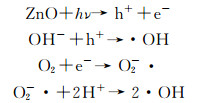
|
酸性品红+·OH→CO2+H2O+其他产物
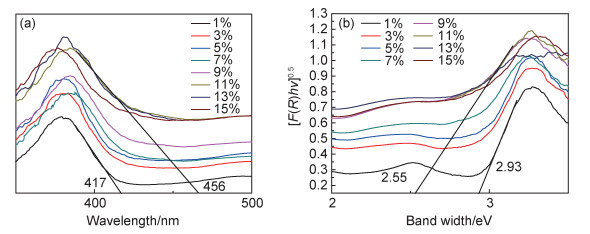
3 电气石增强ZnO光催化的机制分析 3.1 电气石/ZnO UV-Vis DRS光谱分析图 6为不同电气石含量的电气石/ZnO复合材料的UV-Vis DRS分析。可知,电气石/ZnO复合材料的吸收边在400~500nm之间,随着电气石含量的增加复合材料的吸收带均发生了红移。说明电气石中的金属离子在ZnO导带和价带间形成了杂质能级,降低了ZnO的带隙能(Eg),使得电子-空穴对更容易产生。ZnO的禁带宽度可以通过[F(R)hν]0.5的关系曲线来确定[21],当电气石含量为9%时,禁带宽度最低。说明电气石含量的增加有效地降低了复合材料的禁带宽度,增大了可见光响应范围,使复合材料的光催化性能得到提高。
|
图 6 不同含量电气石/ZnO复合材料的紫外漫反射光谱(a)和禁带宽度图(b) Fig. 6 UV-Vis DRS spectra(a) and forbidden band width map(b) of tourmaline/ZnO composites with different contents |
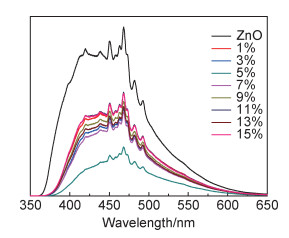
图 7为ZnO及不同含量电气石/ZnO复合材料光致发光谱图。PL谱的产生源于半导体ZnO中光生电子-空穴对被激发分离后的再复合。对于光催化材料,PL谱强度越低,意味着光生电子-空穴对的复合概率越低。发现各个样品均在452nm和470nm处出现了可见光发射峰,但ZnO的强度最大,说明电气石可以有效地降低ZnO电子-空穴复合的效率,并且电气石含量为5%时复合材料的发光强度最弱。以上现象产生的原因是:在电气石自发极化电场的作用和光照条件下,加速了ZnO表面的电子向正极移动,降低电子和空穴复合的效率。但随着复合比例的增加,发光强度增大,这可能是由于过多的电气石之间会发生相互作用,从而削弱或抵消彼此之间的相互作用,不能达到电子和空穴分离的效果,故使得发光峰的发光强度反而升高。
|
图 7 不同含量电气石/ZnO复合材料的PL谱图 Fig. 7 PL spectra of tourmaline/ZnO composites with different contents |
大多数初始浓度较低的光催化降解体系符合Langmuir-Hinshelwood一级动力学模型。因此用准一级反应动力学模型(式(2))对ZnO和5%电气石/ZnO进行光催化量化研究,定性描述电气石的加入对光催化能力的影响。

|
(2) |
式中:k1为准一级反应速率常数,min-1。
ZnO和5%电气石/ZnO降解酸性品红的动力学曲线如图 8所示。可知,两条降解动力学曲线的线性关系较好,且两条曲线R2分别为0.971和0.988,接近于1,这说明降解规律遵循Langmuir-Hinshelwood一级动力学模型。并且5%电气石/ZnO的降解速率ka是ZnO降解速率kb的2.3倍,可见光催化活性增强。

|
图 8 ZnO和5%电气石/ZnO复合材料降解动力学曲线 Fig. 8 Degradation kinetic curves of ZnO and 5% tourmaline/ZnO composites |
式(3),式(4)表示在可见光照射下产生活性羟基的过程,可以依据TAOH的发光强度判断反应过程中羟基形成的多少。
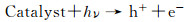
|
(3) |

|
(4) |
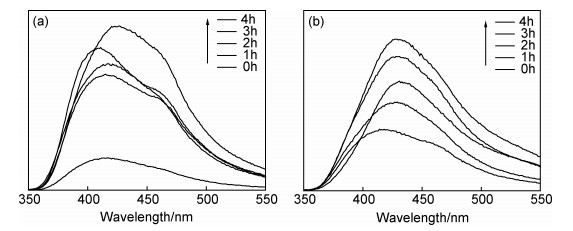
图 9为315nm激发波长下ZnO和5%电气石/ZnO复合材料对TAOH的荧光谱。可以看出,随着光照时间延长TAOH增加,且在相同时刻5%电气石/ZnO要比ZnO产生的TAOH多。这一现象产生的原因是:(1)根据Wang[6]的研究,ZnO的价带电位及OH-/·OH氧化还原电位分别是3.0eV及2.7eV,ZnO的价带电位要比OH-/·OH氧化还原电位更高,在可见光激发下,ZnO价带上的强氧化性空穴能够把OH-氧化为·OH,说明光催化的进行与能带的电位有密切关系;(2)由图 6(b)禁带宽度可知,电气石的加入减小了ZnO的禁带宽度,使其更容易被光激发产生电子-空穴,进而氧化OH-形成·OH,降解染料。
|
图 9 315nm激发波长下5%电气石/ZnO(a)和ZnO对TAOH的荧光谱(b) Fig. 9 Fluorescence spectra of TAOH by 5% tourmaline/ZnO(a) and ZnO(b) at 315nm excitation wavelength |
(1) 采用一步水热法制备了花瓣形貌的ZnO和电气石/ZnO复合材料,发现电气石能与ZnO结合, 且很好地生长在ZnO花瓣上。
(2) 由于电气石自发极性及多金属离子的存在,抑制了ZnO激发产生的电子-空穴对的复合概率,降低了禁带宽度,进而使得ZnO光利用率增大,光催化性能增强。
(3) ZnO和5%电气石/ZnO复合材料对酸性品红降解体系的降解规律遵循Langmuir-Hinshelwood一级动力学模型,并且电气石的加入,使羟基自由基(·OH)随之增多,增大了光催化降解的速率。
| [1] |
杨丰, 王飞, 贾若飞, 等. 零维、一维和二维ZnO纳米材料的应用研究进展[J].
材料工程, 2018, 46 (10): 20–29.
YANG F, WANG F, JIA R F, et al. Application research and progress of 0D, 1D and 2D ZnO nanomaterials[J]. Journal of Materials Engineering, 2018, 46 (10): 20–29. DOI: 10.11868/j.issn.1001-4381.2016.000868 |
| [2] | NEKOUEI F, NEKOUEI S. Comparative study of photocatalytic activities of Zn5(OH)8Cl2·H2O and ZnO nanostructures in ciprofloxacin degradation:response surface methodology and kinetic studies[J]. Science of the Total Environment, 2017, 601/602 : 508–517. DOI: 10.1016/j.scitotenv.2017.05.117 |
| [3] |
芦佳, 王辉虎, 董一帆, 等. RGO/ZnO纳米棒复合材料的合成及光催化性能[J].
材料工程, 2016, 44 (12): 48–53.
LU J, WANG H H, DONG Y F, et al. Synthesis and photocatalytic properties of RGO/ZnO nanorod composites[J]. Jouranl of Materials Engineering, 2016, 44 (12): 48–53. DOI: 10.11868/j.issn.1001-4381.2016.12.008 |
| [4] | LI Z H, LI G, DU Y, et al. Photovoltaic characteristics of ZnO nanoparticles[J]. Chemical Journal of Chinese Universities, 2012, 33 (3): 560–563. |
| [5] | HAN X G, HE H Z, KUANG Q, et al. Controlling morphologies and tuning the related properties of nano/microstructured ZnO crystallites[J]. The Journal of Physical Chemistry C, 2008, 113 (2): 584–589. |
| [6] | WANG J. Synthesis and photocatalytic properties research of ZnO nanomaterials and core-shell structure[D].Changchun: University of Chinese Academy of Sciences, 2016. |
| [7] |
吴闪, 朱延俊, 赵梦媛, 等. Co元素掺杂对CeO2基固态电解质导电行为的影响[J].
材料工程, 2018, 46 (5): 133–138.
WU S, ZHU Y J, ZHAO M Y, et al. Effects of co-dopings on electrical behaviors of CeO2-based solid electrolyte[J]. Journal of Materials Engineering, 2018, 46 (5): 133–138. |
| [8] | ZHANG Z, LIU H, ZHANG H, et al. Synthesis of spindle-like Ag/ZnO heterostructure composites with enhanced photocatalytic performance[J]. Superlattices & Microstructures, 2014, 65 : 134–145. |
| [9] | LIU P, GUO Y, XU Q, et al. Enhanced photocatalytic perfor-mance of ZnO/multi-walled carbon nanotube nanocomposites for dye degradation[J]. Ceramics International, 2014, 40 (4): 5629–5633. DOI: 10.1016/j.ceramint.2013.10.157 |
| [10] | LIAO S, HUANG D, YU D, et al. Preparation and charact-erization of ZnO/TiO2, SO42-/ZnO/TiO2 photocatalyst and their photocatalysis[J]. Journal of Photochemistry & Photobiology A Chemistry, 2004, 168 (1/2): 7–13. |
| [11] | LOW J, CAO S, YU J, et al. Two-dimensional layered composite photocatalysts[J]. Chemical Communications, 2014, 50 (74): 10768–10777. DOI: 10.1039/C4CC02553A |
| [12] | YU L, WANG C, CHEN F, et al. Investigating the synergistic effects in tourmaline/TiO2-based heterogeneous photocatalysis:underlying mechanism insights[J]. Journal of Molecular Catalysis A:Chemical, 2016, 411 : 1–8. DOI: 10.1016/j.molcata.2015.10.006 |
| [13] | GUO Y, XIA Y B, MIN J H, et al. Influence of polar tourmaline substrates on the growth of ZnO nanoplates[J]. Journal of Inorganic Materials, 2010, 25 (7): 717–720. DOI: 10.3724/SP.J.1077.2010.00717 |
| [14] | PRASAD G M, NETAJI K D, DATTATRAY K D, et al. Erratum to:cetyltrimethylammonium bromide capped 9-anthral-dehyde nanoparticles for selective recognition of phosphate anion in aqueous solution based on fluorescence quenching and appli-cation for analysis of chloroquine[J]. Journal of Fluorescence, 2015, 25 (1): 39–39. DOI: 10.1007/s10895-014-1474-0 |
| [15] | HU Y M, CHEN X B, TANG M R. Research development and prospects of functional tourmaline composites[J]. Front Earth Sci, 2014, 21 (5): 331–337. |
| [16] |
郭昀, 夏义本, 闵嘉华, 等. 极性电气石衬底对ZnO纳米片生长的影响[J].
无机材料学报, 2010, 25 (7): 717–720.
GUO Y, XIA Y B, MIN J H, et al. Influence of polar tourmaline substrates on the growth of ZnO nanoplates[J]. Journal of Inorganic Materials, 2010, 25 (7): 717–720. |
| [17] | ZHANG G, QIN X. Efficient photocatalytic degradation of gaseous formaldehyde by the TiO2/tourmaline composites[J]. Materials Research Bulletin, 2013, 48 (10): 3743–3749. DOI: 10.1016/j.materresbull.2013.05.112 |
| [18] | SONG S H, KANG M. Decomposition of 2-chlorophenol using a tourmaline photocatalytic system[J]. Journal Industrial Engineering Chemistry, 2008, 14 : 785–791. DOI: 10.1016/j.jiec.2008.05.002 |
| [19] | LIU W C. Enhanced photocatalytic activity of nanoscaled TiO2 by natural schorl[D]. Harbin: Harbin University of Science and Technology, 2014. |
| [20] | LIU S, TIAN J, WANG L, et al. One-pot synthesis of CuO nanoflower-decorated reduced graphene oxide and its application to photocatalytic degradation of dyes[J]. Catalysis Science & Technology, 2012, 2 : 339–344. |
| [21] | XU B H, LIN B Z, WANG Q Q, et al. Anatase TiO2-pillared hexaniobate mesoporous nanocomposite with enhanced photo-catalytic activity[J]. Microporous and Mesoporous Materials, 2012, 147 (1): 79–85. DOI: 10.1016/j.micromeso.2011.06.003 |
 2019, Vol. 47
2019, Vol. 47


