文章信息
- 黄贤凯, 邵泽超, 常增花, 王建涛
- HUANG Xian-kai, SHAO Ze-chao, CHANG Zeng-hua, WANG Jian-tao
- 导电炭黑对富锂锰基层状氧化物电极性能的影响
- Effect of conductive carbon black on electrochemical performance of Li- and Mn-rich layered oxide electrode
- 材料工程, 2019, 47(8): 13-21
- Journal of Materials Engineering, 2019, 47(8): 13-21.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000129
-
文章历史
- 收稿日期: 2019-02-17
- 修订日期: 2019-04-28
2. 国联汽车动力电池研究院有限责任公司, 北京 101400
2. China Automotive Battery Research Institute Co., Ltd., Beijing 101400, China
随着电动汽车的快速发展,锂离子电池受到了越来越多的关注[1],同时也对锂离子电池的能量密度、循环寿命、安全性及成本提出了更高的要求[2-3]。富锂锰基层状氧化物xLi2MnO3·(1-x)LiMO2(其中M=Co,Ni,Mn等,0<x<1)因具有较高的比容量、较低的原材料成本等优势[4]而被认为是下一代高比能量液态锂离子电池首选正极材料。然而,富锂锰基层状氧化物在实际应用中仍存在一些亟须解决的问题,例如材料的首次库仑效率偏低、充放电循环过程中存在电压衰减、大电流性能差等[5]。针对这些问题,研究者们从材料的组成及结构角度出发,提出了一系列有针对的解决方法,包括组分调制、体相掺杂、表面改性和材料复合等[6],这些方法也在一定程度上能够改善富锂锰基层状氧化物的电化学性能,使富锂锰基层状氧化物从材料开发走向了锂离子电池电极应用开发,为更高比能量液态离子电池的开发提供了坚实的材料研究基础。
在锂离子电池正极电极开发过程中,由于锂离子电池中所采用的正极活性材料(磷酸铁锂、三元材料等)的电子导电性均较差,因此,在锂离子电池正极制备过程中需要添加适量的导电添加剂以提高电极的电子电导率[7-8]。在电极充放电过程中,导电添加剂的使用可以为电子提供快速传输通道,从而能够实现活性材料颗粒之间及活性材料与集流体之间的电子快速转移,有利于电池电化学性能的提升。现有的商业化导电添加剂中,导电炭黑Super P具有比表面积大、电导率高、价格低廉等优点,使其成为锂离子电池中最常用的基础导电添加剂。导电炭黑不仅被广泛应用于LiCoO2[9],LiFePO4[10-11],LiMn2O4[12]等正极中,也被用于石墨[13]和硅[14]负极中,以提高电极的电化学性能。Qi等[15]研究发现LiFePO4正极性能与所使用炭黑导电剂的颗粒尺寸及比表面积存在一定关系,他们认为具有更大比表面积的炭黑与活性材料颗粒之间的接触更多,但Super P表面积大的炭黑颗粒尺寸较小,易阻塞电极的孔隙,不利于电解液浸润电极。Maeyoshi等[16]则发现炭黑导电剂的比表面积还会影响电极表面的副反应,从而影响电极的性能。Oh等[17]用球磨的方法将乙炔黑包覆在LiMnPO4颗粒上,发现适量乙炔黑的包覆可以减少Mn的溶解,并能提高电子电导率,降低电荷转移阻抗,从而提高了电极的电化学性能。Song等[18]将Super P通过湿法包覆在富锂锰基材料Li(Li0.2Mn0.54Ni0.13Co0.13)O2表面上,发现富锂材料表面形成了尖晶石相,从而提高了材料的容量和倍率性能。另外,在复合导电剂的应用中,炭黑也是必不可少的组分,例如炭黑与石墨烯复合[19-20],炭黑与碳纳米管复合[21],炭黑与碳纤维复合[22]等等。在实际的电极构筑过程中,若电极中导电添加剂用量过少,则不足以在电极中形成有效的电子导电网络,从而会出现活性材料颗粒被孤立的现象,影响电池容量的发挥[23];而导电添加剂在电极中为非活性物质,若在电极中用量过多不仅会增加材料成本,更重要的是会降低电池的能量密度[24]。对于导电性较差的富锂锰基层状氧化物而言,在电极中导电剂的合理使用对改善电极的大电流充放电性能尤为重要,因此本工作使用交流阻抗谱等技术手段,探究了Super P添加量对高电压富锂锰基层状氧化物电极电化学稳定性、倍率性能以及电极极化的影响,以期获得Super P添加量的优选,并利用交流阻抗谱等技术手段研究其内在过程机理。
1 实验材料与方法选用江西江特公司生产的RM-1C型无钴富锂锰基层状氧化物作为正极活性材料,选用瑞士特密高公司生产的Super P作为主要导电剂,选用天津贝特瑞公司生产的中间相碳微球(MCMB)作为补充导电剂,选用聚偏二氟乙烯(PVDF)作为黏结剂,正极活性材料、导电剂和黏结剂以质量比90:6:4的比例混合(Super P与MCMB的质量比分别为2:4,3:3,4:2,5:1,6:0,5组电极的名称分别记作LR-2SP,LR-3SP,LR-4SP,LR-5SP,LR-6SP,其中Super P含量分别为2%,3%,4%,5%,6%),分散于N-甲基吡咯烷酮中,混合均匀,然后将所得浆料按照相同的面密度(12mg·cm-2)涂覆在铝箔上,置于80℃的烘箱中干燥3h,使用冲片机制得直径14mm的圆极片,将圆极片辊压至相同的压实密度(2.8g·cm-3),置于100℃的真空烘箱中干燥8h,得到富锂锰基层状氧化物电极极片。以所得极片为工作电极,金属锂为对电极,Celgard2300聚丙烯薄膜为隔膜,滴加适量电解液,在氩气气氛的手套箱(O2和H2O体积分数均小于10-7)中,组装得到CR2032扣式电池。使用CT2001A LAND电池测试系统,以0.1C的电流密度(1C=200mAh·g-1),在2.0~4.8 V的电压范围内对扣式电池进行两周充放电活化,然后在2.0~4.7V的电压范围内以1C放电电流进行循环性能测试, 以不同大小的放电电流进行倍率性能测试。在PGSTAT302N型电化学工作站上进行交流阻抗(EIS)测试,测试频率为105~10-2Hz,交流电压的扰动振幅为5mV。所有的电化学测试均在室温下进行。使用Smart Lab 9KW型X射线衍射仪表征富锂锰基层状氧化物的晶体结构,使用S-4800型场发射扫描电镜观察材料及电极的形貌,并使用扫描电镜所配套的X射线能谱仪(EDS)分析电极的元素分布。
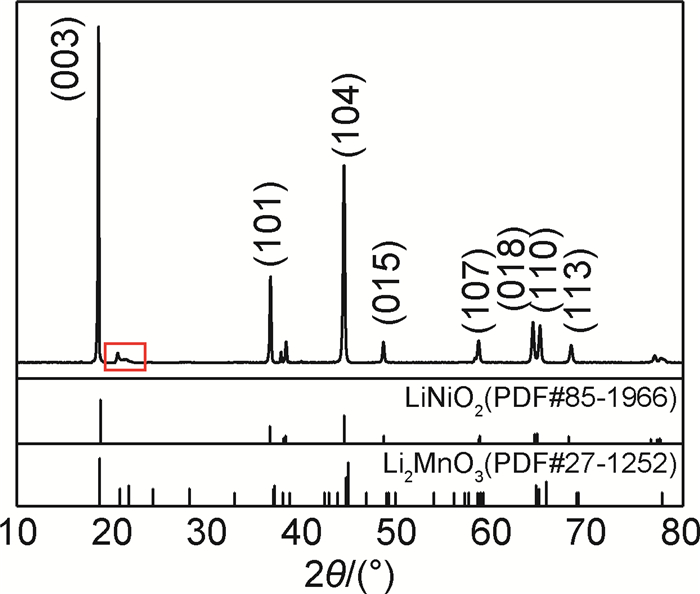
2 结果与分析图 1为RM-1C富锂锰基层状氧化物的XRD图谱。物相分析表明,RM-1C富锂锰基正极材料的XRD图谱的各特征峰与标准卡片LiNiO2(PDF#85-1966)基本相符,为六方晶系的层状岩盐α-NaFeO2结构,空间群为R-3m[25],在65°附近出现的(018)和(110)两个衍射峰发生明显的劈裂,说明该材料具有良好的层状结构。在20°~25°之间存在微弱的衍射峰,这与LiMn6超晶格结构有关,属于C2/m空间群Li2MnO3结构(Li2MnO3(PDF#27-1252))[26]。
|
图 1 RM-1C富锂锰基层状氧化物的XRD图谱 Fig. 1 XRD patterns for RM-1C Li- and Mn-rich layered oxide |
图 2为RM-1C富锂锰基层状氧化物、Super P和MCMB的扫描电镜图片。从图 2(a)可以看出,富锂锰基层状氧化物的一次颗粒尺寸主要分布在0.5~1.1μm范围内,二次颗粒为无规则形状(如图 2(a)虚线部分)。Super P是由尺寸分布在35~60nm范围内的小颗粒聚集而成的团聚体(图 2(b)),而MCMB的形貌则为类球体,颗粒尺寸分布在5~17μm范围内(图 2(c))。图 3为5组电极极片的扫描电镜图,可以看出,尺寸较小的Super P覆盖在RM-1C活性材料颗粒表面,与活性材料有较好的接触,但MCMB颗粒的尺寸较大,与活性材料并未有较好的接触,如图 3(a)所示。图 4为与图 3中LR-2SP(图 3(a)),LR-3SP(图 3(b)),LR-4SP(图 3(c)),LR-5SP(图 3(d)),LR-6SP(图 3(e))电极扫描电镜图片相对应的EDS面扫图片(红色点、绿色点和黄色点分别对应于碳元素、氧元素和锰元素),从图 3和图 4可以看出,在2%~5%(质量分数,下同)范围内,Super P添加量越多,电极极片中的Super P颗粒越多,Super P颗粒与活性材料颗粒之间的接触点也越多。然而,当Super P添加量达到6%时,电极中出现了Super P颗粒大范围团聚的现象(如图 3(e)红色虚线部分所示),从EDS面扫图中也可以证实(如图 4(e-1),(e-3)虚线部分所示)。

|
图 2 RM-1C富锂锰基层状氧化物(a)、Super P(b)以及MCMB(c)扫描电镜图片 Fig. 2 SEM images of RM-1C Li- and Mn-rich layered oxide (a), Super P (b) and MCMB (c) |

|
图 3 5组电极的扫描电镜图片 (a)LR-2SP; (b)LR-3SP; (c)LR-4SP; (d)LR-5SP; (e)LR-6SP Fig. 3 SEM images of the five electrodes (a)LR-2SP; (b)LR-3SP; (c)LR-4SP; (d)LR-5SP; (e)LR-6SP |

|
图 4 5组电极的能量色散X射线谱元素面扫图片 (1)碳元素; (2)氧元素; (3)锰元素 Fig. 4 Energy dispersive X-ray spectrometry element mapping images of the five electrodes (1)C element; (2)O element; (3)Mn element (a)LR-2SP; (b)LR-3SP; (c)LR-4SP; (d)LR-5SP; (e)LR-6SP |
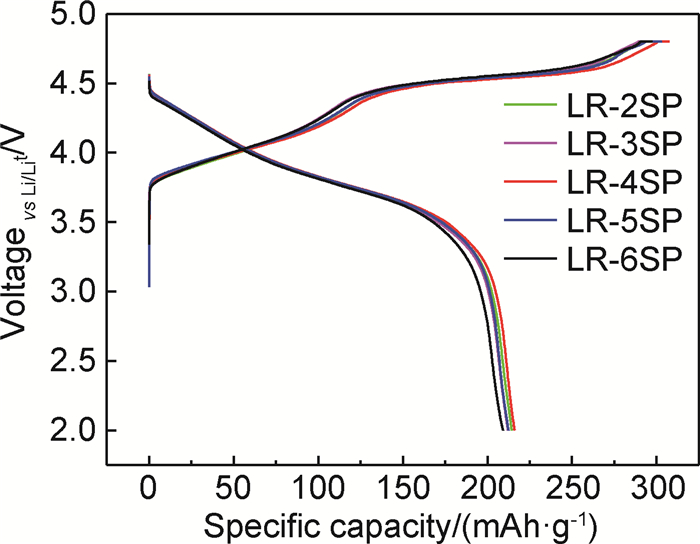
图 5为不同Super P添加量的富锂锰基层状氧化物电极在0.1C电流密度下活化首周的充放电曲线图。不同Super P添加量的电极首周充放电曲线相似,其首周充电曲线在4.45V以下为一段斜线,对应于Ni2+→Ni4+转化的过程,在4.45V以上为一电压平台,对应于Li2MnO3组分的活化过程,通过该组分的活化为材料提供了更多的容量[27];首周放电曲线可分为3段,即4.1V以上、4.1~3.5V之间以及3.5V以下,分别对应于O-→O2-,Ni4+→Ni2+和Mn4+→Mn3+的转化过程[28-29]。不同Super P添加量的电极充放电曲线显示,在一定的Super P添加量范围内,Super P添加量对富锂锰基层状氧化物电极的首周容量影响不大。
|
图 5 0.1C倍率下的活化首周充放电曲线(1C=200mAh·g-1) Fig. 5 Initial activated charge and discharge curves at 0.1C rate (1C=200mAh·g-1) |
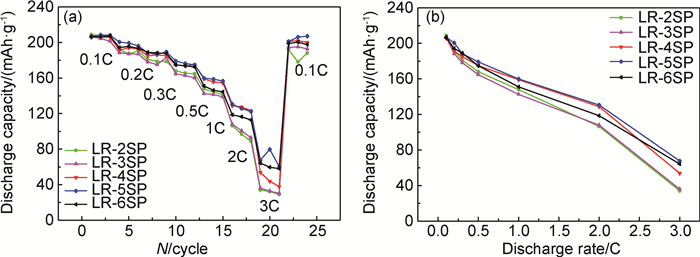
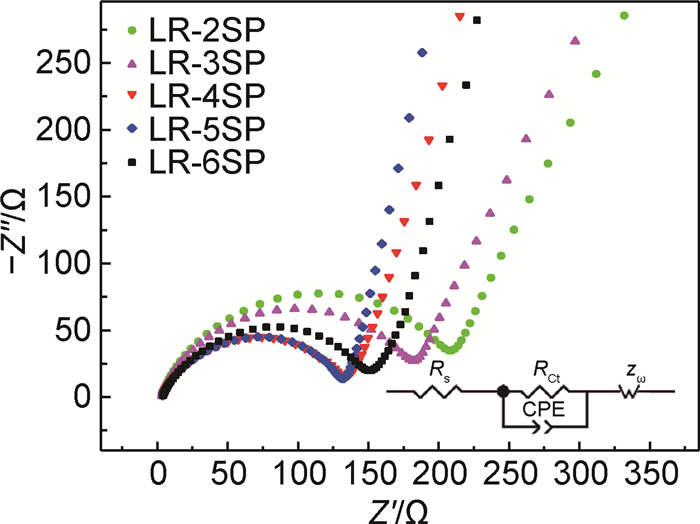
为了研究Super P添加量对富锂锰基层状氧化物电极倍率性能的影响,本工作比较了各组电极在0.1C至3C的放电比容量。如图 6所示,在3C下,LR-2SP,LR-3SP,LR-4SP,LR-5SP,LR-6SP的放电比容量分别为34.0,36.0,53.8,67.7,64.3mAh·g-1,说明在2%~6%范围内,富锂锰基电极的高倍率性能随Super P添加量的增加而先提高后降低,添加5%Super P电极的高倍率性能最优(其在1C和3C的放电比容量分别为159.8mAh·g-1和67.7mAh·g-1,3C放电比容量为1C放电比容量的42.4%)。为了探究这种规律的原因,对充放电循环前的扣式电池进行了交流阻抗测试,结果如图 7所示。5组样品的交流阻抗谱图均由高频区的一个圆弧及低频区的斜线组成,高频区圆弧对应于电极的电荷转移阻抗,低频区斜线对应于锂离子在活性材料中的扩散阻抗[30],根据图 7中所示的等效电路使用Zview软件进行了模拟,得到LR-2SP,LR-3SP,LR-4SP,LR-5SP,LR-6SP的电荷转移阻抗分别为202.9,178.9,135.1,131.3,155.0Ω。由于正极活性材料与Super P颗粒为“点-点”接触[31],电极中Super P添加量越多,正极材料颗粒与Super P颗粒的接触点越多,电极的阻抗越小,因而倍率性能越好;当Super P添加量超过5%时,增加Super P添加量并不能进一步改善电极的性能,这是由于电极中Super P过多,Super P颗粒之间的团聚现象加剧(如图 3(e)所示),从而增大了电极的阻抗,降低了电极的倍率性能。
|
图 6 电极的倍率性能(1C=200mAh·g-1) (a)在不同放电倍率下循环3周的放电比容量;(b)在不同倍率下的首周放电比容量 Fig. 6 Rate performance of the electrodes (1C=200mAh·g-1) (a)discharge capacity during 3 cycles at different rates; (b)initial discharge capacity at different rates |
|
图 7 充放电循环前的电极交流阻抗谱(插图为相对应的等效电路) Fig. 7 Electrode impedance spectroscopy before charge-discharge cycle (the inset is the corresponding equivalent circuit) |
图 8比较了不同Super P添加量的富锂锰基层状氧化物电极在1C放电倍率下的循环性能。在充放电循环200周之后,5组电极LR-2SP,LR-3SP,LR-4SP,LR-5SP,LR-6SP的放电比容量分别为40.5,70.8,94.0,112.4,89.0mAh·g-1,容量保持率分别为25.6%,44.2%,55.9%,68.6%,54.2%。LR-5SP电极的容量保持率最高,与LR-2SP和LR-6SP电极相比,其容量保持率分别提高了43.0%和14.4%。由此可知,在2%~5%范围内,增加Super P的添加量可以提高电极的容量保持率,提升电极的循环性能,但当Super P添加量超过5%时,增加Super P添加量并不利于电极循环性能的提升。

|
图 8 电极的循环性能(1C=200mAh·g-1) (a)放电比容量; (b)容量保持率 Fig. 8 Cycle performance of the electrodes (1C=200mAh·g-1) (a)discharge capacity; (b)capacity retention |
为了探究Super P添加量影响电极循环性能的原因,图 9比较了不同Super P添加量的富锂锰基层状氧化物电极在充放电循环过程中放电初始阶段的欧姆降及充放电平均电压差。欧姆降是由电池的欧姆极化引起的,其反映了电池组分(包括电极材料、电解液、隔膜等)的电阻及各组分之间的接触电阻[32-33],本工作5组电池主要体现在接触电阻的差异。充放电平均电压差是指同一充放电循环中充电过程的平均电压与放电过程的平均电压之间的差值,其数值的变化反映了电极极化的变化[34-35]。从图 9(a)可以看出,在富锂锰基层状氧化物电极循环过程中,尤其是循环75周之后,5组电极的欧姆降呈现的规律为:LR-2SP>LR-3SP>LR-4SP>LR-6SP>LR-5SP,即在2%~5%范围内,增加Super P添加量可以降低电极的欧姆降,当Super P添加量超过5%时,增加Super P添加量反而会提高电极的欧姆降。从图 9(b)可以看出,Super P添加量在2%~6%范围内,电极的充放电平均电压差随Super P添加量增加也呈先降低后升高的趋势,其中LR-5SP的充放电平均电压差最小。在一定范围内提高电极中的Super P添加量,可以在活性材料颗粒与集流体之间、活性材料颗粒之间搭建更多的电子传输通道,有利于降低电极内部的接触电阻,降低电极的极化,从而有利于改善电极的循环性能;但Super P添加量过高则易于发生团聚,破坏了电极中的电子导电网络,从而影响了电极循环性能的提升[36]。

|
图 9 电极在循环过程中的欧姆降(a)和充放电平均电压差(b) Fig. 9 IR drop (a) and the difference between the average charge voltage and the average discharge voltage (b) for the electrodes during the cycling process |
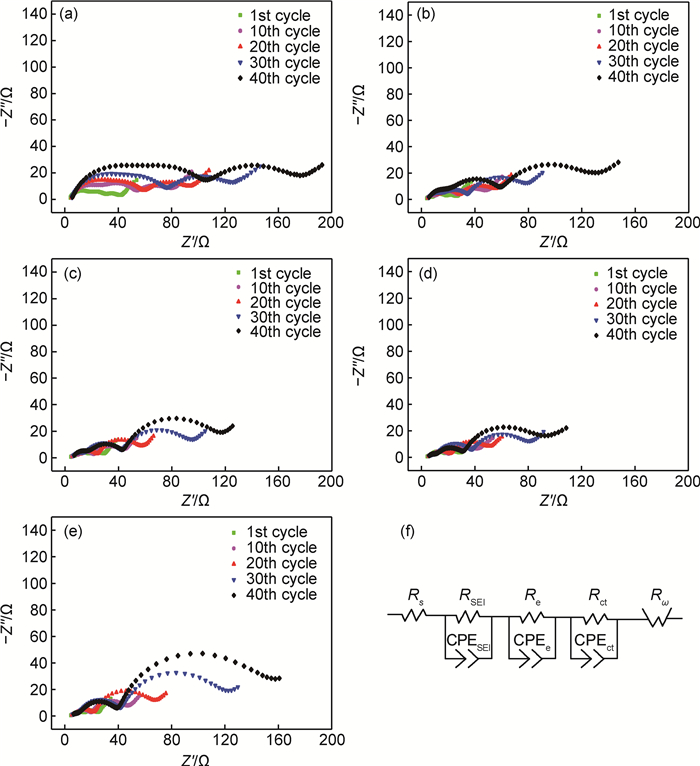
图 10(a)~(e)中给出了5组样品在不同充放电循环周数的交流阻抗谱(测试时电池的荷电状态为50%),这些交流阻抗谱均由3个圆弧以及一段斜线组成,其中,高频区圆弧对应于活性材料与电解液之间的界面膜阻抗RSEI,中高频区圆弧对应于电子通过活性材料的阻抗Re,中频区圆弧对应于电荷转移阻抗Rct,低频区斜线对应于锂离子在活性材料中的扩散阻抗[37]。随着循环周数的增加,电极阻抗不断增大,这可能是由活性材料颗粒表面钝化膜的不断增长及电极组分之间的电接触的破坏等原因造成的[38-39]。采用如图 10(f)所示的等效电路对5组样品不同充放电循环周数的交流阻抗谱进行了模拟,电荷转移阻抗结果示于表 1。其中,充放电循环第40周时5组样品LR-2SP,LR-3SP,LR-4SP,LR-5SP,LR-6SP的电荷转移阻抗分别为90.3,89.0,83.3,67.5,127.3Ω。对比5组样品在充放电循环中的变化趋势,可以看到,在2%~5%范围内,Super P添加量较多的电极在循环过程中阻抗增加较缓慢,但LR-6SP的阻抗增大速率较LR-5SP有所提升,这与其循环性能相符合。添加5% Super P的电极在循环过程中阻抗增大速度最缓慢,循环第40周的阻抗最小,其电极中电子导电网络最完整,因而具有最优的循环性能。
|
图 10 LR-2SP(a), LR-3SP(b), LR-4SP(c), LR-5SP(d), LR-6SP(e)电极在不同循环周数的交流阻抗谱及等效电路图(f) Fig. 10 AC impedance plots for LR-2SP(a), LR-3SP(b), LR-4SP(c), LR-5SP(d), LR-6SP(e) electrodes at different cycles and the equivalent circuit(f) |
| N/cycle | Rct/Ω | ||||
| LR-2SP | LR-3SP | LR-4SP | LR-5SP | LR-6SP | |
| 1 | 8.82 | 5.53 | 8.54 | 8.73 | 7.87 |
| 10 | 26.0 | 18.1 | 19.3 | 17.8 | 24.9 |
| 20 | 41.4 | 35.2 | 39.2 | 33.9 | 51.9 |
| 30 | 67.3 | 63.7 | 60.7 | 50.8 | 87.8 |
| 40 | 90.3 | 89.0 | 83.3 | 67.5 | 127.3 |
(1) 在富锂锰基层状氧化物电极中,Super P添加量从2%提高至5%,有利于增加与富锂锰基层状氧化物颗粒之间的电接触,从而在电极中构建更为完善的电子导电网络,降低电极内部组分之间的阻抗,减小电极的欧姆降及极化,进而可以提高电极的循环性能和倍率性能。
(2) 当Super P添加量超过5%时,继续添加Super P并不能进一步改善电极的性能,这是由于电极中Super P过多,Super P颗粒之间易于发生大范围团聚,不利于充分发挥Super P的导电作用,导致电极的电化学性能降低。
(3) 添加5% Super P的富锂锰基层状氧化物电极阻抗最小,具有最优电化学性能,在3C放电倍率下的容量为67.7mAh·g-1,在1C放电倍率下充放电循环200周后的电极剩余容量为112.4mAh·g-1,容量保持率为68.6%。
(4) 在充放电循环过程中,添加5% Super P的富锂锰基层状氧化物电极,其交流阻抗随循环周数的增加变化最缓慢,且具有最小的极化,这与其优异的电化学性能相一致。
| [1] | NITTA N, WU F, LEE J T, et al. Li-ion battery materials:present and future[J]. Materials Today, 2015, 18 (5): 252–264. DOI: 10.1016/j.mattod.2014.10.040 |
| [2] | DIOUF B, PODE R. Potential of lithium-ion batteries in renewable energy[J]. Renewable Energy, 2015, 76 : 375–380. DOI: 10.1016/j.renene.2014.11.058 |
| [3] | MEISTER P, JIA H, LI J, et al. Best practice:performance and cost evaluation of lithium ion battery active materials with special emphasis on energy efficiency[J]. Chemistry of Materials, 2016, 28 (20): 7203–7217. DOI: 10.1021/acs.chemmater.6b02895 |
| [4] | ZHANG X, SHI J, LIANG J, et al. Suppressing surface lattice oxygen release of Li-rich cathode materials via heterostructured spinel Li4Mn5O12 coating[J]. Advanced Materials, 2018, 30 (29): 1801751. DOI: 10.1002/adma.201801751 |
| [5] | MANTHIRAM A, KNIGHT J C, MYUNG S, et al. Nickel-rich and lithium-rich layered oxide cathodes:progress and perspectives[J]. Advanced Energy Materials, 2016, 6 (1): 1501010. DOI: 10.1002/aenm.201501010 |
| [6] | NAYAK P K, ERICKSON E M, SCHIPPER F, et al. Review on challenges and recent advances in the electrochemical performance of high capacity Li- and Mn-rich cathode materials for Li-ion batteries[J]. Advanced Energy Materials, 2018, 8 (8): 1702397. DOI: 10.1002/aenm.201702397 |
| [7] | BAUER W, NÖTZEL D, WENZEL V, et al. Influence of dry mixing and distribution of conductive additives in cathodes for lithium ion batteries[J]. Journal of Power Sources, 2015, 288 : 359–367. DOI: 10.1016/j.jpowsour.2015.04.081 |
| [8] | NING G, ZHANG S, XIAO Z, et al. Efficient conducting networks constructed from ultra-low concentration carbon nanotube suspension for Li ion battery cathodes[J]. Carbon, 2018, 132 : 323–328. DOI: 10.1016/j.carbon.2018.02.056 |
| [9] | NISHI T, NAKAI H, KITA A. Visualization of the state-of-charge distribution in a LiCoO2 cathode by in situ Raman imaging[J]. Journal of the Electrochemical Society, 2013, 160 (10): A1785–A1788. DOI: 10.1149/2.061310jes |
| [10] | GUO H, SONG X, ZHENG J, et al. Excess lithium storage in LiFePO4-carbon interface by ball-milling[J]. Functional Mate-rials Letters, 2016, 9 (5): 1650053. DOI: 10.1142/S1793604716500533 |
| [11] | LI Y, MEYER S, LIM J, et al. Effects of particle size, electronic connectivity, and incoherent nanoscale domains on the sequence of lithiation in LiFePO4 porous electrodes[J]. Advanced Mate-rials, 2015, 27 (42): 6591–6597. DOI: 10.1002/adma.201502276 |
| [12] | LIU Z, HAN K, CHEN-WIEGART Y K, et al. X-ray nanoto-mography analysis of the microstructural evolution of LiMn2O4 electrodes[J]. Journal of Power Sources, 2017, 360 : 460–469. DOI: 10.1016/j.jpowsour.2017.06.027 |
| [13] | BUROW D, SERGEEVA K, CALLES S, et al. Inhomogeneous degradation of graphite anodes in automotive lithium ion batteries under low-temperature pulse cycling conditions[J]. Journal of Power Sources, 2016, 307 : 806–814. DOI: 10.1016/j.jpowsour.2016.01.033 |
| [14] | LI X, YAN C, WANG J, et al. Stable silicon anodes for lithium-ion batteries using mesoporous metallurgical silicon[J]. Adva-nced Energy Materials, 2015, 5 (4): 1401556. DOI: 10.1002/aenm.201401556 |
| [15] | QI X, BLIZANAC B, DUPASQUIER A, et al. Understanding the influence of conductive carbon additives surface area on the rate performance of LiFePO4 cathodes for lithium ion batteries[J]. Carbon, 2013, 64 : 334–340. DOI: 10.1016/j.carbon.2013.07.083 |
| [16] | MAEYOSHI Y, MIYAMOTO S, MUNAKATA H, et al. Effect of conductive carbon additives on electrochemical performance of LiCoPO4[J]. Journal of Power Sources, 2018, 376 : 18–25. DOI: 10.1016/j.jpowsour.2017.11.059 |
| [17] | OH S M, OH S W, YOON C, et al. High-performance carbon-LiMnPO4 nanocomposite cathode for lithium batteries[J]. Advanced Functional Materials, 2010, 20 (19): 3260–3265. DOI: 10.1002/adfm.201000469 |
| [18] | SONG B, LIU H, LIU Z, et al. High rate capability caused by surface cubic spinels in Li-rich layer-structured cathodes for Li-ion batteries[J]. Scientific Reports, 2013, 3 : 3094. DOI: 10.1038/srep03094 |
| [19] | TANG R, YUN Q, LV W, et al. How a very trace amount of graphene additive works for constructing an efficient conductive network in LiCoO2-based lithium-ion batteries[J]. Carbon, 2016, 103 : 356–362. DOI: 10.1016/j.carbon.2016.03.032 |
| [20] | SHI Y, WEN L, PEI S, et al. Choice for graphene as conductive additive for cathode of lithium-ion batteries[J]. Journal of Energy Chemistry, 2019, 30 : 19–26. DOI: 10.1016/j.jechem.2018.03.009 |
| [21] | DENG Y, ZHANG Q, SHI Z, et al. Synergies of the crystallinity and conductive agents on the electrochemical properties of the hollow Fe3O4 spheres[J]. Electrochimica Acta, 2012, 76 : 495–503. DOI: 10.1016/j.electacta.2012.05.071 |
| [22] | CHO I, CHOI J, KIM K, et al. A comparative investigation of carbon black(Super P)and vapor-grown carbon fibers(VGCFs)as conductive additives for lithium-ion battery cathodes[J]. Rsc Advances, 2015, 5 (115): 95073–95078. DOI: 10.1039/C5RA19056H |
| [23] | NARAYANRAO R, JOGLEKAR M M, INGUVA S. A phenomenological degradation model for cyclic aging of lithium ion cell materials[J]. Journal of the Electrochemical Society, 2013, 160 (1): A125–A137. DOI: 10.1149/2.013302jes |
| [24] | JI X, NAZAR L F. Advances in Li-S batteries[J]. Journal of Materials Chemistry, 2010, 20 (44): 9821–9826. DOI: 10.1039/b925751a |
| [25] | ZHONG Z, YE N, WANG H, et al. Low temperature combustion synthesis and performance of spherical 0.5Li2MnO3-LiNi0.5Mn0.5O2 cathode material for Li-ion batteries[J]. Chemical Engineering Journal, 2011, 175 : 579–584. DOI: 10.1016/j.cej.2011.09.112 |
| [26] | LIN J, MU D, JIN Y, et al. Li-rich layered composite Li[Li0.2Ni0.2Mn0.6]O2 synthesized by a novel approach as cathode material for lithium ion battery[J]. Journal of Power Sources, 2013, 230 : 76–80. DOI: 10.1016/j.jpowsour.2012.12.042 |
| [27] |
严武渭, 柳永宁, 崇少坤, 等. 高能量密度锂离子电池用富锂正极材料[J].
化学进展, 2017, 29 (2/3): 198–209.
YAN W W, LIU Y N, CHONG S K, et al. Lithium-rich cathode materials for high energy-density lithium-ion batteries[J]. Progress in Chemistry, 2017, 29 (2/3): 198–209. |
| [28] | LI X, QIAO Y, GUO S, et al. Direct visualization of the revers-ible O2-/O- redox process in Li-rich cathode materials[J]. Advanced Materials, 2018, 30 (14): 1705197. DOI: 10.1002/adma.201705197 |
| [29] | GUO S, ZHAO S, BI K, et al. Research on electrochemical properties and fade mechanisms of Li-rich cathode materials at low-temperature[J]. Electrochimica Acta, 2016, 222 : 1733–1740. DOI: 10.1016/j.electacta.2016.11.168 |
| [30] | CHONG S, CHEN Y, YAN W, et al. Suppressing capacity fading and voltage decay of Li-rich layered cathode material by a surface nano-protective layer of CoF2 for lithium-ion batteries[J]. Journal of Power Sources, 2016, 332 : 230–239. DOI: 10.1016/j.jpowsour.2016.09.028 |
| [31] | SU F, YOU C, HE Y, et al. Flexible and planar graphene conductive additives for lithium-ion batteries[J]. Journal of Materials Chemistry, 2010, 20 (43): 9644–9650. DOI: 10.1039/c0jm01633k |
| [32] | LIU C, NEALE Z G, CAO G. Understanding electrochemical potentials of cathode materials in rechargeable batteries[J]. Materials Today, 2016, 19 (2): 109–123. DOI: 10.1016/j.mattod.2015.10.009 |
| [33] | XIA M, LIU Q, ZHOU Z, et al. A novel hierarchically structured and highly hydrophilic poly(vinyl alcohol-co-ethylene)/poly(ethylene terephthalate) nanoporous membrane for lithium-ion battery separator[J]. Journal of Power Sources, 2014, 266 : 29–35. DOI: 10.1016/j.jpowsour.2014.04.151 |
| [34] | WANG L, ZHANG B, PANG J, et al. Aging process analysis of LiNi0.88Co0.09Al0.03O2/graphite-SiOx pouch cell[J]. Electroch-imica Acta, 2018, 286 : 219–230. DOI: 10.1016/j.electacta.2018.07.224 |
| [35] | XU J, DESHPANDE R D, PAN J, et al. Electrode side reactions, capacity loss and mechanical degradation in lithium-ion batteries[J]. Journal of the Electrochemical Society, 2015, 162 (10): A2026–A2035. DOI: 10.1149/2.0291510jes |
| [36] | ZHANG H, ZHANG W, CHENG J, et al. Acetylene black agglomeration in activated carbon based electrochemical double layer capacitor electrodes[J]. Solid State Ionics, 2008, 179 (33): 1946–1950. |
| [37] |
庄全超, 徐守冬, 邱祥云, 等. 锂离子电池的电化学阻抗谱分析[J].
化学进展, 2010, 22 (6): 1044–1057.
ZHUANG Q C, XU S D, QIU X Y, et al. Electrochemical impedance spectroscopy in lithium ion batteries diagnosis[J]. Progress in Chemistry, 2010, 22 (6): 1044–1057. |
| [38] | BARRé A, DEGUILHEM B, GROLLEAU S, et al. A review on lithium-ion battery ageing mechanisms and estimations for automotive applications[J]. Journal of Power Sources, 2013, 241 : 680–689. DOI: 10.1016/j.jpowsour.2013.05.040 |
| [39] | VETTER J, NOVáK P, WAGNER M R, et al. Ageing mech-anisms in lithium-ion batteries[J]. Journal of Power Sources, 2005, 147 (1): 269–281. |
 2019, Vol. 47
2019, Vol. 47


