文章信息
- 王聃, 陶德华, 黄秀玲, 华子恺
- WANG Dan, TAO De-hua, HUANG Xiu-ling, HUA Zi-kai
- 聚甲基丙稀酸羟乙酯甘油凝胶仿软骨材料的制备与性能
- Preparation and properties of poly(hydroxyethyl methacrylate) glycerol gel as biomimetic cartilage replacement material
- 材料工程, 2019, 47(7): 71-75
- Journal of Materials Engineering, 2019, 47(7): 71-75.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000101
-
文章历史
- 收稿日期: 2019-01-28
- 修订日期: 2019-04-24
天然软骨由于炎症、磨损或突发外力创伤而受到损伤后,其本身的自我修复能力极其有限[1]。软骨损伤的临床治疗方法主要有清创法、微骨折术、软骨移植[2-4]等,但每种方法或多或少都有不足之处[5]。组织工程为其治疗提供了新的解决方案,通过利用种子细胞、诱导因子和生物支架结合的方式,形成一种有望修复软骨损伤的新途径[6-7]。其中水凝胶由于其良好的吸水性、释药性、可控的力学性能以及能填补任何形状缺损的优异可塑性,而成为仿软骨的选用材料之一[8]。
目前仿软骨材料主要可以分为天然高分子材料和人工合成高分子材料[9]。天然材料主要有透明质酸凝胶、藻酸盐类凝胶等[10-13]。Shi等[12]采用可作为关节腔滑液的透明质酸制备成凝胶,结合诱导因子在兔子体内成功促进软骨分化;尹合勇等[13]将软骨细胞载入藻酸盐凝胶,成功修复大鼠股骨滑车骨软骨缺损。人工合成高分子软骨材料则主要有:聚乙烯醇水凝胶、聚甲基丙稀酸羟乙酯水凝胶等[14-17]。Kobayashi等[16]制备了高含水量聚乙烯醇水凝胶用于修复兔膝关节半月板,证明了其用于治疗软骨损伤的可行性;Bostan等[17]采用甲基丙烯酸羟乙酯(HEMA)和丙烯酸共混制备水凝胶,发现了较为接近天然软骨的润滑性。为了改善单一凝胶某些性能(如硬度、弹性或对人体适应性等方面)的局限性,复合材料凝胶越发得到人们关注[18-19]。为了使研制的材料接近天然软骨,研究者们都试探加入各种不同的调聚剂,但这些调聚剂对人体是否会排异尚待进一步研究。此外,水作为凝胶的主要成分,在体内渗出流失后凝胶是否会变得太硬而失去弹性需进一步验证,关于合成仿软骨的硬度、弹性等重要力学性能,文献详细介绍较少。为此,开发一种人体相容、力学性能良好的凝胶材料是首要工作。聚甲基丙烯酸羟乙酯(PHEMA)是一种性能优异的医用高分子材料,曾经作为隐形眼镜的主要成分,其无毒性和生物相容性良好,不溶于水但亲水性强;其水凝胶内部的多孔结构有着良好的吸水性和弹性,表面质地光滑,但硬度大于天然软骨。采用甘油代替水作为一种硬度调节辅料,由于甘油是体内脂肪的主要代谢产物,其对人体无害且具有生物相容性[20-23]。由于PHEMA和甘油材料优异的性能,聚合而成的凝胶,将对生物相容性有利。
本工作采用HEMA和甘油为原材料,在水浴保温和引发剂条件下,对HEMA单体和甘油进行了聚合,形成了凝胶弹性体。用红外光谱表征了凝胶成分,并对其表面形貌、粗糙度、硬度、抗压性能和弹性等力学性能进行了考察。
1 实验材料与方法 1.1 原材料和试剂甲基丙烯酸羟乙酯(HEMA),分析纯,成都麦卡希试剂有限公司;丙三醇(医用甘油),商丘亮峰卫生用品有限公司;过硫酸铵((NH4)2S2O8),分析纯,成都金山化学试剂有限公司。
1.2 凝胶材料的制备在铝箔坩埚内注入HEMA和甘油,分别按照质量比1:1,1:2,1:3,1:5的比例混合,并加入0.2%(质量分数)引发剂过硫酸铵,将磁力搅拌子放入混合溶液中,将坩埚置于70℃恒温水浴的磁力搅拌器中,均匀搅拌使其预聚合约15min。待溶液至略微黏稠状时,取出搅拌子,70℃恒温水浴保温24~36h,至反应完成,得到制备的PHEMA凝胶人工仿软骨材料。
1.3 材料性能测试使用AVATAR370型傅里叶红外光谱仪对凝胶材料进行红外光谱分析,采用溴化钾压片法,在室温条件下,在4000~400cm-1光谱范围内记录所研究的PHEMA的傅里叶变换红外光谱,并与纯HEMA单体的红外光谱进行对比分析。
使用Leica DCM8型激光共聚焦显微镜,对新制备凝胶表面进行形貌观察。使用形貌分析软件,分别对每一组凝胶表面进行粗糙度测量。
鉴于合成的仿软骨较软,通常硬度仪难于测量。因此本工作采用了改良的润滑脂针入度测试仪,参照GB/T 4985-2010,用2mm麻花钻头作为测量部件替代了原有针状部件作为改良,针入度数值越大表明材质越软。改良的针入度仪可以对凝胶材料及天然软骨的硬度作出横向比对。选取猪的膝关节软骨作为参照物,使用针入度仪对每个样品和软骨的随机5个点进行测量,并取平均值,任意两点间隔大于5mm。作图分析不同比例样品硬度变化趋势,并通过与天然猪软骨对比,选定较好的合成材料比例。
使用拉压力万能试验机对4组样品分别进行抗压和弹性恢复实验,对样品施加轴向压力,加载速率2mm/min,选取600~1000N不同的加载载荷,测定在不同载荷下样品变形量,分析不同混合比例的凝胶的抗压特性;载荷完全移除后,将受压样品静置3min,测量其样品厚度,分析每个样品的弹性恢复能力。
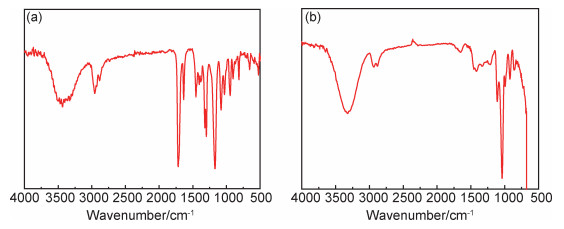
2 结果与分析 2.1 凝胶结构分析使用FTIR红外光谱仪对合成的PHEMA凝胶进行分析,如图 1所示。通过结果对比可以发现:首先凝胶体经过红外光谱测试,HEMA在1650cm-1处由于C=C键振动产生谱峰,如图 1(a)所示,而合成凝胶的谱图和单体谱比较,波长1650cm-1附近的谱峰消失,如图 1(b)所示,由此证明了反应物单体发生聚合;其次,凝胶体红外谱图基本和PHEMA标准谱图一致,证明了凝胶体成分为PHEMA;反应原料甘油大部分以游离状态存在于凝胶体内,其中也有很少部分可能和酯基发生酯交换,而使得红外图谱峰少许位移。
|
图 1 FTIR红外光谱(a)HEMA;(b)凝胶 Fig. 1 FTIR infrared spectroscopy (a)HEMA; (b)gel |
从宏观角度来看,随着甘油在凝胶中比例的不断增大,材料中白色部分逐渐褪去向透明转变,这可能是由于甘油的成分占据了凝胶材料大量空间结构,使得聚合物颜色变淡,如图 2所示(从左至右HEMA:甘油质量比范围为从1:1到1:5)。从微观角度上来看,使用激光共聚焦显微镜对合成软骨样品表面进行拍照观察,放大倍数为500倍,其结果如图 3,根据观察和测量结果,可以发现,随着甘油比例的增加,凝胶材料表面逐渐可以观察到越来越多的孔隙结构。粗糙度方面,HEMA与甘油质量比为1:1和1:2的凝胶粗糙度大致接近,如图 3(a),(b)所示,而随着甘油的增加,1:3和1:5凝胶粗糙度呈增加的趋势,如图 3(c),(d)所示。总体角度来说,甘油比例的增加引起了凝胶材料表面粗糙度的增加。该凝胶作为用于关节软骨的材料,较低的表面粗糙度将可以为关节提供更好的摩擦磨损性能,有效降低表面摩擦力,因此从粗糙度角度来看,HEMA与甘油比为1:1和1:2时较为合适。

|
图 2 PHEMA/甘油凝胶试样 Fig. 2 Samples of PHEMA/glycerol gel |

|
图 3 凝胶表面微观形貌观察(a)1:1;(b)1:2;(c)1:3;(d)1:5 Fig. 3 Observation of the surface morphology of the gel (a)1:1;(b)1:2;(c)1:3;(d)1:5 |
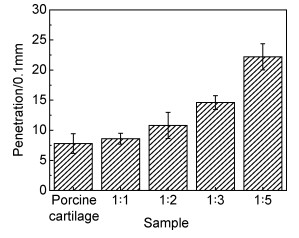
根据硬度测定的针入度曲线,可以观察到当HEMA与甘油质量比从1:1增加到1:5时,凝胶随着甘油比例的不断增高,制备成的材料硬度在逐渐降低,如图 4所示。通过对猪软骨的表面硬度使用同样方法进行测试,得到其表面针入度为0.6~1mm。因此,当比例在1:1~1:3的范围内,凝胶的针入度比较接近猪软骨。
|
图 4 凝胶硬度对比 Fig. 4 Gel hardness comparison |
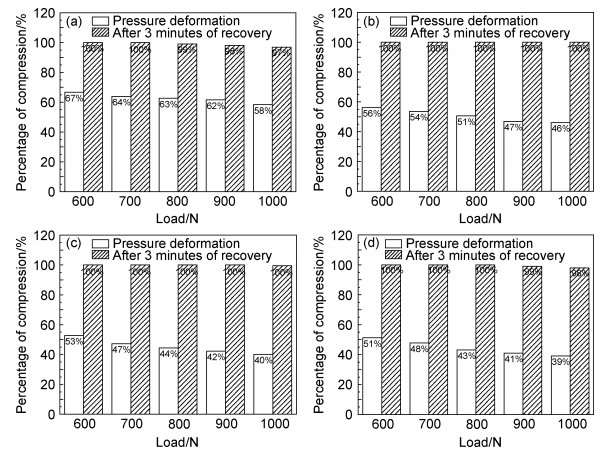
关节软骨在人体中有着缓冲运动压力、保护关节的作用,因此测定人工软骨的抗压性能和弹性是十分重要的[24]。图 5中(a)~(d)依次表示HEMA与甘油质量比为1:1~1:5,根据对比可以发现在受到600~1000N压力的情况下,所有凝胶变形量稳定在原有厚度的40%~70%,在受压后,并未观察到凝胶破裂现象。在移除载荷之后,将凝胶静置3min,可以发现凝胶逐渐恢复至原有厚度的97%~100%,由此证明凝胶的弹性良好。受压实验很好地显示了HEMA和甘油混合凝胶作为人工软骨材料具有很强的潜在可能性,在任何比例下,材料都可以为关节支撑提供良好的力学强度,在受压之后可以迅速恢复至原有结构,可以保证材料的生物力学结构。观察4个材料的受力变形图,当所受压力从600~1000N变化时,图 5(a)显示的1:1的材料维持原有形状的能力较好,抗压能力较强,可以为关节提供良好的力学环境,因此更适合于用作软骨支架材料。
|
图 5 凝胶受压及弹性恢复 (a)1:1;(b)1:2;(c)1:3;(d)1:5 Fig. 5 Gel compression and elastic recovery (a)1:1;(b)1:2;(c)1:3;(d)1:5 |
综上所述,随着甘油比例的增加,凝胶硬度下降,而表面粗糙度却趋向增加。在HEMA与甘油比例为1:1~1:3的条件下,凝胶的硬度较为接近猪软骨;在比例为1:1和1:2的条件下,凝胶较光滑粗糙度较低;综合硬度、弹性和抗压性来看,原材料质量比为1:1时制备的凝胶拥有较优的性能。
3 结论(1) HEMA单体与甘油在70℃衡温水浴和引发剂存在的条件下,可以聚合形成一种性能优异的凝胶结构,其材料有着良好的抗压性能和弹性。
(2) 广泛应用于隐形眼镜、口腔科修补的PHEMA,对人体无毒应用已久;而甘油作为体内脂肪的主要代谢产物又可为人体吸收,在HEMA单体与甘油的聚合凝胶体内能使硬度、弹性等力学性能相对于纯PHEMA得到改善。
(3) 当HEMA单体与甘油聚合材料的质量比为1:1时,得到的凝胶表面光滑粗糙度低,硬度接近天然软骨,抗压性能和弹性最好。
| [1] | JOHNSTONE B, ALINI M, CUCCHIARINI M, et al. Tissue engineering for articular cartilage repair-the state of the art[J]. European Cells & Materials, 2013, 25 (4): 248–267. |
| [2] | MITSUNORI K, MASASHI F, YOSUKE I, et al. Extra-arti-cular debridement of hip joint for management of anterior hip pain[J]. Arthroscopy Techniques, 2018, 7 (6): e651–e655. DOI: 10.1016/j.eats.2018.02.012 |
| [3] | ATILLA H A, LUO T D, STUBBS A J. Arthroscopic micro-fracture of hip chondral lesions[J]. Arthroscopy Techniques, 2017, 6 (6): e2295–e2299. DOI: 10.1016/j.eats.2017.08.040 |
| [4] | STONE A V, CHRISTIAN D R, REDONDO M L, et al. Osteo-chondral allograft transplantation and osteochondral autograft transfer[J]. Operative Techniques in Sports Medicine, 2018, 26 (3): 183–188. DOI: 10.1053/j.otsm.2018.06.007 |
| [5] | NUKAVARAPU S P, DORCEMUS D L. Osteochondral tissue engineering:current strategies and challenges[J]. Biotechnology Advances, 2013, 31 (5): 706–721. DOI: 10.1016/j.biotechadv.2012.11.004 |
| [6] | LIU Y, ZHOU G, CAO Y. Recent progress in cartilage tissue engineering-our experience and future directions[J]. Engineering, 2017, 3 (1): 28–35. DOI: 10.1016/J.ENG.2017.01.010 |
| [7] | TURNBULL G, CLARKE J, PICARD F, et al. 3D bioactive composite scaffolds for bone tissue engineering[J]. Bioactive Materials, 2018, 3 (3): 278–314. DOI: 10.1016/j.bioactmat.2017.10.001 |
| [8] | CHUANG E Y, CHIANG C W, WONG P C, et al. Hydrogels for the application of articular cartilage tissue engineering:a rev-iew of hydrogels[J]. Advances in Materials Science and Enginee-ring, 2018, 2018 : 1–13. |
| [9] | ARMIENTO A R, STODDART M J, ALINI M, et al. Biom-aterials for articular cartilage tissue engineering:learning from biology[J]. Acta Biomaterialia, 2018, 65 : 1–20. DOI: 10.1016/j.actbio.2017.11.021 |
| [10] | BERMEJO-VELASCO D, DOU W, HEERSCHAP A, et al. Injectable hyaluronic acid hydrogels with the capacity for mag-netic resonance imaging[J]. Carbohydrate Polymers, 2018, 197 : 641–648. DOI: 10.1016/j.carbpol.2018.06.028 |
| [11] | PARK H, LEE H J, AN H, et al. Alginate hydrogels modified with low molecular weight hyaluronate for cartilage regeneration[J]. Carbohydrate Polymers, 2017, 162 : 100–107. DOI: 10.1016/j.carbpol.2017.01.045 |
| [12] | SHI D, XU X, YE Y, et al. Photo-cross-linked scaffold with kar-togenin-encapsulated nanoparticles for cartilage regeneration[J]. ACS Nano, 2016, 10 : 1292–1299. DOI: 10.1021/acsnano.5b06663 |
| [13] |
尹合勇, 孙振, 李盼, 等. 微载体/水凝胶复合支架修复大鼠膝关节骨软骨缺损[J].
中国矫形外科杂志, 2016, 24 (16): 1492–1497.
YIN H Y, SUN Z, LI P, et al. Microcarrier/hydrogel com-posite scaffold for repair of articular cartilage defect in rat[J]. Orthopedic Journal of China, 2016, 24 (16): 1492–1497. |
| [14] | YARIMITSU S, SASAKI S, MURAKAMI T, et al. Evaluati-on of lubrication properties of hydrogel artificial cartilage mate-rials for joint prosthesis[J]. Biosurface and Biotribology, 2016, 2 (1): 40–47. DOI: 10.1016/j.bsbt.2016.02.005 |
| [15] | BAVARESCO V P, ZAVAGLIA C A C, REIS M C, et al. Study on the tribological properties of PHEMA hydrogels for use in artificial articular cartilage[J]. Wear, 2008, 265 (3/4): 269–277. |
| [16] | KOBAYASHI M, CHANG Y S, OKA M. A two year in vivo study of polyvinyl alcohol-hydrogel (PVA-H) artificial meniscus[J]. Biomaterials, 2005, 26 (16): 3243–3248. DOI: 10.1016/j.biomaterials.2004.08.028 |
| [17] | BOSTAN L, TRUNFIO-SFARGHIU A M, VERESTIUC L, et al. Mechanical and tribological properties of poly(hydroxyethyl methacrylate) hydrogels as articular cartilage substitutes[J]. Tribology International, 2012, 46 (1): 215–224. |
| [18] |
崔晓彤, 刘金龙, 张德坤, 等. 不同接触尺度下PVA/HA复合水凝胶的滑动摩擦行为[J].
材料工程, 2016, 44 (5): 59–64.
CUI X T, LIU J L, ZHANG D K, et al. Sliding friction beh-avior of PVA/HA composite hydrogels under different contac-ting scales[J]. Journal of Materials Engineering, 2016, 44 (5): 59–64. |
| [19] |
刘东, 赵孔银, 宋欢语, 等. 硅酸钙-海藻酸钙复合水凝胶膜的制备及表征[J].
复合材料学报, 2017, 34 (11): 2401–2406.
LIU D, ZHAO K Y, SONG H Y, et al. Preparation and characterization of calcium silicate-calcium alginate composite hydrogel film[J]. Acta Materiae Compositae Sinica, 2017, 34 (11): 2401–2406. |
| [20] | LUO Z, DENG X, HU H, et al. Preparation and properties of PHEMA hydrogel material[J]. Rare Metal Materials and Engineering, 2016, 45 (Suppl 1): 427–430. |
| [21] | PAULA V A, ANDREIA F R P, SILVA D, et al. Sur-face modification of an intraocular lens material by plasma-assisted grafting with 2-hydroxyethyl methacrylate (HEMA), for controlled release of moxifloxacin[J]. European Journal of Pharmaceutics and Biopharmaceutics, 2017, 120 : 52–62. DOI: 10.1016/j.ejpb.2017.08.006 |
| [22] | PASSOS M F, DIAS D R C, BASTOS G N T, et al. PHEMA hydrogels:synthesis, kinetics and in vitro tests[J]. Journal of Thermal Analysis and Calorimetry, 2016, 125 (1): 361–368. DOI: 10.1007/s10973-016-5329-6 |
| [23] | HERMANSYAH H, WIJANARKO A, DIANURSANTI D, et al. Kinetic model for triglyceride hydrolysis using lipase[J]. Makara Journal of Technology, 2010, 11 (1): 30–35. |
| [24] | FOX A J S, ASHEESH B, RODEO S A. The basic science of articular cartilage:structure, composition, and function[J]. Sports Health, 2009, 1 (6): 461–468. DOI: 10.1177/1941738109350438 |
 2019, Vol. 47
2019, Vol. 47


