文章信息
- 韩栋, 张宝林, 苏礼超, 韩贵华, 汪晟
- HAN Dong, ZHANG Bao-lin, SU Li-chao, HAN Gui-hua, WANG Sheng
- 不同粒径超顺磁性氧化铁纳米粒子的合成及其在交变磁场中的磁热效应
- Synthesis of superparamagnetic iron oxide nanoparticles with different particle sizes and its magneto-calorific effects under alternating current magnetic field
- 材料工程, 2019, 47(4): 84-90
- Journal of Materials Engineering, 2019, 47(4): 84-90.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2018.000470
-
文章历史
- 收稿日期: 2018-04-27
- 修订日期: 2018-12-03
2. 桂林理工大学 材料科学与工程学院, 广西 桂林 541004
2. College of Materials Science and Engineering, Guilin University of Technology, Guilin 541004, Guangxi, China
超顺磁性氧化铁纳米粒子(SPIONs)在交变磁场(ACMF)的作用下,因磁热效应而产生热量[1],这种生热使SPIONs可用于细胞通道激活[2-4]以及肿瘤磁热疗的研究。辣椒素受体TRPV1阳离子细胞通道可以被热刺激(43℃)、辣椒素、外力及pH值等因素触发[5]。Chen等[6]通过磁性纳米粒子在ACMF中生热而触发TRPV1,来引发含TRPV1通道的神经元放电,通过远程控制神经元兴奋而实现深度脑刺激。这种技术可用于神经信号通路研究及神经系统的疾病治疗。磁性纳米粒子在ACMF中由磁热效应产生热量的另一个应用是磁热疗,在ACMF的作用下,将温度升高到40℃以上,达到破坏肿瘤细胞的目的[7]。如果将功能分子如叶酸修饰于SPIONs,可以将SPIONs靶向肿瘤部位[8],实现靶向磁热疗。靶向磁热疗具有效率高及副作用小的特点,因此,有必要系统地研究合成的SPIONs的磁热效应。当ACMF的磁场强度和频率之积高于特定值时,会对健康组织产生有害影响,在实验过程中必须使磁场强度和频率之积低于生物学安全限(5×109A·m-1·s-1)[9]。本工作采用ACMF的固定频率为425kHz,磁场强度为5.3kA·m-1,其乘积小于上述生物学安全值。采用改进型的多醇热解法[10-11],以聚乙二醇(polyethylene glycol, PEG)为溶剂和反应剂,聚乙烯亚胺(polyethylene imine, PEI)为添加剂,乙酰丙酮铁为铁源,制备了8~16nm不同粒径的PEG和PEI共同修饰的SPIONs。研究了ACMF中SPIONs的粒径及浓度对其磁热效应的影响,计算了比能量吸收率(SAR)值,为进一步触发细胞通道及磁热疗相关的生物医学研究打下了基础。
1 实验 1.1 实验材料聚乙二醇(PEG,Mw=1000),化学纯,汕头市西陇化工股份有限公司;聚乙烯亚胺(PEI,Mw=1800),99%,上海阿拉丁生化科技股份有限公司;乙酰丙酮铁(Fe(acac)3),98%,梯希爱(上海)化成工业发展有限公司;甲苯,分析纯,汕头市西陇化工股份有限公司;丙酮,分析纯,汕头市西陇化工股份有限公司。
1.2 实验仪器采用X’Pert PRO X射线粉末衍射仪表征SPIONs的物相;MPMS XL-7超导量子干涉仪测定SPIONs的磁性能;JEM-2100透射电子显微镜观察样品的形貌;ZEN3600纳米粒度&Zeta电位分析仪测定样品的水动力学粒径;Optima 7300DV等离子体原子发射光谱仪测定样品浓度;SPG-10A-Ⅱ高频感应加热设备加热SPIONs水分散液;UNI-T UT321型数字测温仪结合TT-K-30-SLE Omega热电偶测量SPIONs水分散液的温度。
1.3 材料制备称取15g PEG和0.3g PEI加入50mL三口烧瓶中,将三口烧瓶置于智能温度控制器上加热,同时通入氩气。三口烧瓶内反应物升温至80℃时,将0.7g Fe(acac)3加入三口烧瓶内,保温10min。在三口烧瓶上加上回流管。根据回流温度和时间的不同,设计以下合成方案,样品A:升温至260℃,保温40min;样品B:升温至280℃,保温60min;样品C:升温至280℃,保温120min。保温时间结束后,自然冷却至55℃取出样品。
将合成的样品倒入空烧杯中,依次用甲苯及丙酮清洗样品3次,将样品分散于去离子水中,使用磁珠分选器滤去样品中残余的聚合物[12],再加入去离子水并进行超声分散,置于4℃冷藏柜内保存待用。
1.4 磁热效应的测定由高频感应加热设备产生的交变电流在图 1所示的线圈(线圈由空心铜管制成,内通冷却水,线圈外径为5.7cm,内径为4.3cm,圈数为5圈)中产生ACMF磁场,其磁场强度Bm为:
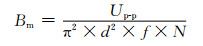
|
(1) |
|
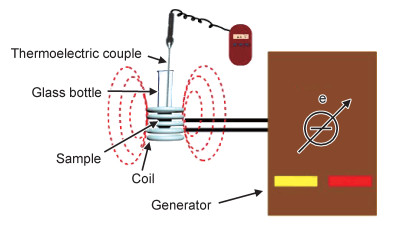
图 1 SPIONs在交变磁场中的磁热效应实验装置示意图 Fig. 1 Schematic diagram of experiment setup for magneto- calorific effects of SPIONs under ACMF |
式中:d为螺线管线圈直径,mm;N为螺线管线圈匝数;f为交变频率,kHz;Up-p为磁感应产生的电压的峰-峰值,mV。打开高频感应加热设备,将连接数字储存示波器(TBS 1052B)的螺线管(d= 6mm,N=10)探头伸入高频感应加热设备所接的线圈中央,测量得到的f为425kHz,Up-p为10V,由式(1)可知Bm为5.3kA·m-1。
利用高频感应加热设备对不同粒径和不同浓度的SPIONs进行磁热效应测定,将A,B,C 3种不同粒径SPIONs样品的去离子水分散液置于外径为2.5cm的玻璃瓶中,浓度分别为2.0,1.0,0.5,0.25mg·mL-1,体积均为5mL。将待测样品放置在图 1所示的线圈中央,加热高频感应加热设备,定时暂停高频设备,将线芯直径为0.255mm的热电偶插入SPIONs水分散液中测试其温度。使用数字测温仪即时记录SPIONs水分散液温度。通过绘制的时间-温度曲线,计算SPIONs的SAR,其计算公式如式(2)所示[2]。
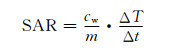
|
(2) |
式中:cw为SPIONs水分散液的比热容,计算为SPIONs和水的质量加权平均数,因SPIONs的浓度很低,氧化铁质量占比很小,其热容量可以忽略不计[2],cw值取为水的比热容(cw= 4.18J·g-1·K-1);m为每克SPIONs水分散液中铁元素的含量;ΔT/Δt为时间-温度曲线的初始斜率。
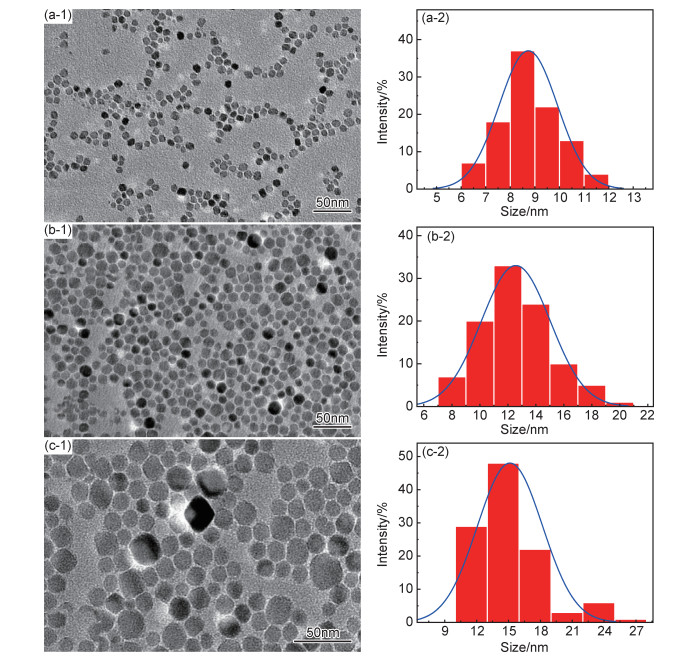
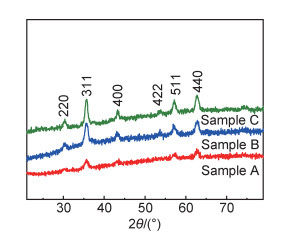
2 结果与分析 2.1 不同粒径SPIONs的表征采用改进的多醇热解法合成了不同粒径的SPIONs,图 2分别为样品A, B, C的TEM图以及粒径柱状分布图。可知,制备的SPIONs分散良好,使用Image J软件测得样品A,B,C的粒径大小分别为(8.7±1.2),(12.6±2.5),(15.3±3.3)nm。当回流温度由260℃升高到280℃,SPIONs的粒径由8.7nm增加到12.6nm;而当回流温度一定(280℃)时,将回流时间增加1倍,SPIONs的粒径由12.6nm增加到15.3nm。说明在合成SPIONs的过程中,改变回流温度和合成时间可以在一定范围内控制晶粒粒径的大小[13]。但合成温度在280℃以上时PEG会发生明显的分解,进一步延长保温时间SPIONs粒径增长缓慢,而且粒度大小分布很不均匀。不同粒径的SPIONs可用于研究在ACMF作用下磁热效应的尺度依赖性。不同条件下合成的SPIONs的物相组成基本不变,图 3为SPIONs样品A,B,C的XRD谱图。该谱图显示,样品A,B,C均在30.09°,35.44°,43.07°,53.43°,56.96°,62.55°处出现衍射峰,对应Fe3O4的PDF标准卡片(JCPDS 01-085-1436)上(220),(311),(400),(422),(511),(440)晶面,表明样品中含有Fe3O4晶相。随着回流温度和回流时间的增加,晶粒增大,样品A,B,C的衍射峰增高,半峰宽减小。
|
图 2 样品的TEM图(1)和粒径分布图(2) (a)样品A;(b)样品B;(c)样品C Fig. 2 TEM images(1) and particle size distribution(2) of the samples (a)sample A; (b)sample B; (c)sample C |
|
图 3 SPIONs样品的XRD谱图 Fig. 3 XRD patterns of the SPIONs samples |
表 1为样品A,B,C合成时的设置参数,粒径和Zeta电位测试结果。SPIONs在去离子水中的胶体稳定性是由吸引力和排斥力之间的平衡引起的,本课题组之前的分析结果表明[14],PEG和PEI在SPIONs表面的结合方式如图 4所示。PEG通过COO—直接连接在SPIONs上;PEI依靠—NH2结合在SPIONs表面;连接在氧化铁表面的PEG或PEI通过氢键彼此结合。从理论上讲,吸引力来自于范德华力、偶极和磁偶极力,而斥力主要来自于静电斥力(表 1所示SPIONs均呈正的表面电性)和聚合物形成的空间位阻效应,这些排斥力使得胶体保持稳定分散[11]。样品的水动力学粒径在3个月后并未有很大变化,说明合成SPIONs之后,其表面修饰层之间的空间位阻效应和静电斥力阻止了SPIONs之间的团聚,使合成的SPIONs在水分散液中表现出稳定分散的特点。
| Reflux temperature/ ℃ |
Reflux time/ min |
Size/ nm |
Hydrodynamic particle size/ nm |
Zeta potential/ mV |
| 260 | 40 | 8.7±1.2 | 22.1 | 28.2 |
| 280 | 60 | 12.6±2.6 | 22.5 | 34.2 |
| 280 | 120 | 15.3±3.3 | 25.8 | 31.2 |

|
图 4 SPIONs的合成及表面修饰示意图 Fig. 4 Schematic diagrams of SPIONs synthesis and surface modification |
一般情况下,大粒径的氧化铁纳米粒子有较强的饱和磁化强度[15],图 5为3种样品在300K下的磁滞回线。样品A,B,C的饱和磁化强度依次为31.4,50.3,60.6A·m2·kg-1,说明饱和磁化强度随粒径减小而降低。纳米粒子表面有结晶性差甚至非晶的表层结构,造成表面电子自旋倾斜而降低了饱和磁化强度[16-18]。纳米粒子粒径越小,表面层占比越大,使得磁性纳米材料的饱和磁化强度越小。图 5中的磁滞回线放大图表明,SPIONs在300K均表现出较小的矫顽力(<2.39kA·m-1),非零的矫顽力很可能是SPIONs在冷冻干燥中制成粉末样品时团聚导致的,但只要矫顽力小于2.39kA·m-1,一般就认为样品是属于超顺磁性的[19]。同时,由电泳粒度结果(表 1)可以看出,SPIONs在水分散液中分散性很好,即实际的SPIONs的剩磁应该更小,属于超顺磁性纳米粒子。

|
图 5 样品A,B,C在300K下的磁滞回线 Fig. 5 Hysteresis loops of sample A, B and C at 300K |
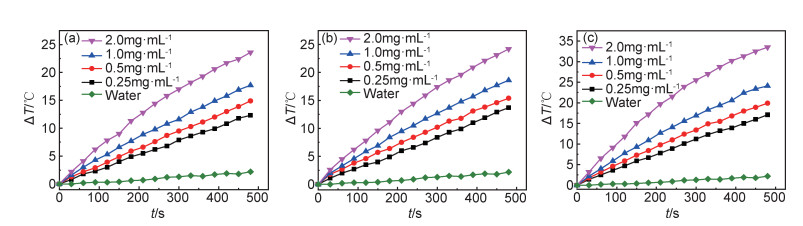
图 6是不同浓度的样品A,B,C的水分散液及纯去离子水在频率425kHz及磁场强度为5.3kA·m-1的ACMF作用下的升温曲线。实验中采用细而灵敏度高的热电偶对SPIONs水分散液进行温度检测。结果表明,在初始温度为20℃时,去离子水温度没有明显变化,说明磁场作用对去离子水未产生影响(较小的温升应是线圈发热后热传导所致)。粒径为8.7,12.6,15.3nm的3种SPIONs的水分散液在480s内温度分别升高了25,27,35℃,样品的浓度越高,温度升高得越快,这些SPIONs均具有用于肿瘤磁热疗和打开膜通道的潜力[20]。2.0mg·mL-1溶液的每克样品含铁量为1.45×10-3g,利用式(2)计算可得样品A,B,C在ACMF作用下的SAR值(表 2)。在相同浓度时,SPIONs的粒径越大,其升温效率越高[21],表明样品的磁热效应具有纳米粒子粒径依赖性。当浓度为0.25mg·mL-1时,样品C的SAR值达到最高,为810W·g-1,但同一粒径的样品由低浓度到高浓度时,SAR值逐渐减小。
|
图 6 样品的水分散液在交变磁场作用下温度随时间变化的曲线 (a)样品A; (b)样品B;(c)样品C Fig. 6 Time dependent temperature curves of the samples in aqueous dispersion under ACMF (a)sample A; (b)sample B; (c)sample C |
| Concentration/ (mg·mL-1) |
SAR value/(W·g-1) | ||
| Sample A | Sample B | Sample C | |
| 2.0 | 140 | 143 | 201 |
| 1.0 | 208 | 218 | 289 |
| 0.5 | 346 | 359 | 473 |
| 0.25 | 590 | 646 | 810 |
SPIONs在ACMF中的磁热效应来自于粒子的弛豫损耗(布朗弛豫损耗和尼尔弛豫损耗)[22],其中布朗弛豫损耗来源于ACMF的作用下,粒子的转动滞后于ACMF的变化,磁性纳米粒子在液体中转动与液体产生的摩擦;尼尔弛豫损耗来源于磁性粒子内的磁矩方向随外磁场方向变化所产生的损耗。弛豫损耗是SPIONs在外磁场中产热的原因,尼尔弛豫和布朗弛豫中弛豫时间越小,对弛豫损耗贡献越大。布朗弛豫时间τB和尼尔弛豫时间τN为:

|
(3) |
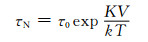
|
(4) |
式中:η是载液的黏度,T=300K时,η=0.85×10-3Pa·s;r是粒子的水动力学半径;k是玻尔兹曼常数,k=1.38×10-23J·K-1;τ0为时间常数,约为10-9;V是粒子的体积;K是各向异性常数,K=1.35×104J·m-3。结合2种弛豫机制,体系中的有效弛豫时间为:
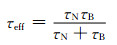
|
(5) |
样品A,B,C的弛豫时间计算结果见表 3。表明尼尔弛豫时间小于布朗弛豫时间,说明在本体系中,导致SPIONs在ACMF下的磁热效应主要来自于尼尔弛豫损耗,而布朗弛豫的贡献相对较小。这与Deatsch等的结论一致,即粒径小于15nm的纳米粒子的产热机制是由尼尔弛豫主导的,随着粒径的增大,布朗弛豫对产热的贡献愈加明显。
| Sample | τB/s | τN/s | τeff/s |
| A | 3.45×10-6 | 3.13×10-9 | 3.13×10-9 |
| B | 3.65×10-6 | 2.94×10-8 | 2.92×10-8 |
| C | 5.53×10-6 | 4.20×10-7 | 3.90×10-7 |
除采用SAR值来衡量磁性纳米粒子在ACMF中的磁热效应外,也可由损耗功率P来表示:

|
(6) |
式中:m为粒子磁矩;ω为角频率(ω=2πf);H为交变磁场的振幅;ρ为铁密度。根据式(6),功率损耗P取决于粒子的弛豫时间和交变磁场频率,当ωτ=1时,P值达到最大。在固定频率为425kHz及磁场强度为5.3kA·m-1的ACMF下,样品A,B,C的ωτ经计算分别为8×10-3,8×10-2,1,即样品C的P值最大,此结果也说明了样品的磁热效应具有纳米粒径大小的依赖性,与之前分析SAR值的测试计算结论一致。
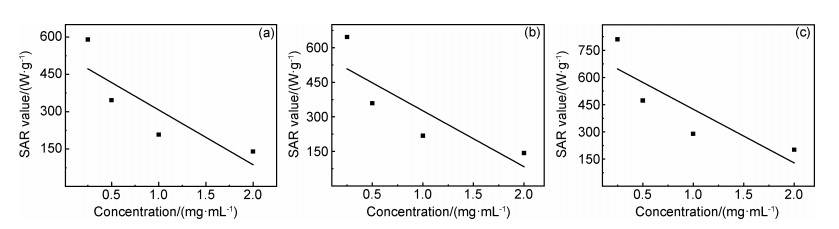
由表 2显示,随着样品浓度的提高,SAR值出现相反的变化趋势。通过绘制SAR值与样品浓度之间的关系图(图 7),可见样品A,B,C的SAR值与样品浓度负相关。本结果与文献[23]的结论一致。当尼尔弛豫效应为主时,磁性纳米粒子的SAR值随浓度增加而减小。浓度较高的情况下,在交变磁场中,邻近粒子之间的相互作用会形成链状结构,这些链状结构内的磁性纳米粒子之间通过偶极相互作用, 而构成比较稳定的磁结构,因此形成较高的有效能垒。从式(4)可见,SPIONs的有效能垒(Eb=KV)与尼尔弛豫时间(τN)呈指数增加的关系,τN的增大降低了SPIONs在ACMF下的升温效率,导致SAR值减小。
|
图 7 交变磁场下样品浓度与SAR值的线性关系 (a)样品A; (b)样品B;(c)样品C Fig. 7 Linear relation of the concentration of the samples and SAR value under ACMF (a)sample A; (b)sample B; (c)sample C |
散热性角度分析,随着SPIONs浓度降低,粒子间的平均距离增大,SPIONs粒子的散热更快,散热效率越高,因此测得的SAR值就越大。磁性纳米粒子的浓度必须控制在尽可能低的范围内,最大限度地提高纳米粒子在ACMF下的散热效率,以便能够测得磁性纳米粒子更本证的SAR值。
3 结论(1) 采用多醇热解法制备了粒径分别为8.7,12.6,15.3nm的SPIONs,SPIONs晶相主要为Fe3O4相。3种SPIONs样品在去离子水中具有较好的分散性,水动力学粒径分别为22.1,22.5,25.8nm,饱和磁化强度依次为31.4,50.3,60.6A·m2·kg-1。3种SPIONs的矫顽力均小于2.39kA·m-1,表现出良好的超顺磁性。
(2) 不同粒径SPIONs的水分散液在固定频率425kHz、磁场强度为5.3kA·m-1的ACMF作用下,随着SPIONs粒径的增大和分散液浓度的增高,升温速率均增高,粒径为8.7,12.6,15.3nm的SPIONs在480s内的温升最大值分别为25,27,35℃。
(3) 尼尔弛豫时间比布朗弛豫时间小,说明SPIONs在ACMF下的磁热效应主要来自于尼尔弛豫损耗。随着SPIONs粒径的增大,SPIONs的SAR值增大,说明SPIONs在ACMF作用下的磁热效应具有纳米粒径依赖性。当SPIONs的粒径为15.3nm、浓度为0.25mg·mL-1时,SAR值最高可达810W·g-1,SAR值与SPIONs的水分散液浓度呈负线性相关。
| [1] | ROSENSWEIG R E. Heating magnetic fluid with alternating magnetic field[J]. Journal of Magnetism and Magnetic Materials, 2002, 252 (1/3): 370–374. |
| [2] | GUPTA J, PRAKASH A, JAISWAL M K, et al. Superparamag-netic iron oxide-reduced graphene oxide nanohybrid-a vehicle for targeted drug delivery and hyperthermia treatment of cancer[J]. Journal of Magnetism and Magnetic Materials, 2018, 448 : 332–338. DOI: 10.1016/j.jmmm.2017.05.084 |
| [3] | HAYASHI K, NAKAMURA M, SAK-AMOTO W, et al. Superparamagnetic nanoparticle clusters for cancer theranostics combining magnetic resonance imaging and hyperthermia treat-ment[J]. Theranostics, 2013, 3 (6): 366–376. DOI: 10.7150/thno.5860 |
| [4] | ZHANG C, JUGOLD M, WOENNE E C, et al. Specific targeting of tumor angiogenesis by RGD-conjugated ultrasmall superpara-magnetic iron oxide particles using a clinical 1.5-T magnetic res-onance scanner[J]. Cancer Research, 2007, 67 (4): 1555–1562. DOI: 10.1158/0008-5472.CAN-06-1668 |
| [5] | STEENLAND H W, KO S W, WU L J, et al. Hot receptors in the brain[J]. Molecular Pain, 2006, 2 (1): 34. |
| [6] | CHEN R, ROMERO G, CHRISTIANSEN M G, et al. Wireless magnetothermal deep brain stimulation[J]. Science, 2015, 347 (6229): 1477–1480. DOI: 10.1126/science.1261821 |
| [7] | XIE J, YAN C, YAN Y, et al. Multi-modal Mn-Zn ferrite nanocrystals for magnetically-induced cancer targeted hyperther-mia:a comparison of passive and active targeting effects[J]. Nan-oscale, 2016, 8 (38): 16902–16915. |
| [8] | HUANG Y, MAO K, ZHANG B, et al. Superparamagnetic iron oxide nanoparticles conjugated with folic acid for dual targetsp-ecific drug delivery and MRI in cancer theranostics[J]. Materials Science & Engineering C, Materials for Biological Applications, 2017, 70 : 763–771. |
| [9] | CELIK O, CAN M M, FIRAT T. Size dependent heating ability of CoFe2O4 nanoparticles in AC magnetic field for magnetic nano-fluid hyperthermia[J]. Journal of Nanoparticle Research, 2014, 16 (3): 1–7. |
| [10] | WANG J, ZHANG B, WANG L, et al. One-pot synthesis of water-soluble superparamagnetic iron oxide nanoparticles and their MRI contrast effects in the mouse brains[J]. Materials Science and Engineering:C, 2015, 48 : 416–423. DOI: 10.1016/j.msec.2014.12.026 |
| [11] | ZHANG B, TU Z, ZHAO F, et al. Superparamagnetic iron oxide nanoparticles prepared by using an improved polyol method[J]. Applied Surface Science, 2013, 266 (2): 375–379. |
| [12] |
王军, 张宝林, 赵方圆, 等. 聚乙二醇/聚乙烯亚胺修饰的超顺磁性氧化铁磁共振造影剂的性能[J].
材料研究学报, 2013, 27 (5): 508–514.
WANG J, ZHANG B L, ZHAO F Y, et al. Properties of SPIO magnetic resonance imaging contrast agents modified with poly(ethylene glycol) and poly(ethylene imine)[J]. Chinese Journal of Materials Research, 2013, 27 (5): 508–514. |
| [13] |
赵海涛, 马瑞廷, 刘瑞萍. 热分解法制备Ni0.5Zn0.5Fe2O4纳米颗粒[J].
材料工程, 2017, 45 (9): 81–85.
ZHAO H T, MA R T, LIU R P. Synthesis of Ni0.5Zn0.5Fe2O4 nanoparticles by thermal decomposition method[J]. Journal of Materials Engineering, 2017, 45 (9): 81–85. |
| [14] | XIE S, ZHANG B, WANG L, et al. Superparamagnetic iron oxide nanoparticles coated with different polymers and their MRI contrast effects in the mouse brains[J]. Applied Surface Scien-ce, 2015, 326 : 32–38. DOI: 10.1016/j.apsusc.2014.11.099 |
| [15] | ZHAO Z, ZHOU Z, BAO J, et al. Octapod iron oxide nanopar-ticles as high-performance T2 contrast agents for magnetic reson-ance imaging[J]. Nature Communications, 2013, 4 : 2266. DOI: 10.1038/ncomms3266 |
| [16] | SUN S, ZENG H. Monodisperse MFe2O4(M=Fe, Co, Mn) nanoparticles[J]. Journal of the American Chemical Society, 2004, 126 (1): 273–279. DOI: 10.1021/ja0380852 |
| [17] | LI Z, CHEN H, BAO H, et al. One-pot reaction to synthesize water-soluble magnetite nanocrystals[J]. Chemistry of Mater-ials, 2004, 16 (8): 1391–1393. DOI: 10.1021/cm035346y |
| [18] | MORALES M P, VEINTEMILLAS-VERDAGUER S, MONT-ERO M I, et al. Surface and internal spin canting in γ-Fe2O3 nanoparticles[J]. Chemistry of Materials, 1999, 11 (11): 3058–3064. DOI: 10.1021/cm991018f |
| [19] | SONG Y, WANG R, RONG R, et al. Synthesis of well-dispersed aqueous-phase magnetite nanoparticles and their metabolism as an MRI contrast agent for the reticuloendothelial system[J]. European Journal of Inorganic Chemistry, 2011 (22): 3303–3313. |
| [20] |
刘杰, 高福平, 唐劲天. 肿瘤主动靶向磁性纳米粒子研究现状及其在肿瘤热疗中的应用[J].
科技导报, 2010, 28 (19): 108–112.
LIU J, GAO F P, TANG J T. Active targeting magnetic iron oxide nanoparticles:current status and novel applications in tumor hyperthermia[J]. Science & Technology Review, 2010, 28 (19): 108–112. |
| [21] | NEMATI Z, SALILI S M, ALONSO J, et al. Superparamagnetic iron oxide nanodiscs for hyperthermia therapy:does size matter?[J]. Journal of Alloys and Compounds, 2017, 714 : 709–714. DOI: 10.1016/j.jallcom.2017.04.211 |
| [22] | COFFEY W T, FANNIN P C. Internal and Brownian mode-coupling effects in the theory of magnetic relaxation and ferroma-gnetic resonance of ferrofluids[J]. Journal of Physics:Condensed Matter, 2002, 14 : 3677–3692. DOI: 10.1088/0953-8984/14/14/301 |
| [23] | PINEIRO-REDONDO Y, BANOBRE-LOPEZ M, PARDINAS-BLANCO I, et al. The influence of colloidal parameters on the specific power absorption of PAA-coated magnetite nanoparticles[J]. Nanoscale Research Letters, 2011, 6 (1): 1–7. |
 2019, Vol. 47
2019, Vol. 47


