文章信息
- 周琦, 王亚飞, 冯基伟, 李志洋
- ZHOU Qi, WANG Ya-fei, FENG Ji-wei, LI Zhi-yang
- 脱合金化制备纳米多孔Ni-Fe合金及其电催化性能
- Preparation and electrocatalytic performance of nanoporous Ni-Fe alloy by dealloying
- 材料工程, 2019, 47(4): 77-83
- Journal of Materials Engineering, 2019, 47(4): 77-83.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2017.000945
-
文章历史
- 收稿日期: 2017-07-25
- 修订日期: 2018-11-06
氢能源作为清洁、可再生的二次能源,被认为是解决能源危机和环境污染问题的最佳选择[1-3]。由于析氢过电位的存在,使工业化电解水制氢的成本大幅增加,因此研制低析氢过电位的电极材料非常必要。Pt, Pd等贵金属具有较低的析氢过电位,但其储量较少,成本较高,不利于广泛应用[4-6]。为此,人们将目光转移到Ni[7], Mo[8], Co[9], Fe[10]等金属或合金上,由于Ni在3d电子层具有未成对的电子,容易与H的1s电子层上电子形成Ni—H键,Ni不仅可以与金属形成合金电极,也可以与S, P等形成Ni-S[11], Ni-P[12]等金属-非金属的合金电极,是目前公认的电化学活性最好的电极材料。Mech等[13]利用恒电流电沉积技术获得了Ni-Mo合金层,选择性激光烧结工艺的加入增加了表面活性,而且提高了沉积层和基体之间的结合力,结果表明,Mo的加入减小了Tafel斜率,提高了析氢催化性能。孔亚鹏等[14]采用脉冲电镀法制备了Ni-Mo-Co合金镀层,80℃时,在质量分数33%的NaOH溶液中的析氢过电位仅为56mV。Han等[15]在NiSO4·6H2O, Na2MoO4·2H2O和Na3C6H5O7·2H2O的镀液体系中,制备出具有非晶结构的Ni-Mo合金电极,结果发现,Mo含量为31.04%(质量分数)的Ni-Mo合金电极具有较高的析氢活性,但经过长时间的析氢实验后发现,合金电极中的Mo元素逐渐被溶解,导致其析氢电催化活性的衰减,因此,制备高稳定性的析氢材料具有重要意义。
利用脱合金化制备纳米多孔结构的金属或合金,可以提高电极材料的有效响应面积,有效解决电极材料稳定性差的问题。本工作通过真空熔炼与固溶处理的方法制备了成分均匀的前驱体合金,采用脱合金化制得纳米多孔Ni及纳米多孔Ni-Fe合金, 研究了材料的表面微观形貌和结构,并运用线性扫描伏安法、电化学交流阻抗、方波电位法及计时电位法研究其在碱性介质中的析氢电催化性能。
1 实验材料与方法实验原料为分析纯Ni粉(质量分数≥99.5%,200目)、Fe粉(质量分数≥99.95%,200目)、Mn粉(质量分数≥99.5%,200目),按Ni, Fe, Mn原子比Ni30-xFexMn70(x=0, 10, 20)配制粉末,球磨混料后,利用等静压机将粉末压制成直径15mm的圆柱坯体。采用高频真空感应炉熔炼,将熔炼后的铸态合金置于真空管式炉中,在氮气保护下加热至1173K保温24h,取出后在水介质中淬火,将淬火得到的合金锭通过冷轧制得长×宽约为1cm×0.5cm,厚50~80μm的长方体前驱体合金薄片。脱合金化在CHI660D电化学工作站进行,采用三电极体系,工作电极为前驱体合金,辅助电极和参比电极分别为10mm×10mm铂片与饱和甘汞电极,电解液为1mol/L (NH4)2SO4溶液。脱合金化得到的纳米多孔Ni及纳米多孔Ni-Fe合金用去离子水与无水乙醇冲洗至中性,室温下真空干燥保存。
采用D8 ADVANCE X射线衍射仪(XRD)分析材料物相组成,扫描速率3(°)/min,CuKα射线。采用JSM-6700场发射扫描电镜对试样的表面形貌进行分析。
在CHI660D电化学工作站进行阴极极化曲线、电化学交流阻抗图谱、方波I-t响应曲线及计时电位曲线测试。电化学阻抗的频率范围为0.01Hz~10kHz,振幅为5mV。采用三电极体系测量,电解液为6mol/L NaOH溶液。
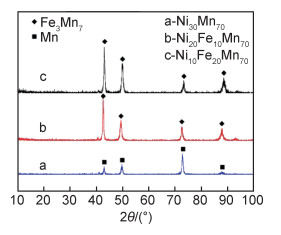
2 结果与讨论 2.1 前驱体合金物相组成文献表明:Ni, Fe, Mn的标准氢电极电位分别为-0.257, -0.447V和-1.135V,Ni, Fe与Mn的电极电位分别相差0.878V和0.688V,且前驱体中Mn的原子分数高达70%,符合脱合金化要求的两个条件:(1)惰性组元与活性组元之间具有大的电极电位差;(2)活性组元的含量要超过脱合金化的临界阈值[16]。图 1为前驱体合金Ni30-xFexMn70(x=0, 10, 20)的XRD图谱。由图 1可知,曲线a由单一的Mn相组成,且衍射峰整体向高角度偏移,这是由于原子半径较小的Ni(0.124nm)溶于Mn(0.132nm)中造成的;曲线b和c由单一的Fe3Mn7相组成,衍射峰同样向右偏移,且未见Ni的衍射峰,同样是Ni溶于Fe3Mn7相中所致。同时,由于前驱体合金Ni30-xFexMn70(x=10, 20)中Fe含量不同,导致曲线b, c偏移量不同(如图 2所示)。
|
图 1 前驱体合金的XRD图谱 Fig. 1 XRD patterns of precursor alloys |

|
图 2 前驱体合金的XRD部分放大图谱 Fig. 2 XRD partial amplification patterns of precursor alloys |
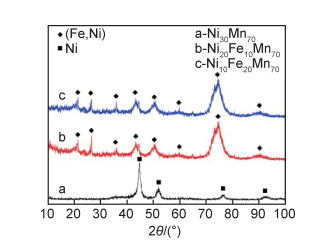
图 3为前驱体合金在1mol/L (NH4)2SO4溶液中电化学脱合金化后的XRD图谱。由曲线a可见,前驱体Ni30Mn70合金脱合金化后形成单一Ni相;曲线b, c表明,前驱体合金Ni20Fe10Mn70与Ni10Fe20Mn70脱合金化后均形成单一(Fe, Ni)合金。
|
图 3 脱合金化后Ni-Fe-Mn合金的XRD图谱 Fig. 3 XRD patterns of Ni-Fe-Mn alloys after dealloying |
根据Scherrer公式D=Kλ/(βcosθ),K为常数,λ为X射线波长,β为衍射峰半高宽,θ为衍射角,计算可知,纳米多孔Ni的晶粒尺寸约为11.8nm,而脱合金化形成的Ni-Fe合金晶粒尺寸分别为6.5nm (Ni20Fe10Mn70)和7.0nm(Ni10Fe20Mn70),可以看到Fe的加入,减小了晶粒尺寸,有利于析氢电催化过程进行。
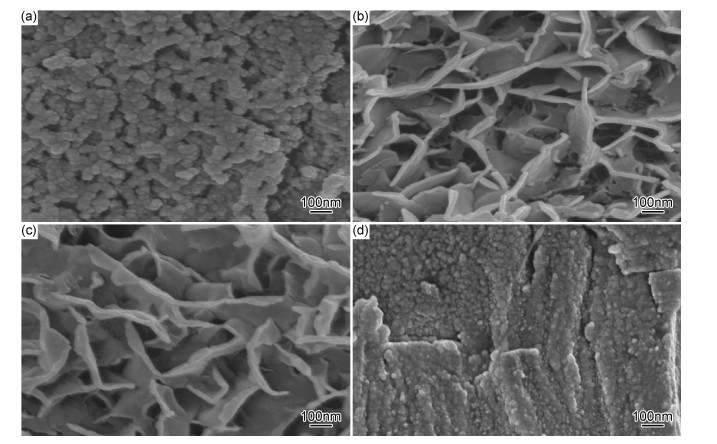
图 4为前驱体合金Ni30-xFexMn70(x=0, 10, 20)脱合金化后的表面形貌以及Ni20Fe10Mn70脱合金化后的截面图。可以看到,合金经脱合金化后表面均得到纳米多孔结构,但其骨架及孔径尺寸明显不同。Ni30Mn70获得的纳米多孔结构骨架由直径为30~50nm的球状颗粒组成,孔径尺寸为50~100nm,如图 4(a)所示。Ni20Fe10Mn70和Ni10Fe20Mn70脱合金化后获得纳米多孔结构骨架均为相互交错的纳米片,但二者形成的骨架尺寸与孔径大小有所差别。Ni20Fe10Mn70的纳米片厚度为10~15nm,孔径尺寸为100~200nm,如图 4(b)所示;Ni10Fe20Mn70的纳米片厚度为10~30nm,孔径尺寸为150~300nm,如图 4(c)所示。同时,从图 4(d)可以看出,前驱体合金Ni20Fe10Mn70通过脱合金化后,横截面由凸起的球状颗粒组成,在一定程度上增大了电极的比表面积,促使析氢反应活性点增多,析氢过电位降低。由图 1可知,3种前驱体合金均形成了单相的固溶体合金,其脱合金化机理均符合Erlebacher模型[17]。
|
图 4 脱合金化后Ni-Fe-Mn合金的SEM图 (a)Ni30Mn70; (b)Ni20Fe10Mn70; (c)Ni10Fe20Mn70; (d)Ni20Fe10Mn70截面 Fig. 4 SEM images of Ni-Fe-Mn alloys after dealloying (a)Ni30Mn70; (b)Ni20Fe10Mn70; (c)Ni10Fe20Mn70; (d)cross section of Ni20Fe10Mn70 |
由图 4可见,Fe的加入对纳米多孔Ni的形貌有很大的改变。3种前驱体合金的脱合金化机理均可以用相分离机制解释。Ni30Mn70形成了Mn(Ni)固溶体,在一定的电位下,固/液界面处首先发生相的分离,贱金属组元Mn溶解到电解液(NH4)2SO4中,而贵金属组元Ni获得连续的化学驱动,聚集成二维簇,随着脱合金化过程的持续进行,与电解液接触的区域不断向合金深处扩展,Mn不断发生溶解,Ni聚集长大,最终形成纳米多孔Ni。而Ni20Fe10Mn70与Ni10Fe20Mn70脱合金化过程中,Mn不断地溶解,Ni, Fe原子获得连续化学驱动力在表面扩散聚集,但由于Ni, Fe扩散系数的不同,根据金属原子扩散系数公式[18]:DS={[d(t)]4kT}/(32rta4),式中:k是波尔兹曼常数;r是原子的表面能;a是晶格常数;d(t)代表脱合金化时间t后的骨架尺寸;T和t分别是脱合金化的温度与时间。结合图 3与图 4分析可得,Fe原子的扩散系数较Ni原子的扩散系数大,在脱合金化过程中Fe原子先于Ni原子形成纳米多孔结构骨架,Ni原子以Fe原子形成的纳米多孔结构为形核位点,形成纳米片状的Ni-Fe合金结构。
2.3 合金电极析氢电催化性能图 5为前驱体合金Ni10Fe20Mn70, Ni20Fe10Mn70与Ni30Mn70脱合金化后形成的纳米多孔Ni电极及Ni-Fe合金电极在室温下6mol/L NaOH溶液中的阴极极化曲线。可以明显看出,在电流密度为0.1A/cm2下,曲线c和曲线b的析氢电位分别较曲线a正移83mV和136mV,Ni20Fe10Mn70脱合金化形成的纳米多孔Ni-Fe合金电极的析氢过电位为56mV,Ni10Fe20Mn70脱合金化形成的纳米多孔Ni-Fe合金电极的析氢过电位为94mV,而Ni30Mn70脱合金化形成的纳米多孔Ni电极的析氢过电位为222mV。

|
图 5 不同电极的阴极极化曲线 Fig. 5 Cathodic polarization curves of different electrodes |
利用图 5中较大极化时的阴极极化曲线数据,作η-lgi(Tafel关系)曲线,以电极的开路电位近似作为体系的平衡电位。根据Tafel关系式:
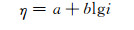
|
(1) |
式中: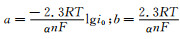
| Electrode | b/V | a/V | i0/(A·cm-2) |
| Ni30Mn70 | 0.164 | 0.336 | 8.939×10-3 |
| Ni20Fe10Mn70 | 0.188 | 0.317 | 2.060×10-2 |
| Ni10Fe20Mn70 | 0.187 | 0.325 | 1.832×10-2 |
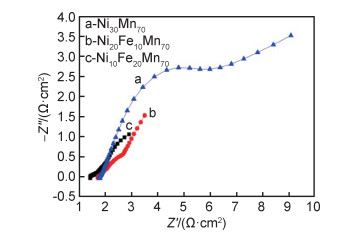
图 6为脱合金化获得纳米多孔Ni电极及纳米多孔Ni-Fe合金电极在平衡电位下的Nyquist图。图 6中曲线a和b所代表的纳米多孔Ni-Fe的电容弧半径均较曲线c代表的纳米多孔Ni的半径小,其中,Ni20Fe10Mn70脱合金化形成的纳米多孔Ni-Fe合金的电容弧半径最小,说明其析氢过程的阻抗最小,有利于析氢过程的进行。
|
图 6 不同电极的Nyquist图 Fig. 6 Nyquist plots of different electrodes |
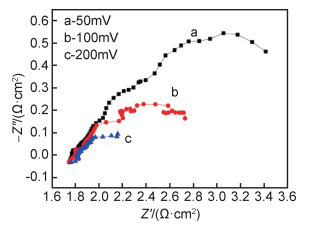
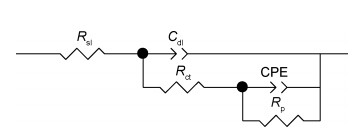
图 7为Ni20Fe10Mn70脱合金化形成的纳米多孔Ni-Fe合金电极在不同过电位下的Nyquist图,同时采用Zview软件对其中数据进行拟合,其模拟等效电路如图 8所示,其中,Rsl为电解液电阻,Rct为电荷转移电阻,Cdl为电极表面的双电层电容,Rp为电化学吸附电阻,CPE为常相位元件,表示与电容的相似程度,电阻元件拟合参数如表 2所示。从表 2数据可以明显看出,随着过电位的增大,电荷转移电阻和电化学吸附电阻都逐渐减小,这与图 7交流阻抗曲线结果相一致。说明随着极化电位的提高,整个纳米多孔Ni-Fe合金电极电阻减小,有利于提高电化学反应速率,也提高了电荷转移与电化学吸附氢的反应速率,使其具有更高的析氢电催化活性。
|
图 7 纳米多孔Ni-Fe合金不同过电位的Nyquist图 Fig. 7 Nyquist plots of nanoporous Ni-Fe alloy at different overpotentials |
|
图 8 纳米多孔Ni-Fe合金电极的等效电路图 Fig. 8 Electrical equivalent circuit of nanoporous Ni-Fe alloy electrode |
| η/mV | Rsl/(Ω·cm2) | Rct/(Ω·cm2) | Rp/(Ω·cm2) |
| 50 | 1.78 | 1.636 | 0.570 |
| 100 | 1.79 | 1.032 | 0.113 |
| 200 | 1.82 | 0.221 | 0.062 |
在碱性溶液中的析氢机制认为有以下3种模式[21]:
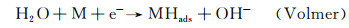
|
(2) |
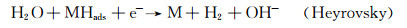
|
(3) |
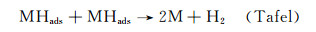
|
(4) |
由于Ni与Fe对氢原子具有非常强的吸附作用,几乎不发生复合脱附过程(Tafel),说明Ni20Fe10Mn70形成的纳米多孔Ni-Fe合金电极析氢机理为Volmer-Heyrovsky。结合对Ni20Fe10Mn70经脱合金化形成的纳米多孔Ni-Fe合金电极在不同过电位下的交流阻抗图谱(图 7与表 2)的分析,随着过电位的增大,整个纳米多孔Ni-Fe合金电极电阻减小,提高了析氢电流密度,有利于提高电化学反应速率。Ni的d电子层3d8与Fe的d电子层3d6能够发生重叠,可以共享彼此的d层电子,而电极表面的H+在电极表面获得电子变成中间体的Hads会与Ni或Fe电子层中空的或半空的d轨道结合,Fe的加入相当于为中间体Hads原子提供更多的结合位点,加快了Ni的电化学吸附过程,使Hads原子能更快地从Ni原子周围离开,加快了Volmer步骤,相对而言,电化学脱附步骤就变慢,成为析氢反应中的控制步骤。
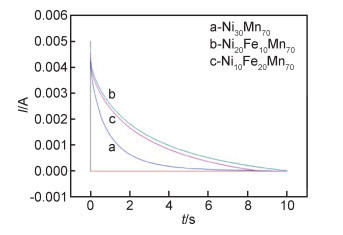
采用恒电位阶跃法测试纳米多孔Ni电极及纳米多孔Ni-Fe合金电极的电化学表面积,方波幅度为10mV,其方波I-t响应曲线如图 9所示。
|
图 9 不同电极的方波I-t响应曲线 Fig. 9 Square wave I-t response curves of different electrodes |
由图 9可知,曲线末端趋近于0,故可认为电流此时仅用于双电层电容充电,并未用于电极反应。根据双电层电容微分公式Cdl=dQ/dE,Q为曲线积分得到的电量,ΔE=10mV。已知纯汞电极的双电层电容值Cdl0为20μF/cm2,由公式Sr=Cdl/Cdl0,r=Sr/Ss计算得到的数值见表 3。可以发现通过Ni20Fe10Mn70制得的纳米多孔Ni-Fe合金电极具有较大的真实表面积,是Ni10Fe20Mn70制得的纳米多孔Ni-Fe合金电极的真实表面积的1.153倍,是Ni30Mn70制得的纳米多孔Ni的真实表面积的2.404倍,可见适量Fe加入,可以在一定程度上增加材料表面积,有利于析氢电催化活性提高。
| Electrode | Cdl/(μF·cm-2) | Sr/cm2 | r |
| Ni30Mn70 | 0.4369 | 21845 | 21845 |
| Ni20Fe10Mn70 | 1.0505 | 52525 | 52525 |
| Ni10Fe20Mn70 | 0.9111 | 45555 | 45555 |
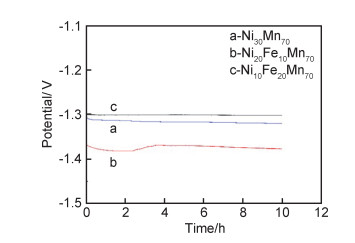
图 10为纳米多孔Ni电极及Ni-Fe合金电极在0.1A/cm2,25℃的6mol/L NaOH溶液中的计时电位(chrono potentiometry, CP)曲线。由图 10可见,Ni30Mn70制得的纳米多孔Ni电极析氢电位由-1.301V负移至-1.321V,经10h连续电解,其析氢电位负移20mV,Ni10Fe20Mn70制得的纳米多孔Ni-Fe合金电极析氢电位由-1.295V负移至-1.302V,其析氢电位负移7mV,而Ni20Fe10Mn70脱合金化制得的纳米多孔Ni-Fe合金电极在连续电解过程中,析氢电位由-1.371V负移至-1.376V,析氢电位仅负移5mV。因此,纳米多孔Ni-Fe合金电极表现出良好的电化学稳定性。
|
图 10 纳米多孔Ni-Fe合金电极的计时电位曲线 Fig. 10 CP curves of nanoporous Ni-Fe alloy electrode |
(1) 3种前驱体合金经脱合金化得到均匀的纳米多孔结构,Fe的加入改变了纳米多孔Ni的形貌,Ni20Fe10Mn70获得厚度为10~15nm的纳米片,孔径尺寸为100~200nm;Ni10Fe20Mn70获得厚度为10~30nm的纳米片,孔径尺寸为150~300nm。
(2) Ni20Fe10Mn70得到的纳米多孔Ni-Fe合金电极具有最大的表面积,Fe的加入与Ni产生协同作用,使其具有更好的析氢电催化活性,在0.1A/cm2电流密度下,其析氢过电位仅为56mV,且表现出良好的电化学稳定性。
| [1] | URSUA A, GANDIA L M, SANCHIS P. Hydrogen production from water electrolysis:current status and future trends[J]. Proceedings of the IEEE, 2012, 100 (2): 410–426. DOI: 10.1109/JPROC.2011.2156750 |
| [2] | KONG D S, WANG H T, LU Z Y, et al. CoSe2nanoparticles grown on carbon fiber paper:an efficient and stable electroca-talyst for hydrogen evolution reaction[J]. Journal of the American Chemical Society, 2014, 136 (13): 4897–4900. DOI: 10.1021/ja501497n |
| [3] | MARINESCU S C, WINKLER J R, GRAY H B. Molecular mechanisms of cobalt-catalyzed hydrogen evolution[J]. Procee-dings of the National Academy of Sciences, 2012, 109 (38): 15127–15131. DOI: 10.1073/pnas.1213442109 |
| [4] |
冉敏, 吴艺辉, 何捍卫. 铁元素对镍基Ni-S合金涂层电极析氢性能的影响[J].
粉末冶金材料科学与工程, 2018, 23 (1): 63–69.
RAN M, WU Y H, HE H W. Effect of Fe on hydrogen evolution performance of Ni-based Ni-S alloy coating electrode[J]. Materials Science and Engineering of Powder Metallurgy, 2018, 23 (1): 63–69. DOI: 10.3969/j.issn.1673-0224.2018.01.009 |
| [5] |
李复丽. Ni-Co-Sn和Ni-Fe-Sn合金电极的制备及其析氢性能研究[D].兰州: 兰州大学, 2016. LI F L. Preparation and hydrogen evolution properties of Ni-Co-Sn and Ni-Fe-Sn alloy electrodes[D]. Lanzhou: Lanzhou University, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10730-1016722846.htm |
| [6] |
王宏智, 张晓振, 黄波, 等. 碳毡基体上电沉积Ni-Mo合金及其催化析氢性能[J].
化学工业与工程, 2017, 34 (1): 53–59.
WANG H Z, ZHANG X Z, HUANG B, et al. Electrodeposition of Ni-Mo alloy from ionic liquids and its catalytic properties for hydrogen evolution[J]. Chemical Industry and Engineering, 2017, 34 (1): 53–59. |
| [7] |
秦海森, 王书亮, 景阳钟, 等. 不同搅拌方式对Ni-Fe-Co镀层组织结构和电催化析氢性能的影响[J].
表面技术, 2018, 47 (6): 38–43.
QIN H S, WANG S L, JING Y Z, et al. Effects of different stirring methods on microstructure and electro-catalytic hydrogen evolution performance of Ni-Fe-Co coatings[J]. Surface Techno-logy, 2018, 47 (6): 38–43. |
| [8] | McKONE J R, SADTLER B F, WERLANG C A, et al. Ni-Mo nanopowders for efficient electrochemical hydrogen evolution[J]. ACS Catalysis, 2013, 3 (2): 166–169. DOI: 10.1021/cs300691m |
| [9] | BADAWY W A, NADY H, NEGEM M. Cathodic hydrogen evolution in acidic solutions using electrodeposited nano-crys-talline Ni-Co cathodes[J]. International Journal of Hydrogen Energy, 2014, 39 (21): 10824–10832. DOI: 10.1016/j.ijhydene.2014.05.049 |
| [10] | BACHVAROY V D, ARNAUDOVA M H, RASHKOV R S, et al. Electrochemical deposition of alloys based on Ni-Fe-Co, containing W, P, and their characterization for hydrogen evol-ution reaction[J]. Bulgarian Chemical Communications, 2011, 43 (1): 115–119. |
| [11] | HAN Q, JIN Y, PU N W, et al. Electrochemical evolution of hydrogen on composite La-Ni-Al/Ni-S alloy film in water electr-olysis[J]. Renewable Energy, 2010, 35 (12): 2627–2631. DOI: 10.1016/j.renene.2010.03.015 |
| [12] | PASEKA I. Hydrogen evolution reaction on Ni-P alloys:the internal stress and the activities of electrodes[J]. Electrochimica Acta, 2008, 53 (13): 4537–4543. DOI: 10.1016/j.electacta.2008.01.045 |
| [13] | MECH K, ZABINSKI P, MUCHA M, et al. Electrodeposition of catalytically active Ni-Mo alloys[J]. Archives of Metallurgy and Materials, 2013, 58 (1): 227–229. DOI: 10.2478/v10172-012-0178-1 |
| [14] |
孔亚鹏, 陈建设, 刘奎仁, 等. 脉冲镀Ni-Mo-Co合金镀层及其析氢性能[J].
东北大学学报(自然科学版), 2016, 37 (6): 815–819.
KONG Y P, CHEN J S, LIU K R, et al. Catalytic property of Ni-Mo-Co alloy coating prepared by pulse plating[J]. Journal of Northeastern University(Natural Science), 2016, 37 (6): 815–819. DOI: 10.3969/j.issn.1005-3026.2016.06.012 |
| [15] | HAN Q, CUI S, PU N W, et al. A study on pulse plating amorphous Ni-Mo alloy coating used as HER cathode in alkaline medium[J]. International Journal of Hydrogen Energy, 2010, 35 (11): 5194–5201. DOI: 10.1016/j.ijhydene.2010.03.093 |
| [16] |
谭秀兰, 唐永建, 刘颖, 等. 去合金化制备纳米多孔金属材料的研究进展[J].
材料导报, 2009, 23 (3): 68–76.
TAN X L, TANG Y J, LIU Y, et al. Progress in research on preparations of nanoporours metals by dealloying[J]. Materials Review, 2009, 23 (3): 68–76. |
| [17] | ERLEBACHER J, AZIZ M J, KARMA A, et al. Evolution of nanoporosity in dealloying[J]. Nature, 2001, 410 (6827): 450–453. DOI: 10.1038/35068529 |
| [18] |
周琦, 吴海涛, 贾建刚, 等. 纳米多孔镍的多层次结构及其影响因素[J].
材料热处理学报, 2013, 34 (8): 11–15.
ZHOU Q, WU H T, JIA J G, et al. Fabrication of nanoporous Ni with multi-hierarchical structure and its influencing factors[J]. Transactions of Materials and Heat Treatment, 2013, 34 (8): 11–15. |
| [19] |
黄金昭, 徐征, 李海玲, 等. 纳米晶Ni-Mo-Fe催化阴极的制备与表征[J].
北京交通大学学报, 2007, 31 (6): 35–37.
HUANG J Z, XU Z, LI H L, et al. Preparation and chara-cterization of nanocrystalline Ni-Mo-Fe as cathode catalyst[J]. Journal of Beijing Jiaotong University, 2007, 31 (6): 35–37. DOI: 10.3969/j.issn.1673-0291.2007.06.009 |
| [20] |
张卫国, 尚云鹏, 刘丽娜, 等. 电化学法制备Ni-W-P纳米线阵列电极及其催化析氢性能[J].
物理化学学报, 2011, 27 (4): 900–904.
ZHANG W G, SHANG Y P, LIU L N, et al. Electrochemical preparation of a Ni-W-P nanowire array and its photoelectrocat-alytic activity for the hydrogen evolution reaction[J]. Acta Physico-Chimica Sinica, 2011, 27 (4): 900–904. DOI: 10.3866/PKU.WHXB20110344 |
| [21] |
王进.镍基Ni-Mo合金电极的制备及其电催化析氢性能研究[D].重庆: 重庆大学, 2013. WANG J. Studies on the electrocatalytic hydrogen evolution of Ni based Ni-Mo alloy electrodes[D]. Chongqing: Chongqing University, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10611-1013044244.htm |
 2019, Vol. 47
2019, Vol. 47


