文章信息
- 黄连根, 郑玉婴
- HUANG Lian-gen, ZHENG Yu-ying
- 树枝状介孔二氧化硅的制备及其负载纳米银的抗菌性
- Preparation of Dendritic Mesoporous Silica and Its Antibacterial Properties of Loaded Nano Ag
- 材料工程, 2018, 46(10): 135-141
- Journal of Materials Engineering, 2018, 46(10): 135-141.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2017.001363
-
文章历史
- 收稿日期: 2017-11-08
- 修订日期: 2018-01-20
多孔二氧化硅不仅拥有比表面积大、化学稳定性好、生物相容性好、孔径大小可调控[1-2]等特点,还可以在其孔道中容纳大量的客体分子,比如生物医药、无机纳米粒子等[3-4]。因此,已被广泛应用于催化、生物医学、环境能源、载体,支架等领域。目前介孔二氧化硅的主要合成方法有溶胶-凝胶法、水热法等。
近几年来学术界致力于研究多孔二氧化硅纳米材料的形态、结构和性能的可控性;如粒子大小、粒子形状、孔隙结构、大的比表面积、生物相容性好、易于功能化等[5-7]。这些精细结构,往往能直接影响其物理化学性能,性能又决定了用途,因此对纳米二氧化硅精细结构的调控十分有意义。Polshettiwar[8]等在微乳液系统下,用环己烷为油相、正戊醇为共溶剂,用溴代十六烷基吡啶(CPB)和十六烷基三甲基溴化铵(CTAB)做模板剂在微波水热法下合成了纤维状的纳米二氧化硅粒子。张坤等[9]用溶胶-凝胶法,以十六烷基三甲基对甲基苯磺酸铵盐(CTATos)为模板剂、小分子的有机胺类做催化剂,大规模的合成了单分散的星射状孔道的介孔二氧化硅。赵东元等[10]在微乳液系统下通过调节疏水油相的类型和油相中正硅酸乙酯浓度(TEOS)来实现对孔道孔径大小的调控,从而合成了树枝状介孔二氧化硅。
如今,纳米银因其超高的比表面积和表面活性和导电率以及抗菌性已经被广泛被应用作催化剂材料、防静电材料、低温超导材料和医用抗菌材料[11-13]。本研究以正硅酸乙酯为硅源(TEOS),十六烷基三甲基溴化铵(CTAB)做模板剂,氨水做催化剂,采用溶胶-凝胶法在乙醚、水、乙醇的共同作用下合成树枝状介孔二氧化硅,并探究不同条件对二氧化硅微球形貌以及性能的影响,从而推理出可能的生成机理。通过对介孔二氧化硅的修饰,原位化学还原在树枝状二氧化硅孔道及其外表面负载上纳米银,并测试其抗菌性能。
1 实验材料与方法 1.1 主要原料及仪器正硅酸乙酯(TEOS,AR)、聚乙烯吡咯烷酮(PVP-K30,GR)、牛肉浸膏,以上试剂购自天津市福晨化学试剂厂;氨水(25%~28%)、乙醇(AR)、乙醚(AR)、甲苯(AR)、盐酸(36%~38%),以上试剂购自天津市恒兴化学试剂制造有限公司;硼氢化钠(AR)、十六烷基三甲基溴化铵(CTAB)、3-氨基丙基三乙氧基硅烷(APTES,98%)、硝酸银(AR)以上试剂购自麦克林;琼脂粉购自天津市致远化学试剂有限公司;蛋白胨购自北京奥博星生物技术有限责任公司;所有实验使用去离子水。
1.2 树枝状介孔二氧化硅的制备在室温下将0.5g的CTAB溶解在70mL的去离子水中,再加入20mL的乙醚、10mL的乙醇和一定量的氨水,磁力搅拌;30min后将2.5mL的TEOS和一定量的APTES滴加入并搅拌4h;4h后加入一定量的盐酸溶液调节pH使得溶液的pH为7,再次搅拌15min。然后将所得的溶液离心分离,分别用乙醇、去离子水洗涤3次,最后于60℃下干燥6h。
1.3 APTES改性树枝状介孔二氧化硅取500mg的树枝状介孔二氧化硅分散在50mL的甲苯中超声1h;取圆底烧瓶,将上述二氧化硅分散液加入烧瓶中而后滴加入2mL的APTES,85℃下回流磁力搅拌15h;然后离心、分离、洗涤、干燥。
1.4 纳米银负载树枝状介孔二氧化硅配制0.002mol·L-1的硝酸银溶液、0.005mol·L-1的硼氢化钠溶液备用;取介孔二氧化硅40mg将其分散在20mL的乙醇当中,超声90min;取20mL新制的硝酸银溶液加入到上述的乙醇溶液中,室温下遮光反应2h[14]。2h后将4mg的PVP-K30分散到10mL的去离子水中[15],然后逐滴加入到反应溶液中,搅拌30min;然后取10mL新制的硼氢化钠溶液滴加入到反应溶液中。滴加完后立即离心,并且用乙醇和去离子水各洗涤3次;最后冷冻干燥15h。
1.5 抗菌实验最低抑菌浓度(MIC)测试:取新鲜的大肠杆菌(E.coli)悬浊液,将其稀释到浓度为1.5×108CFU/mL(根据经验,细菌悬浊液在600nm波长(OD600)处的紫外吸光值为0.5时,细菌悬浊液的浓度为1.5×108CFU/mL)。取一定量的样品,制备一系列浓度的样品溶液和一组空白溶液。取1mL稀释过的细菌悬浊液和1mL一定浓度的样品溶液以及98mL的液体培养基NB将三者分别加入锥形瓶。细菌液悬浮液最后的浓度为1.5×106CFU/mL,样品溶液最后的浓度为10,20,30,40,50,60,80mg·L-1以及一组空白的对照样。将上述的混合液在37℃下摇床培养24h。每隔一段时间测试其OD600的值。而24h后混合液的OD600不再变化的最小浓度就是最低抑菌浓度MIC。
最小杀菌浓度(MBC)测试:取上述24h后OD600不再改变的几组混合液均匀的涂到固体培养基中,放在37℃的恒温箱中继续培养24h,观察菌落的生长情况。没有菌落生长的最小浓度即为最小杀菌浓度MBC。
1.6 表征用FE-SEM, SUPRA 55热场发扫描电子显微镜和JEM-100CXII透射电子显微镜观察样品形貌;用ULTIMA ⅢX射线衍射仪测定样品,X射线源为铜靶,扫描范围2θ为5°~90°,扫描速率为5 (°)/min;用3flex比表面孔径分析仪测试样品,测试前在60℃下脱气8h,样品比表面由BET法算得。用UV-1800紫外分光光度计测试抗菌实验中混合液的吸光度。
2 结果与讨论 2.1 反应条件对二氧化硅微球的影响表 1列出了二氧化硅微球制备过程中药品的添加量以及对应粒径的大小,通过控制药品的单一变量以研究该药品在反应过程中所发挥的作用。
| Sample | Ethanol/mL | Diethyl ether/mL | NH2·OH/mL | H2O/mL | APTES/mL | Particle size/nm |
| 1 | 10 | 0 | 0.80 | 90 | 0.10 | 80-100 |
| 2 | 10 | 20 | 0.80 | 70 | 0.00 | 150-200 |
| 3 | 10 | 20 | 0.80 | 70 | 0.05 | 200-250 |
| 4 | 10 | 20 | 0.80 | 70 | 0.10 | 400-500 |
| 5 | 10 | 20 | 0.80 | 70 | 0.20 | 450-500 |
图 1(a),图 2(a)分别为没有加入乙醚制备得的二氧化硅微球SEM,TEM照片。当没有乙醚参与反应时,生成的SiO2微球只有80~100nm,且表面孔径很小,微球内的孔呈无序状态。图 1(c), (d), (e)SEM照片是加入乙醚后制备得的二氧化硅微球,相较于图 1(a),该微球粒径增大,表面孔径也增大不少。在乙醚条件下制备的SiO2微球内部存在有序的介孔孔道,其由内往外不断增大,如图 2(b);这与杜鑫[16]所阐述的动态乙醚乳液系统原理一致:在室温搅拌下受TEOS水解反应放热的影响,沸点只有34.6℃的乙醚受热在反应体系内气化,气化过程中乙醚气体逃逸促成树枝状孔道生成。

|
图 1 样品1(a),样品2(b),样品3(c),样品4(d),样品5(e)的SEM照片 Fig. 1 SEM images of sample 1(a), sample 2(b), sample 3(c), sample 4(d), sample 5(e) |

|
图 2 样品1(a)和样品4(b)的TEM照片 Fig. 2 TEM images of sample 1(a) and sample 4(b) |
没有加入APTES制备的二氧化硅微球虽有介孔孔道生成,但呈一种扁平的囊泡状,如图 1(b)所示。加入APTES后制备的二氧化硅从扁平囊泡状变成球状,有良好的单分散性,并且在微球的表面能明显地看到介孔,如图 1(c), (d), (e)。图 2(b)树枝状介孔孔道的生成是因为乙醚的逃逸使得二氧化硅微球在生成的过程中内部塌陷,加入APTES后,其含硅氧烷一端参与水解,含有氨基亲油端伸入胶束内,当乙醚逃逸时其能起到弥补、支撑作用,从而减少因乙醚逃逸所产生的塌陷和变形。APTES的加入量对二氧化硅微球的单分散性、粒径和孔径的影响很大。随着APTES量的增加,微球的粒径不断增加,单分散性不断提高,表面孔径不断减小。
微球粒径的增大和单分散性的提高得益于APTES的端氨基(—NH2),虽然此端氨基呈弱碱性,但也能诱发亲核反应(二氧化硅水解反应)[17]。当APTES的量增加,端氨基的数目也相应地增加,效果和增加氨水的量是类似的,故而二氧化硅微球的粒径增大、单分散性增加;而微球孔道变窄,是因为随着APTES量的增大,能够弥补乙醚逃逸的分子数目就变多,因此坍塌变形的程度下降,孔道变窄。
2.1.3 生成机理分子堆积参数P=V/(a·l)[18],其中P为分子堆积参数,V为表面活性剂亲油端所占的有效体积,a为表面活性剂的亲水端所占的有效面积,l为亲油链端的有效长度。
图 3为该树枝状介孔二氧化硅生成机理。乙醇的加入使得水和乙醚相互的溶解性增加,达到增溶的效果,使得CTAB的亲水链端的有效面积减少,因而V/a的值增大,P值也相应增大,这会使得1/2 < P < 2/3,此时会生成具有一定曲率的三维圆柱形胶束[18];加入TEOS后,大量带有负电荷的硅酸酸根缩聚物将与胶束中的CTA+的亲水端相互吸引,界面被无机硅酸根缩聚物填满,此时硅酸根负电荷与胶束正电荷达到平衡,无机二氧化硅与CTAB发生协同作用[19],胶束与CTAB相互作用生成液晶。随着缩聚反应的进行,硅酸根不断减少、负电荷密度下降,为使得正负电荷趋于平衡,界面会向内部凹陷以增大面积,使得正电荷的密度下降,从而达到电荷平衡;因此表面活性剂的疏水链端的有效体积就减少,V/a的值减小,P不断减小;与此同时,TEOS水解生成的热量使胶束内部的乙醚不断挥发向外扩散,增溶效果不断减弱,P再次减小,当P < 1/3时,胶束的排列方式往球形的堆积方式发展。在水解反应产生的热量下,乙醚快速气化分散,使得胶束产生变形,内部发生塌陷;加入APTES后,其一端与TEOS一起生成硅酸缩聚物与胶束CTA+相互吸引,而另一端的有机链端插入胶束内部的疏水相,这使得:(1)对乙醚的扩散起到了一定的阻碍作用;(2)对乙醚逃逸产生的空缺起到了一定的弥补作用。这两点都能减少胶束变形和塌陷,促使二氧化硅微球的树枝状孔道生成。综上所述,二氧化硅是在协同作用理论、电荷密度匹配机理[20]和分子堆积理论的共同作用下往球形发展的;而树枝状孔道的生成是得益于乙醚的逃逸和APTES的加入。

|
图 3 树枝状介孔二氧化硅生成机理 Fig. 3 Formation mechanism of dendritic mesoporous SiO2 |
图 4是4号样品的N2吸附-脱附等温线和孔径分布曲线。其N2吸附脱附曲线类似于Ⅳ型。观察图 4(a),在较低相对压力下的轻微凸起是介孔表面的单分子层吸附引起的;相对压力在0.4时发生转折。并且在0.4~0.9之间有一个明显吸附脱附滞后回环,这是典型的介孔发生毛细管凝聚现象所致。当相对压力大于0.9时再次发生突跃,这说明了样品中还存在更大的孔。图 4(b)在3.8nm左右有一个尖锐的峰,在45~60nm左右有一个宽峰,说明该样品的孔径分布较窄且集中在3.8nm,并且还有相当一部分孔的孔径在50nm左右,这与N2吸附-脱附等温线相吻合而且也与SEM,TEM照片相印证。该样品的比表面积为620.95m2·g-1,孔容为0.70cm3·g-1。

|
图 4 4号样品的比表面孔径分析 (a)N2吸附-脱附等温线;(b)孔径分布曲线 Fig. 4 Specific surface and pore size analysis of sample 4 (a)N2 adsorption-desorption isotherm curves; (b)pore size distribution curves |
图 5为4号样品负载纳米银SEM照片和TEM照片。图 5(a)的白色颗粒和图 5(b)的黑色颗粒均为纳米银,说明纳米银成功负载到二氧化硅上。通过EDS分析可知该样品银的质量分数为8%。

|
图 5 树枝状介孔二氧化硅负载纳米银的SEM(a)和TEM(b)照片 Fig. 5 SEM(a) and TEM(b) images of dendritic mesoporous SiO2 loaded nano Ag |
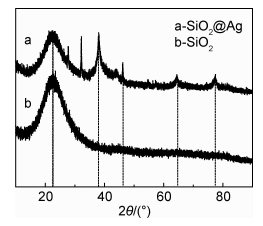
图 6为树枝状介孔二氧化硅负载纳米银前、后的XRD谱图。曲线a,b在2θ=23.06°处的强峰为二氧化硅的特征峰。相较于曲线b,曲线a在38.13°,46.16°,64.40°,77.39°存在特征峰,这与银的JCPDS卡片04-0783一致。两条曲线均无其他杂峰出现,说明该样品纯度高,银元素以单质的形式存在。
|
图 6 二氧化硅和二氧化硅负载纳米银的XRD谱图 Fig. 6 XRD spectra of SiO2 and SiO2 loaded nano Ag |
图 7为不同浓度样品的MIC曲线。图中空白组样品随着时间的推移细菌悬浊液的浓度不断增大,而其他组样品在2~6h的细菌悬浊液的OD600几乎为0,浓度几乎没有增加。表明二氧化硅负载纳米银的确有抗菌功效。随着时间推移浓度在40mg·L-1以下的样品的细菌浓度不断增加,24h后细菌浓度增长到和空白组一样的水平;而浓度≥50mg·L-1的样品的细菌浓度在24h内几乎不变,故而可以断定该样品的MIC在40~50mg·L-1,又因为该样品银的含量为8%,因此该样品中银的MIC在3.16~3.95mg·L-1

|
图 7 不同浓度二氧化硅负载纳米银MIC曲线 Fig. 7 MIC curves of SiO2 loaded nano Ag at different concentrations |
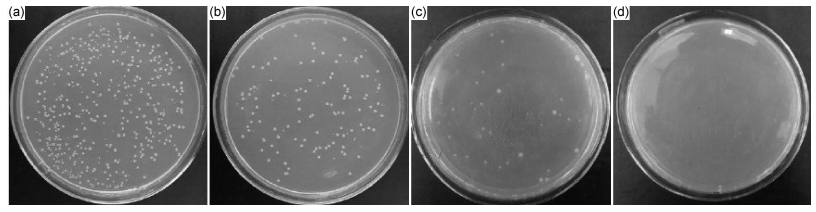
图 8为不同浓度样品的MBC实验,经过24h的繁殖40,50,60mg·L-1的样品都有细菌菌落产生;唯独80mg·L-1浓度的样品没有细菌菌落产生, 故而可以认定MBC为80mg·L-1,因此该样品中银的MBC为6.32mg·L-1。直径为7nm的纯银,对大肠杆菌的MIC和MBC分别为6.5mg·L-1和12.5mg·L-1[21];本文样品中银的MIC在3.16~3.95mg·L-1,MBC为6.32mg·L-1,抗菌效果高于纯纳米银。
|
图 8 不同浓度样品MBC实验 (a)40mg·L-1;(b)50mg·L-1;(c)60mg·L-1;(d)80mg·L-1 Fig. 8 MBC experiment of different concentration samples (a)40mg·L-1; (b)50mg·L-1; (c)60mg·L-1; (d)80mg·L-1 |
(1) 二氧化硅是在协同作用理论、电荷密度匹配机理、和分子堆积理论的共同作用下往球形发展的;而树枝状孔道的生成是得益于乙醚的逃逸和硅烷结构助剂的加入。APTES的加入弥补乙醚逃逸带来的坍塌,并且其端氨基能够起到催化的作用有利于二氧化硅微球单分散性的增加和球形状态的维持。
(2) 树枝状介孔二氧化硅是不具备抗菌效果的,当负载上纳米银后抗菌效果明显提升;该样品中银对大肠杆菌的MIC在3.16~3.95mg·L-1,MBC为6.32mg·L-1,均低于纯纳米银。也就是说本文制备的二氧化硅负载纳米银的抗菌效果大于纯银的抗菌效果,因此可降低抗菌成本,在抗菌领域上具有很大的前景。
| [1] |
吴巧利, 权桂兰, 洪瑜, 等. 介孔二氧化硅/乙基纤维素缓释骨架的制备与释放行为的研究[J].
药学学报, 2015, 50 (4): 492–499.
WU Q L, QUAN G L, HONG Y, et al. Preparation and release behaviour of mesoporous silica/ethylcellulose sustained-release mini-matrix[J]. Acta Pharmaceutica Sinica, 2015, 50 (4): 492–499. DOI: 10.3969/j.issn.1008-7303.2015.04.17 |
| [2] |
杨惠, 黄超, 廖世军. 具有特殊形貌的介孔氧化硅的合成及其应用研究进展[J].
化工进展, 2014 (8): 2089–2095.
YANG H, HUANG C, LIAO S J. Progress of synthesis and application of mesoporous silica with special morphology[J]. Chemical Industry and Engineering Progress, 2014 (8): 2089–2095. |
| [3] |
郝晓红, 张翠妙, 刘小龙, 等. 基于介孔二氧化硅的多功能纳米药物输送体系研究进展[J].
生物化学与生物物理进展, 2013, 40 (10): 1014–1022.
HAO X H, ZHANG C M, LIU X L, et al. Recent advances of mesoporous silica based multifunctional nano drug delivery systems[J]. Progress in Biochemistry and Biophysics, 2013, 40 (10): 1014–1022. |
| [4] | SHE X, CHEN L, VELLEMAN L, et al. Fabrication of high specificity hollow mesoporous silica nanoparticles assisted by Eudragit for targeted drug delivery[J]. Journal of Colloid and Interface Science, 2015, 445 : 151–160. DOI: 10.1016/j.jcis.2014.12.053 |
| [5] | TANG F, LI L, CHEN D. Mesoporous silica nanoparticles:synthesis, biocompatibility and drug delivery[J]. Advanced Materials, 2012, 24 (12): 1504–1534. DOI: 10.1002/adma.201104763 |
| [6] |
郑玉婴, 曹宁宁. 氧化石墨烯纳米带杂化粒子和石墨烯纳米带的研究进展[J].
材料工程, 2017, 45 (6): 118–128.
ZHENG Y Y, CAO N N. Research progress on graphene oxide nanoribbons nano hybrids and graphene nanoribbons[J]. Journal of Materials Engineering, 2017, 45 (6): 118–128. |
| [7] | HE Q, SHI J. MSN anti-cancer nanomedicines:chemotherapy enhancement, overcoming of drug resistance, and metas tasis inhibition[J]. Advanced Materials, 2014, 26 (3): 391–411. DOI: 10.1002/adma.201303123 |
| [8] | POLSHETTIWAR V, CHA D, ZHANG X, et al. High-surface-area silica nanospheres (KCC-1) with a fibrous morphology[J]. Angewandte Chemie, 2010, 122 (50): 9846–9850. DOI: 10.1002/ange.201003451 |
| [9] | ZHANG K, XU L L, JIANG J G, et al. Facile large-scale synthesis of monodisperse mesoporous silica nanospheres with tunable pore structure[J]. Journal of the American Chemical Society, 2013, 135 (7): 2427–2430. DOI: 10.1021/ja3116873 |
| [10] | SHEN D, CHEN L, YANG J, et al. Ultradispersed palladium nanoprticles in three-dimensional dendritic mesoporous silica nanospheres:toward active and stable heterogeneous catalysts[J]. ACS Applied Materials & Interfaces, 2015, 7 (31): 17450–17459. |
| [11] |
郑辉东, 邱洪峰, 郑玉婴, 等. 负载纳米银EVA复合发泡材料的制备及其抗菌性能[J].
材料工程, 2016, 44 (7): 107–112.
ZHENG H D, QIU H F, ZHENG Y Y, et al. Preparation and antibacterial property of EVA composite foams supported by nano-silver[J]. Journal of Materials Engineering, 2016, 44 (7): 107–112. |
| [12] | JIANG H, MANOLACHE S, WONG A C L, et al. Plasma-enhanced deposition of silver nanoparticles onto polymer and metal surfaces for the generation of antimicrobial characteristics[J]. Journal of Applied Polymer Science, 2004, 93 (3): 1411–1422. DOI: 10.1002/(ISSN)1097-4628 |
| [13] |
邓城, 漆小鹏, 李倩, 等. 沉淀法与水热法合成载银羟基磷灰石及其抗菌性能[J].
材料工程, 2017, 45 (4): 113–120.
DENG C, QI X P, LI Q, et al. Synthesis and antibacterial property of silver doped hydroxyapatite by precipitation and hydrothermal method[J]. Journal of Materials Engineering, 2017, 45 (4): 113–120. |
| [14] |
叶伟杰, 陈楷航, 蔡少龄, 等. 纳米银的合成及其抗菌应用研究进展[J].
材料工程, 2017, 45 (9): 22–30.
YE W J, CHEN K H, CAI S L, et al. Progress in research on synthesis and antibacterial applications of silver nanoparticles[J]. Journal of Materials Engineering, 2017, 45 (9): 22–30. |
| [15] |
曹洋, 刘平, 魏红梅, 等. 液相化学还原法制备纳米银焊膏及其连接性[J].
材料工程, 2015, 43 (4): 79–84.
CAO Y, LIU P, WEI H M, et al. Synthesis of silver nanoparticles paste by aqueous reduction and its connectivity[J]. Journal of Materials Engineering, 2015, 43 (4): 79–84. |
| [16] |
杜鑫, 赵彩霞, 黄洪伟, 等. 树枝状多孔二氧化硅纳米粒子的制备及其在先进载体中的应用[J].
化学进展, 2016, 28 (8): 1131–1147.
DU X, ZHAO C X, HUANG H W, et al. Synthesis of dendrimer-like porous silica nanoparticles and their applications in advanced carrier[J]. Progress in Chemistry, 2016, 28 (8): 1131–1147. |
| [17] |
曹红霞, 冯晓静, 霍冀川. 单分散二氧化硅微球的制备及表面化学修饰[J].
人工晶体学报, 2016, 45 (8): 2050–2055.
CAO H X, FENG X J, HUO J C. Synthesis and surface chemical modification of the monodisperse silica microsphere[J]. Journal of Synthetic Crystals, 2016, 45 (8): 2050–2055. DOI: 10.3969/j.issn.1000-985X.2016.08.012 |
| [18] |
陈永.
多孔材料制备与表征[M]. 合肥: 中国科学技术大学出版社, 2010: 138-140.
CHEN Y. Preparation and characterization porous material[M]. Hefei: University of Science & Technology China Press, 2010: 138-140. |
| [19] | HUO Q, MARGOLESE D I, CIESLA U, et al. Organization of organic molecules with inorganic molecular species into nanocomposite biphase arrays[J]. Chemistry of Materials, 1994, 6 (8): 1176–1191. DOI: 10.1021/cm00044a016 |
| [20] | MONNIER A, SCHVTH F, HUO Q, et al. Cooperative formation of inorganic-organic interfaces in the synthesis of silicate mesostructures[J]. Science, 1993, 261 (5126): 1299–1303. DOI: 10.1126/science.261.5126.1299 |
| [21] | CHEMOUSOVA S, EPPLE M. Silver as antibacterial agent:ion, nanoparticle, and metal[J]. Angewandte Chemie International Edition, 2013, 52 (6): 1636–1653. DOI: 10.1002/anie.v52.6 |
 2018, Vol. 46
2018, Vol. 46


