文章信息
- 李高锋, 李智敏, 宁涛, 张茂林, 闫养希, 向黔新
- LI Gao-feng, LI Zhi-min, NING Tao, ZHANG Mao-lin, YAN Yang-xi, XIANG Qian-xin
- 锂离子电池正极材料表面包覆改性研究进展
- Research Progress of Cathode Materials Modified by Surface Coating for Lithium Ion Batteries
- 材料工程, 2018, 46(9): 23-30
- Journal of Materials Engineering, 2018, 46(9): 23-30.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2017.001182
-
文章历史
- 收稿日期: 2017-09-21
- 修订日期: 2018-04-25
2. 贵州振华新材料有限公司, 贵阳 550016
2. Guizhou Zhenhua E-chen Co., Ltd., Guiyang 550016, China
锂离子二次电池具有工作电压高、容量大、体积小、重量轻、循环寿命长等优点,在便携式电子产品、电动自行车、电动汽车、能源存储等领域具有广泛的应用。正极材料作为影响锂离子电池性能和应用的关键因素,近年来备受各国研究人员关注,得到了迅速的发展[1]。
目前研发的锂离子电池正极材料按照其结构主要分为3类:(1)具有六方层状结构的锂金属化合物LiMO2(M=Co,Ni,Mn),属于R-3m空间群,代表性材料为钴酸锂(LiCoO2)、三元镍钴锰酸锂(NCM)和镍钴铝酸锂(NCA);(2)具有Fd-3m空间群的尖晶石结构正极材料,代表性材料为锰酸锂(LiMn2O4)[2];(3)聚阴离子结构的正极材料,代表性材料主要有橄榄石结构的磷酸亚铁锂LiFePO4、硅酸亚铁锂(Li2FeSiO4)和磷酸钒锂(LiVPO4)等。虽然正极材料得到了不断的开发,但是其仍存在结构稳定性差、阳离子混排、过渡金属溶解、电压衰减、倍率性能和高温性能差、首次库伦效率低等问题,限制了锂离子电池的进一步商业化应用[3]。
为了解决正极材料的上述缺陷,研究人员做了大量的改性研究工作,主要包括体掺杂、表面包覆、纳米结构及优化合成工艺等[4-5]。其中,体掺杂的目的是抑制阳离子混排,进一步稳定正极材料的结构,以提高锂离子电池的循环稳定性及安全性。但是,掺杂离子多为非电化学活性离子(如Al3+,Y3+,Mg2+等),会降低锂离子电池的比容量。具有纳米结构的正极材料虽然可以有效缩短Li+的传输路径,提高Li+离子的传输速率,但是纳米结构使正极材料与电解液接触面积增大,会导致电解液副反应增强。另外,纳米结构正极材料的合成条件苛刻,形貌难以控制。在正极材料的制备技术方面,目前常采用的方法有固相法、共沉淀法、溶胶-凝胶法及气相沉积法等[6-8]。对合成工艺的优化可以减小阳离子混排的程度,提高正极材料的结构与电化学稳定性。而包覆作为一种材料表面修饰的常用方法,其在稳定正极材料结构、抑制阳离子溶解与提高电化学稳定性等方面表现出积极的作用,经常与体掺杂一起作为正极材料改性的有效手段。鉴于此,本文主要系统讨论正极材料包覆改性的研究进展。
1 正极材料表面包覆机理表面包覆是改善锂离子电池正极材料热稳定性及结构稳定性,提高粒子表面活性,使粒子具有新的物理、化学和力学性能的有效方法之一[9]。目前,关于正极材料的包覆改性机理主要有以下3种:(1)表面包覆物能够阻止正极活性材料与电解液的直接接触,避免过渡金属溶解[10],例如,采用ZrO2包覆LiCoO2可以减少钴在电解液中的溶解[11]。(2)抑制John-Teller效应,进而抑制相变,使正极活性材料在循环过程中保持结构稳定[12]。LiNixMn2-xO4包覆LiMn2O4正极材料后,可导致其晶格收缩,增强Mn—O键的强度,提高LiMn2O4尖晶石相结构的稳定性,抑制充放电过程中LiMn2O4表面的John-Teller扭曲[13]。(3)提高活性材料的导电性。一般而言,导电包覆层的电阻比较低,可以增强表面Li+的传导,降低电池极化及正极材料/电解液的界面电阻[14]。
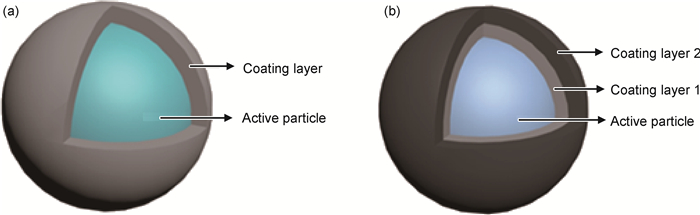
包覆结构主要有两种形式:一是在正极材料颗粒表面包覆几纳米厚度的异质材料层,如图 1(a)所示;另一种是对正极材料表面进行两种或两种以上的复合材料包覆,如图 1(b)所示。
|
图 1 包覆结构示意图(a)单一包覆; (b)复合包覆 Fig. 1 Schematic diagram of coating structure (a)single coating; (b)composite coating |
研究发现,大多数氧化物包覆可以稳定活性物质的结构,起到抑制电解液反应的作用,能够很好地改善锂离子电池的电化学性能。同时,氧化物和导电材料(如碳材料)复合包覆活性材料,可以提高正极材料的导电性,进一步提高电池的倍率性能[15]。显然,两种或多种包覆材料的协同作用,使得包覆修饰的效果会更好一些。
2 正极材料表面包覆研究进展 2.1 氧化物包覆作为一种典型的包覆材料,氧化物在锂离子电池正极材料表面包覆改性中的应用十分广泛。用于包覆正极材料的氧化物有Al2O3,MgO,TiO2,ZnO,ZrO2,SiO2,CeO2,RuO2等,其中,以Al2O3,MgO,TiO2和ZrO2氧化物包覆最为常见。包覆的方法主要有固相法、溶胶-凝胶法、沉淀法、水热法及气相沉积法等。
Lee等[16]采用固相法在LiNi0.6Co0.2Mn0.2O2正极材料表面包覆Al2O3,发现包覆Al2O3后电池的循环性能得到提高,在0.5C下循环100次的容量保持率从91%提高到92.8%。研究表明,Al2O3包覆层有效地抑制了活性材料与电解液的副反应。He等[17]采用Sb掺杂的SnO2包覆LiNi0.8Co0.15Al0.05O2,结果表明,SnO2可以有效抑制电极界面副反应和LiNi0.8Co0.15Al0.05O2的相变,电池在1C下循环200次后容量保持率为91.7%,表现出很好的循环性能。同时,Sb掺杂SnO2可以增强正极材料导电性,提高电池的倍率性能。Tao等[18]在LiNi0.5Mn1.5O4正极材料表面包覆TiO2后,其在15C下放电比容量为74.5mAh·g-1,在2C下循环500次后的容量保持率为88.5%,表现出很好的倍率性能和循环稳定性,而未包覆TiO2的LiNi0.5Mn1.5O4循环500次后的容量保持率仅为33.0%。Kumar等[19]采用沉淀法,在0.5Li2MnO3-0.5LiNi0.5Mn0.5O2表面包覆了一层MgO纳米颗粒,结果表明,MgO包覆可以增强材料的结构稳定性,但是降低了活性材料的离子和电子电导率,影响电池的倍率性能。对于橄榄石型磷酸盐正极材料,Saroha等[20]在LiFePO4表面包覆ZnO,发现经2.5%(质量分数,下同)ZnO包覆后,LiFePO4在0.1C下的放电比容量达到(160±5)mAh·g-1,而未包覆的仅为85mAh·g-1。这是因为ZnO包覆层表面存在大量的悬挂键能够快速吸附O2-和O-,改变材料的表面能,极大地改善了LiFePO4的导电性。此外,Zhou等[21]在富镍层状LiNi0.915Co0.075Al0.01O2(NCA)颗粒表面包覆一层非晶SiO2,如图 2所示。可以明显看出在NCA颗粒表面包覆一层非晶SiO2,厚度约50nm。性能测试表明,SiO2包覆提高了材料的循环稳定性、高倍率性能及热稳定性。包覆后的NCA在1C倍率下放电比容量为181.3mAh·g-1,经过50次循环后容量保持率为90.7%;并且在60℃温度下,以1C倍率循环50次后的容量保持率比未包覆正极材料提高了12.5%。以上研究均表明,在锂离子电池正极材料表面包覆氧化物能够很好地抑制正极材料与电解液副反应发生,抑制正极材料的相变,以及提高材料的导电性。
另外,氧化物包覆层还可以与电解质如LiPF6分解产生的HF反应生成氟化物,减少电解液中HF的含量,缓解过渡金属的溶解,从而提高了正极材料的结构稳定性。Myung等[22]研究证明了Al2O3包覆层与HF反应生成AlF3的过程为:
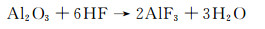
|
(1) |
在Al2O3包覆层表面生成的AlF3,可以有效地阻止电解液对Al2O3包覆层的侵蚀,从而起到稳定正极材料结构的作用。
2.2 氟化物包覆氟化物也是在锂离子电池正极材料包覆改性中被广泛研究应用的材料之一。锂离子电池电化学性能衰减的一个关键因素是电解质LiPF6在电池工作过程中会不断分解产生高腐蚀性的氢氟酸(HF),导致正极材料中活泼金属的溶解。LiPF6的分解反应如式(2)所示[23]:
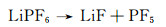
|
(2) |
反应生成的LiF沉积在活性材料表面, 其具有较低的Li+及电子透过率;并且PF5可以进一步与微量的H2O反应产生HF,如式(3)所示。
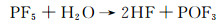
|
(3) |
因此,提高锂离子电池容量保持率的一种重要的方法就是减缓活性材料中过渡金属的溶解。大多数氧化物在HF中不具有热力学稳定性,氧化物包覆层将会被HF腐蚀,转变为氟化物包覆层。由于氟化物与氧化物的摩尔体积差别较大,会生成应力,进一步导致生成的氟化物层开裂甚至脱落[24]。另外,反应式(3)会进一步增强电极与电解液界面的不稳定性。因此,直接采用氟化物包覆正极材料在锂离子电池中得到应用。一方面,锂离子电池常用的电解液为LiPF6,F-可以有效地抑制界面副反应的发生[25];另一方面,研究发现F-的加入可以降低电荷转移电阻,提高导电性,从而改善正极材料的倍率性能和循环性能[26]。目前研究的包覆用氟化物有AlF3,MgF2,CaF2,YF3,LaF3,GaF3和LiF等[27-29]。
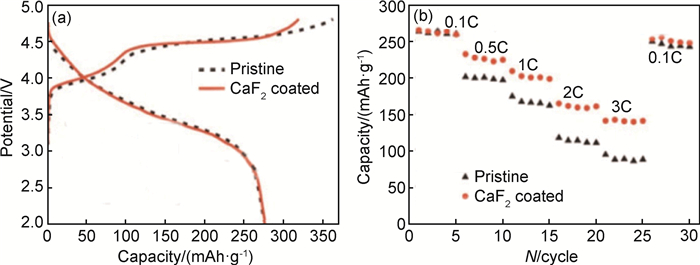
文献[30]研究表明,采用MgF2包覆可以有效地抑制电解液分解产生的HF对正极材料的表面侵蚀作用,提高了电池的循环寿命。同时,Liu等[31]采用化学沉积法在Li1.2Mn0.54Ni0.13Co0.13O2表面包覆约几个纳米厚度的CaF2,图 3为CaF2包覆前和包覆后的TEM照片[31],可以看出,CaF2成功地包覆在Li1.2Mn0.54Ni0.13Co0.13O2颗粒表面。图 4显示了材料包覆后的电化学性能,在0.05C下首次放电比容量为277.3mAh·g-1,库伦效率从76%提高到89.6%;倍率性能也得到明显提高,在3C条件下,放电比容量到达141.5mAh·g-1。另外,CaF2包覆后的Li1.2Mn0.54Ni0.13Co0.13O2在1C下循环100次后的放电比容量为191mAh·g-1,而未包覆材料仅为130mAh·g-1。研究表明,CaF2包覆层可以有效地抑制电解液对Li1.2Mn0.54Ni0.13Co0.13O2的腐蚀,缓解由活性氧产生的电解液氧化副反应的发生;同时,在低电流密度下,CaF2包覆能够诱导Li1.2Mn0.54Ni0.13Co0.13O2从层状结构到尖晶石相结构的转变,提高首次库仑效率。另外,AlF3包覆同样具有诱导Li[Li0.19Ni0.16Co0.08Mn0.57]O2等富锂镍锰氧化物正极材料相变和提高循环稳定性的效果[32-33]。
FeF3作为一种正极材料,其在充电范围2.0~4.5V之间插入一个锂离子时的理论比容量为237mAh·g-1[34],最终反应产物为LiF和Fe,如反应式(4)所示。它可以作为保护层抑制电解液的副反应,同时增强正极材料的结构稳定性[35]。Li等[36]采用FeF3包覆Li[Li0.2Mn0.54Ni0.13Co0.13]O2正极材料,发现FeF3不仅能够提高放电比容量,而且可以提高充放电过程中的循环稳定性。包覆材料在0.5C循环100次后,放电比容量为190mAh·g-1,容量保持率高达95%,而未包覆情况下,放电比容量为170mAh·g-1,容量保持率仅为89%。

|
(4) |
除氧化物、氟化物包覆外,利用复合物包覆来改善正极材料的性能也得到了较多的关注。目前,复合物包覆改性锂离子正极材料主要是含锂的复合氧化物,包括LiAlO2,Li2ZrO3,Li2TiO3,ZnAl2O4和Li2Si2O5等。
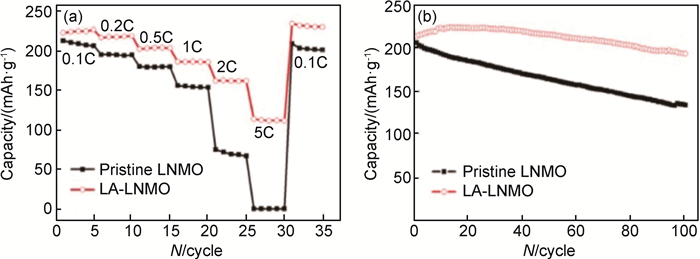
Zhang等[37]采用LiAlO2 (LA)包覆富锂层状氧化物正极材料Li1.2Ni0.6Mn0.2O2(LNMO),使电池的循环稳定性及倍率性能都得到了提高,如图 5所示。同时,其在长循环和高倍率下的电压衰减得到一定程度的抑制。研究发现[38],LiAlO2在有机电解液中具有化学惰性且高温稳定性好,能够抑制电极/电解液界面副反应的发生,提高电极材料的结构稳定性及热稳定性;另外,LiAlO2中的Li+可以部分占据材料内部的Li+位置而具有良好的锂离子电导率,提高了锂离子电池在高倍率下的Li+传输问题,增强了电池的高倍率性能[39]。
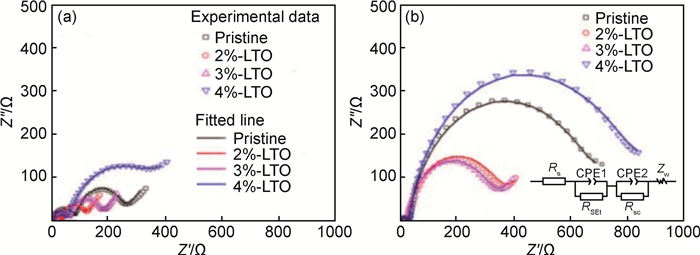
Li2TiO3(LTO)也是一种常见的复合物包覆材料。研究表明[40]:Li2TiO3包覆Li[Li0.2Mn0.51Ni0.19Co0.1]O2(LMNCO)正极材料能够显著提高电池的库仑效率、倍率性能和循环稳定性,其中,3% Li2TiO3的包覆效果最好。同样地,Li2TiO3包覆LMNCO不仅可以稳定正极材料结构,抑制过渡金属溶解,而且Li2TiO3是Li+导体,能够提高Li+在正极材料表面的传输速率,从而提升正极材料的倍率性能。图 6为Li2TiO3包覆LMNCO的EIS图谱,结果表明:Li2TiO3包覆可以有效降低电极材料的阻抗[40]。
另外,Liu等[41]在LiNi0.6Co0.2Mn0.2O2表面包覆Li2Si2O5化合物,在0.1C和10C时的放电比容量分别为213.9mAh·g-1和121.6mAh·g-1,而未包覆的放电比容量分别仅为196.8mAh·g-1和92.1mAh·g-1。显然,与单纯氧化物包覆相比,含锂化合物由于具有较好的Li+通过性能,在改善正极材料结构稳定性的同时,还能够提升材料的倍率性能。
2.4 磷酸盐包覆由于磷酸盐中的PO43-与金属离子之间的化学键具有较强的共价键性,其对正极材料包覆后,会阻碍正极材料与电解液之间的反应,提高材料的稳定性。目前发展的包覆用磷酸盐主要有FePO4,AlPO4和Co3(PO4)2等[42]。
Wang等[43]用FePO4包覆Li1.2Mn0.54Ni0.13Co0.13O2正极材料,发现电池的首次库伦效率、倍率性能、循环性能以及热稳定性都得到提高。3% FePO4包覆的活性材料在0.05C下的放电比容量高达271.7mAh·g-1,并且在0.5C下循环100次后放电比容量仍保持为202.6mAh·g-1。Wu等[44]采用AlPO4包覆Li[Li0.2Fe0.1Ni0.15Mn0.55]O2正极材料,发现5% AlPO4包覆的正极材料在0.1C下循环50次后的比容量为220.4mAh·g-1,表现出很好的循环性能。另外,电极材料颗粒表面固体电解质膜(SEI)的生成与其表面成分密切相关,并且在形成过程中受电化学环境影响。显然,对正极材料表面包覆强价键的磷酸盐,可以稳定电极/电解质界面,影响SEI膜的形成和厚度[45]。
2.5 碳材料包覆随着大功率电子器件的不断发展,提高锂离子电池的高倍率性能成为一个亟待解决的问题。采用导电碳材料包覆技术,可以作为保护层缓解电解质的分解,增强正极材料的稳定性[46];同时,因为具有良好的导电性,碳包覆能够提高电池的高倍率性能[47]。特别是碳材料的成本低,采用它包覆有利于大规模的商业化生产。常见的碳包覆材料有多孔碳、碳纳米线、石墨烯及碳纳米管等。
与其他正极材料相比,橄榄石结构的LiFePO4电导率较差,为了提高LiFePO4的电子电导率,Noerochim等[48]采用多孔碳对其进行包覆,明显增强了电池的稳定性。同样地,已经证明石墨烯包覆LiFePO4纳米颗粒,可以提高正极材料的倍率性能及循环稳定性。Zhou等[49]在LiFePO4纳米颗粒表面包覆3D网状石墨烯,在30C下放电比容量为86mAh·g-1,而多孔碳包覆材料的放电比容量仅为54mAh·g-1。这是因为石墨烯包覆层和LiFePO4纳米颗粒之间形成了较多的空洞,不仅促进了电子快速转移,而且有利于Li+的扩散。
碳材料包覆除了应用于导电性较差的正极材料外,也被应用于其他电极材料中。Cao等[46]采用碳包覆LiCoO2正极材料,在0.1C下放电比容量从110mAh·g-1提高到130mAh·g-1,在1C下碳包覆放电比容量为123mAh·g-1,而纯相仅为31.4mAh·g-1,明显提高了LiCoO2材料的倍率性能。
2.6 金属单质包覆与碳材料包覆相似,在正极材料表面包覆金属单质主要是为了提高正极材料的导电性,从而提高电池的倍率性能,同时起到缓解电极/电解液界面反应的作用,其用于包覆改性锂离子电池正极材料并不多见。可采用气相沉积或原子层沉积的方法进行包覆,包覆物主要为Ag,Al,Au等导电性良好的材料[50]。
Sun等[51]采用电子束气相沉积法在LiNi0.5Mn1.5O4表面包覆Al,发现Al包覆层厚度对LiNi0.5Mn1.5O4性能有较大影响,如果厚度太薄,包覆物不能对活性材料进行有效的保护,而包覆太厚又不利于锂离子的快速扩散。Park等[52]采用Ag包覆LiFePO4来提高其导电率,在0.2C下的首次放电比容量从121mAh·g-1提高到139mAh·g-1,倍率性能从0.2C到1C之间的容量损失率仅为13%,而未包覆Ag的电池容量损失率高达29%。另外,当倍率小于0.25C时,Au包覆LiMn1.5Ni0.5O4材料可以提高20%的比容量,但是在高倍率情况下,因为Au包覆增加了Li+扩散的能垒,比容量又开始衰减[53]。
金属单质包覆的工艺复杂,成本较高,它与氧化物、磷酸盐、碳包覆等的包覆效果相比,没有显著优势,因此,金属单质包覆并没有在锂离子电池正极材料中被广泛应用。
2.7 其他包覆材料除了上述的包覆材料,用于锂离子电池正极材料包覆改性的材料还有硅酸盐、聚合物、玻璃及活性材料梯度包覆等。其中,具有良好导电性的聚合物是一种很好的包覆材料,通过包覆不仅可以提高正极材料的导电性,而且其本身还具有电化学活性。另外,具有良好润湿性及低黏度的玻璃,可以实现极少量的均匀包覆,又玻璃具有良好的离子电导率,利于Li+传输[54]。而梯度包覆主要采用活性材料,除了提高电池材料的结构和电化学稳定性外,其本身具有电化学活性,同时可以提高正极材料的容量。
3 结束语近年来,大量的研究证明:包覆技术可以有效地缓解锂电池中电解液的分解副反应,并稳定正极材料的结构以及提高其电导率。在此基础上,各国研究人员发展了多种包覆物,包括各类氧化物、氟化物、磷酸盐、复合物、碳材料及聚合物等,并取得了很好的成果。但是,继续寻找成本低、制备工艺可控、性能优良的包覆材料,以及深入探讨相关的机理仍是未来正极材料包覆改性的研究重点。另外,优化包覆工艺以实现正极材料的均匀包覆也是一个需要解决的关键技术问题。综合分析各类包覆物的改性机理,诸如聚合物这种既具有良好导电性又兼具电化学活性的包覆材料,未来在锂离子电池正极材料改性方面有着很好的应用前景。
| [1] |
董鹏, 张英杰, 刘嘉铭, 等. 纳米磷酸铁包覆锂离子电池正极材料LiNi0.5Co0.2Mn0.3O2的制备及其电化学性能[J].
材料工程, 2017, 45 (11): 49–57.
DONG P, ZHANG Y J, LIU J M, et al. Fabrication and electrochemical performance of LiNi0.5Co0.2Mn0.3O2 coated with nano FePO4 as cathode material for lithium-ion batteries[J]. Journal of Materials Engineering, 2017, 45 (11): 49–57. |
| [2] | GUO W, MAO F, MA J. Research progress on design strategies, synthesis and performance of LiMn2O4-based cathodes[J]. RSC Advances, 2015, 5 (127): 105248–105258. DOI: 10.1039/C5RA21777F |
| [3] | CHEN Z, DAHN J R. Methods to obtain excellent capacity retention in LiCoO2 cycled to 4.5V[J]. Electrochimica Acta, 2004, 49 (7): 1079–1090. DOI: 10.1016/j.electacta.2003.10.019 |
| [4] | KUMAR S K, GHOSH S, MARTHA S K. Synergistic effect of magnesium and fluorine doping on the electrochemical performance of lithium-manganese rich (LMR)-based Ni-Mn-Co-oxide (NMC) cathodes for lithium-ion batteries[J]. Ionics, 2017, 23 (7): 1655–1662. DOI: 10.1007/s11581-017-2018-9 |
| [5] | LEE S W, KIM M S, JEONG J H, et al. Li3PO4 surface coating on Ni-rich LiNi0.6Co0.2Mn0.2O2 by a citric acid assisted sol-gel method:improved thermal stability and high-voltage performance[J]. Journal of Power Sources, 2017, 360 : 206–214. DOI: 10.1016/j.jpowsour.2017.05.042 |
| [6] | LI L, CAO Y, ZHENG H, et al. AlPO4 coated LiNi1/3Co1/3Mn1/3O2 for high performance cathode material in lithium batteries[J]. Journal of Materials Science:Materials in Electronics, 2017, 28 (2): 1925–1930. DOI: 10.1007/s10854-016-5745-1 |
| [7] | PARK J S, MANE A U, ELAM J W, et al. Atomic layer deposition of Al-W-fluoride on LiCoO2 cathodes:comparison of particle-and electrode-level coatings[J]. ACS Omega, 2017, 2 (7): 3724–3729. DOI: 10.1021/acsomega.7b00605 |
| [8] | XIAO B, WANG B, LIU J, et al. Highly stable Li1.2Mn0.54Co0.13Ni0.13O2, enabled by novel atomic layer deposited AlPO4 coating[J]. Nano Energy, 2017, 34 : 120–130. DOI: 10.1016/j.nanoen.2017.02.015 |
| [9] | YANO A, SHIKANO M, UEDA A, et al. LiCoO2 degradation behavior in the high-voltage phase transition region and improved reversibility with surface coating[J]. Journal of the Electrochemical Society, 2017, 164 (1): A6116–A6122. DOI: 10.1149/2.0181701jes |
| [10] | MENG H, LI L, LIU J, et al. Surface modification of Li-rich layered Li[Li0.17Ni0.17Co0.10Mn 0.56]O2 oxide with LiV3O8 as a cathode material for Li-ion batteries[J]. Journal of Alloys and Compounds, 2017, 690 : 256–266. DOI: 10.1016/j.jallcom.2016.08.089 |
| [11] | YONG J K, CHO J, KIM T J, et al. Suppression of cobalt dissolution from the LiCoO2 cathodes with various metal-oxide coatings[J]. Journal of the Electrochemical Society, 2014, 150 (12): A1723–A1725. |
| [12] | LU J, CHEN Z, MA Z, et al. The role of nanotechnology in the development of battery materials for electric vehicles[J]. Nature Nanotechnology, 2016, 11 (12): 1031–1038. DOI: 10.1038/nnano.2016.207 |
| [13] | LI X, XU Y, WANG C. Suppression of Jahn-Teller distortion of spinel LiMn2O4 cathode[J]. Journal of Alloys and Compounds, 2009, 479 (1/2): 310–313. |
| [14] | LI C, ZHANG H P, FU L J, et al. Cathode materials modified by surface coating for lithium ion batteries[J]. Electrochimica Acta, 2006, 51 (19): 3872–3883. DOI: 10.1016/j.electacta.2005.11.015 |
| [15] | ZHANG C, SHEN L, LI H, et al. Enhanced electrochemical properties of MgF2 and C co-coated Li3V2(PO4)3 composite for Li-ion batteries[J]. Journal of Electroanalytical Chemistry, 2016, 762 : 1–6. DOI: 10.1016/j.jelechem.2015.12.022 |
| [16] | LEE Y S, SHIN W K, KANNAN A G, et al. Improvement of the cycling performance and thermal stability of lithium-ion cells by double-layer coating of cathode materials with Al2O3 nanoparticles and conductive polymer[J]. ACS Applied Materials & Interfaces, 2015, 7 (25): 13944–13951. |
| [17] | HE X, DU C. Electronically conductive Sb-doped SnO2 nanoparticles coated LiNi0.8Co0.15Al0.05O2 cathode material with enhanced electrochemical properties for Li-ion batteries[J]. Electrochimica Acta, 2017, 236 : 273–279. DOI: 10.1016/j.electacta.2017.03.215 |
| [18] | TAO S, KONG F, WU C, et al. Nanoscale TiO2 membrane coating spinel LiNi0.5Mn1.5O4 cathode material for advanced lithium-ion batteries[J]. Journal of Alloys and Compounds, 2017, 705 : 413–419. DOI: 10.1016/j.jallcom.2017.02.139 |
| [19] | KUMAR A, NAZZARIO R, TORES-CASTRO L, et al. Electrochemical properties of MgO-coated 0.5Li 2MnO3-0.5LiNi0.5Mn0.5O2 composite cathode material for lithium ion battery[J]. International Journal of Hydrogen Energy, 2015, 40 (14): 4931–4935. DOI: 10.1016/j.ijhydene.2015.01.104 |
| [20] | SAROHA R, JAIN A, PANWAR A K. Effect of ZnO coating on physicochemical properties of LiFePO4 cathode material for lithium ion batteries[J]. Advanced Materials Proceedings, 2016, 1 (1): 104–108. DOI: 10.5185/amp |
| [21] | ZHOU P, ZHANG Z, MENG H, et al. SiO2-coated LiNi0.915Co0.075Al0.01O2 cathode material for rechargeable Li-ion batteries[J]. Nanoscale, 2016, 8 (46): 19263–19269. DOI: 10.1039/C6NR07438C |
| [22] | MYUNG S T, IZUMI K, KOMABA S, et al. Role of alumina coating on Li-Ni-Co-Mn-O particles as positive electrode material for lithium-ion batteries[J]. Chemistry of Materials, 2005, 17 (14): 3695–3704. DOI: 10.1021/cm050566s |
| [23] | KAWAMURA T, OKADA S, YAMAKI J. Decomposition reaction of LiPF6-based electrolytes for lithium ion cells[J]. Journal of Power Sources, 2006, 156 (2): 547–554. DOI: 10.1016/j.jpowsour.2005.05.084 |
| [24] | AYKOL M, KIRKLIN S, WOLVERTON C. Thermodynamic aspects of cathode coatings for lithium-ion batteries[J]. Advanced Energy Materials, 2014, 4 (17): 6832–6840. |
| [25] | PARK J S, MANE A U, ELAM J W, et al. Amorphous metal fluoride passivation coatings prepared by atomic layer deposition on LiCoO2 for Li-ion batteries[J]. Chemistry of Materials, 2015, 27 (6): 1917–1920. DOI: 10.1021/acs.chemmater.5b00603 |
| [26] | YUE P, WANG Z, LI X, et al. The enhanced electrochemical performance of LiNi0.6Co0.2Mn0.2O2 cathode materials by low temperature fluorine substitution[J]. Electrochimica Acta, 2013, 95 (11): 112–118. |
| [27] | ZHU Z, CAI F, YU J. Improvement of electrochemical performance for AlF3[J]. Ionics, 2016, 22 (8): 1353–1359. DOI: 10.1007/s11581-016-1653-x |
| [28] | CHEN L, YANG Y, WANG Z, et al. Enhanced electrochemical performances and thermal stability of LiNi1/3Co1/3Mn1/3O2 by surface modification with YF3[J]. Journal of Alloys and Compounds, 2017, 711 : 462–472. DOI: 10.1016/j.jallcom.2017.03.130 |
| [29] | LI C D, YAO Z L, XU J, et al. Surface-modified Li[Li0.2Mn0.54Ni0.13Co0.13]O2 nanoparticles with LaF3 as cathode for Li-ion battery[J]. Ionics, 2017, 23 (3): 549–558. DOI: 10.1007/s11581-016-1823-x |
| [30] | KRAYTSBERG A, DREZNER H, AUINAT M, et al. Atomic layer deposition of a particularized protective MgF2 film on a Li-ion battery LiMn1.5Ni0.5O4 cathode powder material[J]. Chem Nano Mat, 2015, 1 (8): 577–585. |
| [31] | LIU X, LIU J, HUANG T, et al. CaF2-coated Li1.2MnNi0.13Co0.13O2 as cathode materials for Li-ion batteries[J]. Electrochimica Acta, 2013, 109 : 52–58. DOI: 10.1016/j.electacta.2013.07.069 |
| [32] | SUN Y K, LEE M J, YOON C S, et al. The role of AlF3 coatings in improving electrochemical cycling of Li-enriched nickel-manganese oxide electrodes for Li-ion batteries[J]. Advanced Materials, 2012, 24 (9): 1192–1196. DOI: 10.1002/adma.v24.9 |
| [33] | KE X, ZHAO Z, LIU J, et al. Improvement in capacity retention of cathode material for high power density lithium ion batteries:the route of surface coating[J]. Applied Energy, 2017, 194 : 540–548. DOI: 10.1016/j.apenergy.2016.09.040 |
| [34] | JUNG H, SONG H, KIM T, et al. FeF3 microspheres anchored on reduced graphene oxide as a high performance cathode material for lithium ion batteries[J]. Journal of Alloys and Compounds, 2015, 647 : 750–755. DOI: 10.1016/j.jallcom.2015.06.191 |
| [35] | ZHAO T, LI L, CHEN R, et al. Design of surface protective layer of LiF/FeF3 nanoparticles in Li-rich cathode for high-capacity Li-ion batteries[J]. Nano Energy, 2015, 15 : 164–176. DOI: 10.1016/j.nanoen.2015.04.013 |
| [36] | LI C D, XU J, XIA J S, et al. Influences of FeF3 coating layer on the electrochemical properties of Li[Li0.2Mn0.54Ni0.13Co0.13]O2 cathode materials for lithium-ion batteries[J]. Solid State Ionics, 2016, 292 : 75–82. DOI: 10.1016/j.ssi.2016.04.024 |
| [37] | ZHANG L L, CHEN J J, CHENG S, et al. Enhanced electrochemical performances of Li1.2Ni0.2 Mn0.6O2 cathode materials by coating LiAlO2 for lithium-ion batteries[J]. Ceramics International, 2016, 42 (1): 1870–1878. DOI: 10.1016/j.ceramint.2015.09.154 |
| [38] | LEUNG K, QI Y, ZAVADIL K R, et al. Using atomic layer deposition to hinder solvent decomposition in lithium ion batteries:first-principles modeling and experimental studies[J]. Journal of the American Chemical Society, 2011, 133 (37): 14741–14754. DOI: 10.1021/ja205119g |
| [39] | ROBERTSON A D, WEST A R, RITCHIE A G. Review of crystalline lithium-ion conductors suitable for high temperature battery applications[J]. Solid State Ionics, 1997, 104 (1/2): 1–11. |
| [40] | KONG J Z, REN C, JIANG Y X, et al. Li-ion-conductive Li2TiO3-coated Li[Li0.2Mn0.51Ni0. 19Co0.1]O2 for high-performance cathode material in lithium-ion battery[J]. Journal of Solid State Electrochemistry, 2016, 20 (5): 1435–1443. DOI: 10.1007/s10008-016-3150-6 |
| [41] | LIU S, WU H, HUANG L, et al. Synthesis of Li2Si2O5-coated LiNi0.6Co0.2Mn0.2O2 cathode materials with enhanced high-voltage electrochemical properties for lithium-ion batteries[J]. Journal of Alloys and Compounds, 2016, 674 : 447–454. DOI: 10.1016/j.jallcom.2016.03.060 |
| [42] | FENG X, ZHANG J, YIN L. Enhanced cycling stability of Co3(PO4)2-coated LiMn2O4 cathode materials for lithium ion batteries[J]. Powder Technology, 2016, 287 : 77–81. DOI: 10.1016/j.powtec.2015.09.031 |
| [43] | WANG Z, LIU E, HE C, et al. Effect of amorphous FePO4 coating on structure and electrochemical performance of Li1.2Ni0.13Co0.13Mn0.54O2 as cathode material for Li-ion batteries[J]. Journal of Power Sources, 2013, 236 : 25–32. DOI: 10.1016/j.jpowsour.2013.02.022 |
| [44] | WU F, ZHANG X, ZHAO T, et al. Multifunctional AlPO4 coating for improving electrochemical properties of low-cost Li[Li0.2Fe0.1Ni0.15Mn0.55]O2 cathode materials for lithium-ion batteries[J]. ACS Applied Materials & Interfaces, 2015, 7 (6): 3773–3781. |
| [45] | GU Z, UETSUKA H, TAKAHASHI K, et al. Cover picture:structural color and the lotus effect[J]. Angewandte Chemie International Edition, 2003, 42 (8): 863–863. |
| [46] | CAO Q, ZHANG H P, WANG G J, et al. A novel carbon-coated LiCoO2 as cathode material for lithium ion battery[J]. Electrochemistry Communications, 2007, 9 (5): 1228–1232. DOI: 10.1016/j.elecom.2007.01.017 |
| [47] | LEE S, CHO Y, SONG H K, et al. Carbon-coated single-crystal LiMn2O4 nanoparticle clusters as cathode material for high-energy and high-power lithium-ion batteries[J]. Angewandte Chemie International Edition, 2012, 51 (35): 8748–8752. DOI: 10.1002/anie.v51.35 |
| [48] | NOEROCHIM L, YURWENDRA A O, SUSANTI D. Effect of carbon coating on the electrochemical performance of LiFePO4/C as cathode materials for aqueous electrolyte lithium-ion battery[J]. Ionics, 2016, 22 (3): 341–346. DOI: 10.1007/s11581-015-1560-6 |
| [49] | ZHOU X, WANG F, ZHU Y, et al. Graphene modified LiFePO4 cathode materials for high power lithium ion batteries[J]. Journal of Materials Chemistry, 2011, 21 (10): 3353–3358. DOI: 10.1039/c0jm03287e |
| [50] | GÖKTEPE H, ŞAHAN H, PATAT Ş. Effect of silver and carbon double coating on the electrochemical performance of LiFePO4 cathode material for lithium ion batteries[J]. International Journal of Hydrogen Energy, 2016, 41 (23): 9774–9779. DOI: 10.1016/j.ijhydene.2016.03.074 |
| [51] | SUN P, MA Y, ZHAI T, et al. High performance LiNi0.5Mn1.5O4 cathode by Al-coating and Al3+-doping through a physical vapor deposition method[J]. Electrochimica Acta, 2016, 191 : 237–246. DOI: 10.1016/j.electacta.2016.01.087 |
| [52] | PARK K S, SON J T, CHUNG H T, et al. Surface modification by silver coating for improving electrochemical properties of LiFePO4[J]. Solid State Communications, 2004, 129 (5): 311–314. DOI: 10.1016/j.ssc.2003.10.015 |
| [53] | ARREBOLA J, CABALLERO A, ERNAN L, et al. Effects of coating with gold on the performance of nanosized LiNi0.5Mn1.5O4 for lithium batteries[J]. Journal of the Electrochemical Society, 2007, 154 : A178–A184. DOI: 10.1149/1.2426799 |
| [54] | EDDRIEF M, DZWONKOWSKI P, JULIEN C, et al. The ac conductivity in B2O3-Li2O films[J]. Solid State Ionics, 1991, 45 (1/2): 77–82. |
 2018, Vol. 46
2018, Vol. 46