文章信息
- 曾斌, 陈小华, 汪次荣
- ZENG Bin, CHEN Xiao-hua, WANG Ci-rong
- 石墨烯负载硫化锌/硫化铜异质结的制备及光催化性能
- Synthesis and Photocatalytic Properties of Reduced Graphene Oxides Loaded-nano ZnS/CuS Heterostructures
- 材料工程, 2017, 45(12): 99-105
- Journal of Materials Engineering, 2017, 45(12): 99-105.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2015.001112
-
文章历史
- 收稿日期: 2015-09-08
- 修订日期: 2017-05-19
2. 湖南大学 材料科学与工程学院, 长沙 410082
2. College of Materials Science and Engineering, Hunan University, Changsha 410082, China
水污染是全球面临的一个重要问题[1-3],作为一种Ⅱ-Ⅳ周期的半导体材料,硫化锌在光照下能够产生大量的光生电子-空穴,在水处理工业中展现出潜在的应用价值[4]。目前,人们常采用减小颗粒尺寸来达到提高硫化锌的光催化效率。Wu等[5]在室温下制备了500nm大小的硫化锌球,60min就完全降解了水中的罗丹明B;Muruganandham等[6]使用水热法制备了由10nm颗粒组成的空心硫化锌球,降解有机污染物的效率进一步降低到30min。然而,纳米结构光催化材料虽然在一定程度上提高了光催化性能,但是,纳米结构增大的比表面积,一方面使颗粒之间更易团聚而影响其性能,另一方面,由于硫化锌纳米结构本身导电性差,不利于光生载流子的快速转移,导致光生电子的大量堆积,致使金属硫化物发生光腐蚀反应[7]。为了解决硫化锌的团聚和光腐蚀的问题,并进一步提高量子产率,近年来,人们将目光转移到硫化锌与具有优良导电性、多孔的碳材料复合研究中[8, 9]。石墨烯作为一种二维平面结构的碳材料,具有高的比表面积和良好的导电性能,在催化领域里具有非常重要的作用[10]。例如,石墨烯的二维平面结构可以作为催化物质的承载基底,均匀地分布活性物质,阻止其团聚[11, 12];石墨烯优良的导电能力,能有效导出光催化颗粒中的光生电子,有效阻止光生电子-空穴的复合,提高量子产率和降低光腐蚀反应[13]。同时,石墨烯基材料由于高的比表面以及共轭π-π键的作用,对有色染料具有一定的吸附能力,能够增加催化剂周围染料的浓度。新型的石墨烯基复合材料将能够极大地提高其催化效率和抗光腐蚀的能力。但是,由于硫化锌自身的禁带宽度为3.7eV,吸收光谱处于紫外区域,而紫外光在太阳光中仅占4%左右,这严重限制硫化锌在光催化领域中的实际应用。因此,如何使硫化锌在可见光区域里具有高效的光催化性能是需要解决的一个问题[14]。最近,研究人员发现,通过离子交换反应形成硫化锌与硫化铜的异质结,在可见光照射下,可以发生界面电子转移现象(即硫化锌价带内的电子通过界面转移到铜离子簇内)[15]。发生界面电子转移的异质结内,铜离子簇内的电子能够有效还原氧气形成超氧自由基,硫化锌价带内的空穴能够氧化氢氧根,形成羟基自由基,也就是说,通过界面电子转移过程,铜离子内的电子表现出良好的还原能力,硫化锌内的空穴表现出良好的氧化能力。因此形成硫化锌/硫化铜异质结,是解决硫化锌对可见光利用率不高的有效手段。
本工作采用微波辅助加热的方法制备了石墨烯负载硫化锌纳米颗粒,并通过离子交换反应获得了石墨烯负载硫化锌/硫化铜异质结的复合物。研究氧化石墨烯含量、不同硫源和微波加热时间对复合物形貌和光催化性能的影响,并探讨了复合物优异的可见光光催化效果的原因。
1 实验 1.1 氧化石墨烯溶液的制备使用Hummers法[16]制备氧化石墨烯。将3g石墨粉末和3g硝酸钠加入150mL冰浴的浓硫酸中,然后缓慢加入9g KMnO4,搅拌一段时间后升温到40℃后保温2h。接着加入150mL水,将温度升高到98℃,20min后加入30mL的35%H2O2(体积分数)溶液,搅拌10min后,加入1000mL去离子水。溶液过滤后用去离子水反复清洗,直到pH值等于7,对溶液超声12h后离心去除其中的杂质,即得到氧化石墨烯溶液。
1.2 石墨烯-硫化锌/硫化铜制备将30mL 1g·L-1的氧化石墨烯加入到250mL2g·L-1的乙酸锌溶液中,超声15min后,加入100mL 2g·L-1硫代乙酰胺溶液,将混合溶液搅拌15min后微波处理30min,得到灰色的沉淀,将沉淀真空抽滤并反复用去离子水清洗,去除多余的硫代乙酰胺,将获得的粉末放入100mL 0.15g·L-1的硝酸铜溶液中,搅拌10min后微波处理30min,将铜离子置换出部分硫化锌中的锌离子。最后,将得到的产物真空抽滤,并反复用去离子水清洗,将获得的产物在真空60℃下烘干,即得到黑色粉末样品。
1.3 石墨烯-硫化锌/硫化铜复合粉末表征使用PW 1710型X射线衍射分析仪进行物相分析;采用S-4800型场发射扫描电子显微镜和JEOL-3010型透射电子显微镜进行形貌观察。
1.4 光催化性能在300mL 20mg·L-1的甲基橙溶液中加入20mg光催化剂和2mL过氧化氢(体积分数为30%),暗处放置30min达到吸附平衡,再使用500W的可见光照射,每隔5min取5mL样品,离心处理后测量紫外-可见光吸收光谱,溶液中甲基橙降解率为:
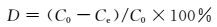
|
(1) |
式中:D为降解率;C0为光照前达到吸附平衡时溶液中甲基橙的浓度;Ce为光照t时间后溶液中甲基橙浓度。
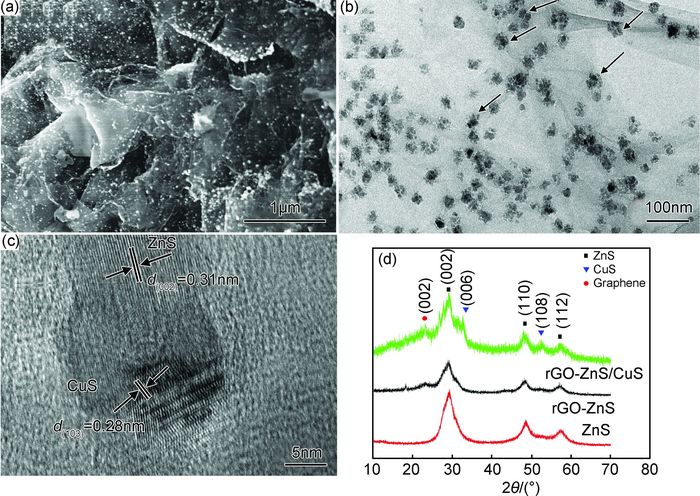
2 结果与讨论 2.1 石墨烯-硫化锌/硫化铜的结构和相分析图 1为石墨烯-硫化锌/硫化铜的SEM,TEM,HRTEM和XRD谱图。从图 1(a)可知,石墨烯为片状结构,负载的硫化锌/硫化铜颗粒尺寸为20nm左右,并且均匀地分布在石墨烯表面,没有任何的团聚现象。图 1(b)是石墨烯-硫化锌/硫化铜的TEM图,可以看出,石墨烯表面负载着大量的纳米颗粒,并且发现每个纳米颗粒一部分颜色较深一部分颜色较浅(箭头所示)。对单个纳米颗粒进行高分辨电镜观察(见图 1(c)),发现单个纳米颗粒由两部分组成,一部分是硫化锌的(002)晶面的晶格条纹,另一小部分是硫化铜的(103)晶面的晶格条纹。图 1(d)是硫化锌、石墨烯-硫化锌和石墨烯-硫化锌/硫化铜的X射线衍射谱图。可以看出,石墨烯-硫化锌/硫化铜的XRD中存在6个峰,其中28.64°, 47.75°和56.53°代表硫化锌的(002), (110)和(112)晶面(JCPDS No. 36-1450)。32.85°和52.71°代表硫化铜的(006)和(108)晶面(JCPDS No.04-0836)。25°峰的位置对应石墨的(002)晶面。在XRD图中没有其他的峰出现,表明粉末样品中没有其他的物相。通过上述观察,可以发现石墨烯作为一种承载基底可以起到均匀分散纳米颗粒的作用,并且,通过透射和高分辨都可以证明存在硫化锌/硫化铜的异质结。由于硝酸铜加入的是不含有杂质的硫化锌悬浮液中,根据微量硝酸铜与硫化锌在高温下能发生离子交换反应的特性(Cu(NO)2+ZnS→Zn(NO)2+CuS),也可以判断溶液中将生成硫化锌/硫化铜的异质结。
|
图 1 石墨烯-硫化锌/硫化铜的扫描图(a),透射图(b),高分辨图(c)和X射线衍射谱图(d) Fig. 1 SEM(a), TEM(b), HRTEM(c) images and XRD spectra(d) of rGO-ZnS/CuS |
图 2给出了微波时间60min和硫代乙酰胺为硫源的条件下,不同氧化石墨烯含量制备的复合物的SEM图。当氧化石墨烯加入量为0%(质量分数,下同)时,形成的颗粒大小为200nm左右,并且团聚现象明显(图 2(a));氧化石墨烯加入量为5%时,颗粒大小得到一定改善(约为50~100nm),但是团聚现象依然非常严重(图 2(b));进一步增加氧化石墨烯含量至10%,纳米颗粒尺寸降低到20nm以下,并且全部均匀分布在整个石墨烯的表面,团聚现象已经完全消除(见图 2(c));然而将氧化石墨烯的含量增加到20%时,纳米颗粒数量明显减少,甚至有些石墨烯表面上没有负载任何颗粒(图 2(d))。上述结果表明,石墨烯作为一种有效的承载基体,能阻止纳米颗粒的团聚并促进细小纳米颗粒的形成,这是因为氧化石墨烯表面存在大量带负电的功能团,这些功能团能够铆接住生成的纳米颗粒,阻止纳米颗粒的团聚和长大。在其他实验条件不变的条件下,认为氧化石墨烯含量的最佳值为10%。

|
图 2 不同氧化石墨烯含量的rGO-ZnS/CuS的SEM像(a)0%;(b)5%;(c)10%;(d)20% Fig. 2 SEM images of rGO-ZnS/CuS with different GO content (a)0%;(b)5%;(c)10%;(d)20% |
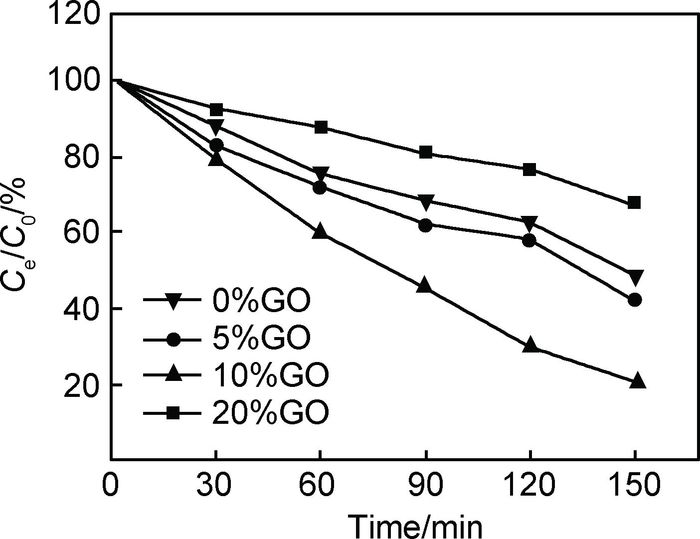
图 3给出了不同氧化石墨烯含量制备的复合物对甲基橙的降解率。可以看出,10%氧化石墨烯含量制备的复合物显示了明显的可见光催化效果,150min后甲基橙降解了81.2%。而使用0%,5%,20%氧化石墨烯含量制备的复合物,在150min后,只分别降解了51.6%,58.2%和31.6%,说明10%氧化石墨烯含量制备的复合物在降解有色染料中具有更大的优势。光催化实验结果表明,加入适量的氧化石墨烯,一方面能够明显降低纳米颗粒的大小,增加活性物质的比表面积;另一方面,还原后的氧化石墨烯(即石墨烯)可以作为一种良好的导电基底,分离催化反应过程中的光生电子,降低光生电子的复合,这都使得复合物具有较高的催化能力。
|
图 3 不同GO含量的rGO-ZnS/CuS光催化降解率 Fig. 3 Photocatalytic degradation efficiency of rGO-ZnS/CuSwith different GO content |
图 4为氧化石墨烯含量10%和微波时间60min条件下,使用不同硫源制备的石墨烯-硫化锌/硫化铜复合物SEM像。当硫化钠(Na2S)作为硫源时,生成的纳米颗粒非常细小,但是团聚现象严重(图 4(a));而使用硫代硫酸钠(Na2S2O3)作为硫源时,颗粒尺寸为微米级别, 并表现出一定的团聚现象(图 4(c))。只有选择硫代乙酰胺(TAA)作为硫源时,才能给得到均匀分布的细小纳米颗粒(图 4(b))。这种现象可以使用硫化锌的生长机制来解释:当乙酸锌溶液与氧化石墨烯混合时,在静电作用力下锌离子吸附到氧化石墨烯的表面,以硫化钠为硫源时,硫化钠在水中迅速电离出大量的硫离子,并与水中已电离的锌离子迅速发生反应生成大量的纳米颗粒,由于时间极短,迅速生成的纳米颗粒来不及均匀分布。而采用硫代乙酰胺和硫代硫酸钠时,它们在微波作用下首先分解出硫化氢气体,然后与锌离子反应,这样就减缓了反应速率。对于硫代乙酰胺而言,微波作用下能够迅速释放硫化氢气体,因而使生成的颗粒细小均匀;而对于硫代硫酸钠,释放硫化氢气体缓慢,生成的硫化锌能够随着释放的硫化氢气体缓慢长大而形成较大颗粒。这样就导致采用不同的硫源会产生不同大小的硫化锌纳米颗粒,最后通过置换反应,得到硫化锌/硫化铜的异质结纳米颗粒。实验结果分析认为,在其他实验条件不变的条件下,最佳的硫源为硫代乙酰胺。

|
图 4 不同硫源下rGO-ZnS/CuS的SEM像(a)Na2S;(b)TAA;(c)Na2S2O3 Fig. 4 SEM images of rGO-ZnS/CuS obtained at different sulfide sources (a)Na2S; (b)TAA; (c)Na2S2O3 |
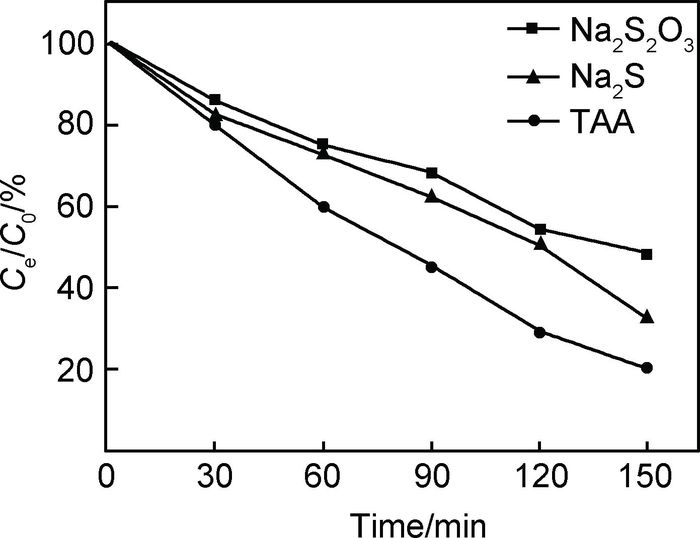
图 5是不同硫源制备的复合物对甲基橙的降解率。当采用硫代硫酸钠和硫化钠作为硫源获得的产品,对甲基橙的降解率为51.2%和69.3%,而采用硫代乙酰胺作为硫源的复合物,催化效果明显高于前两者。光催化实验结果进一步证实,石墨烯表面负载均匀细小的纳米颗粒有助于光催化反应。
|
图 5 不同硫源下rGO-ZnS/CuS的光催化降解率 Fig. 5 Photocatalytic degradation efficiency of rGO-ZnS/CuSat different sulfide sources |
图 6给出了氧化石墨烯含量10%和硫代乙酰胺为硫源时,离子交换反应前不同微波时间制备的石墨烯-硫化锌复合物的形貌图。微波15min后,已经出现了大量的纳米级硫化锌颗粒,并且分布较均匀,但是显然有一些区域硫化锌颗粒稀少(图 6(a));随着微波时间延长到30min,整个区域内都出现了均匀分布的纳米颗粒(图 6(b));进一步将微波时间延长到45min,发现纳米颗粒在一定程度上得到长大(图 6(c))。因此,在其他实验条件不变的条件下,微波时间的最佳值为30min,然后通过离子交换反应,可以得到石墨烯表面负载均匀的硫化锌/硫化铜异质结。

|
图 6 不同微波反应时间下rGO-ZnS的SEM像(a)15min;(b)30min;(c)45min Fig. 6 SEM images of rGO-ZnS at different microwave reaction time (a)15min; (b)30min; (c)45min |
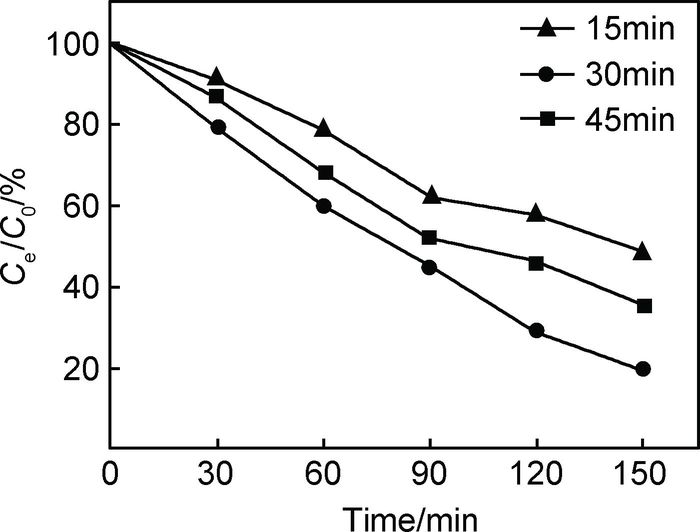
图 7是将微波反应时间为15,30,45min的产物通过离子交换获得的石墨烯-硫化锌/硫化铜催化剂对甲基橙的降解率。可知,甲基橙分别降解了52.2%,65.1%,81.2%。实验结果表明,石墨烯表面形成均匀负载细小纳米颗粒是保证优良光催化性能的关键,这是因为细小纳米颗粒具有更高的比表面积,能够提供更大的催化点,同时在催化反应过程中,细小纳米颗粒将有助于光生电子迅速达到活性物质表面,参与催化反应。而颗粒过少(减少活性物质的量)或颗粒过大(减少活性物质的比表面积)都会损害到催化效果。
|
图 7 不同微波反应时间下rGO-ZnS/CuS的光催化降解率 Fig. 7 Photocatalytic degradation efficiency of rGO-ZnS/CuS at different microwave reaction time |
光催化剂的稳定性也是评价光催化性能的重要参数。图 8为微波时间60min,氧化石墨烯含量10%,硫源为硫代乙酰胺时,rGO-ZnS/CuS的循环光催化降解曲线图。可知,当复合物循环使用3次以后,催化活性并没有出现明显的下降,表明形成的rGO-ZnS/CuS不仅光催化降解速率高,而且催化稳定性也很好。

|
图 8 可见光照射下催化剂的光催化循环特性 Fig. 8 Cycling runs in the photocatalytic reaction under visible light |
石墨烯负载硫化锌/硫化铜异质结的可见光催化机理如图 9所示。在可见光照射下,由于硫化锌的禁带宽度大,可见光无法激发其电子从价带直接跃迁到导带,同时,可见光也不能使硫化铜内的价带电子发生跃迁[17]。但是当硫化锌和硫化铜形成异质结后,可见光使硫化锌价带上的电子通过硫化锌/硫化铜界面转移到硫化铜上,这种现象称为界面电子转移现象[15],转移的电子能够将硫化铜部分还原为硫化亚铜,形成硫化铜/硫化亚铜簇,由于硫化铜/硫化亚铜簇的还原电势为-0.5V(vs SHE, pH=0),因此从硫化锌的价带到硫化铜/硫化亚铜簇的界面电子转移需要的能量为2.94eV,通过计算可以得出硫化锌/硫化铜异质结能够吸收350~450nm可见光,而这正是由于界面电子转移造成的。同时硫化铜/硫化亚铜簇铆接在石墨烯表面,并且由于纳米异质颗粒与石墨烯形成了紧密的结合,石墨烯可以作为电子受体和传输体,将电子转移到石墨烯上,因而提高了光生电子空穴的分离,促进了光催化效果。同时带电石墨烯的电势大概为-0.08V (vs SHE, pH = 0) [18],低于硫化铜/硫化亚铜簇的电势,反过来又进一步促进光生电子的转移和分离。最后,石墨烯上的电子与溶液中的氧气反应,生成超氧自由基,而留在硫化锌内部的空穴,将会与溶液中的氢氧根作用,生成羟基自由基[19],这两种基团都对甲基橙具有良好的降解效果[20]。电子转移过程以及光催化机理为:

|
图 9 石墨烯-硫化锌/硫化铜对甲基橙(MO)的光催化机理 Fig. 9 Photocatalytic mechanism of rGO-ZnS/CuS to MO |
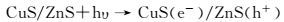
|
(2) |
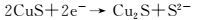
|
(3) |

|
(4) |
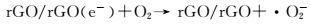
|
(5) |
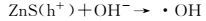
|
(6) |
(1) 使用两步法,即先制备石墨烯负载硫化锌的纳米复合物,再通过离子交换反应,制备了石墨烯负载硫化锌/硫化铜的复合物。在这种复合物中,石墨烯表面均匀负载着大量的纳米颗粒,并且每个纳米颗粒由硫化锌和硫化铜共同组成,即形成了石墨烯负载硫化锌/硫化铜异质结的纳米复合物。
(2) 微波时间60min,氧化石墨烯含量10%,硫源为硫代乙酰胺条件下,获得的产物在可见光照射下,150min降解水中81.2%的有机污染物。
| [1] |
赵斯琴, 娜米拉, 长山. 钛酸钠纳米线制备TiO2纳米线的反应条件[J].
材料工程, 2015, 43 (2): 58–62.
ZHAO S Q, NAMILA, ASUHA. Reaction conditions for synthesis of TiO2 nanowires from sodium titanate nanowires[J]. Journal of Materials Engineering, 2015, 43 (2): 58–62. |
| [2] |
刘春玲, 毕菲非, 张文杰, 等. 负载型SrTiO3/HZSM-5光催化材料制备与性能研究[J].
材料工程, 2016, 44 (2): 22–27.
LIU C L, BI F F, ZHANG W J, et al. Preparation and properties of supported SrTiO3/HZSM-5 photocatalyst[J]. Journal of Materials Engineering, 2016, 44 (2): 22–27. |
| [3] |
鲍艳, 张永辉, 马建中. 溶液法制备ZnO纳米阵列的影响因素及光催化活性[J].
材料工程, 2015, 43 (8): 19–24.
BAO Y, ZHANG Y H, MA J Z, et al. Influence factors and photocatalytic activity of ZnO nanoarrays synthesiszed via solution method[J]. Journal of Materials Engineering, 2015, 43 (8): 19–24. DOI: 10.11868/j.issn.1001-4381.2015.08.004 |
| [4] | HE T S, MA H H, ZHOU Z F, et al. Preparation of ZnS-Fluoropolymer nanocomposites and its photocatalytic degradation of methylene blue[J]. Polymer Degradation and Stability, 2009, 94 (12): 2251–2256. DOI: 10.1016/j.polymdegradstab.2009.08.012 |
| [5] | WU X, LI K, WANG H. Facile synthesis of ZnS nanostructured spheres and their photocatalytic properties[J]. Journal of Alloys and Compounds, 2009, 487 : 537–544. DOI: 10.1016/j.jallcom.2009.08.010 |
| [6] | MURUGANANDHAM M, AMUTHA R, REPO E, et al. Controlled mesoporous self-assembly of ZnS microsphere for photocatalytic degradation of Methyl Orange dye[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2010, 216 : 133–141. DOI: 10.1016/j.jphotochem.2010.06.008 |
| [7] | SHEN S L, WANG Q B. Rational tuning the optical properties of metal sulfide nanocrystals and their applications[J]. Chemistry of Materials, 2013, 25 (8): 1166–1178. DOI: 10.1021/cm302482d |
| [8] | ZHANG Y, ZHANG N, TANG Z R, et al. Graphene transforms wide band gap ZnS to a visible light photocatalyst. the new role of graphene as a macromolecular photosensitizer[J]. ACS Nano, 2012, 6 (11): 9777–9779. DOI: 10.1021/nn304154s |
| [9] | MICHAEL J C, GALIT L, DENNIS W, et al. Synthesis of optically active ZnS-carbon nanotube anocomposites in supercritical carbon dioxide via a single source diethyldithiocarbamate precursor[J]. Industrial and Engineering Chemistry Research, 2012, 51 (36): 11710–11716. DOI: 10.1021/ie301553g |
| [10] | HUA H T, WANG X B, LIU F M, et al. Rapid microwave-assisted synthesis of graphene nanosheets-zinc sulfide nanocomposites:optical and photocatalytic properties[J]. Synthetic Metals, 2011, 161 : 404–410. DOI: 10.1016/j.synthmet.2010.12.018 |
| [11] |
杨文彬, 张丽, 刘菁伟, 等. 石墨烯复合材料的制备及应用研究进展[J].
材料工程, 2015, 43 (3): 91–97.
YANG W B, ZHANG L, LIU J W, et al. Progress in research on preparation and application of graphene composites[J]. Journal of Materials Engineering, 2015, 43 (3): 91–97. DOI: 10.11868/j.issn.1001-4381.2015.03.016 |
| [12] |
郑玉婴. 功能化氧化石墨烯纳米带/EVA复合材料薄膜的制备及表征[J].
材料工程, 2015, 43 (2): 96–102.
ZHENG Y Y. Preparation and characterization of functionalized graphene oxide nanoribbons/EVA composite films[J]. Journal of Materials Engineering, 2015, 43 (2): 96–102. DOI: 10.11868/j.issn.1001-4381.2015.02.016 |
| [13] |
刘欣伟, 陈勇, 陈昌兵, 等. N掺杂纳米TiO2/电气石复合材料的制备及其光催化性能[J].
材料工程, 2016, 44 (6): 104–109.
LIU X W, CHEN Y, CHEN C B, et al. Preparation and photocatalytic activity of nitrogen-doped nano TiO2/tourmaline composites[J]. Journal of Materials Engineering, 2016, 44 (6): 104–109. DOI: 10.11868/j.issn.1001-4381.2016.06.016 |
| [14] | LI C X, JIANG D Y, ZHANG L L, et al. Controlled synthesis of ZnS quantum dots and ZnS quantum flakes with graphene as a template[J]. Langmuir, 2012, 28 : 9729–9734. DOI: 10.1021/la300310m |
| [15] | ZHANG J, YU J G, ZHANG Y M, et al. Visible light photocatalytic H2-production activity of CuS/ZnS porous nanosheets based on photoinduced interfacial charge transfer[J]. Nano Letters, 2011, 11 : 4774–4779. DOI: 10.1021/nl202587b |
| [16] | OFFEMAM R, HUMMERS W. Preparation of graphitic oxide[J]. J Am Chem Soc, 1958, 80 (6): 1339. DOI: 10.1021/ja01539a017 |
| [17] | ZENG B, ZENG W J. Ion-exchange synthesis of graphene loaded-ZnS/Bi2S3 nanoplates with high photocatalytic activity[J]. Digest Journal of Nanomaterials and Biostructures, 2016, 11 (4): 1105–1111. |
| [18] | ZENG B, LONG H. ZnS nanoflowers on graphene for use as a high-performance photocatalyst[J]. Nano, 2014, 9 (8): 1450097–1450104. DOI: 10.1142/S1793292014500970 |
| [19] | ZENG B, CHEN X H, NING X T, et al. Electrostatic-assembly three-dimensional CNTs/rGO implanted Cu2O composite spheres and its photocatalytic properties[J]. Applied Surface Science, 2013, 276 : 482–486. DOI: 10.1016/j.apsusc.2013.03.120 |
| [20] | LIU S, TIAN J Q, WANG L, et al. One-pot synthesis of CuO nanoflower-decorated reduced graphene oxide and tis application to photocatalytic degradation of dyes[J]. Catalysis Science and Technology, 2012 (2): 339–344. |
 2017, Vol. 45
2017, Vol. 45


