文章信息
- 胡志海, 江国栋, 熊剑, 朱星, 袁颂东
- HU Zhi-hai, JIANG Guo-dong, XIONG Jian, ZHU Xing, YUAN Song-dong
- TiO2-NTs/rGO复合材料的制备及电化学性能
- Preparation and Electrochemical Performance of TiO2-NTs/rGO Composite
- 材料工程, 2017, 45(12): 93-98
- Journal of Materials Engineering, 2017, 45(12): 93-98.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2016.001380
-
文章历史
- 收稿日期: 2016-11-23
- 修订日期: 2017-08-31
2. 催化材料湖北省协同创新中心, 武汉 430068
2. The Synergistic Innovation Center of Catalysis Materials of Hubei Province, Wuhan 430068, China
锂离子电池自从1991年被索尼公司商业化以来,近年来在全世界迅速发展,现已成为一种成熟的,高效的能源存储解决方案[1]。而应用最广泛的石墨负极材料易在碳酸丙烯酯为添加剂的电解质体系中发生溶剂共嵌,导致石墨层间距扩大,引起结构破坏[2],从而使其表现出较差的倍率和循环性能以及较低的安全性,因此寻求开发一种高倍率、长寿命和高安全性的锂电负极材料既是市场发展的需求,也是负极材料改性的重要方向。
在无机纳米管材料中,氧化物纳米管因其较小的电子和离子传输路径,近年来在储能材料领域受到广泛关注。而众多氧化物纳米管中,B型的TiO2-NTs最适合作为锂电负极材料,因其在脱/嵌锂过程中体积效应小( < 3%),安全性高,倍率性能好,理论比容量较高(335mAh/g),是一种前景可观的锂电负极材料[3, 4]。然而,其电子导电性和离子导电性较低,高倍率性能受到限制,因此对其改性尤为必要。常见的策略是负载或包覆其他导电材料来提高导电性,比如碳层[5, 6]或负载石墨烯[7]。
本研究通过碱液水热法制备TiO2-NTs,并对其负载石墨烯得到复合材料TiO2-NTs/rGO,因为纳米结构可以减小电子和离子运输路径,负载石墨烯可以提高导电性,两方面结合起来改善材料的电化学性能。电学测试表明,复合材料表现出较高的倍率和循环性能,在动力汽车,智能电网等领域有重要的应用前景。
1 实验材料与方法 1.1 材料制备 1.1.1 实验材料实验所用的材料如下:二氧化钛(P25,德固赛公司)、鳞片石墨(≥99.9%,青岛奥科石墨公司)、导电炭黑(Super-C65,上海汇普公司)、CMC(美国杜邦公司),氢氧化钠(NaOH)、浓硫酸(H2SO4)、硝酸钠(NaNO3)、高锰酸钾(KMnO4)、过氧化氢(H2O2)、浓硝酸(HNO3),均为国药集团化工试剂有限公司购买。实验所用试剂为分析纯,未做进一步纯化。
1.1.2 氧化石墨烯(GO)的制备氧化石墨烯(GO)的制备采用改进的Hummers法[8]。在46mL浓H2SO4中分别加入1g NaNO3和1g鳞片石墨,0℃搅拌30min后,加入6g KMnO4,低于5℃,搅拌2h;温度升至35℃,搅拌2h后,加入46mL去离子水,升温到98℃,搅拌15min后,滴加20mL H2O2(质量分数30%)和100mL去离子水;混合液静置后,下层沉淀洗涤至中性,将得到的沉淀物重新分散到去离子水中,80W功率超声1h,得到亮黄色氧化石墨烯(GO)分散液。
1.1.3 TiO2纳米管/还原氧化石墨烯(TiO2-NTs/rGO)复合材料的制备0.1g P25于60mL10mol/L NaOH溶液中分散完全后转移至100mL反应釜中,在135℃条件下反应24h,搅拌速率为500r/min,反应完后自然冷却至室温,抽滤洗涤至中性,得到钛酸盐前驱体;将得到的钛酸盐前驱体在0.1mol/L HNO3溶液中离子置换3次,得到TiO2-NTs前驱体;将TiO2-NTs前驱体分散于30mL去离子水中,并加入适量GO(浓度为0.33mg/mL),充分混合后抽滤,干燥。最后,在N2保护下于400℃煅烧2h即得TiO2-NTs/rGO复合材料。单纯TiO2-NTs的制备与上述复合物制备过程相同,只是不加入GO。
1.2 材料表征使用Empyrean X射线衍射仪对样品进行物相表征,测量条件:射线为Cu靶Kα射线,管电压/电流为40kV/40mA,扫描速率为4(°)/min。利用JSM6390LV扫描电子显微镜(SEM)和Tecnai G2 20透射电子显微镜(TEM)表征样品形貌。使用波长为532nm激光光源的Renishaw拉曼光谱仪对样品进行拉曼测试。利用Nicolet iS 50傅里叶红外光谱仪对样品进行红外表征。利用BELSORP-mini-Ⅱ氮气吸脱附仪测试样品的比表面积。
1.3 电化学测试活性物质:CMC:SBR按照质量比90:5:5搅拌8~10h混合成均匀浆料,涂覆于铜箔上,控制浆料的面密度为1.0~2.0mg/cm2。然后在95℃下干燥10h以上。直径为14mm金属锂片为对电极和参比电极,隔膜为Celgard2400,厚度为20μm,电解液为1mol/L LiPF6/EC+DMC (EC与DMC体积比为1:1),在真空手套箱(水氧含量 < 1×10-7)中组装成CR2032纽扣半电池。
组装好的纽扣电池在45℃条件下活化10h,使用Arbin测试仪对电池进行循环和倍率测试,1C倍率电流为335mA/g,充放电窗口电压为1~3V。使用Zennium电化学工作站对电池进行循环伏安测试和电化学阻抗谱表征(扰动振幅为5mV,频率为0.01~100kHz)。
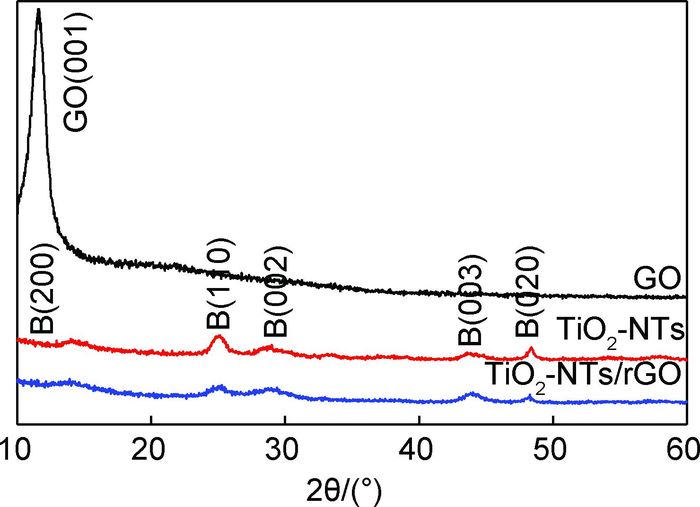
2 结果与分析 2.1 物相表征图 1为不同样品的XRD衍射谱图。由图 1可以看出,氧化石墨烯在11°处显示其特征峰[9],对应于GO(001)晶面衍射,计算得到GO层间距为0.9nm[4, 10]。煅烧之后,GO在该位置的特征峰消失,但是在25°处出现一个新的宽的衍射峰,这说明GO被还原为rGO[9]。图 1中TiO2-NTs和TiO2-NTs/rGO的XRD谱图与标准PDF卡片(JCPDS 46-1237)完全一致,不存在其他衍射峰,表明合成的TiO2-NTs是高纯度的B型晶相,这说明石墨烯负载后并未改变其晶相。与TiO2-NTs相比,TiO2-NTs/rGO的衍射峰强度较弱,并且峰变宽,表明复合材料中TiO2-NTs的尺寸小于纯的TiO2-NTs[10]。
图 2为GO和TiO2-NTs/rGO的拉曼光谱及红外光谱。由图 2可见,两个样品都有拉曼特征峰,其中D峰(1350cm-1)对应sp2杂化碳的无序度,G峰(1581cm-1)则对应sp2杂化的碳[11]。D峰与G峰的峰强度比值R(ID/IG)可以表示材料结构的无序程度。由图 2(a)还可以看到,400℃煅烧后,与GO的R=1.19相比,复合材料TiO2-NTs/rGO的R=1.01,这表明复合材料中石墨烯的有序度增加,缺陷减小,这是由于煅烧过程中石墨烯表面有机官能团脱去,结构恢复。由此可知,煅烧能够实现GO的还原。采用红外光谱进一步分析上述两个样品,如图 2(b)所示。由图 2(b)可见,与GO相比,TiO2-NTs/rGO复合材料中C=O官能团位于1724cm-1处的伸缩振动峰明显减弱,C—OH基团在1047cm-1处的振动峰消失,表明煅烧后氧化石墨烯表面的含氧官能团被脱去,GO被还原为rGO,这与XRD及拉曼分析结果一致。

|
图 2 GO及TiO2-NTs/rGO的拉曼光谱(a)和红外光谱(b) Fig. 2 Raman spectra(a) and FTIR spectra (b) of GO, TiO2-NTs/rGO |
图 3和图 4分别为离子置换后的TiO2-NTs前驱体的SEM图及TiO2-NTs, TiO2-NTs/rGO复合材料的TEM图。由图 3可见,经过离子置换后的TiO2-NTs前驱体已经形成了管状结构。TEM分析可知,复合物中TiO2-NTs为空心结构,单根管径约为25~30nm,多根管聚集成管束后直径为200~300nm。SEM及TEM显示,经过热处理之后,TiO2-NTs的形貌主要取决于其离子置换后的前驱体。与石墨烯复合后,如图 4(b)所示,TiO2-NTs负载在褶皱的石墨烯的表面,这将有助于提高TiO2-NTs的导电能力,从而改善其电化学性能。

|
图 3 离子置换后的TiO2-NTs前驱体的SEM图 Fig. 3 SEM image of TiO2-NTs precursor after ion exchange |

|
图 4 TiO2-NTs(a)和TiO2-NTs/rGO复合材料(b)的TEM图 Fig. 4 TEM images of TiO2-NTs (a) and TiO2-NTs/rGO composite(b) |
分别将TiO2-NTs, TiO2 -NTs/rGO与金属锂片组装成模拟电池测试其电化学性能,结果如图 5所示。从图 5可以看出,石墨烯负载的TiO2-NTs和没有负载的TiO2-NTs的比容量在前5次充放电循环中都有轻微的衰减,这主要是由于SEI膜的形成消耗了部分Li+,导致其容量损失。在随后的充放电循环中,库伦效率接近100%,说明脱锂/嵌锂完全可逆。当充放电电流密度增大时,两种材料均出现了短暂的容量滞后现象,但是经过随后的充放电之后容量又恢复稳定,这主要是由于在较大的电流密度下,不同倍率下电池的极化程度不同而导致的。负载石墨烯的TiO2-NTs/rGO在所有倍率下的可逆容量均高于单纯TiO2-NTs。在15C高倍率下,纯的TiO2-NTs和TiO2-NTs/rGO复合物的可逆容量分别为80mAh/g和100mAh/g,并且复合材料倍率性能好于Shen等[12]报道的。这主要是归因于石墨烯的引入使得复合材料具有较大的比表面积(84.9m2/g),同时提高了复合材料与电解液之间的浸润能力,另外石墨烯能够提高电极材料的电子导电性,从而加速了电荷迁移速率,使得复合材料的倍率性能得到改善。当电池的电流由高倍率减小到小倍率(0.2C)时,TiO2-NTs和TiO2-NTs/rGO的可逆容量均恢复,表明TiO2-NTs和TiO2-NTs/rGO的电化学性能较稳定。从倍率性能对比可知,石墨烯的加入显著地改善了材料电化学性能,尤其是高倍率性能。

|
图 5 TiO2-NTs和TiO2-NTs/rGO不同倍率性能 Fig. 5 Different rate capabilities of TiO2-NTs and TiO2-NTs/rGO |
图 6为TiO2-NTs和TiO2-NTs/rGO复合物的循环伏安曲线。由图 6可见,曲线中的一对氧化还原峰对应于Li+在材料中的脱出和嵌入。当扫描速率为0.2mV/s时,两个样品均出现了一对氧化还原峰,这是TiO2(B)储锂的赝电容行为[13],电化学反应可以表示为:TiO2+xLi++xe- →LixTiO2[14]。此外,还发现TiO2-NTs/rGO的氧化还原峰电位差为80mV,小于TiO2-NTs的100mV,表明Li+在石墨烯负载后的TiO2-NTs/rGO复合物中嵌入/脱出的可逆性更好,这归因于石墨烯的引入改善了电极材料电化学过程,这与倍率测试的结果相一致。随着扫描速率增大,两种材料的氧化还原峰的峰电位差均逐渐增大,表明电极极化增加。但是在相同的扫描速率下,TiO2-NTs/rGO极化小于TiO2-NTs,表明石墨烯的引入可以改善电极极化,从而提高倍率性能。通过将不同循环伏安曲线中氧化还原峰电流对扫描速率的平方根作图(如图 6中的插图)发现,氧化还原峰电流与扫描速率的平方根之间呈现良好的线性关系,表明电极反应是扩散控制过程[15]。

|
图 6 TiO2-NTs (a)和TiO2-NTs/rGO(b)的循环伏安曲线 Fig. 6 Cyclic voltammetry curves of TiO2-NTs(a) and TiO2-NTs/rGO(b) |
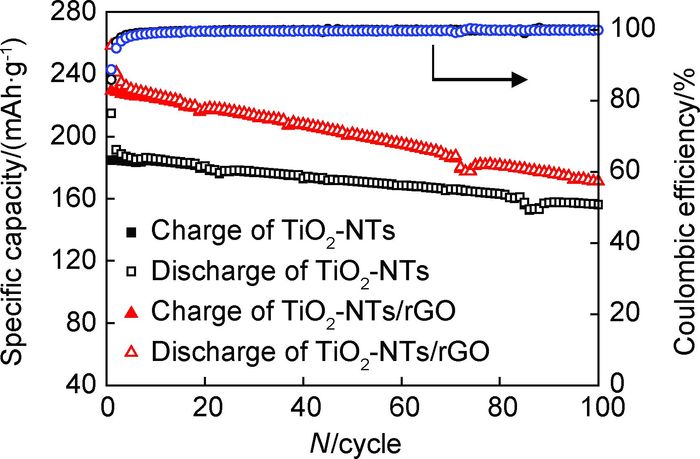
图 7为TiO2-NTs和TiO2-NTs/rGO在1C倍率下循环图。由图 7可知,TiO2-NTs/rGO和TiO2-NTs首次到第二次容量有所衰减,这对应于电极材料活化过程,消耗部分Li+从而在电解质与电极材料界面形成SEI膜,造成容量损失。TiO2-NTs和TiO2-NTs/rGO首次放电容量分别为214.9mAh/g和258.5mAh/g,对应的首次库伦效率分别为86%和89%,尽管与石墨烯复合后,TiO2-NTs/rGO首次库伦效率提高的不明显,但是经过活化过程形成稳定的SEI膜后,其库伦效率达到100%,可逆容量为230mAh/g,明显高于TiO2-NTs(190mAh/g),且在整个循环过程中,TiO2-NTs/rGO复合材料可逆容量均高于单纯TiO2-NTs,表明石墨烯负载TiO2-NTs后,电化学性能得到改善。这主要是由于石墨烯的负载提高了材料的导电性,降低了极化,改善了动力学反应过程。
|
图 7 TiO2-NTs和TiO2-NTs/rGO在1C倍率下循环性能 Fig. 7 Cycle performance of TiO2-NTs and TiO2-NTs/rGO at the rate of 1C |
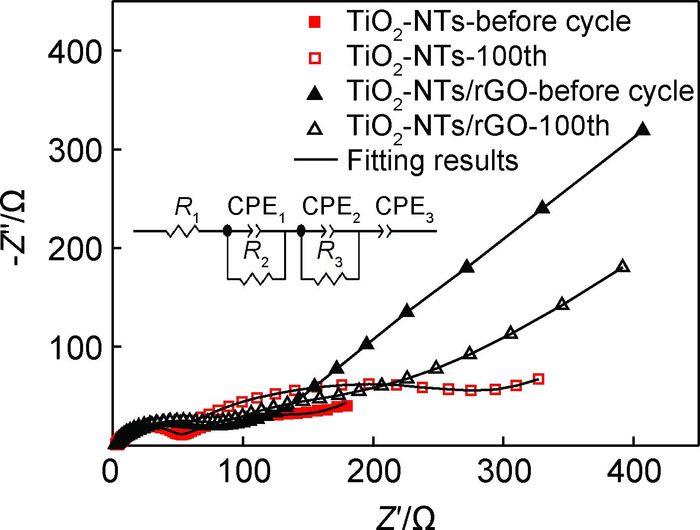
锂离子电池电化学反应涉及电荷转移和离子扩散。为探究电极材料的动力学反应过程,可以使用电化学阻抗表征,它是一种非常有效的理解电极动力学过程的方法,因为对电池不会造成破坏,可以用于电池的预先诊断[16-18]。图 8为两种材料的电化学阻抗谱的Nyquist图,并根据图中的等效电路进行拟合。从图 8可以看出,Nyquist图由高频区较小的圆弧、中频区较大的圆弧和低频区的直线组成[17]。高频区的圆弧对应电极材料界面接触电阻及与其有关的电容,与活性材料表面SEI膜形成有关,可以用CPE1和R2并联表示;中频区的圆弧与电极双电层电容和法拉第电荷转移有关,用CPE2和R3并联来模拟;低频区的斜线表示锂离子在活性材料和电解质之间的扩散过程,可用常相位角CPE3表示[19, 20]。通过拟合发现,拟合结果与实验测试数据吻合,结果如表 1所示。
|
图 8 循环前和第100次循环后Nyquist曲线(插图为等效电路) Fig. 8 Nyquist curves of before cycle and cycled 100th (inset is proposed equivalent circuit) |
| Sample | R1/Ω | CPE1 | R2/Ω | CPE2 | R3/Ω | CPE3 | |||
| Y1/(Ω·sn) | n1 | Y2/(Ω·sn) | n2 | Y3/(Ω·sn) | n3 | ||||
| TiO2-NTs-before cycle | 2.25 | 2.82×10-5 | 0.83 | 45.65 | 5.61×10-3 | 0.56 | 101.3 | 7.10×10-2 | 0.47 |
| TiO2-NTs-100th | 3.84 | 8.35×10-5 | 0.72 | 42.34 | 1.74×10-3 | 0.57 | 213.6 | 2.94×10-2 | 0.38 |
| TiO2-NTs/rGO-before cycle | 1.82 | 1.39×10-5 | 0.83 | 41.17 | 0.31×10-3 | 0.70 | 49.3 | 0.88×10-2 | 0.50 |
| TiO2-NTs /rGO-100th | 1.51 | 11.31×10-5 | 0.60 | 78.81 | 2.77×10-3 | 0.60 | 108.4 | 1.30×10-2 | 0.45 |
从表 1可以看出电极材料TiO2-NTs和TiO2-NTs/rGO复合物在充放电循环之后,电荷转移电阻R3较充放电之前增大,这主要是由于在循环之后电极表面形成稳定的SEI膜。另外,与石墨烯复合后,TiO2-NTs/rGO的电荷转移电阻R3在充放电循环前后都比单纯TiO2-NTs要小,表明负载石墨烯可以改善TiO2-NTs电子转移动力学,提高其电化学性能。
3 结论(1) 通过碱液水热法制备晶相为B型的TiO2-NTs,单根管径为25~30nm,多根管聚集形成的管束直径为200~300nm。
(2) 在1C倍率下循环100次,复合材料TiO2-NTs/rGO的循环性能高于纯的TiO2-NTs。在15C高倍率下,石墨烯负载的TiO2-NTs可逆容量为100mAh/g,高于纯的TiO2-NTs(80mAh/g),表明TiO2-NTs/rGO可以用作锂离子电池倍率型材料。
(3) 石墨烯负载后,电极极化和电荷转移电阻均减小,这归因于石墨烯的引入提高了材料的电子导电能力,改善其动力学反应过程,从而提高其电化学性能。
| [1] | ARMAND M, TARASCON J M. Building better batteries[J]. Nature, 2008, 451 (7179): 652–657. DOI: 10.1038/451652a |
| [2] | LIU C, LI F, MA L P, et al. Advanced materials for energy storage[J]. Advanced materials E, 2010, 22 (8): 28–62. DOI: 10.1002/adma.v22:8 |
| [3] | DYLLA A G, HENKELMAN G, STEVENSON K J. Lithium insertion in nanostructured TiO2(B) architectures[J]. Accounts of Chemical Research, 2013, 46 (5): 1104–1112. DOI: 10.1021/ar300176y |
| [4] | ETACHERI V, YOUREY J E, BARTLETT B M. Chemically bonded TiO2-bronze nanosheet/reduced graphene oxide hybrid for high-power lithium ion batteries[J]. ACS Nano, 2014, 8 (2): 1491–1499. DOI: 10.1021/nn405534r |
| [5] | PARK S J, KIM H, KIM Y J, et al. Preparation of carbon-coated TiO2 nanostructures for lithium-ion batteries[J]. Electrochimica Acta, 2011, 56 (15): 5355–5362. DOI: 10.1016/j.electacta.2011.03.119 |
| [6] | TANG Y, ZHANG Y, LI W, et al. Rational material design for ultrafast rechargeable lithium-ion batteries[J]. Chemical Society Reviews, 2015, 44 (17): 5926–5940. DOI: 10.1039/C4CS00442F |
| [7] |
杨程, 陈宇滨, 田俊鹏, 等. 功能化石墨烯的制备及应用研究进展[J].
航空材料学报, 2016, 36 (3): 40–56.
YANG C, CHEN Y B, TIAN J P, et al. Development in preparation and application of graphene functionalization[J]. Journal of Aeronautical Materials, 2016, 36 (3): 40–56. |
| [8] | HUMMERS W S, OFFEMAN R E. Preparation of graphitic oxide[J]. Journal of the American Chemical Society, 1958, 80 (6): 1339–1339. DOI: 10.1021/ja01539a017 |
| [9] | LIU H, CAO K, XU X, et al. Ultrasmall TiO2 nanoparticles in situ growth on graphene hybrid as superior anode material for sodium/lithium ion batteries[J]. ACS Applied Materials & Interfaces, 2015, 7 (21): 11239–11245. |
| [10] | ZHEN M, GUO S, GAO G, et al. TiO2-B nanorods on reduced graphene oxide as anode materials for Li ion batteries[J]. Chemical Communications, 2015, 51 (3): 507–510. DOI: 10.1039/C4CC07446G |
| [11] | CAO H, LI B, ZHANG J, et al. Synthesis and superior anode performance of TiO2@reduced graphene oxide nanocomposites for lithium ion batteries[J]. Journal of Materials Chemistry, 2012, 22 (19): 9759–9766. DOI: 10.1039/c2jm00007e |
| [12] | SHEN T, ZHOU X, CAO H, et al. TiO2(B)-CNT-graphene ternary composite anode material for lithium ion batteries[J]. RSC Advances, 2015, 5 (29): 22449–22454. DOI: 10.1039/C5RA01337B |
| [13] | LAN T, DOU J, XIE F, et al. Ultrathin TiO2-B nanowires with enhanced electrochemical performance for Li-ion batteries[J]. Journal of Materials Chemistry A, 2015, 3 (18): 10038–10044. DOI: 10.1039/C5TA01061F |
| [14] | OLSON C L, NELSON J, ISLAM M S. Defect chemistry, surface structures, and lithium insertion in anatase TiO2[J]. The Journal of Physical Chemistry B, 2006, 110 (20): 9995–10001. DOI: 10.1021/jp057261l |
| [15] | ZHANG Y, FU Q, XU Q, et al. Improved electrochemical performance of nitrogen doped TiO2-B nanowires as anode materials for Li-ion batteries[J]. Nanoscale, 2015, 7 (28): 12215–12224. DOI: 10.1039/C5NR02457A |
| [16] | OSAKA T, MOMMA T, MUKOYAMA D, et al. Proposal of novel equivalent circuit for electrochemical impedance analysis of commercially available lithium ion battery[J]. Journal of Power Sources, 2012, 205 (14): 483–486. |
| [17] | OSAKA T, NAKADE S, RAJAM KI M, et al. Influence of capacity fading on commercial lithium-ion battery impedance[J]. Journal of Power Sources, 2003, 119/121 : 929–933. DOI: 10.1016/S0378-7753(03)00233-7 |
| [18] | SEKI S, KIHIRA N, MITA Y, et al. AC Impedance study of high-power lithium-ion secondary batteries-effect of battery size[J]. Journal of The Electrochemical Society, 2011, 158 (2): A163–A166. DOI: 10.1149/1.3525277 |
| [19] | DENG Z, ZHANG Z, LAI Y, et al. Electrochemical impedance spectroscopy study of a lithium/sulfur battery:modeling and analysis of capacity fading[J]. Journal of the Electrochemical Society, 2013, 160 (4): A553–A558. DOI: 10.1149/2.026304jes |
| [20] | ZHUANG Q C, QIU X Y, XU S D, et al. Diagnosis of electrochemical impedance spectroscopy in lithium ion batteries[J]. Progress in Chemistry, 2010, 22 (6): 1044–1057. |
 2017, Vol. 45
2017, Vol. 45