文章信息
- 董鹏, 张英杰, 刘嘉铭, 李雪
- DONG Peng, ZHANG Ying-jie, LIU Jia-ming, LI Xue
- 纳米磷酸铁包覆锂离子电池正极材料LiNi0.5Co0.2Mn0.3O2的制备及其电化学性能
- Fabrication and Electrochemical Performance of LiNi0.5Co0.2Mn0.3O2 Coated with Nano FePO4 as Cathode Material for Lithium-ion Batteries
- 材料工程, 2017, 45(11): 49-57
- Journal of Materials Engineering, 2017, 45(11): 49-57.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2015.001257
-
文章历史
- 收稿日期: 2015-10-20
- 修订日期: 2017-07-17
2. 云南省先进电池及材料工程实验室, 昆明 650093
2. Yunnan Province Engineering Laboratory for Advanced Batteries and Materials, Kunming 650093, China
LiCoO2是应用最为广泛的商品化锂离子电池正极材料,但其存在着容量利用率低、毒性较高且钴资源价格高昂等问题[1, 2]。因此,开发新型正极材料以替代LiCoO2的应用已成为现阶段研究的热点[3, 4]。
由于LiNi1-x-yCoxMnyO2三元正极材料具有容量较高、成本低廉、热稳定性好等优点,其研究受到了广泛的重视,而成为最有可能取代LiCoO2的正极材料之一[5, 6]。目前研究较多的有LiNi1/3Co1/3Mn1/3O2, LiNi0.8Co0.1Mn0.1O2, LiNi0.5Co0.2Mn0.3O2等[7]。然而,在LiNi1-x-yCoxMnyO2材料晶格中,Li+(0.076nm), Ni2+(0.069nm)的原子半径比较接近,容易发生阳离子混排,降低材料的可逆性[8];同时,材料在充放电循环过程中,因直接与电解液接触,会导致过渡金属离子在电解液中溶解并发生副反应,使其电化学性能恶化[9]。包覆是改善正极材料综合性能的有效手段之一,其改性机理一般有以下两种理论[10, 11]:(1)阻止正极材料与电解液直接接触,从而避免正极材料中的过渡金属离子溶于电解液或与电解液发生副反应,使材料保持较高的活性;(2)与正极材料表面的SEI膜相互作用,改变SEI膜形成机制。研究发现,在LiNi1-x-yCoxMnyO2正极材料表面包覆金属氧化物,如Al2O3,ZnO,MgO,TiO2,ZrO2,CeO2等[12-18],金属磷酸盐,如AlPO4,Sn3(PO4)2,Mg3(PO4)2等[19, 20],Li-X-O,C,氟化物[21-23]均可以解决上述问题并改善其电化学性能。
有报道表明[24, 25],通过磷酸铁包覆可以有效地改善正极材料的电化学性能,而采用磷酸铁包覆LiNi0.5Co0.2Mn0.3O2鲜见报道。因此,本工作采用自制的纳米磷酸铁悬浮液,通过控制热处理温度与包覆量,探索磷酸铁包覆对LiNi0.5Co0.2Mn0.3O2的循环性能和倍率性能的影响。
1 实验 1.1 材料的制备原料NH4H2PO4,Fe(NO3)3,NH3·H2O均为分析纯,购自天津科密欧化学试剂有限公司,LiNi0.5Co0.2Mn0.3O2购自中科院上海微系统与信息研究所,纯度≥99%。分别配置0.2mol/L的NH4H2PO4溶液、Fe(NO3)3溶液,量取等体积80mL上述溶液同时快速倒入到高压反应釜(反应釜体积为100mL)中,将混合液加热到80℃后用氨水调节pH值,使其pH=2.0,将密封好的反应釜置于箱式电阻炉中120℃保温10h,冷却至室温后,便得到水热法制备的纳米磷酸铁悬浮液;按照磷酸铁与LiNi0.5Co0.2Mn0.3O2正极材料的质量比,量取一定体积的纳米磷酸铁悬浮液置于烧杯中,将正极材料缓慢加入其中,持续搅拌一段时间后,停止搅拌。将混合浆料静置、过滤、洗涤3~5次,在不同的温度下进行热处理,得到待测包覆试样。
1.2 材料表征采用Minflex型X射线衍射分析仪(XRD)分析材料的物相和晶体结构。扫描角度2θ为10°~90°;步长为0.0167°,每步停留10s。采用SDT-Q600型TG-DTA分析仪进行热重-差热分析,加热速率5℃/min,工作气氛为空气,温度范围为25~800℃。采用JSM-560OLV型扫描电子显微镜(SEM),实现对制备材料的表面形貌、颗粒大小的观察。采用HT7700型透射电镜(TEM),观测制备材料微小区域的精细结构。采用ULTIMA2型光谱仪,分析包覆前后材料的过渡金属元素的溶出量。
1.3 电池的组装和测试将正极材料、PVDF(聚偏二氟乙烯)、导电石墨KS-6和Supper P按质量比85:6:3:3充分混合,并加入一定量的溶剂NMP(1-甲基-2-吡咯烷酮)制成浆料。待正极浆料混合均匀后涂布在铝箔上,将涂覆好的极片置于真空干燥箱内120℃下干燥12h。压片后利用电池切片机制得直径为1.4cm的正极片。通过组装CR2025扣式电池测试包覆前后材料的电化学性能。负极选用金属锂片,隔膜为Celgard 2400多孔聚乙烯膜,电解液是1mol/L的LiPF6溶于碳酸乙烯酯(EC)、碳酸二甲酯(DMC)和碳酸甲乙酯(EMC)(体积比1:1:1)中的混合溶液。电池在整个组装过程中均在具有氩气气氛的手套箱(南京米开罗娜2440/750)中,水和氧含量均小于10-6。
采用LAND电池测试系统(CT-2001A),检测材料的比容量、循环性能及倍率性能。在恒流充放电测试中,电压测试范围是:2.75~4.3V(vs Li+/Li),采用普林斯顿4000电化学工作站,对扣式电池进行循环伏安(CV)和交流阻抗(EIS)测试。CV测试条件为:电位扫描区间为3.0~4.4V,扫描速率为0.1mV/s;EIS的测试条件为:开路电位测试,交流电位振幅为5mV,频率范围为10-2~105 Hz。
2 结果与讨论 2.1 纳米磷酸铁悬浮液的制备与表征将制备的磷酸铁混合溶液过滤、洗涤、干燥,并在不同的温度下进行热处理,采用XRD,TG-TDA,TEM测试手段,表征制备的磷酸铁试样的物相、组成和形貌;并通过沉降实验,将制备好的磷酸铁混合溶液置于试管中一周,观察混合溶液的液相状态。
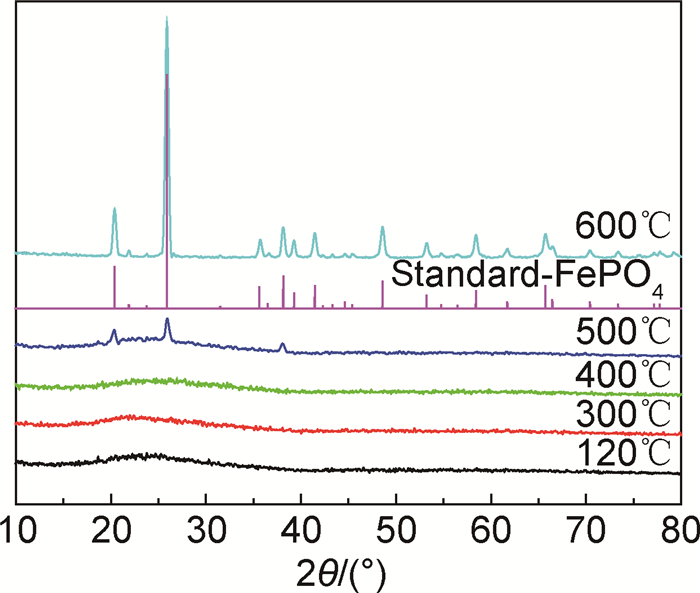
图 1是制备的磷酸铁试样在120,300,400,500,600℃下干燥12h后的XRD图谱。可以看出,热处理温度低于400℃时,在20°~40°之间有非晶态宽峰出现,由此可判断制备的FePO4·xH2O呈无定形非晶态。当温度升高至500℃时,在22°,27°和38°附近有部分α-石英结构FePO4的衍射峰出现,600℃时,其XRD图谱的衍射峰与纯相FePO4的JCPDS NO.29-0715完全吻合,完全转变为α-石英结构FePO4。
|
图 1 不同热处理温度下磷酸铁的XRD图谱 Fig. 1 XRD patterns of FePO4 at different heat treatment temperatures |
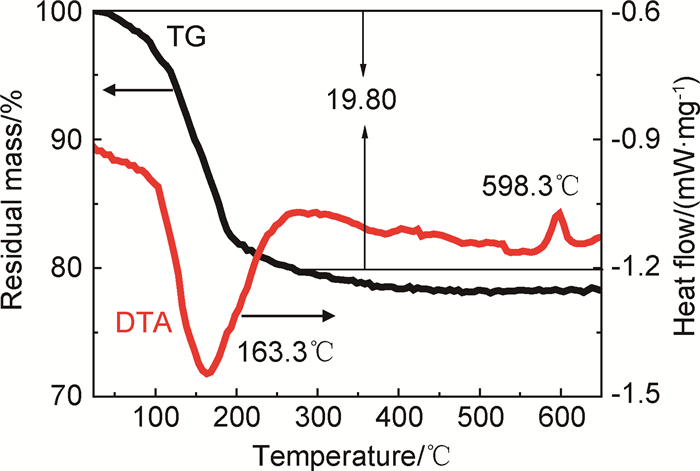
图 2是制备FePO4·xH2O的TG-DTA曲线。可以看出,FePO4·xH2O在低于278.3℃下失重明显,在280~450℃之间失重变化缓慢,而在450℃以后基本没有质量变化。278.3℃下的质量减少19.80%,这是由FePO4·xH2O失去结晶水引起,经计算x=2.10,与FePO4·2H2O的理论值非常接近,可以确定水热法制备的磷酸铁的组成为FePO4·2H2O。DTA曲线上能够看到在163.3℃附近出现明显的吸热峰,可以判断此峰的形成与FePO4·2H2O失去结晶水有关,而在598.3℃放热峰的附近,对应的TG曲线没有明显的质量变化,可以得出在此温度下FePO4发生了相变,由无定形态转化为α-石英结构。
|
图 2 水热法制备FePO4·xH2O的热重-差热曲线 Fig. 2 TG-DTA curves of hydrothermal preparation FePO4·xH2O |
图 3是磷酸铁混合液的沉降实验图和80℃干燥后的SEM,TEM图。可以看出,混合液没有分层现象,溶液呈浅黄色,可以判断制备的磷酸铁颗粒细小且在溶液中分布均匀;观察SEM图和TEM图可以发现,制备的磷酸铁一次颗粒尺寸分布在8~10nm之间,这证明了此方法制备的磷酸铁混合液为纳米悬浮液。

|
图 3 磷酸铁混合液的沉降实验图(a),80℃干燥后的磷酸铁SEM图像(b)和TEM图像(c) Fig. 3 Sedimentation experiment of FePO4 mixture (a), SEM image (b) and TEM image (c) of as-prepared FePO4 after 80℃ drying |
磷酸铁包覆LiNi0.5Co0.2Mn0.3O2(以下简称LNCMO)过程主要分两步:第一,液相反应过程,使一定质量分数的磷酸铁均匀地附着在正极材料表面;第二,固相反应过程,通过控制热处理温度,使磷酸铁和正极材料的表面结构更匹配,提高产物的稳定性。
2.2.1 热处理温度对LNCMO性能的影响将2%FePO4包覆的LNCMO试样在120,300,400,500,600℃下烧结12h,将制得的包覆材料组装电池测试,探索固相反应温度对包覆试样的电化学性能影响。
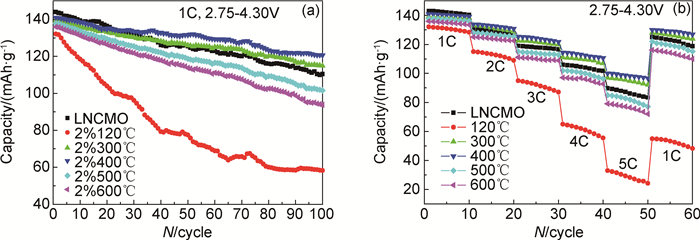
图 4(a),(b)分别是LNCMO及不同热处理温度下包覆试样的循环性能和倍率性能曲线。在图 4(a)中,LNCMO和120,300,400,500,600℃热处理的包覆试样,首次放电容量分别是144.1,132.1,139.2,140.9,137.8,135.9mAh/g,100次循环后放电容量为110.4,58.3,114.8,120.6,101.6,93.7mAh/g,相应的容量保持率分别是76.61%,44.13%,82.47%,85.59%,73.73%,68.90%,可以得出,包覆试样通过适当的温度进行热处理,可以改善材料的循环性能。包覆试样经300,400℃热处理后,可以改善正极材料的循环性能,而120,500,600℃热处理的包覆试样循环性能恶化明显。倍率性能测试的充放电电流分别是:1,2,3,4,5,1C,其中1C=180mAh/g。从图 4(b)中可以明显地发现,300,400℃热处理的包覆试样倍率性能优于LNCMO,而其他温度下热处理的包覆试样倍率性能变差。
|
图 4 LNCMO及不同烧结温度下包覆试样的循环曲线(a)和倍率性能曲线(b) Fig. 4 Cycle performance(a) and rate performance(b) of the as-prepared samples at different sintering temperatures |
为进一步揭示包覆磷酸铁改善LNCMO电化学性能的原因,结合图 1,2分析可知,不同热处理温度下,包覆在正极材料表面上的磷酸铁结构与组分有所差异。120℃热处理时,磷酸铁的结晶水没有失去,组成为FePO4·2H2O,在材料循环过程中FePO4·2H2O失去结晶水,破坏了电解液的稳定性,从而导致材料的电化学性能恶化;300,400℃热处理时,磷酸铁是无定形FePO4,当温度升高至500℃时,有部分α-石英结构FePO4的衍射峰出现,600℃时则完全转变为α-石英结构FePO4。Zhang等[26]研究锂离子在不同晶型结构FePO4中的扩散系数时发现,与结晶态FePO4相比,无定形FePO4能够提供了更多的锂离子扩散通道,且随着烧结温度的增加,锂离子在其中的扩散系数有增大趋势。同时,在LNCMO表面形成的包覆层又能避免电解液与活性物质直接接触,减少了电池循环过程副反应的发生,从而稳定了LNCMO的表面结构,改善其循环性能和倍率性能。经以上分析,确定400℃为制备磷酸铁包覆材料的最佳烧结温度。
2.2.2 包覆量对LNCMO性能的影响为探索包覆量对三元正极材料结构及电化学性能影响,选择烧结时间为12h,热处理温度400℃,本实验按照FePO4在包覆材料中质量分数为1%, 2%, 3%对LNCMO进行包覆。并通过XRD,SEM等手段表征了包覆试样的结构、形貌,通过组装扣式电池测试其电化学性能。
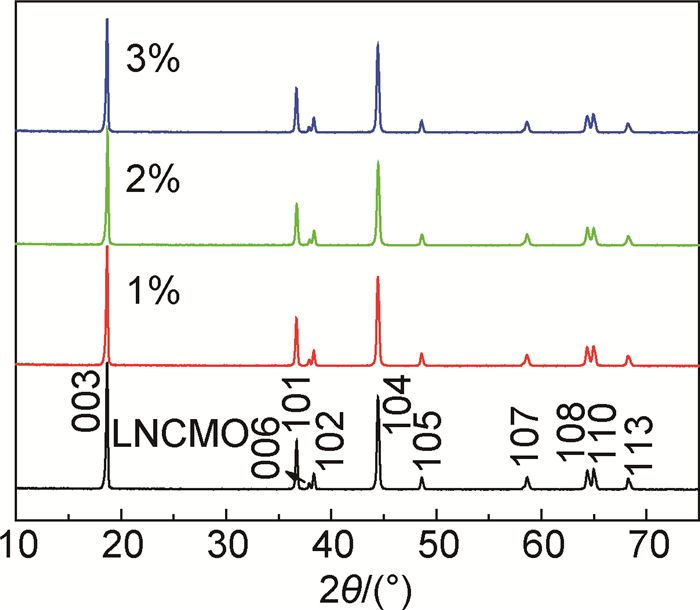
图 5是包覆前后材料的XRD衍射图谱。可以发现,包覆不同含量磷酸铁的试样与LNCMO的特征衍射峰基本一致,结构相同,都具有α-NaFeO2型层状结构,空间群为R3m,属于六方晶系。XRD图谱中(006),(102)和(108),(110)这两对峰分裂明显,说明包覆前后材料晶体的层状结构均比较理想。在图 5中没有观察到FePO4的衍射峰是因为在此温度下烧结其存在呈无定形态。
|
图 5 包覆不同含量磷酸铁LNCMO的XRD图谱 Fig. 5 XRD patterns of the pristine and FePO4-coated LNCMO |
利用Jade 6软件,根据XRD数据计算得到了不同包覆量LNCMO的晶胞参数、c/a和I003/I104值,见表 1。I003/I104是评价阳离子混排的重要指标,当I003/I104>1.2时,阳离子混排较小,且其比值越大,阳离子混排程度越低,层状结构越理想。c/a值通常用来分析层状材料的六方晶系特征,当c/a>4.899时,材料具有良好的结晶稳定性。从表 1中可以看出,包覆前后a,c,c/a的数值变化不大。但包覆后I003/I104的比值都有所增加,说明通过表面包覆磷酸铁,可以有效地降低阳离子混排对LNCMO电化学性能的不利影响。
| Content | a/nm | c/nm | c/a | I003/I104 |
| LNCMO | 0.28602 | 1.42252 | 4.973 | 1.205 |
| 1% | 0.28611 | 1.42248 | 4.972 | 1.302 |
| 2% | 0.28626 | 1.42235 | 4.969 | 1.372 |
| 3% | 0.28653 | 1.42225 | 4.964 | 1.344 |
包覆不同含量磷酸铁试样的SEM图像如图 6所示,图 6(a),(b),(c),(d)对应的包覆量分别是LNCMO,1%,2%,3%。从图中可以观察到,未包覆的LNCMO表面光滑、晶粒晶界清晰,随着包覆量的增大,包覆试样表面开始逐渐模糊不清,晶界轮廓不再明显,包覆1% FePO4试样有部分表面没有包覆完全,包覆量为2%时,材料表面包覆较完全且没有明显的FePO4聚集情况,当包覆量达到3%时,从图 6(d)中可以明显地看到有过量的FePO4堆积在正极材料表面上。

|
图 6 包覆不同含量磷酸铁LNCMO的SEM图像 (a)LNCMO; (b)1%;(c)2%;(d)3% Fig. 6 SEM images of LNCMO coated with different contents of FePO4 (a)LNCMO; (b)1%;(c)2%;(d)3% |
图 7是包覆2% FePO4试样的EDS分析图,(a)图是检测区域试样的SEM图像,从中可以观察到,在测定区域中,P, Fe元素的分布比较均匀,且与Ni, Co, Mn元素分布基本一致,可以证明在正极材料表面均匀地包覆了一层磷酸铁。

|
图 7 包覆2% FePO4(LNCMO)试样的EDS分析图 (a)检测区域的SEM图像;(b)Mn; (c)Ni; (d)Co; (e)P; (f)Fe Fig. 7 EDS images of LNCMO coated with 2% FePO4 (a)SEM image of detection area; (b)Mn; (c)Ni; (d)Co; (e)P; (f)Fe |
图 8是包覆2% FePO4试样的透射电镜分析图,从图 8(a)中可以看到,在正极材料表面明显有一层包覆膜存在,其厚度大约有20nm,图 8(b)是正极材料包覆后单个晶粒的轮廓图,除了个别区域发现FePO4聚集外,整个晶粒轮廓清晰、表面光滑。这说明了通过包覆磷酸铁可以在正极材料表面获得纳米包覆层。

|
图 8 包覆2% FePO4(LNCMO)试样的TEM图像 (a)高倍照片;(b)低倍照片 Fig. 8 TEM images of LNCMO coated with 2% FePO4 (a)high magnification photo; (b)low magnification photo |
图 9(a),(b)是包覆不同含量磷酸铁LNCMO对应的循环性能和倍率性能曲线。从图 9(a)中可以看到随着包覆量的增加,包覆试样的容量保持率先提高后降低,并且其首次放电容量也随着包覆量的增加而有所减少。LNCMO和包覆量为1%, 2%, 3%试样的首次放电容量分别为144.0,142.5,140.5,138.1mAh/g,对应的容量保持率分别是76.12%, 82.70%, 85.54%, 67.70%。随着包覆层趋于完整,正极材料与电解液直接接触的机会减少,能够避免电解液与正极材料副反应的发生,从而改善其循环性能。但当包覆量过大时,包覆层过厚,会增加锂离子在包覆层中的扩散距离,从而降低其扩散系数,导致循环性能恶化。从图 9(b)中可以得出,包覆量低于2%时,正极材料的倍率性能提高显著,而当包覆量达到3%时,在充放电电流高于2C时,倍率性能恶化明显。这说明只有选择适当的包覆量,才能改善正极材料的电化学性能,通过以上分析,选择2%作为最佳包覆量。

|
图 9 包覆不同含量磷酸铁LNCMO的循环性能(a)和倍率性能(b) Fig. 9 Cycle performance(a) and rate performance(b) of the as-prepared samples with different coating contents of FePO4 |
为探索包覆改善LNCMO正极材料电化学性能的机理,通过CV、EIS测试、包覆前后正极材料的浸泡实验解释包覆改善材料电化学性能的原因。
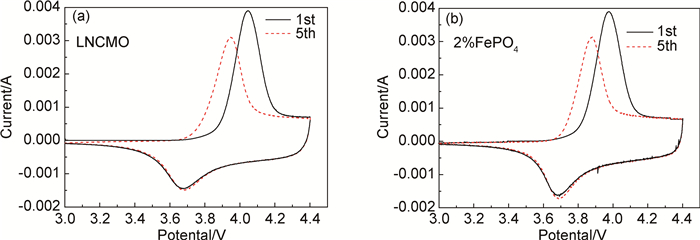
图 10是LNCMO和400℃热处理12h、包覆2% FePO4试样的循环伏安测试曲线。可以看出,包覆前后材料的曲线形状基本相同,并且只存在一对氧化还原峰,对应的是Ni4+/Ni2+的氧化还原反应。包覆前后试样首次充放电对应的氧化峰位分别是4.048V和3.986V,还原峰位为3.681V和3.688V;第5次充放电对应的氧化峰位分别是3.953V和3.888V,还原峰位为3.679V和3.684V。通过包覆的正极材料首次氧化峰较未包覆材料左移0.062V,而还原峰右移0.007V,其氧化还原峰差值ΔE减小了0.069V。这说明包覆材料具有更高的首次充放电库伦效率,即减小了电极反应的极化,使首次充放电的不可逆容量损失减少;经过5次循环后,包覆材料的ΔE仍比未包覆材料小0.070V,说明在循环过程中,经过包覆处理的正极材料锂离子脱出、嵌入的可逆性更好,因而其循环性能优良。
|
图 10 LNCMO(a)和包覆2%FePO4试样(b)的循环伏安测试曲线 Fig. 10 CV curves of LNCMO(a) and LNCMO coated with 2%FePO4(b) |
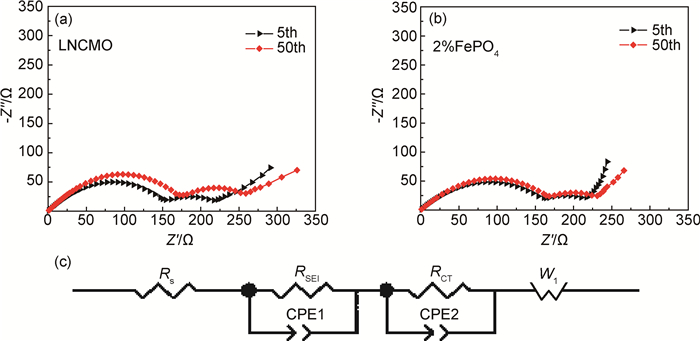
图 11(a),(b)分别是包覆前后试样的交流阻抗测试图谱,应用Zview软件对测得的电化学阻抗进行拟合,拟合结果见表 2,其等效电路图如图 11(c)。所有图谱均由高频区的半圆、中频区半圆和低频区的斜线组成。Rs是锂离子在电解液中扩散的阻抗,高频区的半圆与正极材料表面的SEI膜阻抗有关,RSEI是固液界面膜阻抗,中频区的半圆反应Li+在SEI膜和活性物质的界面发生电子交换,与电荷转移有关,Rct被称为电荷转移阻抗,低频区部分的斜线反映锂离子在固体中的扩散阻抗W1。通过对比第5次和第50次拟合结果发现,循环过程中Rs变化不大,但是未包覆的正极材料的RSEI,Rct明显增大,而包覆材料的RSEI,Rct只有少许增加。这说明通过包覆减慢了LNCMO在循环过程中锂离子扩散的电荷转移阻抗和膜阻抗增加速率。
|
图 11 未包覆(a)、包覆2% FePO4试样(b)的交流阻抗图谱和等效电路图(c) Fig. 11 EIS analysis of LNCMO(a), LNCMO coated with 2% FePO4(b) and the corresponding equivalent-circuit diagram(c) |
| Sample | Rs/Ω | RSEI/Ω | Rct/Ω |
| LNCMO(5th) | 6.65 | 140.24 | 60.85 |
| LNCMO(50th) | 6.23 | 225.70 | 100.56 |
| 2%(5th) | 7.56 | 150.35 | 65.43 |
| 2%(50th) | 6.89 | 162.30 | 70.78 |
电极反应的交换电流密度大小可由式(1)计算:
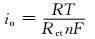
|
(1) |
式中: io是交换电流密度,A/m2;R是气体常数,8.314J/(mol·K);T是温度,K;Rct是电荷转移阻抗,Ω;n是反应得失电子数;F是法拉第常数,96485C/mol。可以看出,io与Rct成反比关系,根据表 2的模拟结果分析,即通过包覆FePO4,增加了LNCMO参与电极反应的交换电流密度,有利于改善材料的动力学特性,提高其倍率性能。
将LNCMO和400℃热处理12h, 2%FePO4包覆试样分别制成扣式电池,充电至4.3V时,然后在手套箱中将扣式电池拆解开,取出正极片,使用碳酸二甲酯洗去残留在正极片上的电解液,然后将正极片置于电解液中(按正极材料与电解液质量比1:50),将其密封好在室温下浸泡30天后,用离心机分离出电解液,将电解液进行消解稀释,采用ICP测试电解液中的Ni, Co, Mn元素的浓度。表 3是LNCMO和2% FePO4包覆试样在电解液中过渡金属的溶出量。
| Sample | Release of metals/(mol·L-1) | ||
| Ni | Co | Mn | |
| LNCMO | 2.2× 10-3 | 1.1×10-3 | 1.4×10-3 |
| 2% | 1.9×10-6 | 1.3 ×10-6 | 1.2×10-6 |
可以看出,LNCMO和包覆试样在电解液中浸泡30天都有过渡金属溶出,但包覆试样的Ni,Co,Mn溶出量明显低于LNCMO。原因是电解液中有痕量水与电解液中的LiPF6反应生成HF,HF能溶解过渡金属离子。正极材料表面的过渡金属在电解液中溶解造成了正极材料表面结构的破坏,使得材料局部结构坍塌,同时表面也会沉积高阻抗的金属氟化物,造成锂离子在脱嵌过程阻抗增大,导致材料在循环过程中的容量衰减[27]。
正极材料表面包覆适量的FePO4后,FePO4在正极材料的表面形成紧密的包覆层。一方面,电化学测试结果表明,包覆磷酸铁提高了正极材料的动力学性能,减小了电极反应极化,增加了锂离子脱出、嵌入的可逆性;另一方面,减少了Ni, Co, Mn的溶解,避免了电解液与材料因直接接触而发生的副反应,稳定了正极材料的结构,从而提高了材料的循环寿命。众所周知,在电解液与活性材料表面之间存在着由聚合物形成的固液界面膜(SEI)。有文献报道[25],FePO4可以与SEI膜中的聚合物组分相互作用形成了有利于锂离子传输的界面层,从而改善正极材料的表面动力学性能。
3 结论(1) 通过水热法,合成出纳米磷酸铁悬浮液,随着烧结温度的升高,FePO4将由无定形态转化为α-石英结构,悬浮液中FePO4一次颗粒粒径在8~10nm之间,适合用于包覆正极材料。
(2) 采用共沉淀法将纳米FePO4包覆在锂离子电池正极材料LiNi0.5Co0.2Mn0.3O2表面,并研究热处理温度和包覆量对材料性能的影响,FePO4包覆虽然会略微降低正极材料容量,但是能够减少正极材料与电解液直接接触的机会,避免电解液与正极材料副反应的发生,从而改善其循环性能。当烧结温度为400℃、包覆量为2%情况下,无定形FePO4能够提供了更多的锂离子扩散通道,LiNi0.5Co0.2Mn0.3O2的100次循环后的容量保持率为85.54%,倍率性能提高显著,是最佳的包覆条件,说明通过磷酸铁包覆,能够改善LiNi0.5Co0.2Mn0.3O2的电化学性能。
| [1] | BOK J S, LEE J H, LEE B K, et al. Effects of synthetic conditions on electrochemical activity of LiCoO2 prepared from recycled cobalt compounds[J]. Solid State Ionics, 2004, 169 (1/4): 139–144. |
| [2] | LUO W B, DAHN J R. Comparative study of Li[Co1-zAlz]O2 prepared by solid-state and co-precipitation methods[J]. Electrochimica Acta, 2009, 54 (20): 4655–4661. DOI: 10.1016/j.electacta.2009.03.068 |
| [3] | MCBREEN J. The application of synchrotron techniques to the study of lithium-ion batteries[J]. Journal of Solid State Electrochemistry, 2009, 13 (7): 1051–1061. DOI: 10.1007/s10008-008-0685-1 |
| [4] | JEFF T. Car industry:charging up the future[J]. Nature, 2008, 456 (7221): 436–440. DOI: 10.1038/456436a |
| [5] | OHZUKU T, MAKIMURA Y. Layered lithium insertion material of LiCo1/3Ni1/3Mn1/3O2 for lithium-ion batteries[J]. Chemistry Letters, 2001, 1 (7): 642–643. |
| [6] | KOYAMA Y, TANAKA I, ADACHI H, et al. Crystal and electronic structures of superstructural Li1-x[LiCo1/3Ni1/3Mn1/3]O2(0 ≤ x ≤ 1)[J]. Journal of Power Sources, 2003, 119 : 644–648. |
| [7] | YOSHIO M, NOGUCHI H, ITON J I, et al. Preparation and properties of LiCoyMnxNi1-x-yO2 as a cathode for lithium ion batteries[J]. Journal of Power Sources, 2000, 90 (2): 176–181. DOI: 10.1016/S0378-7753(00)00407-9 |
| [8] | HE Y S, MA Z F, LIAO X Z, et al. Synthesis and characterization of submicron-sized LiNi1/3Co1/3Mn1/3O2 by a simple self-propagating solid-state metathesis method[J]. Journal of Power Sources, 2007, 163 (2): 1053–1058. DOI: 10.1016/j.jpowsour.2006.09.061 |
| [9] | WANG Z Y, LIU E, HE C N, et al. Effect of amorphous FePO4 coating on structure and electrochemical performance of Li1.2Ni0.13Co0.13Mn0.54O2 as cathode material for Li-ion batteries[J]. Journal of Power Sources, 2013, 236 : 25–32. DOI: 10.1016/j.jpowsour.2013.02.022 |
| [10] | ZHI Y, LI X H, WANG Z X, et al. Surface modification of spherical LiNi1/3Co1/3Mn1/3O2 with A12O3 using heterogeneous nucleation process[J]. Transactions of Nonferrous Metals Society of China, 2007, 17 (6): 1319–1323. DOI: 10.1016/S1003-6326(07)60269-6 |
| [11] | SINHA N N, MUNICHANDRAIAH N. Synthesis and characterization of carbon-coated LiNi1/3Co1/3Mn1/3O2 in a single step by an inverse microemulsion route[J]. ACS Applied Materials & Interfaces, 2009, 1 (6): 1241. |
| [12] | KIM Y, KIM H S, MARTIN S W. Synthesis and electrochemical characteristics of A12O3-coated LiNi1/3Co1/3Mn1/3O2 cathode materials for lithium ion batteries[J]. Electrochimica Acta, 2006, 52 (3): 1316–1322. DOI: 10.1016/j.electacta.2006.07.033 |
| [13] | RILEY L A, ATTA S V, CAVANAGH A S, et al. Electrochemical effects of ALD surface modification on combustion synthesized LiNi1/3Co1/3Mn1/3O2 as a layered-cathode material[J]. Journal of Power Sources, 2011, 196 (6): 3317–3324. DOI: 10.1016/j.jpowsour.2010.11.124 |
| [14] | WU Y. High capacity, surface-modified layered Li[Li(1-x)/3Mn(2-x)/3Nix/3Cox/3]O2 cathodes with low irreversible capacity loss[J]. Electrochemical and Solid-State Letters, 2006, 9 (5): 221–224. DOI: 10.1149/1.2180528 |
| [15] | WU F, WANG M, SU Y F, et al. Effect of TiO2-coating on the electrochemical performances of LiCo1/3Ni1/3Mn1/3O2[J]. Journal of Power Sources, 2009, 191 (2): 628–632. DOI: 10.1016/j.jpowsour.2009.02.063 |
| [16] | LI Y, YANG Q, Yao J, et al. Effect of synthesis temperature on the phase structure and electrochemical performance of nickel hydroxide[J]. Ionics, 2010, 16 (3): 221–225. DOI: 10.1007/s11581-009-0397-2 |
| [17] | LI H J, CHEN G, ZHANG B, et al. Advanced electrochemical performance of Li[Ni(1/3-x)FexCo1/3Mn1/3]O2 as cathode materials for lithium-ion battery[J]. Solid State Communications, 2008, 146 (3/4): 115–120. |
| [18] | GUO R, SHI P F, CHENG X Q, et al. Effect of ZnO modification on the performance of LiNi0.5Co0.25Mn0.25O2 cathode material[J]. Electrochimica Acta, 2009, 54 (24): 5796–5803. DOI: 10.1016/j.electacta.2009.05.034 |
| [19] | LEE H J, KIM Y J, HONG Y S, et al. Structural characterization of the surface-modified LixNi0.9Co0.1O2 cathode materials by MPO4 coating (M=Al, Ce, Sr, and Fe) for Li-ion cells[J]. Journal of the Electrochemical Society, 2015, 153 (153): 781–786. |
| [20] | KIM H S, KIM W S, GU H B, et al. Electrochemical performance of SnPO4-coated LiNi1/3Co1/3Mn1/3O2 cathode materials[J]. Journal of New Materials for Electrochemical Systems, 2009, 12 (4): 207–212. |
| [21] | DOU J Q, KANG X Y, WUMAIER T, et al. Effect of lithium boron oxide glass coating on the electrochemical performance of LiNi1/3Co1/3Mn1/3O2[J]. Journal of Solid State Electrochemistry, 2012, 16 (4): 1481–1486. DOI: 10.1007/s10008-011-1550-1 |
| [22] | SUN Y K, LU W. On the safety of the Li4Ti5O12/LiMn2O4 lithium-ion battery system[J]. Journal of the Electrochemical Society, 2007, 154 (12): 1083–1087. DOI: 10.1149/1.2783770 |
| [23] | KIM H S, KIM Y. Enhanced electrochemical properties of LiNi1/3Co1/3Mn1/3O2 cathode material by coating with LiAlO2 nanoparticles[J]. Journal of Power Sources, 2006, 161 (1): 623–627. DOI: 10.1016/j.jpowsour.2006.03.092 |
| [24] | LI G, YANG Z, YANG W. Effect of FePO4 coating on electrochemical and safety performance of LiCoO2 as cathode material for Li-ion batteries[J]. Journal of Power Sources, 2008, 183 (2): 741–748. DOI: 10.1016/j.jpowsour.2008.05.047 |
| [25] | QING C, BAI Y, YANG J. Enhanced cycling stability of LiMn2O4 cathode by amorphous FePO4 coating[J]. Electrochimica Acta, 2011, 56 (19): 6612–6618. DOI: 10.1016/j.electacta.2011.04.131 |
| [26] | ZHANG S M, ZHANG J X, XU S J, et al. Li ion diffusivity and electrochemical properties of FePO4 nanoparticles acted directly as cathode materials in lithium ion rechargeable batteries[J]. Electrochimica Acta, 2013, 88 (2): 287–293. |
| [27] | LEE B R, NOH H J, MYUNG S T, et al. High-voltage performance of Li[Ni0.55Co0.15Mn0.30]O2 positive electrode material for rechargeable Li-ion batteries[J]. Journal of Electrochemical Society, 2011, 158 : A180–A186. DOI: 10.1149/1.3525247 |
 2017, Vol. 45
2017, Vol. 45


