文章信息
- 刘天娇, 陈惠鹏, 张卫方, 娄伟涛
- LIU Tian-jiao, CHEN Hui-peng, ZHANG Wei-fang, LOU Wei-tao
- B10铜镍合金海水加速腐蚀行为
- Accelerated Corrosion Behavior of B10 Cu-Ni Alloy in Seawater
- 材料工程, 2017, 45(5): 31-37
- Journal of Materials Engineering, 2017, 45(5): 31-37.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2015.000411
-
文章历史
- 收稿日期: 2015-04-15
- 修订日期: 2016-08-31
B10铜镍合金具有优良的耐海水腐蚀性能,广泛用于海洋制造业中,在舰船上主要用作螺旋桨、冷凝器、海水管系、泵阀及结构件等[1]。虽然这种合金已投入使用多年,但其服役过程中,仍然存在很多隐患,经研究,大部分失效是由海水腐蚀引起的。目前,国内外研究人员对这种合金的耐海水腐蚀性能进行了大量研究,随着检测手段越来越先进,如电化学技术、显微镜观测技术、能谱分析技术等,关于B10合金的腐蚀失效机理也越来越清晰,并提出了很多有效的控制措施。
杜鹃等[2]采用旋转圆桶冲刷腐蚀试验机并结合电化学测试、表面分析等手段,研究了B10铜镍合金管件海水冲刷腐蚀行为,结果表明,B10合金在不同实验流速的海水中腐蚀速率随腐蚀时间的变化规律相似,在海水腐蚀过程中合金表面都会形成内、外双层保护性的腐蚀产物膜,产物膜会随着海水流速增加而变薄,腐蚀反应阳极区随海水流速和时间变化较大,腐蚀受阳极反应和传质过程控制。迟长云等[3]用电化学的方法研究了B30铜镍合金的海水腐蚀行为,结果表明,B30铜镍合金在海水中浸泡,表面生成的氧化膜使合金在海水中的阻抗值随浸泡时间的延长呈现先增大后减小的规律,B30铜镍合金在海水中的点蚀倾向加重。海水中存在大量的Cl-,Cl-在海水腐蚀中有至关重要的作用,一般室内模拟海水腐蚀铜合金时会采用NaCl溶液代替天然海水。刘伟华等[4]利用电化学阻抗谱技术研究了Cl-对铸态Cu-40Ni合金的影响,研究表明,在腐蚀介质中,Cl-含量的增加会导致腐蚀速率加快,腐蚀介质中加入Cl-后,腐蚀过程由电化学控制,阻抗谱呈单一容抗弧特征,没有出现Warburg阻抗的性质,腐蚀过程中存在一定弥散效应。国外对Cu-Ni合金海水管路材料的海水腐蚀开展了大量实验研究[5-9],1995年,美军水面防务中心的技术报告中报道了美军海水管系材料在海水环境中腐蚀的极化曲线图集,介绍了铜镍合金在静态海水和流动海水中进行腐蚀实验的实验装置和测试方法,对B10和B30铜镍合金等材料进行了静止海水和2.4m/s流动海水中的极化曲线测量。英国轮机规范研究制定了不同管径条件下,B10铜镍合金海水管允许设计流速值,以此来控制海水冲刷引起的管路腐蚀。Drach等[10]将8种铜合金浸泡在南大西洋1年,通过失重、环境扫描、拉伸等测试方法对比了8种铜合金的腐蚀行为,对腐蚀速率和生物腐蚀性能作了定量分析。Bautista等[11]也对海水腐蚀中的生物因素影响做了研究。
通常,在实验室内模拟海水腐蚀实验,都是以3.0%或3.5%NaCl溶液代替海水作为腐蚀介质进行研究[12-15],事实上,天然海水包含很多复杂的成分,有文献[16, 17]指出,海水中的碳酸氢根离子和硝酸根离子可以提高铝合金的腐蚀电位。故采用天然海水并加入双氧水H2O2作为加速剂进行腐蚀实验,该方法在文献[18, 19]中,分别以高强度-低合金钢和2024-T3铝合金为研究对象,得到了良好的验证,本工作针对船用国产B10铜镍合金,采用失重测试、扫描电子显微镜(SEM)技术、XPS和拉曼光谱技术以及电化学阻抗谱技术研究了B10合金在海水全浸加速腐蚀实验中的腐蚀行为,通过分析失重规律、表面膜成分、表面腐蚀形貌以及不同腐蚀周期的电化学阻抗谱特征探究了B10合金的腐蚀机理。
1 实验材料与方法实验所用材料为B10铜镍合金,其化学成分如表 1所示。
| Si | P | Fe | S | Zn | Ni | Mn | Cu |
| < 0.15 | < 0.02 | 1.20 | 0.0013 | < 0.3 | 9.76 | 0.74 | Bal |
腐蚀失重试样尺寸为100mm×50mm×3mm,呈银白色,试样打孔做标识,每组3个平行样。利用电游标卡尺精确测量长、宽、厚,用乙醇清洗2~3遍后,干燥并称重。为了真实模拟合金在海水中的腐蚀状态,腐蚀介质为厦门天然海水+0.05mol/L H2O2,恒温水浴锅控制实验温度为30℃。腐蚀周期设定为1,3,7,14,21,28,42,56,112d,共9个周期。腐蚀介质每3d更换一次。
试样在腐蚀初期,定期取样在显微镜下观察表面腐蚀产物膜的生长情况。腐蚀不同周期并干燥后,利用XPS和拉曼光谱技术分析腐蚀产物成分。将试样浸泡在稀释10倍后的相对密度为1.84的硫酸溶液中,静置3min,硬毛刷清除腐蚀产物,干燥24h,称重,计算样品的平均失重。随后在扫描电镜下观察试样表面的微观腐蚀形貌。
电化学测试在Autolab电化学工作站上进行,采用三电极测试体系,辅助电极采用316L不锈钢,参比电极为Ag/AgCl电极,实验介质为厦门天然海水。试样用线切割制为10mm×10mm×3mm,工作面积1cm2。用环氧树脂将试样固封在直径为25mm,长为20mm的PVC管中,试样背面用锡焊接一定长度的铜导线,用150#,400#,1000#,1500#,2000#水磨砂纸逐级打磨试样后,经蒸馏水、丙酮、无水乙醇清洗,干燥24h后备用。
2 结果与分析 2.1 腐蚀失重腐蚀的平均速率可用失重法来测量,v=(m0-mt)/AT,其中,v是平均腐蚀速率;m0,mt,A分别为试样腐蚀前后的质量和试样全浸的表面积;T为腐蚀时间(d)。图 1为B10试样平均腐蚀速率随腐蚀周期的变化规律。由图 1可知,腐蚀初期,平均腐蚀速率最大,随着腐蚀时间的增大,平均腐蚀速率几乎呈指数规律下降,腐蚀28d后,平均腐蚀速率趋于平稳,这与文献[20, 21]的结论是吻合的。反应初期,试样表面快速形成保护性的氧化膜层,并随着腐蚀时间延长,氧化膜逐渐致密完整,有效地阻碍了腐蚀介质与基体的接触,从电化学的角度来看,氧化膜降低了材料表面阴、阳极反应的传质速率和电荷转移速率,从而降低了腐蚀速率。当腐蚀发展到一定程度,表面氧化膜被破坏,合金质量损失会进一步增大。

|
图 1 B10试样平均腐蚀速率随时间变化趋势 Fig. 1 The tendency of B10 sample average corrosion rate vs corrosion time |
B10铜镍合金浸泡在海水中表面会形成一层氧化膜,这层氧化膜的形成质量、致密程度及其破坏对于B10铜镍合金耐海水腐蚀性能具有重要的影响。
图 2为B10腐蚀早期的表面微观形貌,比较直观地展示了试样表面腐蚀产物膜的生长情况,试样浸入腐蚀介质初期,表面形成非常小的颗粒状产物,并且颗粒之间间隙较大,随着腐蚀时间的延长,颗粒尺寸逐渐增大,且局部区域形成平坦的片状腐蚀产物膜,依然能看到试样表面未被覆盖的基体,膜正处于生长的阶段。腐蚀72h(3d)后,小片的腐蚀产物膜开始成块附着在试样表面,膜疏松、多孔。腐蚀168h(1周)后,腐蚀产物渐已致密,且表面出现了明显的点蚀坑,蚀坑内的金属表面处于活态,电位较负;而蚀孔外的金属表面处于钝态,电位较正,于是孔内和孔外构成一个活态-钝态微电偶腐蚀电池,电池具有大阴极-小阳极的面积比结构,阳极电流密度很大,点蚀加深很快[22, 23]。研究表明[24],B10铜镍合金在腐蚀中发生脱镍腐蚀, 本研究对B10铜镍合金的腐蚀表面做了能谱分析, 如表 2所示,Cu和Ni的含量随腐蚀时间的延长不断下降,Ni含量的下降率更大,证实B10铜镍合金在海水腐蚀中发生了脱镍腐蚀,Cl和O的含量不断增加,说明其参与腐蚀反应,作为腐蚀产物的成分沉淀在合金表面。

|
图 2 B10铜镍合金腐蚀初期的表面微观形貌 (a)2h;(b)8h;(c)72h;(d)168h Fig. 2 Surface morphology of B10 Cu-Ni alloy at the early stages of corrosion (a)2h;(b)8h;(c)72h;(d)168h |
| Time/h | Cu | Ni | O | Cl |
| 2 | 79.93 | 10.4 | 9.55 | 0.12 |
| 8 | 72.56 | 9.2 | 18.24 | 0 |
| 72 | 67.19 | 8.83 | 23.98 | 0 |
| 168 | 59.71 | 2.47 | 27.8 | 10.02 |
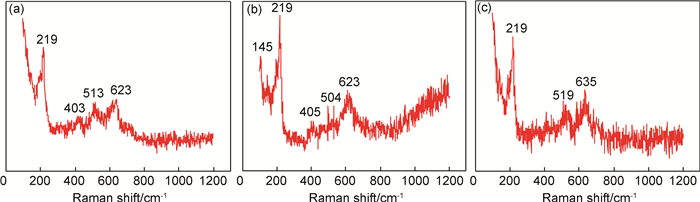
为了分析腐蚀产物的最终成分状态,对腐蚀7d之后不同腐蚀周期的腐蚀产物作了XPS和拉曼光谱分析,图 3是B10合金腐蚀7,14,28,56d时腐蚀产物中Cu 2p XPS窄谱扫描图,谱图上出现Cu 2p3/2和Cu 2p1/2双峰,其峰位分别为931.88~932.63.0 eV和951.52~952.15eV,这表明,腐蚀产物中含碱式氯化铜(Cu2(OH)3Cl)或氢氧化铜(Cu(OH)2)[25],另外,在28d的谱图上出现振激峰S且强度随时间增大,这表明有二价Cu2+存在于腐蚀产物中,结合图 4中B10腐蚀7,14,28d后表面腐蚀产物的拉曼光谱图,出现峰位分别为219,623cm-1(14d),219,635cm-1(28d)的谱图,断定腐蚀产物中含有Cu2(OH)3Cl[26]越多,另外腐蚀1周的拉曼光谱图上有峰位219,513cm-1,可以断定在腐蚀后试样表层的氧化物中含有Cu2O,且由峰的强度可知,其厚度随腐蚀时间逐渐增大。文献[25]指出,Cu2O膜分为内外层,外层是由溶解的Cu+再沉淀生成,内层是由Cu2O膜向内生长而成,且内层膜更加致密,更具有保护性。关于Cu2O膜的分层,有待进一步研究。将试样表面酸洗后,在显微镜下观察其表面的腐蚀状态,如图 5所示,腐蚀1d的表面比较光滑平整,基体腐蚀不明显,14d后,表面出现大小不一的腐蚀坑,发生了严重的点蚀,点蚀深入发展,到28d时,腐蚀沿着晶界进行,可以看到明显的晶间腐蚀[27],这与晶界析出相有关, 在海水介质中,铜镍合金中的Ni和Fe有向表面富集的趋势,合金元素向表面的扩散主要通过晶界来实现,合金元素的扩散会加速合金晶界原有的析出物形核的粗化[28],由于析出物自身已经形成了腐蚀微电池,如果暴露在海水介质中,腐蚀便会沿晶进行,在腐蚀56d的试样表面已经发展为大片的剥蚀坑,这说明,B10铜镍合金的腐蚀形态经历了点蚀-晶间腐蚀-剥蚀的历程。

|
图 3 B10铜镍合金在不同腐蚀周期下腐蚀产物XPS Cu 2p窄谱扫描图 Fig. 3 XPS spectra of Cu 2p for the surface of the corrosion products formed on B10 Cu-Ni alloy with different corrosion time |
|
图 4 B10铜镍合金腐蚀拉曼光谱 (a)7d;(b)14d;(c)28d Fig. 4 Raman spectra of the corroded B10 Cu-Ni alloy (a)7d;(b)14d;(c)28d |

|
图 5 B10试样海水腐蚀不同周期后的表面微观形貌(酸洗后)(a)7d;(b)14d;(c)28d;(d)56d Fig. 5 Surface morphology of B10 sample immersed in seawater for different time(with corrosion products removed)(a)7d;(b)14d;(c)28d;(d)56d |
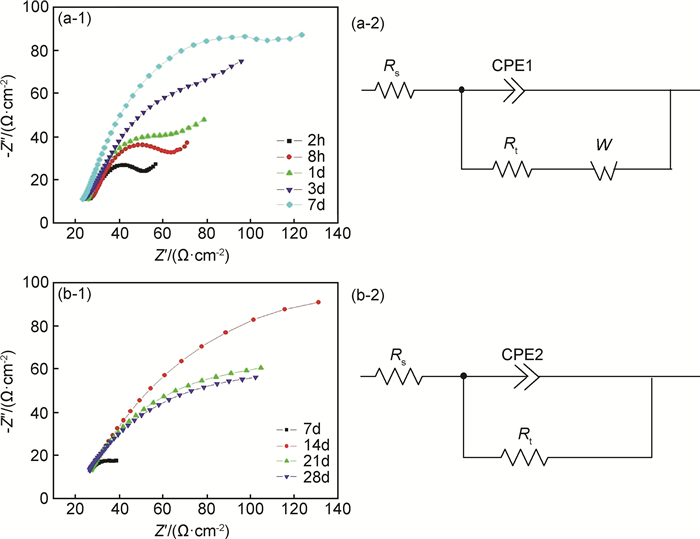
图 6所示为B10合金腐蚀不同时间的电化学阻抗谱,由图 6可知,腐蚀2,8h,1,3,7d的阻抗谱都是由两个时间常数的容抗弧组成,腐蚀14,21,28d的阻抗谱呈现单一容抗弧特征,双容抗弧特征表示,B10合金在浸入海水初期,表面迅速生成保护性的氧化膜,在这段时间,试样的阻抗值不断增大,表明氧化膜越来越致密,14d时,试样的阻抗值达到最大,且出现了单一容抗弧,表明这时的氧化膜生长已达到了外层溶解内层生长的动态平衡,此后,试样的阻抗值不断下降,表明氧化膜处于不断被溶解的过程,合金基体暴露在海水介质中,开始了点蚀-晶间腐蚀-剥蚀的历程,此后的海水腐蚀速率随着表层氧化膜的溶解会不断增大。在前期,阻抗谱在低频区出现了扩散,在高频区为容抗弧,这种状况表明阴极反应的溶解氧出现浓度扩散梯度,整个过程受扩散控制[29],因此等效电路应包含溶液电阻(Rs)、合金/界面阻抗(CPE1)(常相位元件,n=1时为等效电容)、电荷转移电阻(Rt)以及Warburg阻抗(W)。在后期,表面膜受到了破坏,海水中Cl-优先于溶解氧攻击合金基体,阻抗值降低,腐蚀速率增大,等效电路应包含溶液电阻(Rs)、合金/界面阻抗(CPE2)、电荷转移电阻(Rt),且各阻值都发生了变化,利用Zsimpwin软件计算由等效电路得到的电荷转移电阻Rt值,可以通过Rt值的大小来判断电荷转移过程的难易程度,Rt值越大,电荷转移过程越难以进行[30, 31],Rt值在2h时测得为5.61×10-1Ω,随着时间的增加,在14d时达到最大,为2.46×103Ω,之后又随时间减小,到28d时,减小至2.04×103Ω,这表明合金基体从14d之后开始溶解在海水中。
|
图 6 B10铜镍合金海水腐蚀不同时间的Nyquist图(1) 及其等效电路图(2) (a)2h~7d;(b)7~28d Fig. 6 Electrochemical impedance spectroscopy(EIS) of B10 Cu-Ni alloy exposed in seawater for different time (1) and the corresponding equivalent circuits (2) (a)2h-7d;(b)7-28d |
(1) B10铜镍合金在海水腐蚀初期,平均腐蚀速率随时间呈幂函数规律下降,在后期,随着表面氧化膜被破坏,质量损失量会进一步增大。
(2) B10铜镍合金在海水腐蚀中发生脱镍腐蚀,腐蚀产物中包含Cu2(OH)3Cl,Cu2O,合金表面的氧化膜破坏由点蚀开始,点蚀进一步发展为晶间腐蚀,最后发展为剥蚀。
(3) B10铜镍合金在海水腐蚀初期的阻抗谱呈双容抗弧特征,腐蚀过程受溶解氧扩散控制,合金表面形成致密完整的保护膜,加速腐蚀14d后,氧化膜遭到破坏,腐蚀过程受电化学反应控制,合金基体直接暴露在海水介质中,电荷传递加快,腐蚀速率加快。
| [1] | 张智强, 郭泽亮, 雷竹芳. 铜合金在舰船上的应用[J]. 材料开发与应用, 2006, 21 (5): 43–46. ZHANG Z Q, GUO Z L, LEI Z F. Applications of copper alloy in shipbuilding[J]. Development and Application of Materials, 2006, 21 (5): 43–46. |
| [2] | 杜娟, 王洪仁, 杜敏, 等. B10铜镍合金流动海水冲刷腐蚀电化学行为[J]. 腐蚀科学与防护技术, 2008, 20 (1): 12–18. DU J, WANG H R, DU M, et al. Electrochemical corrosion behavior of B10 Cu-Ni alloy in flowing seawater[J]. Corrosion Science and Protection Technology, 2008, 20 (1): 12–18. |
| [3] | 迟长云, 李宁, 薛建军, 等. B30铜镍合金在海水中的电化学行为[J]. 材料保护, 2009, 42 (8): 19–22. CHI C Y, LI N, XUE J J, et al. Electrochemical behavior of B10 Cu-Ni alloy in seawater[J]. Material Protection, 2009, 42 (8): 19–22. |
| [4] | 刘伟华, 曹中秋, 郑志国. Cl-含量对铸态Cu-40Ni合金电化学腐蚀行为的影响[J]. 沈阳师范大学学报, 2004, 22 (3): 220–223. LIU W H, CAO Z Q, ZHENG Z G. The effect of Cl- content on corrosion electrochemical behavior of CA Cu-40Ni Alloy[J]. Journal of Shenyang Normal University (Natural Science), 2004, 22 (3): 220–223. |
| [5] | SYRETT B C, MACDONALD D D. The validity of electrochemical methods for measuring corrosion rates of copper-nickel alloys in sea water[J]. Corrosion, 1979, 35 (11): 505–509. |
| [6] | MELCHERS R E. Temperature effect on seawater immersion corrosion of 90/10 copper-nickel alloy[J]. Corrosion, 2001, 57 (5): 440–444. |
| [7] | CROUSIER J, BECCARIA A M. Behavior of Cu-Ni alloys in natural sea water and NaCl solution[J]. Materials and Corrosion, 1990, 41 (4): 185–189. |
| [8] | DHAR H P, WHITE R E, BURNELL G., et al. Corrosion of Cu and Cu-Ni alloys in 0.5 M NaCl and in synthetic seawater[J]. Corrosion, 1985, 41 (6): 317–323. |
| [9] | HODGKIESS T, VASSILIOU G. Complexities in the erosion corrosion of copper-nickel alloys in saline water[J]. Desalination, 2005, 183 (1): 235–247. |
| [10] | DRACH A, TSUKROV I, DECEW J, et al. Field studies of corrosion behavior of copper alloys in natural seawater[J]. Corrosion Science, 2013, 76 (1): 453–464. |
| [11] | BAUTISTA B E T, WIKIEL A J, DATSENKO I, et al. Influence of extracellular polymeric substances (EPS) from Pseudomonas NCIMB 2021 on the corrosion behavior of 70Cu-30Ni alloy in seawater[J]. Journal of Electroanalytical Chemistry, 2015, 737 (1): 184–197. |
| [12] | ROSSANA G, MARK A B, JAMES E C, et al. Corrosion behavior of a 2219 aluminum alloy treated with a chromate conversion coating exposed to a 3.5% NaCl solution[J]. Corros Sci, 2011, 53 : 1214–1223. |
| [13] | 陈红梅, 赵茂密, 王戎丞, 等. Al-Zr-Nd合金在3.5%NaCl溶液中的腐蚀行为[J]. 腐蚀与防护, 2013, 34 (12): 1072–1076. CHEN H M, ZHAO M M, WANG R C, et al. Corrosion behavior of Al-Zr-Nd alloys in 3.5% NaCl solution[J]. Corrosion and Protection, 2013, 34 (12): 1072–1076. |
| [14] | LI S H, ZHANG H R, LIU J H. Corrosion behavior of aluminum alloy 2024-T3 by 8-hydroxy-quinoline and its derivative in 3.5% chloride solution[J]. Trans Nonferrous Met Soc China, 2007, 17 (2): 318–325. |
| [15] | 祁星, 宋仁国, 祁文娟, 等. pH值对7050铝合金膜致应力和应力腐蚀敏感性的影响[J]. 材料工程, 2016, 44 (5): 86–92. QI X, SONG R G, QI W J, et al. Influence of pH values on passive film-induced stress and susceptibility to stress corrosion cracking in 7050 aluminum alloy[J]. Journal of Materials Engineering, 2016, 44 (5): 86–92. |
| [16] | 陈翔峰. LF6M铝镁合金发生包铝鼓泡的机理研究[C]//水环境腐蚀与防护学术研讨会论文集. 北京: 北京科技大学出版社, 2010. CHEN X F. Study on the blistering mechanism of LF6M Al magnesium alloy [C]//Chinese Institute of Corrosion and Protection, Corrosion and Protection of Water Environment Symposium Set. Beijing: Beijing University of Science and Technology Press, 2010. |
| [17] | AN B G, ZHANG X Y, HAN E H. The effect of salt species during the precipitation in the atmosphere on the corrosion of LY12CZ alloy[C]//International Corrosion Council, 15th International Corrosion Congress.Spain: Corrosion Engineering Science & Technology the International Journal of Corrosion Processes & Corrosion Control, 2002. |
| [18] | 杨超, 张慧霞, 郭为民, 等. 添加双氧水对高强度低合金钢在海水中腐蚀影响研究[J]. 中国腐蚀与防护学报, 2013, 33 (3): 205–210. YANG C, ZHANG H X, GUO W M, et al. Effects of H2O2 addition on corrosion behavior of high strength low-alloy steel in seawater[J]. Journal of Chinese Society for Corrosion and Protection, 2013, 33 (3): 205–210. |
| [19] | ONES K, HOEPPNER D W. Prior corrosion and fatigue of 2024-T3 aluminum alloy[J]. Corrosion Science, 2006, 48 (10): 3109–3122. |
| [20] | 尹承军. B10合金在模拟海水中的冲刷腐蚀研究[D]. 哈尔滨: 哈尔滨工程大学, 2012. YIN C J. Erosion-corrosion of 90/10 alloy in artificial seawater [D]. Harbin: Harbin Engineering University, 2012. |
| [21] | 郭瑞金, 火时中. 小孔腐蚀诱发过程的研究[J]. 中国腐蚀与防护学报, 1986, 6 (2): 113–122. GUO R J, HUO S Z. An investigation of pitting initiation process[J]. Journal of Chinese Society for Corrosion and Protection, 1986, 6 (2): 113–122. |
| [22] | YIN B, YIN Y, LEI Y, et al. Experimental and density functional studies on the corrosion behavior of the copper-nickel-tin alloy[J]. Chemical Physics Letters, 2011, 509 (4): 192–197. |
| [23] | 陈海燕, 朱有兰. B10铜镍合金在NaCl溶液中腐蚀行为的研究[J]. 腐蚀与防护, 2006, 27 (8): 404–407. CHEN H Y, ZHU Y L. Selective corrosion of BFe10-1-1 alloy in NaCl solution[J]. Corrosion and Protection, 2006, 27 (8): 404–407. |
| [24] | MA A L, JIANG S L, ZHENG Y G, et al. Corrosion product film formed on the 90/10 copper-nickel tube in natural seawater: Composition/structure and formation mechanism[J]. Corrosion Science, 2015, 91 (1): 245–261. |
| [25] | MANSFELD F, LIU G, XIAO H, et al. The corrosion behavior of copper alloys, stainless steels and titanium in seawater[J]. Corrosion Science, 1994, 36 (12): 2063–2095. |
| [26] | WAGNER C D. Handbook of X-ray photoelectron spectroscopy: a reference book of standard data for use in X-ray photoelectron spectroscopy[M]. USA: Perkin-elmer Corporation Physical Electronics Division, 1992. |
| [27] | 林乐耘, 刘少峰. 铜镍合金海水腐蚀的表面与界面特征研究[J]. 腐蚀科学与防护技术, 1999, 11 (1): 37–43. LIN Y Y, LIU S F. Surface and interface characteristics of Cu-Ni alloy corroded in seawater[J]. Corrosion Science and Protection Technology, 1999, 11 (1): 37–43. |
| [28] | 林乐耘, 刘少峰, 朱小龙. 海水腐蚀导致铜镍合金的沿晶析出[J]. 中国腐蚀与防护学报, 1997, 17 (1): 1–6. LIN Y Y, LIU S F, ZHU X L. Seawater corrosion-induced intergranular precipitation in Cu-Ni alloy[J]. Journal of Chinese Society for Corrosion and Protection, 1997, 17 (1): 1–6. |
| [29] | 赵永韬, 李海洪, 陈光章. 铜合金在海水中电化学阻抗谱特征研究[J]. 海洋科学, 2005, 29 (7): 21–25. ZHAO Y T, LI H H, CHEN G Z. EIS characteristics of Cu-based alloy in seawater[J]. Marine Sciences, 2005, 29 (7): 21–25. |
| [30] | ROBERGE P R, HALLIOP E. Electrochemical impendance spectroscopy as an erosion corrosion rate monitoring technique[J]. Corrosion, 1990, 23 (27): 1–11. |
| [31] | IJSSELING F P. General guidelines for corrosion testing of materials for marine applications: Literature review on sea water as test environment[J]. British Corrosion Journal, 1989, 24 (1): 53–78. |
 2017, Vol. 45
2017, Vol. 45


