文章信息
- 梁银, 李朋, 裴旺, 段晋辉, 黄峰, 赵昆渝
- LIANG Yin, LI Peng, PEI Wang, DUAN Jin-hui, HUANG Feng, ZHAO Kun-yu
- 阳极氧化疏松钛膜制备高光催化活性的透明TiO2纳米多孔涂层
- Preparation of Transparent TiO2 Nanoporous Coating with Highly Photocatalytic Activity by Anodizing Ti Film with Loose Structure
- 材料工程, 2016, 44(7): 99-106
- Journal of Materials Engineering, 2016, 44(7): 99-106.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2016.07.017
-
文章历史
- 收稿日期: 2014-10-10
- 修订日期: 2016-03-27
2. 中国科学院 宁波材料技术与工程研究所, 浙江 宁波 315201
2. Ningbo Institute of Materials Technology and Engineering, Chinese Academy of Sciences, Ningbo 315201, Zhejiang, China
随着高层建筑逐渐兴起,其外围护墙很少再采用传统的砖墙,取而代之的是高透光率的玻璃幕墙。但空气中存在的大量灰尘、有机污染物等很容易使玻璃幕墙变脏而影响美观。随之带来的玻璃清洁问题变得越来越突出,尤其对高层建筑玻璃幕墙的清洁还存在危险性,因此发展自清洁玻璃具有广阔的应用前景。通过在玻璃表面形成TiO2光催化薄膜,能有效地利用太阳光中紫外线的能量,将玻璃表面的绝大部分有机污染物完全氧化并分解掉,并且使得玻璃表面具有超亲水性,然后在雨水的冲刷下将玻璃表面的污染物带离玻璃表面,保持玻璃表面清洁如新。
目前大多数自清洁玻璃都是利用镀膜技术,在玻璃表明镀制一层纳米级的TiO2薄膜。常用的技术有:溶胶-凝胶(Sol-gel)法、浸渍提拉法、物理气相沉积法(PVD)和化学气相沉积(CVD)法等[1, 2]。这些方法共同的特点都是将纳米级的TiO2颗粒固定在玻璃基底上形成薄膜。研究表明:当纳米级的TiO2颗粒固定在基底上后,一方面与原TiO2纳米颗粒相比比表面积减小,降低了对降解物的吸附;另一方面,固定后的TiO2纳米颗粒会增加对入射光的散射,单位光强激发出的光生电子和空穴减少,从而使TiO2薄膜光催化降解的能力较TiO2纳米颗粒显著降低[3, 4]。如Bhattacharyya等[5]、Fukahori等[6]的实验研究表明固定后的纳米TiO2涂层较未固定的纳米TiO2颗粒光催化降解能力降低了66%~80%。为了弥补固定后纳米TiO2涂层光催化能力的损失,大多数做法都是增加TiO2催化剂的含量,如增加纳米TiO2涂层的厚度等[7, 8]。但纳米TiO2涂层的透光率会随涂层厚度的增加而降低,影响自清洁玻璃的透光性和光泽度。
2005年,美国宾夕法尼亚大学Grimes研究小组,通过阳极氧化钛膜制备出透明且高度有序的TiO2纳米管涂层,该涂层在380~800nm可见光范围内透光率可达80%以上,且表现出与基底较好的结合力[9],随后,德国埃尔兰根-纽伦堡大学Macak等[10]和中国厦门大学的庄惠芳等[11]发现该涂层具有较高的光催化活性,从而为自清洁玻璃的制备提供了一种新的方法。
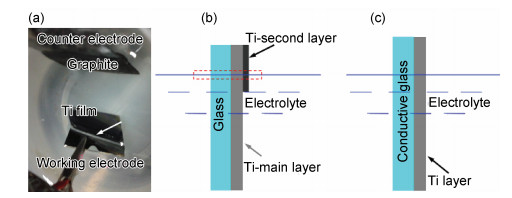
但采用阳极氧化钛膜的方法制备透明TiO2涂层时,存在如图 1所示的问题。在固-液-气接触的三相区(图 1(a)箭头所示),钛膜的氧化与刻蚀速率较快。一旦该三相区全变为TiO2,氧化电流就会变为零,产生断电现象,阳极氧化过程就会终止。从而出现因氧化不完全而形成不了透明的TiO2涂层。为了克服上述不足,获得透明的TiO2涂层。目前,大致的方法分为两类,分别如图 1(b),(c)所示。图 1(b)通过增加三相区钛膜的厚度来延长反应时间,进而克服三相区刻蚀速率过快而导致钛膜浸入电解液部分氧化不完全,不能变透明的问题[9, 12]。图 1(c)是通过在导电玻璃(如ITO, FTO)上沉积一层钛膜,利用基底玻璃的导电性来克服阳极氧化过程中因断电而导致的氧化不完全,不能变透明的问题[13-15]。虽然上述方法成功地实现了透明TiO2涂层的制备,但无论是从钛膜制备上或基底选择上都存在许多不足,如沉积双层钛膜制备工艺复杂,选择导电基底,增加了自清洁玻璃的成本。
|
图 1 阳极氧化钛膜制备透明TiO2涂层示意图 (a)三相区;(b)双层结构示意图(c)导电玻璃示意图 Fig. 1 Schematic diagram of preparing transparent TiO2 coatings by anodization (a)solid-liquid-gas region; (b)double Ti layer; (c)conducting glass substrate |
本工作首先通过磁控溅射法并调整溅射参数,在普通玻璃基底上预先沉积一层特殊结构的钛膜。接着,该特殊结构的钛膜经过电化学阳极氧化和退火后,可直接在普通玻璃基底上形成一层透明的TiO2涂层,该涂层具有纳米多孔结构。最后对该涂层的透光率、光催化活性、亲水性及与基底结合力进行了表征。
1 实验 1.1 样品制备首先,以康宁玻璃(Corning)为基底,采用磁控溅射法制备600~1000nm厚的钛膜,其中工作气体为高纯Ar气(纯度99.9995%),中频电源频率为100kHz、占空比为60%,钛靶功率密度为4.3W/cm2,具体溅射参数如表 1所示。接着,将制备好的钛膜在直流两电极体系的电化学池中进行阳极氧化。其中制备的钛膜为阳极,阴极为石墨,将质量分数为0.75% NH4F和体积分数为3% H2O加入乙二醇中配制成电解液,调整两极电压为40V。阳极氧化完后,所有样品依次分别在丙酮、乙醇、0.05%(质量分数)HF溶液中超声清洗各20s,之后用去离子水冲洗并吹干。最后,将所有吹干的样品放在退火炉中于大气环境和450℃下退火3h并随炉冷却至室温,得到纳米TiO2涂层。
| Sample | Pressure/Pa | Bias/V | Temperature/℃ |
| Ti1# | 0.2 | -20 | 300 |
| Ti2# | 1.0 | Floating | RT |
制备的钛膜和纳米TiO2涂层用D8多晶X射线衍射仪(CuKα射线, λ=0.154178nm)进行晶体结构的分析。用S4800场发射高倍电子扫描电镜(发射枪电压4kV)对钛膜及其阳极氧化后形成的TiO2膜层进行微观形貌观察,并通过观察其断面形貌确定膜层的厚度。膜层的透光率和溶液的吸光度用Lambda 950紫外可见分光光度计在波长200~800nm范围内进行测量。TiO2膜层的结合力利用Revetest划痕测试仪在1~20N范围内进行测试,划痕的长度为3mm。最后,利用OCA 20视频接触角测量仪对涂层的亲水性能进行测试,其中液滴大小为2μL。
光催化实验是在XPA系列光化学反应仪中进行,采用光源为高压汞灯,功率300W,特征波长365nm。整个反应装置置于暗箱环境中,以去除干扰光源对实验的影响。具体操作过程为:将40mL浓度为1×10-5mol/L,pH=4.5的亚甲基蓝溶液(MB)置于石英试管中,试管与紫外灯之间的距离为10cm,且绕紫外灯旋转,转速为10r/min,以保证光照均匀,整个装置通有循环水来控制恒定的温度。将切割好的1.5cm×1.5cm大小的TiO2纳米管涂层玻璃样品置于试管的底部。然后开启磁力搅拌,于暗箱环境搅拌30min,使样品与亚甲基蓝溶液之间达到脱吸附平衡,之后开启紫外灯,并开始计时与取样,在持续照射的2h过程中,每隔30min取样1次,每次取样1mL,用紫外-可见分光光度计测其在λ=664nm处的吸光度值,根据Beer-Lambert定律,溶液的吸光度与溶液的浓度存在正比例关系,所以用公式(1)来定量的评价3种涂层的光催化活性。
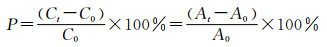
|
(1) |
式中:P为降解率;Ct为相应反应时间的残余浓度;C0为初始浓度;At为相应反应时间溶液的吸光度;A0为初始浓度溶液的吸光度。
2 结果与讨论 2.1 透明TiO2纳米多孔涂层的制备钛膜的结构对后续阳极氧化形成透明的TiO2纳米管或纳米多孔涂层有着重要的影响[16, 17]。Paulose等[18],Zheng等[19],Biswas等[12]用阳极氧化钛膜制备了透明TiO2纳米管涂层,其共同特点是:(1)需要在导电玻璃(如FTO,ITO)上沉积钛膜;(2)沉积钛膜时都需要较高的基底温度(>300℃)和对钛靶施加射频(RF)电源,从而使得钛原子在沉积过程中充分扩散,获得致密的结构。(3)对应的XRD图谱中都显现出钛膜沿(002)方向择优生长[18, 19, 12]。
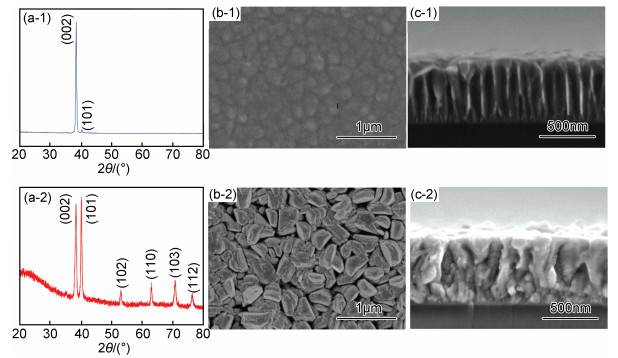
为了对比,本实验设计了如表 1所示的两种沉积参数,两种参数下在普通玻璃基底上沉积得到的钛膜结构与微观形貌如图 2所示。可以看出Ti1#条件下制备出的钛膜与文献[12, 18, 19]报道的一样,300℃下主要沿(002)方向择优生长,见图 2(a-1);对应SEM形貌图(见图 2(b-1),(c-1))可以看出膜层结构致密,晶粒比较均匀,截面呈柱状晶生长形貌,膜层平整;然而Ti2#条件下制备的钛膜表现出较大的结构差异,其不再以(002)方向择优生长,(101)方向成为主要的生长方向,此时钛的(102),(110),(103),(112)衍射峰也变得较为明显,见图 2(a-2);对应的SEM形貌图(见图 2(b-2),(c-2))中可以看出,钛膜结构疏松,表面存在许多孔洞,截面不再呈现均匀的柱状晶形貌,膜层粗糙度增大。
|
图 2 两种沉积参数下制备的钛膜结构与SEM形貌图 (1)Ti1#; (2)Ti2#;(a)XRD谱图;(b)表面;(c)截面 Fig. 2 Crystal structure and SEM morphology of deposited Ti films at different conditions (1)Ti1#; (2)Ti2#; (a)XRD pattern; (b)top view; (c)cross-sectional view |
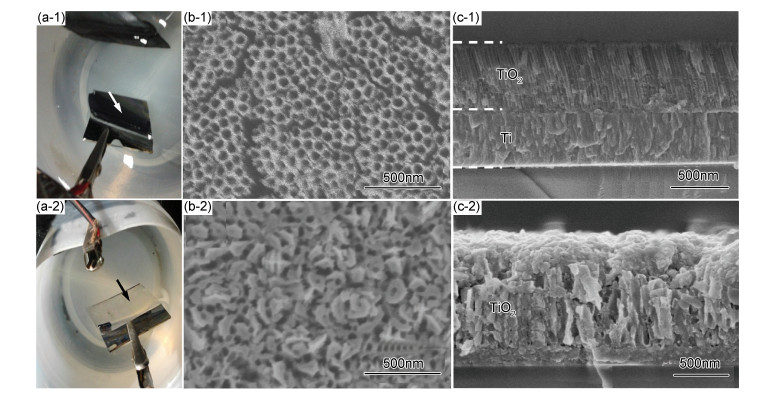
图 3为Ti1#和Ti2#的钛膜分别在乙二醇电解液中,40V电压下阳极氧化45 min后的数码照片和膜层微观SEM形貌图。首先,如图 3(a-1)所示,Ti1#制备的钛膜经过氧化后只是三相区变透明;而Ti2#制备的钛膜在同等氧化条件下,整部分变透明,见图 3(a-2)。其次,氧化后形成的TiO2膜层微观形貌也呈现出截然不同的特征,钛膜Ti1#经过阳极氧化后出现了TiO2纳米管形貌,并出现了分层现象,上层为TiO2纳米管,下层为残余钛膜,膜层总厚度约为1.3μm,见图 3(b-1),3(c-1);而钛膜Ti2#经过阳极氧化后出现了TiO2纳米多孔形貌,未有残余的钛存在,膜层厚度约为1.2μm。进一步对比发现钛膜Ti1#氧化后之所以不透明,是氧化不完全的缘故,可从图 3(c-1)明显可以看出,存在着较厚的残余钛,厚度约为520nm;钛膜Ti1#阳极氧化后不能变透明,但Ti2#单层钛膜同等氧化条件下却能变透明,这说明了钛膜的结构差异是氧化后能否变透明的一个重要原因。从图 2明显看出,制备的钛膜结构最大的不同是Ti1#致密(见图 2(b-1),(c-1)),Ti2#疏松(见图 2(b-2),(c-2))。钛膜的阳极氧化伴随着氧化与选择性溶解相互作用的一个过程[20, 21],结构疏松的钛膜,电解液中的F-或者O2-会沿着孔洞或缝隙进入钛膜内部,因而阳极氧化过程可以在整个膜内顺利进行,从而钛膜阳极氧化后能变透明,但由于膜内孔洞或缝隙排列的无序性,从而氧化后会形成疏松的TiO2多孔结构,见图 3(b-2)和3(c-2)。然而,致密的钛膜结构比较严实,电解液中的F-或者O2-只能从钛膜表面逐渐向钛膜内部进行氧化,但氧化过程中存在三相区反应过快而导致的断电问题,所以氧化不能变透明,这与文献[9, 12]的报道一致,因为致密的钛膜在氧化过程中逐渐有序的进行,所以会形成高度有序的TiO2纳米管,见图 3(b-2),(c-2)。
|
图 3 Ti1#(1)和Ti2#(2)钛膜经过阳极氧化后的数码和SEM图片 (a)数码照片; (b)表面; (c)截面 Fig. 3 Digital and SEM images of as-anodized Ti1# (1) and Ti2# (2) films (a)digital image; (b)top view; (c)cross-sectional view |
Ti2#钛膜阳极氧化后可在普通玻璃基底上直接形成透明的TiO2纳米多孔涂层,所以对该涂层的性能进行表征。
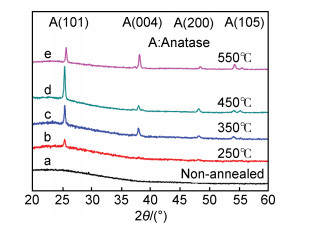
钛膜经阳极氧化后一般为无定型的非晶态(见图 4曲线a),不具有光催化活性。众多学者认为,锐钛矿相的TiO2较金红石相的具有更好的光催化活性[22-24, 10],通过退火工艺可以获得锐钛矿相的TiO2纳米多孔涂层。图 4为Ti2#形成的TiO2纳米多孔涂层在各个温度退火下的XRD图谱。可以看出,250℃左右开始出现锐钛矿相(101)晶面,随着温度的提高,锐钛矿相的含量逐步增加;当温度提高到450℃左右时,锐钛矿相(101)晶面呈现高度择优取向(图 4曲线d);进一步提高温度至550℃(图 4曲线e),此时锐钛矿相(101)晶面衍射强度明显减弱,(004)晶面衍射峰开始变强。由于450℃退火下的TiO2纳米多孔涂层具有较高的锐钛矿相含量,所以选择450℃热处理的样品作为后续的透光率和光催化性能测试。
|
图 4 Ti2#阳极氧化后形成的TiO2纳米多孔涂层在各个温度下退火的XRD图谱 Fig. 4 XRD patterns of TiO2 nanoporous coatings annealed at different temperatures which formed by anodizing Ti2# film |
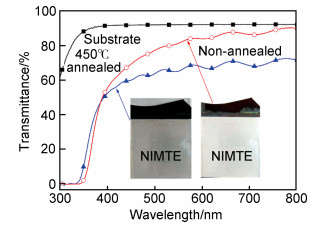
图 5为Ti2#钛膜阳极氧化后及450℃退火后的数码照片与透光率曲线。可以看出Ti2#钛膜阳极氧化后形成的1.2μm TiO2纳米多孔涂层具有较高的透光率,在380~800nm可见光范围内透光率平均值可到达60%,经过450℃退火后透光率进一步提高,提高至80%,退火后透光率提高可能是涂层形成了晶体结构的原因。
|
图 5 TiO2纳米多孔涂层退火前和退火后的透光率 Fig. 5 Transmittance of TiO2 nanoporous coatings before and after annealing |
以亚甲基蓝(MB)为模拟污染物,对制备的TiO2纳米多孔涂层进行光催化性能评价,主要有3方面原因:(1)亚甲基蓝是工业有机污染物中最常见的一种;(2)亚甲基蓝在光催化降解过程中会发生颜色变化,观察起来比较直接;(3)多数报道以亚甲基蓝为待测物进行了光催化活性方面的评价[25, 10, 22]。图 6(a)为存在该TiO2纳米多孔涂层的亚甲基蓝溶液在紫外光的照射下,溶液的吸光度随时间的变化图。可以看出,随光照时间的延长,溶液的吸光度图谱发生了蓝移现象(664~636nm)。这是由于在紫外光的照射下,TiO2受光激发产生光生电子(e-)与空穴(h+),光生电子和空穴会与TiO2表面吸附的O2和H2O等作用,生成HO2·,·OH,·O等强氧化性活性基团,这些活性基团会使MB溶液发生一系列去氨基作用而使有机物MB被分解[26, 27]。图 6(b)显示了MB溶液的颜色随光照时间的变化,可以看出溶液的颜色逐渐变浅。所以该TiO2纳米多孔涂层确实使MB溶液发生了分解。

|
图 6 存在TiO2纳米多孔涂层的亚甲基蓝溶液随紫外光照射时间的变化 (a)吸光度变化;(b)亚甲基蓝溶液颜色变化 Fig. 6 Changes of methylene blue solution existing with the TiO2 nanoporous coating under UV light illumination (a)changes of absorbance; (b)change in color |
为了比较光催化活性,如图 7所示,制备了与TiO2纳米多孔涂层(TNP)厚度相差不多的TiO2纳米管涂层(TNT)以及P25颗粒固定后的纳米颗粒涂层(P25)。其中,图 7(a-1),(b-1)分别为TNT涂层的表面和截面形貌,可以看出制备的TiO2纳米管阵列排布整齐,分布均匀,管径约为50nm,管长约为1.2μm。

|
图 7 TNT(1)和P25(2)涂层形貌 (a)表面形貌;(b)截面形貌 Fig. 7 Morphology of TNT (1) and P25 (2) coatings (a)top view; (b)cross-sectional view |
图 7(a-2),(b-2)分别为热喷涂方法制备的P25涂层的表面与截面形貌,可以看出涂层呈颗粒状,颗粒粒径约为30~80nm之间,涂层厚度约为1.3μm。用公式(1)来定量地评价3种涂层的光催化活性。
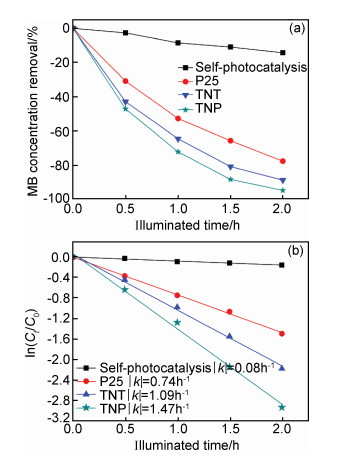
图 8(a)为P25, TNT, TNP 3种类型的涂层光催化降解亚甲基蓝的降解率随时间变化的曲线。可以看出没有TiO2催化剂存在,只有紫外光照射2h的情况下,亚甲基蓝发生了轻微的降解,降解率只有14%。当存在P25, TNT, TNP 3种类型的TiO2催化剂时,同样紫外光照射2h,其降解率分别达到了77%,88%,94%,这说明了TiO2光催化剂的加入显著增加了亚甲基蓝溶液的分解。将P25,TNT,TNP 3种涂层降解亚甲基蓝溶液的残余浓度按照一级反应动力学方程ln(Ct/C0)=kt处理并作图,线性拟合效果如图 8(b)所示,其中k为反应速率常数。可以看出3种类型的涂层对亚甲基蓝溶液的光催化降解反应符合一级动力学方程,其中,P25, TNT, TNP 3种类型的涂层反应速率常数分别为0.74,1.09, 1.47h-1。TNP涂层的反应速率常数最高。
|
图 8 P25,TNT,TNP 3种涂层的光催化活性 (a)降解率曲线;(b)反应速率曲线 Fig. 8 Photocatalytic performance of P25, TNT and TNP coatings (a)curve of degradation rate; (b)curve of reaction rate |
通过上述比较,制备的TNP涂层相比与同等厚度的P25和TNT涂层,表现出较高的光催化活性。这可能与TNP涂层大的活性表面积和特殊的多孔结构有关。如图 3(b-2),(c-2)所示的TNP多孔涂层相比于P25颗粒状涂层(见图 7(a-2),(b-2)),表面积更大,从而使光催化反应位点增多,而表现出较高的光催化活性;相比于规则排列的TNT涂层(见图 7(a-1),(b-1)),TNP无序的多孔结构,增加了对紫外光的吸收,这点可从图 5的透光率曲线看出,对波段300~350nm的紫外光几乎全部吸收,从而可以激发出更多的光生电子和空穴, 进而表现出较高的光催化活性。
2.4 亲水性图 9为制备的TNP涂层的接触角测试,可以看出没有涂层的玻璃基底接触角为29°(图 9(a))。而施加了TNP涂层后,退火前接触角可降低至13°(图 9(b))。经过450℃退火后,水滴可在涂层表面完全铺展开来,接触角小于6°(图 9(c)),满足了自清洁玻璃的要求。

|
图 9 TNP涂层的接触角测试 (a)玻璃基底;(b)退火前;(c) 450℃退火后 Fig. 9 Contact angles of water droplet on the surface of TNP coating (a)glass substrate; (b)non-annealed TNP; (c)TNP annealed at 450℃ |
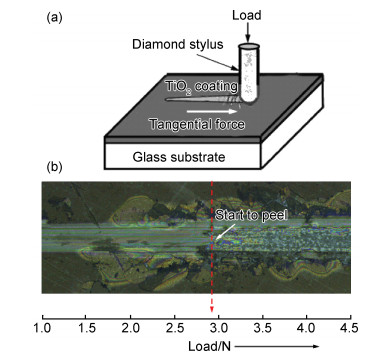
TNP涂层与玻璃基底之间结合力的好坏是衡量自清洁玻璃使用寿命的一个重要指标,结合力差的涂层容易在使用过程中发生脱落。利用示意图如图 10(a)所示的划痕仪对TNP涂层和玻璃基底间的结合力进行测试。金刚石划针以持续增大的加载力和恒定的速度沿TNP涂层内部切向划动,当涂层出现剥落的时候,此时所示的加载力为该涂层与基底之间的结合力。从图 10(b)所示的划痕测试结果中明显可以看出,当加载力为2.9N时,此时的TNP涂层开始出现剥落,说明了TNP涂层与基底间的结合力为2.9N。该结合力与Celik溶胶-凝胶法制备的TiO2涂层相比结合力提高了3000倍[28],可与磁控溅射镀膜技术制备的TiO2薄膜与基底之间结合力相比拟[29]。
|
图 10 TNP涂层与基底间的结合力 (a)划痕测试原理示意图; (b)TNP涂层划痕形貌 Fig. 10 Adhesion between TNP coating and glass substrate (a)diagram of scratch test; (b)digital image of scratch track |
(1) 通过磁控溅射法在玻璃基底上沉积一层结构疏松且以(101)为主要晶面取向的钛膜。该钛膜在质量分数为0.75% NH4F和体积分数为3% H2O的乙二醇电解液中40V电压下阳极氧化后,可直接在玻璃基底上形成一层透明的TiO2纳米多孔涂层。
(2) 厚度为1.2μm的TiO2纳米多孔涂层,经过450℃退火3h后,在可见光范围内的透光率可达到80%以上,表面具有超亲水性(接触角< 6°),对浓度为1×10-5mol/L的亚甲基蓝溶液2h内降解率可达到94%,光催化反应速率常数为1.47h-1,涂层与玻璃基底间的结合力为2.9N。
| [1] | TAVARES C J, VIEIRA J, REBOUTA L, et al. Reactive sputtering deposition of photocatalytic TiO2 thin films on glass substrates[J]. Materials Science and Engineering:B,2007, 138 (2) : 139 –143. DOI: 10.1016/j.mseb.2005.11.043 |
| [2] | 段琼娟, 王彪, 王华平, 等. 自清洁玻璃的研究进展[J]. 化工新型材料,2009, 37 (9) : 11 –12. DUAN Q J, WANG B, WANG H P, et al. Research progress of the self-cleaning glass[J]. New Chemical Materials,2009, 37 (9) : 11 –12. |
| [3] | PAZ Y, LUO Z, RABENBERG L, et al. Photooxidative self-cleaning transparent titanium dioxide films on glass[J]. Journal of Materials Research,2011, 10 (11) : 2842 –2848. |
| [4] | HASHIMOTO K, IRIE H, FUJISHIMA A. TiO2 photocatalysis:a historical overview and future prospects[J]. Japanese Journal of Applied Physics,2005, 44 (12) : 8269 –8285. DOI: 10.1143/JJAP.44.8269 |
| [5] | BHATTACHARYYA A, KAWI S, RAY M B. Photocatalytic degradation of orangeⅡby TiO2 catalysts supported on adsorbents[J]. Catalysis Today,2004, 98 (3) : 431 –439. DOI: 10.1016/j.cattod.2004.08.010 |
| [6] | FUKAHORI S, ICHIURA H, KITAOKA T, et al. Photocatalytic decomposition of bisphenol a in water using composite TiO2-zeolite sheets prepared by a papermaking technique[J]. Environmental Science & Technology,2003, 37 (5) : 1048 –1051. |
| [7] | XIANYU W X, PARK M K, LEE W I. Thickness effect in the photocatalytic activity of TiO2 thin films derived from sol-gel process[J]. Korean Journal of Chemical Engineering,2001, 18 (6) : 903 –907. DOI: 10.1007/BF02705616 |
| [8] | WU C Y, LEE Y L, LO Y S, et al. Thickness-dependent photocatalytic performance of nanocrystalline TiO2 thin films prepared by sol-gel spin coating[J]. Applied Surface Science,2013, 280 : 737 –744. DOI: 10.1016/j.apsusc.2013.05.053 |
| [9] | MOR G K, VARGHESE O K, PAULOSE M, et al. Transparent highly ordered TiO2 nanotube arrays via anodization of titanium thin films[J]. Advanced Functional Materials,2005, 15 (8) : 1291 –1296. DOI: 10.1002/(ISSN)1616-3028 |
| [10] | MACAK J M, ZLAMAL M, KRYSA J, et al. Self-organized TiO2 nanotube layers as highly efficient photocatalysts[J]. Small,2007, 3 (2) : 300 –304. DOI: 10.1002/(ISSN)1613-6829 |
| [11] | ZHUANG H F, LIN C J, LAI Y K, et al. Some critical structure factors of titanium oxide nanotube array in its photocatalytic activity[J]. Environmental Science & Technology,2007, 41 (13) : 4735 –4740. |
| [12] | BISWAS S, SHAHJAHAN M, HOSSAIN M F, et al. Synthesis of thick TiO2 nanotube arrays on transparent substrate by anodization technique[J]. Electrochemistry Communications,2010, 12 (5) : 668 –671. DOI: 10.1016/j.elecom.2010.03.002 |
| [13] | LIM S L, LIU Y, LI J, et al. Transparent titania nanotubes of micrometer length prepared by anodization of titanium thin film deposited on ITO[J]. Applied Surface Science,2011, 257 (15) : 6612 –6617. DOI: 10.1016/j.apsusc.2011.02.087 |
| [14] | JI Y, LIN K C, ZHENG H, et al. Solar-light photoamperometric and photocatalytic properties of quasi-transparent TiO2 nanoporous thin films[J]. ACS Appl Mater Interfaces,2010, 2 (11) : 3075 –3082. DOI: 10.1021/am100579g |
| [15] | BERGER S, GHICOV A, NAH Y C, et al. Transparent TiO2 nanotube electrodes via thin layer anodization:fabrication and use in electrochromic devices[J]. Langmuir,2009, 25 (9) : 4841 –4844. DOI: 10.1021/la9004399 |
| [16] | MOR G K, SHANKAR K, PAULOSE M, et al. Use of highly-ordered TiO2 nanotube arrays in dye-sensitized solar cells[J]. Nano Lett,2006, 6 (2) : 215 –218. DOI: 10.1021/nl052099j |
| [17] | SADEK A Z, ZHENG H, LATHAM K, et al. Anodization of Ti thin film deposited on ITO[J]. Langmuir,2009, 25 (1) : 509 –514. DOI: 10.1021/la802456r |
| [18] | PAULOSE M, SHANKAR K, VARGHESE O K, et al. Application of highly-ordered TiO2 nanotube-arrays in heterojunction dye-sensitized solar cells[J]. Journal of Physics D:Applied Physics,2006, 39 (12) : 2498 –2503. DOI: 10.1088/0022-3727/39/12/005 |
| [19] | ZHENG H, SADEK A Z, BREEDON M, et al. Fast formation of thick and transparent titania nanotubular films from sputtered Ti[J]. Electrochemistry Communications,2009, 11 (6) : 1308 –1311. DOI: 10.1016/j.elecom.2009.05.001 |
| [20] | BERGER S, HAHN R, ROY P, et al. Self-organized TiO2 nanotubes:factors affecting their morphology and properties[J]. Physica Status Solidi (b),2010, 247 (10) : 2424 –2435. DOI: 10.1002/pssb.201046373 |
| [21] | 李朋, 赵昆渝, 郭军, 等. TiO2纳米孔到纳米管结构转变的因素及其机理研究[J]. 材料工程,2014 (1) : 58 –63. LI P, ZHAO K Y, GUO J, et al. Factors and mechanism for transition of TiO2 from nanopores to nanotubes[J]. Journal of Materials Engineering,2014 (1) : 58 –63. |
| [22] | LAI Y, SUN L, CHEN Y, et al. Effects of the structure of TiO2 nanotube array on Ti substrate on its photocatalytic activity[J]. Journal of The Electrochemical Society,2006, 153 (7) : D123 . DOI: 10.1149/1.2203112 |
| [23] | AUGUSTYNSKI J. The role of the surface intermediates in the photoelectrochemical behaviour of anatase and rutile TiO2[J]. Electrochimica Acta,1993, 38 (1) : 43 –46. DOI: 10.1016/0013-4686(93)80008-N |
| [24] | LINSEBIGLER A L, LU G, YATES J T. Photocatalysis on TiO2 surfaces:principles, mechanisms, and selected results[J]. Chemical Reviews,1995, 95 (3) : 735 –758. DOI: 10.1021/cr00035a013 |
| [25] | ARBUJ S S, HAWALDAR R R, MULIK U P, et al. Preparation, characterization and photocatalytic activity of TiO2 towards methylene blue degradation[J]. Materials Science and Engineering:B,2010, 168 (1-3) : 90 –94. DOI: 10.1016/j.mseb.2009.11.010 |
| [26] | ZHANG T, OYAMA T, AOSHIMA A, et al. Photooxidative N-demethylation of methylene blue in aqueous TiO2 dispersions under UV irradiation[J]. Journal of Photochemistry and Photobiology A:Chemistry,2001, 140 (2) : 163 –172. DOI: 10.1016/S1010-6030(01)00398-7 |
| [27] | ZHANG T, OYAMA T K, HORIKOSHI S, et al. Photocatalyzed N-demethylation and degradation of methylene blue in titania dispersions expos-ed to concentrated sunlight[J]. Solar Energy Materials and Solar Cells,2002, 73 (3) : 287 –303. DOI: 10.1016/S0927-0248(01)00215-X |
| [28] | CELIK E, YILDIZ A Y, AZEM N F A, et al. Preparation and characterization of Fe2O3-TiO2 thin films on glass substrate for photocatalytic applications[J]. Materials Science and Engineering:B,2006, 129 : 193 –199. DOI: 10.1016/j.mseb.2006.01.013 |
| [29] | KELLY P J, BEEVERS C F, HENDERSON P S, et al. A comparison of the properties of titanium-based films produced by pulsed and continuous DC magnetron sputtering[J]. Surface and Coatings Technology,2003, 174-175 : 795 –800. DOI: 10.1016/S0257-8972(03)00356-6 |
 2016, Vol. 44
2016, Vol. 44


