文章信息
- 赵海涛, 张强, 刘瑞萍, 丁学勇, 马瑞廷.
- ZHAO Hai-tao, ZHANG Qiang, LIU Rui-ping, DING Xue-yong, MA Rui-ting.
- 单分散纳米锌铁氧体的制备及其磁性能
- Synthesis and Magnetic Properties of Monodisperse ZnFe2O4 Nanoparticles
- 材料工程, 2016, 44(1): 103-107
- Journal of Materials Engineering, 2016, 44(1): 103-107.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2016.01.016
-
文章历史
- 收稿日期: 2015-05-18
- 修订日期: 2015-11-27
2. 东北大学材料与冶金学院, 沈阳 110189
2. School of Materials and Metallurgy, Northeastern University, Shenyang 110189, China
锌铁氧体是一种典型的尖晶石型铁氧体材料,磁性能优异,具有较大的磁导率,是一种良好的电磁波吸收材料,也可以用于磁共振成像造影剂[1, 2]。纳米锌铁氧体由于具有亚铁磁性能,还可以在交变磁场中产热,且具有一定的温稳特性,有望用于肿瘤磁热疗法,在医学领域有广阔的应用前景[3, 4, 5, 6]。锌铁氧体的性能与其粒径密切相关,当颗粒的尺寸达到纳米级时,表现出更加优异的磁性能,如具有超顺磁性等;但纳米锌铁氧体由于其表面能高,容易发生团聚,导致纳米特性消失,严重影响了其应用。如何制备单分散、尺寸均一、形貌可控、性能稳定的纳米锌铁氧体成为近年来研究的热点。
铁氧体的主要制备方法有化学共沉淀法[7]、水热法[8]、溶胶-凝胶法[9]、热分解法[10, 11, 12]等。为了得到单分散的纳米粉体,近年来研究较多的有多元醇法。由于多元醇沸点较高,可以使反应在较高温度下进行,产物的结晶性较好,并且多元醇具有很好的亲水性,包覆在纳米颗粒表面,可以使样品在水等极性溶剂中稳定的分散,为后续应用提供了可能。Salado等[13]用多元醇法合成了单分散的、尺寸可控的磁性纳米Fe3O4,改变合成条件可以得到粒径在3.5~7.1nm的纳米颗粒,并研究了纳米颗粒的尺寸对其磁性能的影响。Chen等[14]用一步多元醇法制备了尺寸可控、单分散的Fe3O4纳米粒子,并通过控制油酸的加入可以得到疏水性和亲水性的纳米粒子。Wu等[15]用微波辅助多元醇法合成了Ni1-xZnxFe2O4/MWCNT的纳米复合材料,并研究了其磁性能,其表现为超顺磁性。闫共芹等[16]用柠檬酸根辅助多元醇法制备了直径和磁性能可控的单分散Fe3O4亚微球,并可以在一定范围内调控Fe3O4亚微球的直径,从而得到粒径均一的超顺磁Fe3O4亚微球。目前用多元醇法制备得到单分散的纳米锌铁氧体的报道相对较少,本工作主要以乙酰丙酮铁和乙酰丙酮锌为前驱体,以三乙二醇为溶剂,采用多元醇法制备单分散的锌铁氧体,并研究纳米颗粒的磁性能和磁热性能。
1 实验材料与方法 1.1 ZnFe2O4的制备按Fe∶Zn摩尔比2∶1称取乙酰丙酮铁(Fe(acac)3)和乙酰丙酮锌(Zn(acac)2),加入到 50mL三乙二醇(TEG)中,加入一定量的柠檬酸三钠,搅拌使其充分溶解,通氩气保护后在80℃保温10min,缓慢升温至190℃保温10min,快速升温到多元醇的沸点,沸腾回流 1h,停止加热,冷却至室温。加入30~50mL的无水乙醇,得到黑色粒子沉淀液,磁分离后用无水乙醇反复洗涤,最后把洗涤后的黑色沉淀物置于60℃真空干燥箱中干燥24h,得到ZnFe2O4纳米粒子。
1.2 试样的表征物相分析用PW-3040型衍射仪,扫描范围2θ为20°~70°。用WCT-2型微机差热天平分析原料的热分解行为。用Philips EM 420型透射电镜观察粉体的形貌。利用Nanomeasure软件从透射电镜照片上随机选取100个颗粒得到产物的粒径分布图。用WQF-410傅里叶红外光谱仪对粉体的表面修饰情况进行表征。采用VSM-2000型振动样品磁强计分析产物的磁性能。采用感应加热设备的交变磁场发生器测定样品的磁热效应,其工作频率为382kHz。将50mg和100mg 的样品分别置于盛有1mL蒸馏水的密封装置内,然后放在交变磁场的线圈中用温度计测量不同时间内的水温。
2 结果与讨论 2.1 前驱体的热重分析图 1为前驱体乙酰丙酮锌和乙酰丙酮铁在25~500℃,N2 气氛中进行热重分析得到的TG-DSC曲线。从图 1(a)中可以看出,乙酰丙酮锌的失重过程主要分为三个阶段。第Ⅰ阶段为82~135℃,曲线缓慢下降,出现质量损失,约为8.4%,同时相应的DSC曲线上在100~150℃出现了波动的吸热峰,这可能归因于乙酰丙酮锌中自由水和结晶水的损失吸热,以及部分样品熔化吸热。第Ⅱ阶段为135~330℃,该阶段有较大幅度的质量损失,这是由乙酰丙酮锌分解所致。在DSC曲线上,213℃处的吸热峰,即为乙酰丙酮锌分解过程的吸热峰。第Ⅲ阶段为330℃以上,随着温度继续升高,曲线趋于平稳,说明生成了稳定的新相ZnO[17]。
 |
图 1 乙酰丙酮锌(a)和乙酰丙酮铁(b)的TG-DSC曲线 Fig.1 TG-DSC curves of zinc acetylacetonate(a) and iron acetylacetonate(b) |
图 1(b)为乙酰丙酮铁的TG-DSC曲线。从图中可以看出样品的失重过程可以分为三个阶段。第Ⅰ阶段为183~220℃,开始缓慢失重,质量损失约为7.3%。第Ⅱ阶段为220~450℃,曲线急剧下降,样品明显失重,这主要是因为乙酰丙酮铁分解。在DSC曲线上200℃左右出现相应的吸热峰,即为乙酰丙酮铁分解的吸热峰。第Ⅲ阶段为450℃以上,随着温度继续升高,曲线趋于平稳,说明生成了稳定的新相Fe2O3。
由热重分析结果可知,反应过程中前驱体乙酰丙酮锌和乙酰丙酮铁逐渐分解形成ZnO和Fe2O3,随后ZnO和Fe2O3反应生成ZnFe2O[18]4。
2.2 物相与形貌分析图 2为制备的ZnFe2O4纳米粒子的XRD图谱。由图 2可见,制备的产物的衍射峰与ZnFe2O4标准图谱(JCPDS-74-2397)一致,表明所制备的纳米粒子是立方系尖晶石结构。衍射峰尖锐,且无杂质峰,说明所得样品的结晶性良好,纯度较高。衍射峰有明显的宽化现象,表明样品的尺寸达到了纳米尺度,宽化现象主要是由于纳米粒子的小尺寸效应、无序的晶间结构以及晶体缺陷使点阵间距连续变化所引起的。根据图 2中 最强衍射峰(311)晶面的半高宽,利用谢乐公式计算样品的尺寸:

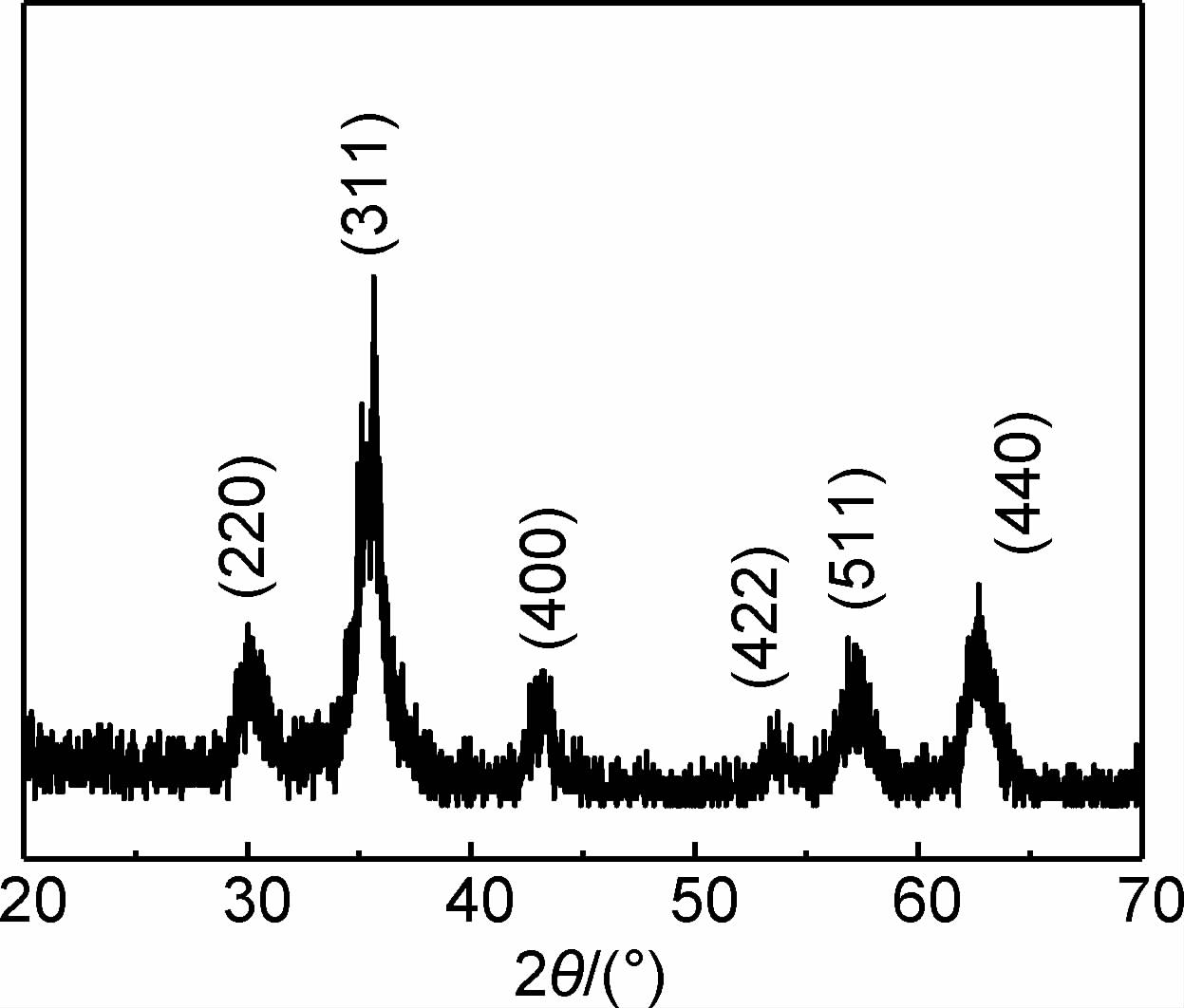 |
图 2 ZnFe2O4纳米粒子的XRD图 Fig.2 XRD pattern of ZnFe2O4 nanoparticles |
式中:D为晶粒尺寸,nm;λ为X射线的波长,取0.154178nm;β为衍射峰半高宽,rad;θ为布拉格衍射角,(°)。计算结果表明,样品的晶粒尺寸为5.6nm。
图 3为制备的ZnFe2O4纳米粒子的透射电镜照片,选区电子衍射照片和粒径分布图。由图 3(a)可见,制备的ZnFe2O4纳米粒子粒径较小,分散性较好,尺寸均一,形状近似球形。相应的选区电子衍射(SAED)照片见图 3(b),衍射图像为同心衍射环,由里到外可以观察到五个衍射环,分别对应ZnFe2O4纳米粒子的(220),(311),(400),(511)和(440)晶面。由粒径分布图可知(图 3(c)),纳米粒子尺寸分布很窄,产物的平均粒径为6nm,此结果与谢乐公式计算的结果一致。
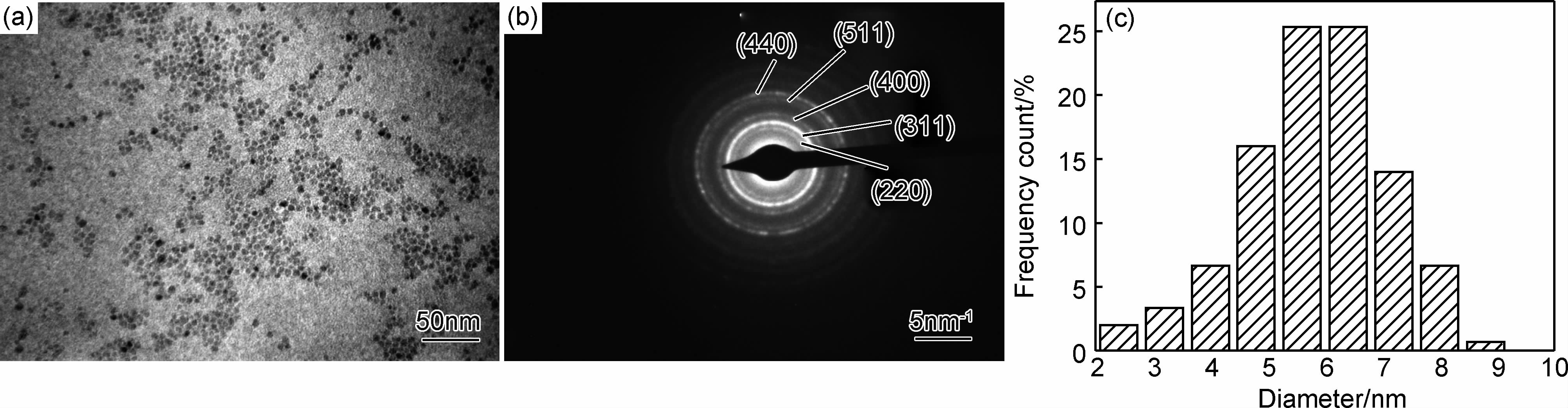 |
图 3 ZnFe2O4纳米颗粒的透射电镜照片(a),选区电子衍射照片(b)和粒径分布图(c) Fig.3 TEM image (a) and SEAD pattern (b) of ZnFe2O4 nanoparticles and corresponding particle core size histogram(c) |
图 4为ZnFe2O4纳米颗粒的傅里叶红外光谱图。图中3454cm-1处的吸收峰为—OH的特征吸收峰[19],2912cm-1处的吸收峰为C—H键的不对称伸缩振动特征峰,1579cm-1和1401cm-1处的吸收峰为羧酸盐—COOM(M为金属离子) 耦合反对称和对称伸缩振动吸收峰[4],1073cm-1处为C—O—C键的伸缩振动特征峰。此外,在576cm-1处存在M—O(M为金属离子)的特征峰,该峰为铁氧体的特征峰[14]。以上特征峰的存在说明:(1)表面活性剂柠檬酸三钠成功吸附在ZnFe2O4纳米颗粒的表面,并以共价键的形式和金属离子结合;(2)多元醇不仅作为溶剂,也可以作为稳定剂包覆在纳米颗粒表面,有效地阻碍颗粒的团聚。
2.4 样品的磁性能 |
图 4 ZnFe2O4纳米颗粒的傅里叶红外光谱图 Fig.4 FT-IR spectrum of ZnFe2O4 nanoparticles |
图 5为ZnFe2O4 纳米颗粒在室温(300K)下的磁滞回线。可以看出ZnFe2O4 纳米颗粒的饱和磁化强度为18.10A·m2/kg,此数据比Wu等[15]用微波辅助多元醇法制备的锌铁氧体的饱和磁化强度大。纳米颗粒的剩磁较小,矫顽力为9355A/m,在室温下表现出亚铁磁性。铁氧体的饱和磁化强度与金属离子在间隙中的占位密切相关,ZnFe2O4是典型的正尖晶石结构的铁氧体,非磁性离子Zn2+全部占据四面体间隙(A位),磁性离子Fe3+全部占据八面体间隙(B位),这样导致A-B之间超交换作用减弱,B-B之间交换作用占主导地位,而B位的磁矩反向平行,相互抵消,净磁矩为零,因此,锌铁氧体通常表现为反铁磁性。但当颗粒尺寸达到纳米尺度时,部分Zn2+可以进入B位,部分Fe3+也可进入A位,导致A-B之间超交换作用的离子对数增多,耦合作用增强,A-B之间超交换作用增强,具有部分反尖晶石结构,表现出一定的亚铁磁性[20]。从图 5还可以看出曲线没有达到明显的饱和,这可能与纳米粒子高度无序的表面自旋结构有关。图 6(a)为ZnFe2O4纳米粒子的水溶液,可以看出产物可以在水中稳定分散,这是因为多元醇不仅作为溶剂还可以作为稳定剂包覆在纳米颗粒的表面从而使产物可以在水等极性溶剂中稳定分散。当存在外加磁场的条件下,ZnFe2O4纳米粒子被吸引到磁铁一侧(图 6(b)),展现出很强的磁响应特性,当磁场撤离时,ZnFe2O4纳米粒子又重新分散于水中(图 6(c))。
 |
图 5 ZnFe2O4纳米颗粒磁滞回线 Fig.5 Magnetic hysteresis loop for ZnFe2O4 nanoparticles |
 |
图 6 ZnFe2O4纳米粒子的水溶液(a)、 外加磁场的 响应图片(b)和撤离磁场后振荡图片(c) Fig.6 Oscillating pictures of aqueous solution of ZnFe2O4 nanoparticles (a), its response under external magnetic field (b) and withdraw from external magnetic field(c) |
图 7为不同浓度样品在382kHz交变磁场下的时间-温度关系曲线。由图 7可以看出,样品在初始时间段内温度变化明显,随着时间的延长,由于材料产热和环境散热逐渐趋于平衡,温度变化不大。随着样品浓度升高,其升温的速率和幅度增加,升温量和最终温度也越高,600s时二者最终的温度分别可达22℃和30℃。
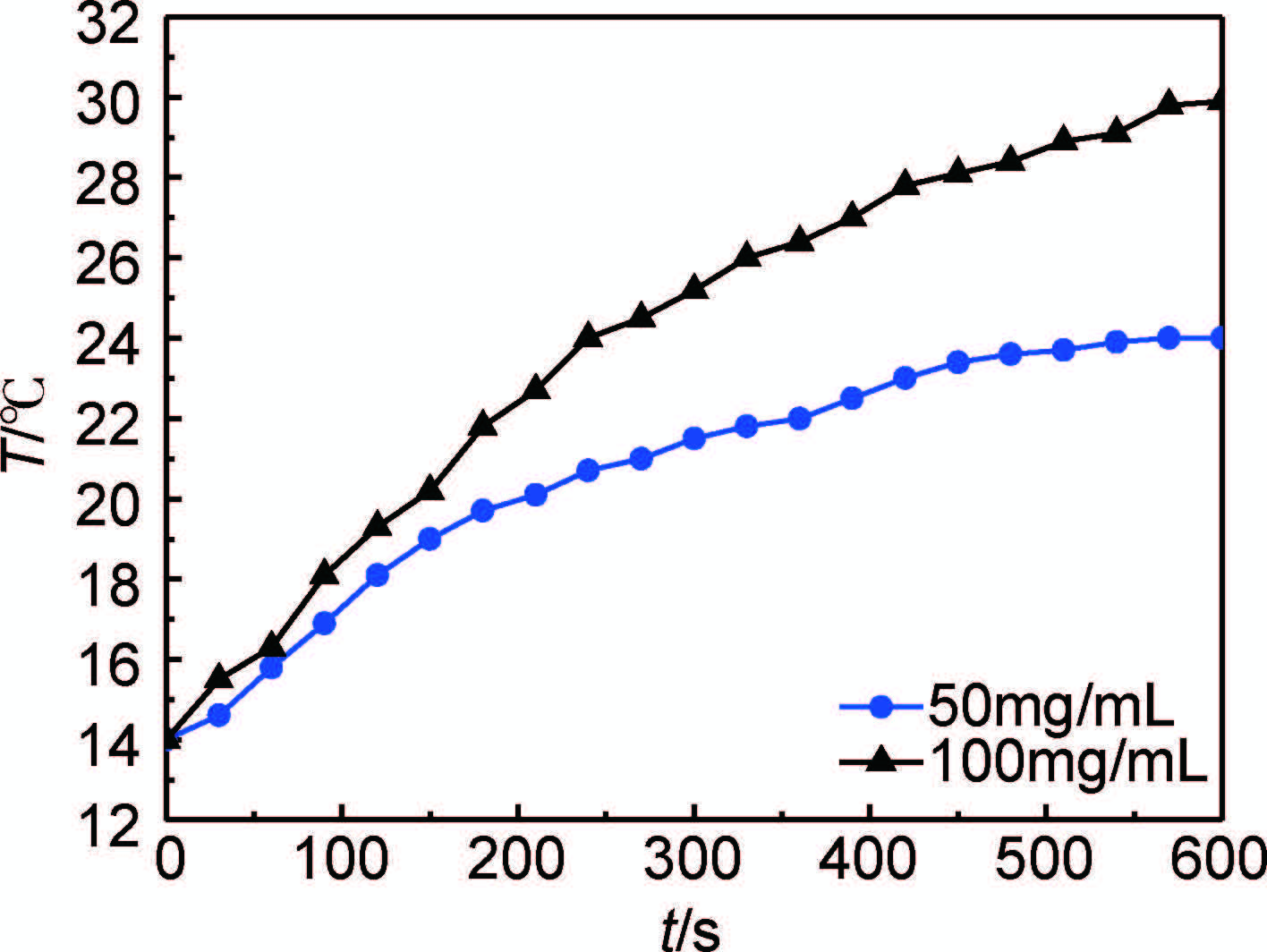 |
图 7 样品在交变磁场下的时间-温度关系 Fig.7 Time-temperature curves of samples under AC field |
铁氧体在交变磁场中发热主要是将电磁能损耗转化为了热能,而电磁能的损耗包括涡流损耗、磁滞损耗和剩余损耗[21]。涡流损耗是指铁磁体内的涡流使磁芯产生热量,使电磁能转化成热能损耗掉。剩余损耗指在铁磁性材料的总损耗中除涡流损耗和磁滞损耗以外剩余的所有其他损耗。在交变磁场中磁滞损耗为磁性材料由于磁滞现象而损耗的功率,磁滞损耗是在不可逆的畴壁位移和磁化矢量移动过程产生的不可逆转的磁化程。单位体积样品磁化一周的磁滞损耗可以粗略地表示为[22]:
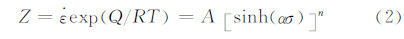
式中:Phys为磁性材料在外磁场中的磁滞损耗功率,W;phys为常数;f 为外磁场频率,Hz;Ms 为饱和磁化强度,A·m2/kg;Hc 为矫顽力,A/m。由此可见,磁滞损耗的大小与外磁场频率、材料的饱和磁化强度和矫顽力成正比。
3 结论(1)采用多元醇法制备出了单分散、近似球形、平均粒径为5.6nm的ZnFe2O4纳米颗粒。
(2)制备的ZnFe2O4纳米颗粒在室温下饱和磁化强度为18.10A·m2/kg,剩磁较小,矫顽力为9355A/m,表现出亚铁磁性。产物可以在水溶液中稳定分散,在外加磁场中表现出很强的磁响应特性。
(3)将50,100mg 的产物分别置于盛有lmL 蒸馏水的密封装置内,测量样品在交变磁场下的磁热性能,发现样品浓度升高,升温速率和幅度增加,600s时二者最终的温度分别可达22℃和30℃,表现出一定的磁热性能。
| [1] | 张晏清,张雄.纳米锌铁氧体的制备与微波吸收性能研究[J].材料科学与工程学报, 2006, 24(4):504-507. ZHANG Yan-qing, ZHANG Xiong. Preparation and microwave absorptivity of zinc ferrite nanopowder[J]. Journal of Materials Science & Engineering,2006, 24(4):504-507. |
| [2] | 陈瑾.高温多元醇法制备超顺磁CoFe2O4纳米颗粒磁共振造影剂[J].无机材料学报, 2009, 24(5):967-972. CHEN Jin. High temperature polyol synthesis of superparamagnetic CoFe2O4 nanoparticles for magnetic resonance imaging contrast agents[J]. Journal of Inorganic Materials,2009, 24(5):967-972. |
| [3] | SADAT M E, RONAK P, BUD'KO S L, et al. Dipole-interaction mediated hyperthermia heating mechanism of nanostructured Fe3O4 composites[J]. Materials Letters, 2014,129:57-60. |
| [4] | BAI L Z, ZHAO D L, XU Y, et al. Inductive heating property of graphene oxide-Fe3O4 nanoparticles hybrid in an AC magnetic field for localized hyperthermia[J]. Materials Letters, 2012,68:399-401. |
| [5] | KUMAR C S S R, MOHAMMAD F. Magnetic nanomaterials for hyperthermia-based therapy and controlled drug delivery[J]. Advanced Drug Delivery Reviews, 2011, 63(9):789-808. |
| [6] | ARA U ' JO-NETO R P, SILVA-FREITAS E L, CARVALHO J F, et al. Monodisperse sodium oleate coated magnetite high susceptibility nanoparticles for hyperthermia applications[J]. Journal of Magnetism and Magnetic Materials, 2014,364:72-79. |
| [7] | RUIZMORENO R G, MARTÍNEZ A I, FALCONY C, et al. One pot synthesis of water compatible and monodisperse magnetite nanoparticles[J]. Materials Letters, 2013,92:181-183. |
| [8] | YAN J, MO S B, NIE J R, et al. Hydrothermal synthesis of monodisperse Fe3O4 nanoparticles based on modulation of tartaric acid[J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2009, 340(1-3):109-114. |
| [9] | 焦清介,任慧,付小芬,等.溶胶-凝胶法制备纳米ZnFe2O4复合材料及宽频吸波性能研究[J].稀有金属材料与工程, 2009, 38(增刊2):963-966. JIAO Qing-jie, REN Hui, FU Xiao-fen, et al. Preparation of ZnFe2O4 by sol-gel and its broad-band absorbent properties[J]. Rare Metal Materials and Engineering, 2009, 38(Suppl 2):963-966. |
| [10] | ZHANG G Q, WU H P, GE M Y, et al. Ultrasonic-assisted preparation of monodisperse iron oxide nanoparticles[J]. Materials Letters, 2007, 61(11-12):2204-2207. |
| [11] | LI D, JIANG D L, CHEN M, et al. An easy fabrication of monodisperse oleic acid-coated Fe3O4 nanoparticles[J]. Materials Letters, 2010, 64(22):2462-2464. |
| [12] | SONG M J, ZHANG Y, HU S L, et al. Influence of morphology and surface exchange reaction on magnetic properties of monodisperse magnetite nanoparticles[J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2012,408:114-121. |
| [13] | SALADO J, INSAUSTI M, GIL DE MURO I, et al. Synthesis and magnetic properties of monodisperse Fe3O4 nanoparticles with controlled sizes[J]. Journal of Non-Crystalline Solids,2008,354:5207-5209. |
| [14] | CHEN F H, ZHAO T N, CHEN Q T, et al. Size-controlled monodisperse hydrophobic and hydrophilic magnetite nanoparticles:one-pot synthesis, characterization, and the mechanism study[J]. Materials Research Bulletin, 2013, 48(10):4093-4099. |
| [15] | WU H Q, ZHANG N,MAO L, et al. Controlled synthesis and magnetic properties of monodisperse Ni1-xZnxFe2O4/MWCNT nanocomposites via microwave-assisted polyol process[J]. Journal of Alloys and Compounds, 2013, 554:132-137. |
| [16] | 闫共芹,王维,孙志刚,等.柠檬酸根辅助多元醇法制备直径和磁性可控的Fe3O4亚微球[J].物理化学学报, 2010, 26(11):3120-3126. YAN Gong-qin, WANG Wei, SUN Zhi-gang, et al. Magnetite sub-microspheres with controlled diameter and magnetic properties synthesized by the citrate-assisted polyol process[J]. Acta Physico-Chimica Sinica, 2010, 26(11):3120-3126. |
| [17] | ARⅡ T, KISHI A. The effect of humidity on thermal decomposition of zinc acetylacetonate monohydrate[J]. Journal of Thermal Analysis and Calorimetry, 2006, 83:253-260. |
| [18] | 徐波,朱城荣,曹伟.共沉淀法合成ZnFe2O4纳米颗粒及其电磁性能研究[J].功能材料, 2015, 46(1):01121-01124. XU Bo, ZHU Cheng-rong, CAO Wei. Study on synthesis and electromagnetic properties of ZnFe2O4 nanoparticles prepared by co-precipitation method[J]. Journal of Functional Materials, 2015, 46(1):01121-01124. |
| [19] | 肖旺钏,魏彦,张雪清,等.改进多元醇法合成超小超顺磁性Fe3O4纳米颗粒[J].人工晶体学报, 2014,43(6):1549-1554. XIAO Wang-chuan, WEI Yan, ZHANG Xue-qing, et al. Synthesis of ultra small superparamagnetism Fe3O4 nanoparticles by modified polyol process[J]. Journal of Synthetic Crystals, 2014,43(6):1549-1554. |
| [20] | SURINWONG S, RUJIWATRA A. Ultrasonic cavitation assisted solvothermal synthesis of superparamagnetic zinc ferrite nanoparticles[J]. Particuology, 2013, 11(5):588-593. |
| [21] | 章林,王德平,姚爱华,等. Zn2+对MnZn铁氧体结构、磁性能和磁热效应的影响[J].功能材料, 2007, 38(7):1086-1088. ZHANG Lin, WANG De-ping, YAO Ai-hua, et al. Effect of Zn2+ on structure, magnetic properties and thermomagnetic effect of MnZn ferrites[J]. Journal of Functional Materials, 2007, 38(7):1086-1088. |
| [22] | 张小川,王德平,姚爱华,等. Mn0.2Zn0.8Fe2O4/MgAl-LDHs复合材料的磁性能和磁热效应[J].无机材料学报, 2008, 23(4):677-682. ZHANG Xiao-chuan, WANG De-ping, YAO Ai-hua, et al. Magnetic properties and thermomagnetic effect in Mn0.2Zn0.8-Fe2O4/MgAl-LDHs composite[J]. Journal of Inorganic Materials, 2008, 23(4):677-682. |
 2016, Vol. 44
2016, Vol. 44


