文章信息
- 王先飞, 潘冶, 吴继礼, 李星洲.
- WANG Xian-fei, PAN Ye, WU Ji-li, LI Xing-zhou.
- Cu-Ti合金与H2O2直接氧化法制备Cu掺杂TiO2薄膜
- Preparation of Cu Doped TiO2 Films Through Direct Oxidation of Cu-Ti Alloys with Hydrogen Peroxide Solution
- 材料工程, 2016, 44(1): 26-32
- Journal of Materials Engineering, 2016, 44(1): 26-32.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2016.01.004
-
文章历史
- 收稿日期: 2014-08-11
- 修订日期: 2015-07-30
因具有低成本、无毒以及化学稳定的优点,锐钛矿型晶态TiO2薄膜已成为异相光催化法所需的理想的半导体光催化剂[1, 2]。TiO2在紫外光照射下,产生空穴(h+)和电子(e-)对,空穴迁移至半导体表面,参与光化学反应生成羟基自由基(OH·),OH·可将有机污染物氧化成CO2,H2O和其他小分子化合物,从而实现降解[3, 4]。目前,晶态TiO2薄膜的制备方法主要有溶胶-凝胶法、水热合成法、阴极电沉积法和金属钛与H2O2的直接氧化法等[5, 6, 7, 8]。吴进明等[8, 9, 10]开发的金属钛与H2O2直接氧化法具有操作流程简单、对TiO2薄膜不引入外部杂质离子以及所需制备温度较低等优点,利于TiO2薄膜的大规模制备。他们利用该方法已成功制备具有多孔[8]、纳米棒[9]和纳米花[10]结构的TiO2薄膜。
除了探索低成本大规模TiO2薄膜制备方法,提高TiO2薄膜的光催化效率也是研究重点之一。在TiO2薄膜中掺杂过渡金属离子使其作为电子捕获中心,能够阻止空穴(h+)和电子(e-)的再结合,从而提高两者分离效率以提高TiO2薄膜的光催化效率[11]。大量研究表明Cu的掺杂可使TiO2薄膜光催化效率得到较大提高[12, 13]。本工作制备了非晶Cu-Ti二元合金,采用H2O2直接氧化法制备Cu掺杂的TiO2薄膜,对薄膜形貌、成分及生长过程进行分析,并采用该薄膜对罗丹明B进行光催化降解研究。
1 实验材料与方法Cu-Ti二元合金采用单辊熔体旋淬法进行制备。首先采用电弧熔炼炉在高纯氩气气氛(-0.05MPa)中将配好的高纯Cu(99.99%,质量分数,下同)和Ti(99.99%)进行熔炼(反复5次),得到成分均匀的母合金锭。然后利用熔体快淬甩带炉对母合金锭进行再次熔炼,并利用熔体上部与腔体的压力差将熔体喷射到快速旋转的铜辊表面,得到连续的Cu-Ti合金条带,条带宽约为2mm,厚约为20~30μm。本工作制备了Cu50Ti50和Cu30Ti70两种二元合金。
采用H2O2直接氧化法制备所需薄膜,将Cu-Ti二元合金置于密封玻璃容器内的氧化性溶液中,氧化性溶液由H2O2,H2SO4以及聚碳酸酯或聚乙烯乙酸酯混合而成,溶液中H2O2的质量分数为30%,H2SO4的浓度为10mmol/L,聚碳酸酯或聚乙烯乙酸酯的加入可影响TiO2的形成[3],加入量为300~6000mg/L,Cu-Ti合金的总面积与氧化性溶液的体积比例保持在200cm2/L。然后将密封玻璃容器放入80℃的水浴中保温不同时间,形成薄膜,再将薄膜取出,使用乙醇及去离子水清洗后吹干,部分薄膜置于空气中450℃保温1h。利用扫描电子显微镜(SEM)、能谱仪(EDS)和X射线衍射仪(XRD)对薄膜的形貌、化学成分和相结构进行分析。
光催化降解实验在10mL的小型烧杯中进行,将总面积为25cm2的薄膜置于5mL的20mg/L的罗丹明B溶液中,首先在黑暗条件下放置4h使薄膜与罗丹明B达到吸附平衡,然后在12W的紫外光下照射4h,紫外光源置于溶液上方5cm处。溶液中罗丹明B浓度的变化由紫外-可见光谱(UV-Vis)在554nm处的强度变化进行分析。
2 结果与分析 2.1 Cu掺杂TiO2薄膜的生成图 1所示为Cu-Ti二元合金在不同条件下处理后样品表面的SEM形貌。保温处理时,溶液基本组成为H2O2和H2SO4,温度80℃,保温时间10h;热处理气氛为空气,温度450℃,时间1h。
 | 图1 Cu-Ti合金在不同条件下处理后样品表面SEM形貌 (a)Cu50Ti50,热处理;(b)Cu50Ti50,溶液保温,热处理; (c)Cu50Ti50,添加聚碳酸酯溶液保温;(d)Cu50Ti50,添加聚碳酸酯溶液保温,热处理;(e)Cu50Ti50, 添加聚乙烯乙酸酯溶液保温,热处理;(f)Cu30Ti70,添加聚碳酸酯溶液保温,热处理 Fig.1 SEM morphologies of Cu-Ti alloys surface handled under different conditions (a)Cu50Ti50,heat treatment;(b)Cu50Ti50, reaction in solution and heat treatment;(c)Cu50Ti50,reaction in solution containing polycarbonate;(d)Cu50Ti50,reaction in solution containing polycarbonate and heat treatment;(e)Cu50Ti50,reaction in solution containing polyvinyl acetate and heat treatment;(f)Cu30Ti70,reaction in solution containing polycarbonate and heat treatment | |
由图 1可知,Cu50Ti50合金在热处理后,表面平坦(图 1(a));当Cu50Ti50合金在H2O2和H2SO4的混合溶液中保温且热处理后,表面形貌没有明显变化,依然平坦,只有少量白色沉积物(图 1(b))。但是,当该合金在含有H2O2,H2SO4和聚碳酸酯(6000mg/L)的混合溶液中保温后,样品表面生成了尺寸约为10μm的块状沉积物,其均匀分布并相互连接成完整的薄膜结构(图 1(c));对其进行热处理,发现表面形貌变化不大(图 1(d)),表明沉积物与合金基体结合牢固。当将聚碳酸酯更换为聚乙烯乙酸酯时,能够形成类似的表面沉积物且形貌相同(图 1(e))。此外,将Cu30Ti70合金在含有H2O2,H2SO4和聚碳酸酯的混合溶液中保温并热处理后,同样可以形成具有上述形貌的表面薄膜,但沉积物的尺寸稍小,约为6~8μm(图 1(f))。
对图 1中所示样品表面进行EDS和XRD分析,其结果分别示于图 2和图 3。
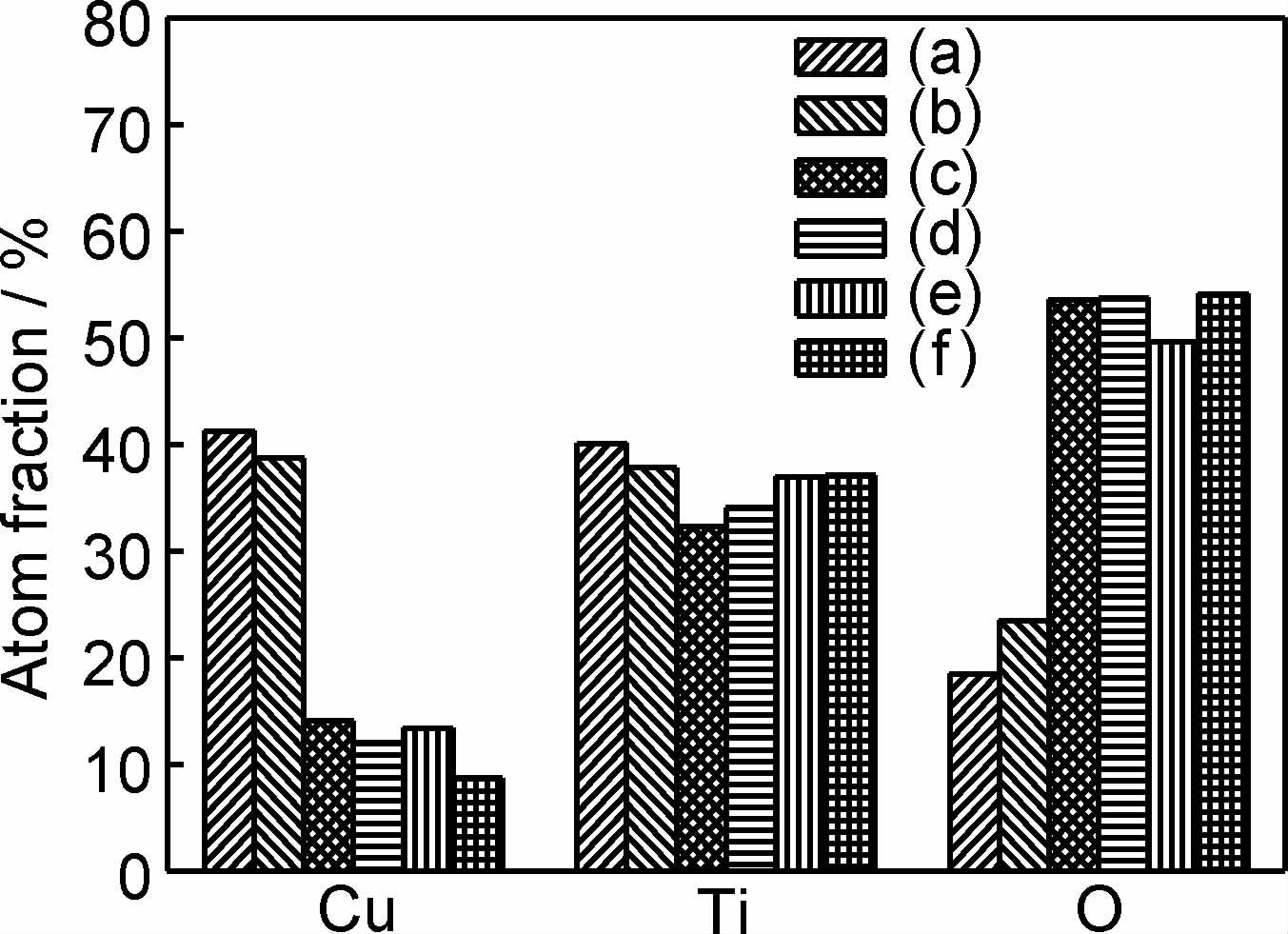 | 图2 图1中所示合金表面的EDS成分分析 Fig.2 EDS composition analysis of alloys surface shown in fig.1 | |
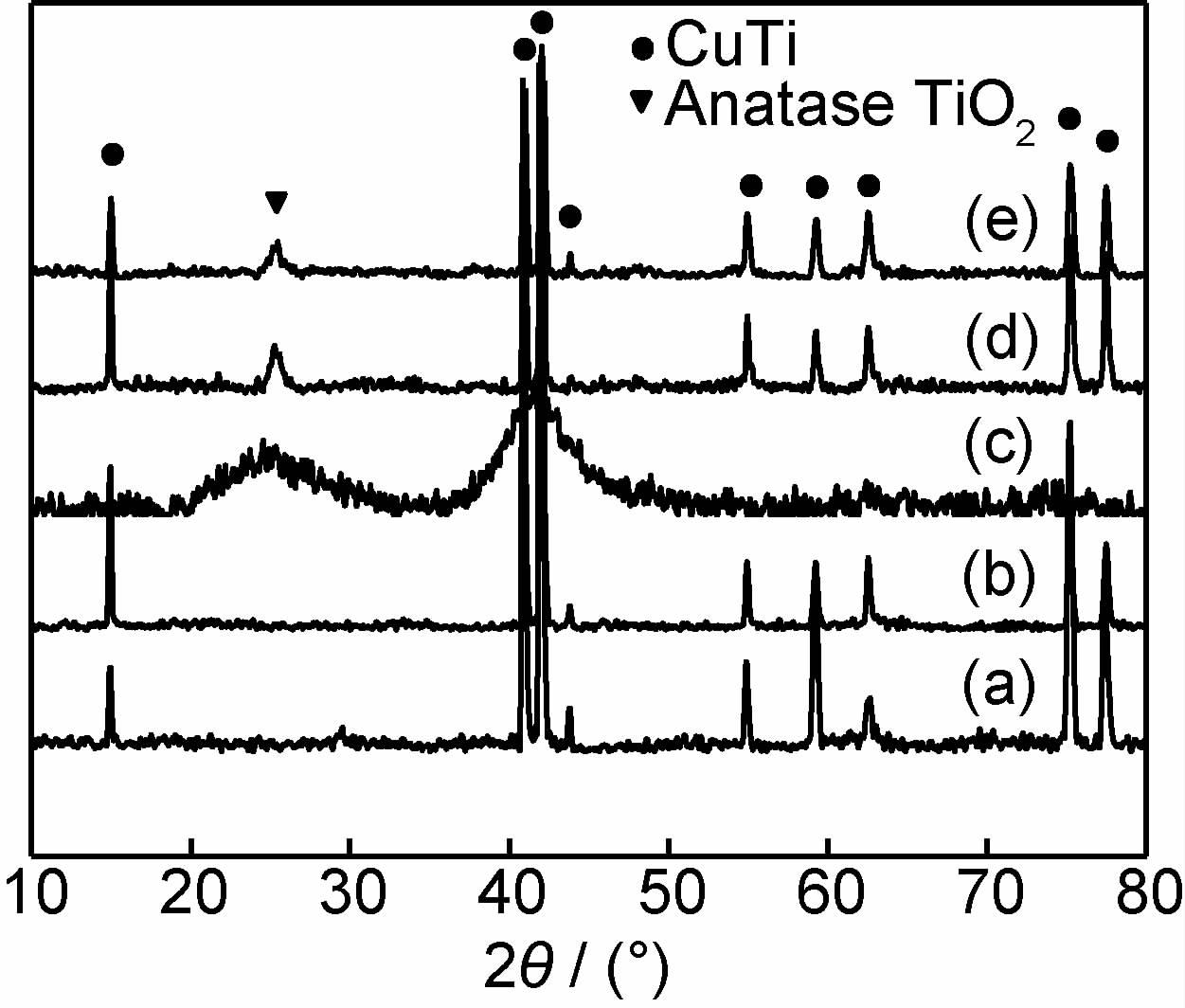 | 图3 图1(a)~(e)所示合金的XRD谱图 Fig.3 XRD patterns of the alloys shown in fig.1(a)-(e) | |
由图 2可知,6个样品表面的Ti元素含量相差不大,均在35%(原子分数,下同)左右。Cu50Ti50原始样及在H2O2和H2SO4溶液中保温后样品进行热处理之后(表面平坦),表面Cu元素含量约为40%,O元素含量约为20%,而当样品表面有块状沉积物形成时(图 1(c)~(e)),样品表面的Cu元素含量下降为约12%;O元素含量上升为约50%。此外,Cu30Ti70合金在表面形成块状沉积物后,样品表面的Cu元素含量下降为7%左右。
由图 3则可知,Cu50Ti50原始样及在H2O2和H2SO4溶液中保温后样品进行热处理之后,XRD谱图表明其只含有基体的CuTi析出相(图 3(a),(b))。当该合金在含H2O2,H2SO4和聚碳酸酯溶液中保温并在样品表面形成块状沉积物时,XRD谱图含有两个宽峰(图 3(c)),在2θ为42°处对应的宽峰表明原始二元Cu-Ti合金为非晶合金,而在2θ为25°处对应的宽峰表明样品表面沉积了非晶态的TiO2;当对该样品进行热处理后,非晶态TiO2发生结晶形成锐钛矿型的TiO2(图 3(d))。此外,Cu50Ti50合金在含聚乙烯乙酸酯(图 3(e))以及Cu30Ti70合金在含聚碳酸酯(XRD谱图未示出)溶液中保温并热处理后,同样形成了锐钛矿型的TiO2;因此,结合图 2与图 3的结果可知,通过上述H2O2直接氧化方法,生成了Cu掺杂的TiO2薄膜。
2.2 添加酯对TiO2薄膜形成的影响由图 1可见,只有当二元合金在含有一定量的聚碳酸酯或聚乙烯乙酸酯溶液中保温后才会形成TiO2薄膜。图 4所示为Cu50Ti50合金在含H2O2,H2SO4及不同含量的聚乙烯乙酸酯溶液中80℃保温10h后的表面SEM形貌。由图 4可知,当溶液中未加入聚乙烯乙酸酯时,样品表面没有形成TiO2薄膜(图 4(a));而当溶液中加入300,2000mg/L的聚乙烯乙酸酯时,样品表面有少量TiO2薄膜形成(图 4(b),(c)),但形成的薄膜不连续,且厚度不均匀,有较多突起沉积物(图 4(e));只有当溶液中聚乙烯乙酸酯的含量提高到6000mg/L时,样品表面才能够形成连续分布且厚度均匀的TiO2薄膜(图 4(d),(f))。由于所加聚乙烯乙酸酯具有高的热与化学稳定性,能够通过氢键吸附于合金表面氧化物,其低的界面张力和高的离子强度有利于TiO2的结晶形核[14, 15],从而促进TiO2在合金表面的沉积(下文中证实其为溶解-沉积机理)并聚集形成连续薄膜。
 | 图4 Cu50Ti50合金在含H2O2,H2SO4及不同含量的聚乙烯乙酸酯溶液中80℃保温10h后的表面SEM形貌 (a)0mg/L;(b)300mg/L;(c)2000mg/L;(d)6000mg/L;(e)图(c)中薄膜的放大像;(f)图(d)中薄膜的放大像 Fig.4 SEM morphologies of Cu50Ti50 alloy surface after reaction in solution containing H2O2, H2SO4 and different concentration of polyvinyl acetate at 80℃ for 10h (a)0mg/L;(b)300mg/L;(c)2000mg/L; (d)6000mg/L;(e)magnified image of fig.(c);(f)magnified image of fig.(d) | |
图 5所示为Cu30Ti70合金在含H2O2,H2SO4及6000mg/L的聚碳酸酯溶液中80℃保温不同时间后的表面SEM形貌,图 6则所示为不同时间沉积的薄膜的EDS成分分析。
 | 图5 Cu30Ti70合金在含H2O2,H2SO4及6000mg/L的聚碳酸酯溶液中80℃保温不同时间后的表面SEM形貌 (a)2h;(b)图(a)中薄膜的放大像;(c)6h;(d)图(c)中薄膜的放大像;(e)10h;(f)图(e)中薄膜的放大像 Fig.5 SEM morphologies of Cu30Ti70 alloy surface after reaction in solution containing H2O2,H2SO4 and 6000mg/L polycarbonate at 80℃ for different time (a)2h;(b)magnified image of fig.(a);(c)6h; (d)magnified image of fig.(c);(e)10h;(f)magnified image of fig.(e) | |
当合金在溶液中开始保温时,随着Ti(IV)离子的溶解,溶液首先变成橘黄色[16];当保温时间达到2h时,合金表面开始生成白色沉积物(图 5(a));随着时间的延长,合金表面的沉积物也逐渐增多(图 5(c))并最终覆盖整个合金表面(图 5(e))。此时,溶液也变成淡蓝色(Cu被H2O2和H2SO4氧化成Cu(II))。从图 5(b),(d),(f)可以看出,沉积的薄膜形貌变化不大,而由图 6可以看出,薄膜成分也变化不大,因此,Cu-Ti二元合金表面的Cu掺杂TiO2薄膜是通过溶解-沉积机理而形成。
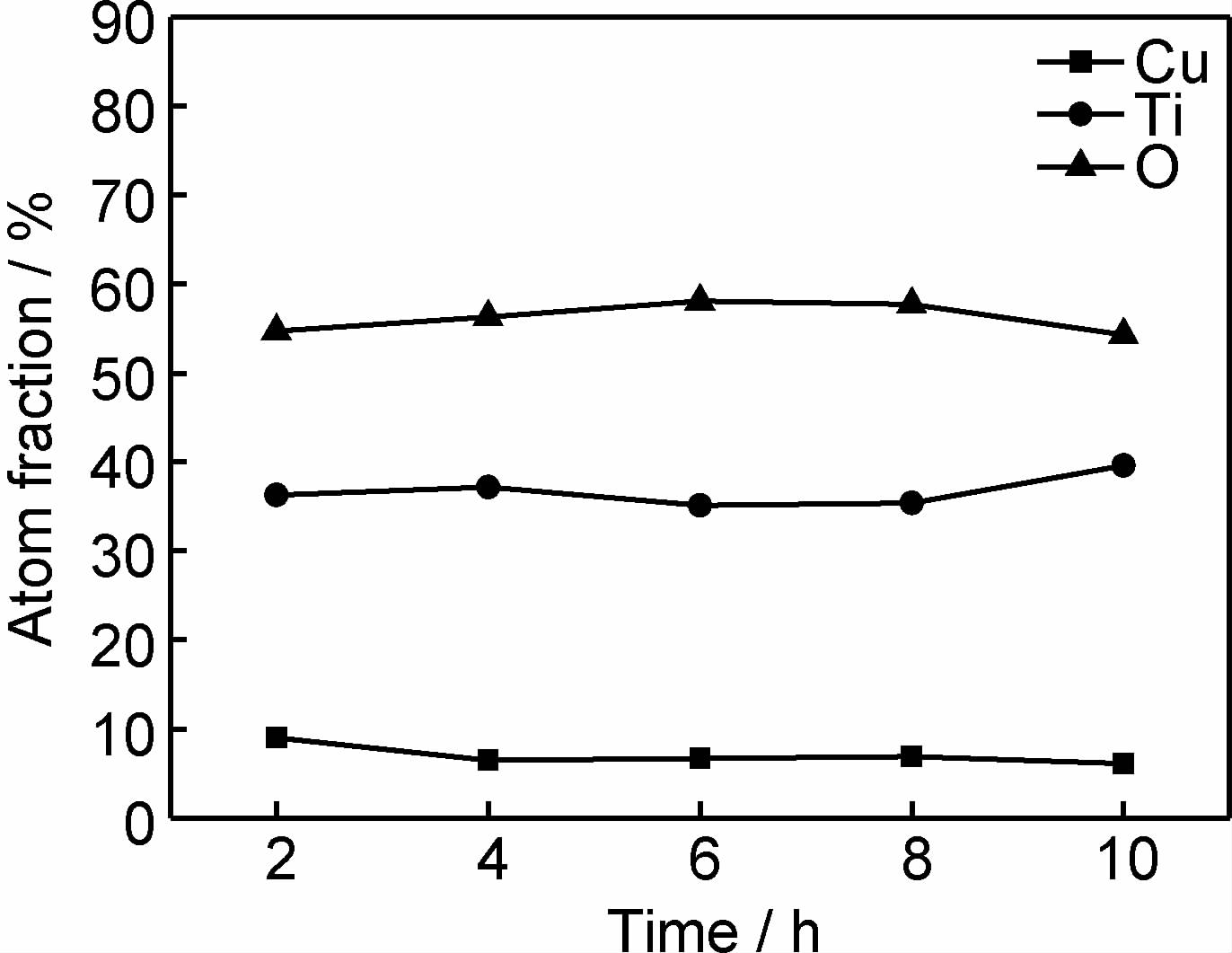 | 图6 Cu30Ti70合金在含H2O2,H2SO4及6000mg/L的聚碳酸酯 溶液中80℃保温不同时间所沉积薄膜的EDS成分分析 Fig.6 EDS composition analysis of the films formed on Cu30Ti70 alloy surface after reaction in solution containing H2O2,H2SO4 and 6000mg/L polycarbonate at 80℃ for different time | |
图 7所示为图 1中不同样品对20mg/L罗丹明B溶液的降解效率。
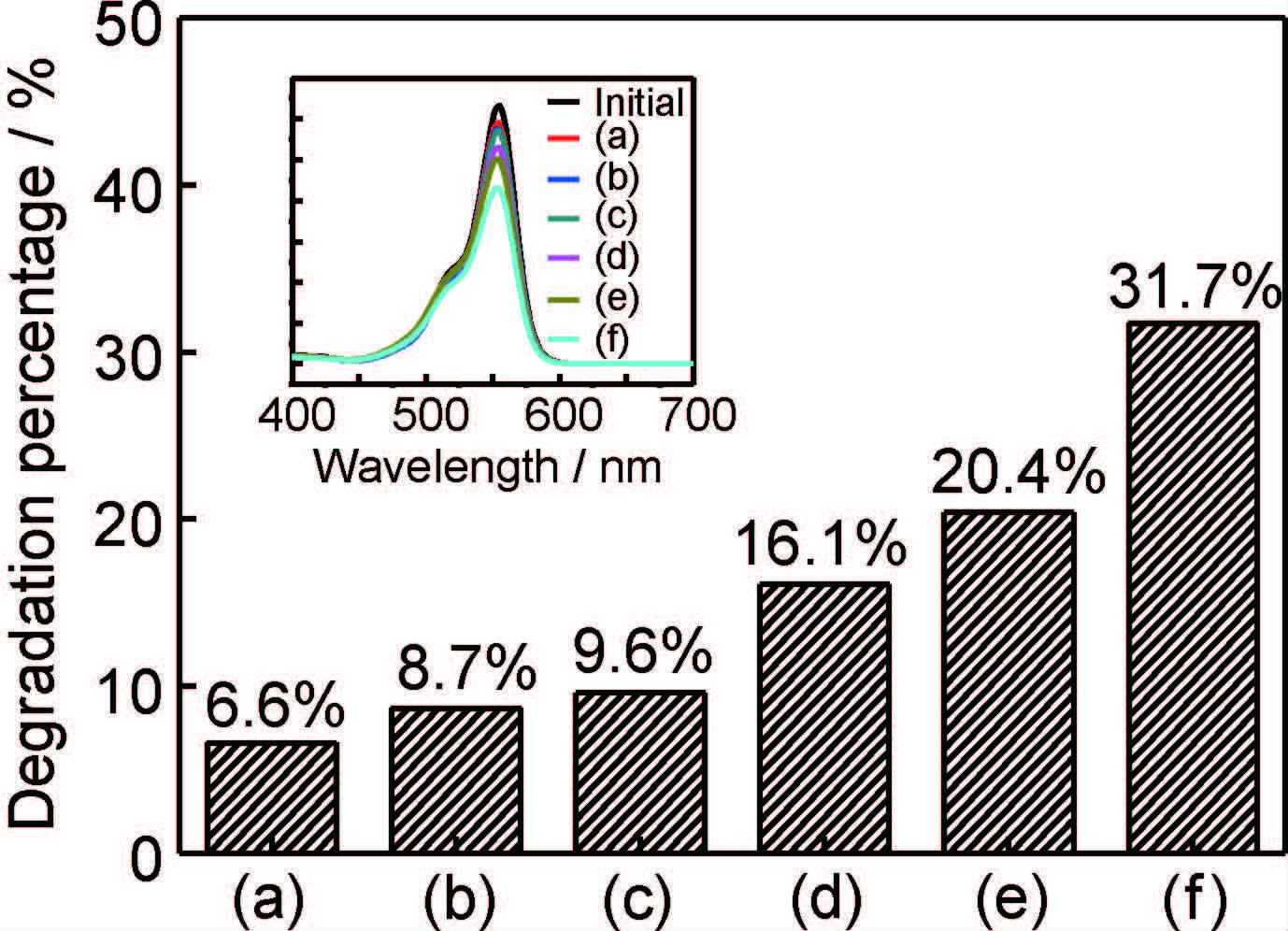 | 图7 图1中所示不同薄膜对罗丹明B的降解效率 (插图为所示薄膜对罗丹明B降解的紫外-可见吸收谱) Fig.7 Degradation efficiency of rhodamine B by different films shown in fig.1(inset shows the UV-Vis spectra for rhodamine B degraded by the films) | |
所有样品在黑暗下放置4h后对罗丹明B的吸附率均约为5.5%。在12W的紫外光下照射4h后,Cu50Ti50合金进行热处理后的样品对罗丹明B的降解率约为6.6%(图 7(a)),考虑黑暗下的吸附率为5.5%,可知该样品对罗丹明B几乎没有降解作用;当该合金在H2O2和H2SO4溶液中保温10h并热处理,以及该合金在含聚碳酸酯溶液中保温10h后,样品对罗丹明B的降解作用略有提高,但都较小,可以忽略(图 7(b),(c))。当该合金在含H2O2,H2SO4和聚碳酸酯或聚乙烯乙酸酯溶液中保温10h并450℃热处理后,样品对罗丹明B具有明显的降解作用,分别可达16.1%和20.4%(图 7(d),(e)),这主要是缘于合金表面锐钛矿型晶态TiO2薄膜的生成[17]。
当Cu30Ti70合金在含H2O2,H2SO4和聚碳酸酯溶液中保温10h并450℃热处理后,合金表面形成的Cu掺杂TiO2薄膜对罗丹明B的降解效率达到31.7%(图 7(f))。这主要是缘于掺杂的Cu离子(EDS测定含量约7%,图 2)可作为电子捕获中心,提高空穴与电子的分离效率,从而提高光催化降解作用。而对于Cu50Ti50合金表面形成的薄膜,Cu离子含量达到13%(图 2),提高了薄膜中的氧空穴含量,其又成为空穴与电子的再结合中心[18, 19],因此,与Cu30Ti70合金表面TiO2薄膜相比,光催化降解效率相对较低。
3 结论(1)本工作所制Cu掺杂TiO2薄膜通过溶解-沉积机理形成,Cu-Ti合金与含H2O2溶液首先相互作用产生Ti(IV)和Cu(II)并溶入溶液中;随后Cu掺杂非晶态TiO2在合金表面沉积,溶液中加入一定量的聚碳酸酯或聚乙烯乙酸酯能够促进非晶态TiO2在合金表面的沉积;最后经空气中450℃热处理1h获得Cu掺杂的锐钛矿型晶态TiO2薄膜。
(2)所制薄膜对罗丹明B具有优异的光催化降解作用,在12W紫外光下照射4h后,Cu30Ti70合金表面形成的薄膜比Cu50Ti50合金表面的薄膜具有更好的降解作用,其对罗丹明B溶液的降解率达到31.7%,因前者含有适量的掺杂Cu含量。该方法操作简单,可实现Cu掺杂TiO2薄膜的大面积制备。
| [1] | PENPOLCHAROEN M, AMAL R, BRUNGS M. Degradation of sucrose and nitrate over titania coated nano-hematite photocatalysts[J]. Journal of Nanoparticle Research, 2001, 3(4):289-302. |
| [2] | 祁洪飞,刘大博. TiO2基紫外探测器的制备及退火工艺对光电性能的影响[J].航空材料学报,2012, 32(2):1-5. QI Hong-fei, LIU Da-bo. Preparation of TiO2 UV detector and effect of annealing process on photoelectronic properties[J]. Journal of Aeronautical Materials, 2012, 32(2):1-5. |
| [3] | ZHANG A C, XUE H X, WU J M. Photocatalytic active titania thin films through oxidation of metallic Ti in aqueous H2O2 solutions containing various block copolymers[J]. Rare Metal Materials and Engineering, 2011, 40(10):1703-1707. |
| [4] | 张高洁,吴进明,黄兵,等.纳米TiO2光催化薄膜的自然时效[J].浙江大学学报(工学版),2008, 42(7):1266-1270. ZHANG Gao-jie, WU Jin-ming, HUANG Bing, et al. Natural ageing of nanostructured titania photocatalyst films[J]. Journal of Zhejiang University (Engineering Science), 2008, 42(7):1266-1270. |
| [5] | OLOFINJANA A O, BELL J M, JAMTING A K. Evaluation of the mechanical properties of sol-gel-deposited titania films using ultra-microindentation method[J]. Wear, 2000, 241(2):174-179. |
| [6] | NATARAJAN C, NOGAMI G. Cathodic electrodeposition of nanocrystalline titanium dioxide thin film[J]. Journal of Electrochemistry Society, 1996, 143(5):1547-1550. |
| [7] | KARUPPUCHAMY S, AMALNERKAR D P, YAMAGUCHI K, et al. Cathodic electrodeposition of TiO2 thin films for dye-sensitized photoelectrochemical applications[J]. Chemistry Letters, 2001, 30(1):78-79. |
| [8] | WU J M, HAYAKAWA S, TSURU K, et al. Porous titania films prepared from interactions of titanium with hydrogen peroxide solution[J]. Scripta Materialia, 2002, 46(1):101-106. |
| [9] | 张高洁,吴进明,刘少光,等.纳米复合结构二氧化钛薄膜的制备及其光降解水中罗丹明B的能力[J].硅酸盐学报,2007, 35(4):442-446. ZHANG Gao-jie, WU Jin-ming, LIU Shao-guang, et al. Fabrication of composite nanostructure titania thin film and its ability to photodegrade rhodamine B in water[J]. Journal of the Chinese Ceramic Society, 2007, 35(4):442-446. |
| [10] | WU J M, QI B. Low-temperature growth of a nitrogen-doped titania nanoflower film and its ability to assist photodegradation of rhodamine B in water[J]. The Journal of Physical Chemistry C, 2007, 111(2):666-673. |
| [11] | 郑树凯,吴国浩,张俊英,等. Sn掺杂锐钛矿TiO2薄膜的光催化活性及其能带结构[J].材料工程,2014, (1):70-74. ZHENG Shu-kai, WU Guo-hao, ZHANG Jun-ying, et al. Energy band structure and photocatalytic activity of Sn-doped TiO2 thin film[J]. Journal of Materials Engineering, 2014, (1):70-74. |
| [12] | CARVALHO H W P, BATISTA A P L, HAMMER P,et al. Photocatalytic degradation of methylene blue by TiO2-Cu thin films:theoretical and experimental study[J]. Journal of Hazardous Materials, 2010, 184(1-3):273-280. |
| [13] | WANG J Y, JI G B, LIU Y S, et al. Cu2O/TiO2 heterostructure nanotube arrays prepared by an electrodeposition method exhibiting enhanced photocatalytic activity for CO2 reduction to methanol[J]. Catalysis Communications, 2014, 46(2):17-21. |
| [14] | PARVULESCU V I, HARDACRE C. Catalysis in ionic liquids[J]. Chemical Reviews, 2007, 107(6):2615-2665. |
| [15] | LI H, ZHANG J, CHEN X F, et al. Ionic-liquid-assisted growth of flower-like TiO2 film on Ti substrate with high photocatalytic activity[J]. Journal of Molecular Catalysis A:Chemical, 2013, 373(7):12-17. |
| [16] | BAILAR J C, EMELEUS H T, NYHOLM R, et al. Comprehensive Inorganic Chemistry[M]. London:Pergamon Press Ltd, 1975. 361-365. |
| [17] | 王正平,陈兴娟,李辰砂.中孔TiO2的制备及光催化降解罗丹明性能的研究[J].材料工程,2005, (6):27-30. WANG Zheng-ping, CHEN Xing-juan, LI Chen-sha. Preparation of mesoporous TiO2 and the photocatalytic activity of degradating rhodamine[J]. Journal of Materials Engineering, 2005,(6):27-30. |
| [18] | LI G Z, ZHANG W Y, ZHANG J, et al. A novel way to fabricate Fe doped TiO2 nanotubes by anodization of TiFe alloys[J]. Rare Metal Materials and Engineering, 2011, 40(9):1510-1513. |
| [19] | XIN B F, WANG P, DING D D, et al. Effect of surface species on Cu-TiO2 photocatalytic activity[J]. Applied Surface Science, 2008, 254(9):2569-2574. |
 2016, Vol. 44
2016, Vol. 44


