文章信息
- 王敏, 郑浩岩, 杨长秀, 高兴莹, 董竹希文, 罗洋, 陈垚. 2015.
- WANG Min, ZHENG Hao-yan, YANG Chang-xiu, GAO Xing-ying, DONG Zhu-xi-wen, LUO Yang, CHEN Yao. 2015.
- pH值对乙二醇溶胶-凝胶法制备BiVO4光催化性能的影响
- Effect of pH Value on Photocatalytic Properties of BiVO4 Prepared by Ethylene Glycol Sol-gel
- 材料工程, 43(9): 6-11
- Journal of Materials Engineering, 43(9): 6-11.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2015.09.002
-
文章历史
- 收稿日期: 2014-12-01
- 修订日期: 2015-07-07
随着能源短缺和环境污染问题的日益严重,节能环保已经成为当今世界各国面临的重要课题。近年来,光催化剂在环保方面表现出的优良特性,获得了人们的广泛关注[1, 2, 3]。其中TiO2以其低成本,无毒性和良好的光催化性能,已经在环境治理方面得到了一定的应用[4, 5, 6],但由于其光响应区域只局限于紫外光范围,限制了TiO2的进一步发展[7],因此促使科学家们寻求利用可见光作为能源的替代材料[8, 9]。
科学家们发现禁带宽度为2.4eV的单斜型BiVO4在可见光下具有良好的光催化效果,从而能够利用可见光催化降解污染物,使其成为最有前景的可见光催化材料之一[10, 11, 12, 13]。
目前BiVO4合成方法基本都采用水热法[14],Zhang等[15]采用水热法合成了复合相的BiVO4光催化剂,并研究了不同反应pH对催化剂形貌及活性的影响。Obregón等[16]采用水热法,通过改变基本反应条件合成了不同形貌的BiVO4光催化剂,结果表明当BiVO4的形貌为针状时表现出最高的光催化活性。而采用溶胶-凝胶法制备BiVO4的研究鲜见报道[17]。本工作以硝酸铋、偏钒酸铵为原料,乙二醇为溶剂,采用溶胶-凝胶法合成钒酸铋前驱体,通过改变前驱体反应pH值,制备得到系列BiVO4光催化材料,同时利用XRD,SEM,XPS和UV-Vis等手段对样品的物相、形貌、元素价态和光吸收性能进行表征和分析,并通过降解模拟废水(甲基橙溶液),探讨了pH值与制备的系列样品的光催化性能之间的关系。与传统柠檬酸溶胶-凝胶法相比,乙二醇溶胶-凝胶法具有反应成胶可控性好、前驱体易得、煅烧充分等优势,为BiVO4的合成提供了新的途径。
1 实验材料与方法 1.1 光催化剂的制备本实验以Bi(NO3)3·5H2O(97%,质量分数,下同),NH4VO3(98.5%)为源物质,乙二醇为溶剂,采用溶胶-凝胶过程制备BiVO4粉体。将5mmol Bi(NO3)3·5H2O和5mmol NH4VO3分别溶于25mL乙二醇溶剂中,持续加热(80℃)搅拌15min,Bi(NO3)3·5H2O完全溶解,形成无色透明溶液A,NH4VO3完全溶解,形成棕色溶液B;然后将溶液B缓慢加入溶液A中,通过改变氨水添加量,调节溶液的pH值(分别为5,7,9,11和13),形成黄色乳状液,持续恒温搅拌,使溶剂大量蒸发,直到形成灰色溶胶;之后将其前躯体置于80℃的烘箱中烘干,研磨后在马弗炉中以550℃煅烧5h,自然冷却取出后,加无水乙醇二次研磨待用。
1.2 光催化剂的表征采用D/max-RB X射线衍射仪(XRD)(Cu靶,Kα射线,40kV,100mA,λ=0.15418nm)对催化剂的晶相进行分析;采用Hitach S-3400N 扫描电子显微镜(SEM)观察样品的微观结构和表面形貌。采用Hitach 1800紫外-可见吸收光谱仪(UV-Vis),积分球,BaSO4为背底,扫描速率为200nm/min。采用 Thermo ESCALAB 250Xi X射线光电子能谱(XPS)分析催化剂的元素组成和价态,以本体的污染碳C1s结合能(284.6eV)为标准,对样品进行校正,从而确定元素的结合能。
1.3 催化剂活性评价向250mL烧杯中加入50mL质量浓度为15mg/L的甲基橙溶液和0.03g催化剂样品。首先避光磁力搅拌30min,以建立吸附-脱附平衡及暗态反应平衡。磁力搅拌使催化剂在甲基橙溶液中呈悬浮状态。采用250W金属卤化物灯为可见光光源,灯距上液面14cm,并且在光源下放置一片滤光光阑(型号:UPG-320,λ为400~1100nm,厚度为2mm),使λ>400nm的可见光通过光阑,以保证光催化反应是在可见光下进行。在实验过程中不断磁力搅拌,每隔10min取样1次,静置片刻,取其上层清液用45μm滤膜过滤后再用紫外-可见分光光度仪在波长452nm处测定其吸光度,计算甲基橙的降解率。
2 结果与讨论 2.1 样品的XRD分析图1为不同pH值下制备的样品的XRD图谱,样品在(110),(011),(121),(040),(200)等晶面出现了较强的衍射峰。从图1可以看出,在给定的实验条件下,当pH为5,7,9,11和13时所制备的样品的衍射峰与标准卡号JSCD 14-688衍射数据相吻合,样品中没有出现其他杂质的峰,说明样品的纯度较好,所制得样品均为单斜型BiVO4。由(110)晶面,通过Scherrer公式d=0.89λ/β cosθ,计算各pH值下制备的样品的晶体粒径分别为44.39,43.90,42.08,43.20,43.66nm,这说明酸性条件下,随着反应溶液pH的增大,晶体的粒径随之减小。在碱性条件下,随着反应溶液pH的增大,晶体的粒径随之增大。这与SEM表征结果基本相符。通过进一步计算得到样品的晶胞体积及晶胞参数见表1。晶胞体积的变化规律与计算所得的平均粒径结果相符。
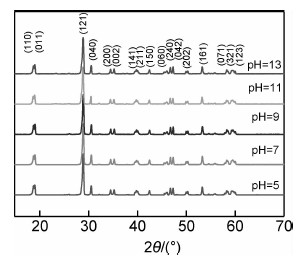 | 图1 不同pH值下制备的BiVO4的XRD图谱 Fig.1 XRD patterns of BiVO4 samples at different pH values | |
| Sample | a/nm | b/nm | c/nm | v/nm 3 |
| JSCD 14-688 | 5.19600 | 11.70100 | 5.09200 | 309.52 |
| pH=5 | 5.20109 | 11.71136 | 5.09649 | 310.44 |
| pH=7 | 5.19964 | 11.69326 | 5.09557 | 309.81 |
| pH=9 | 5.19448 | 11.70017 | 5.09002 | 309.39 |
| pH=11 | 5.19982 | 11.69928 | 5.09517 | 309.96 |
| pH=13 | 5.20112 | 11.70148 | 5.09609 | 310.15 |
图2为不同pH值下制备的BiVO4样品的SEM图。由图2可以看出,不同pH值下制得样品的形貌呈现一定规律的变化,当反应pH为5时样品是无规则的片状结构,并且夹杂着少量的颗粒状结构;当pH值逐渐升高到7,9,11,13时片状结构大量减少,表现为明显的颗粒状结构;当反应pH为7,9时制得的样品的颗粒分布均匀,无明显的粘连现象,并且可以看出,样品的颗粒较pH为5时制得的样品颗粒有所减小;当反应pH升高到11,13时样品的团聚现象愈加明显。从图2中还可以看出,随着pH的逐渐升高样品颗粒呈现先减小后增大的趋势,这与XRD表征结果的规律是一致的。当反应pH为9时,所制得样品的颗粒分布均匀,并且无明显的团聚现象,这可能是该样品较其他样品活性高的原因之一。
 | 图2 不同pH值下制备的BiVO4的SEM图 (a)pH=5;(b)pH=7;(c)pH=9;(d)pH=11;(e)pH=13 Fig.2 SEM images of BiVO4 at different pH values (a)pH=5;(b)pH=7;(c)pH=9;(d)pH=11;(e)pH=13 | |
图3为不同pH值下制备的BiVO4样品的紫外-可见漫反射光谱。由图3(a)可以看出,不同pH值下制备的样品在可见光(390~770nm)区域都有较强的吸收性能,且不同pH值下制备的BiVO4对可见光的吸收相似。作为一种半导体光催化材料,BiVO4的禁带宽度遵循如下公式:
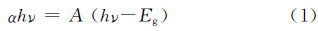
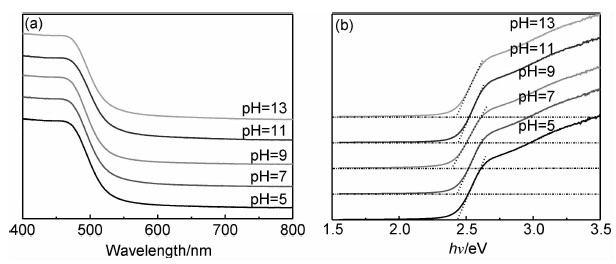 | 图3 样品的UV-Vis图(a)与样品的禁带宽度图(b) Fig.3 UV-Vis absorption (a) and band gap spectra(b) of samples | |
为了研究样品的价态和化学组成,对pH=9时制备的样品进行XPS表征,图4(a)为pH=9时制得样品的XPS全扫描图谱,图谱显示样品中含有Bi,V,O和C元素,其中C元素为检测仪中污染所致,这与预期结果相符。
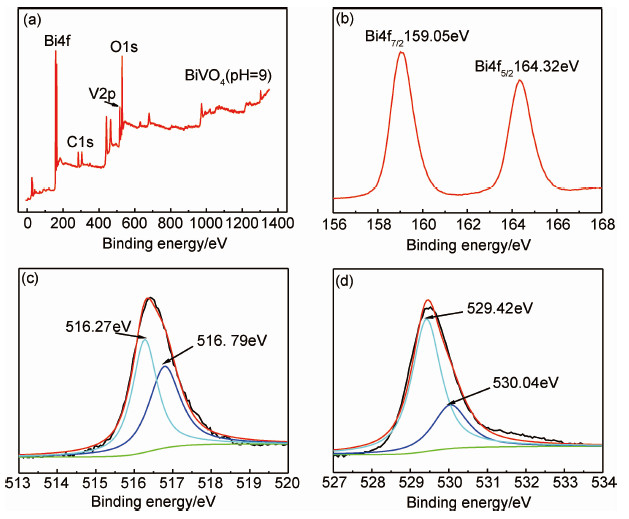 | 图4 样品pH=9时BiVO4的XPS谱图 (a)全扫描;(b)Bi4f;(c)V2p;(d)O1s Fig.4 XPS spectra of BiVO4 samples at pH=9 (a)full scan;(b)Bi4f;(c)V2p;(d)O1s | |
图4(b)为pH=9时BiVO4样品Bi4f的高分辨率双峰能图谱,其中样品的Bi4f在Eb=159.05,164.32eV处出现两个明显的特征峰,分别为Bi4f7/2与Bi4f5/2的结合能,与特征图谱对比,可以得出所制备的样品中Bi均以+3价态存在[18]。
图4(c)为pH=9时BiVO4样品V2p2/3的高分辨率能图谱,其中不对称的V2p2/3特征峰,可以分解为两个结合能位于516.79eV 和516.27eV的两个特征峰,与特征图谱对比,两个特征峰值分别对应的是V4+和V5+,根据电中性原理,可以推测所制备的BiVO4样品存在氧空位。
图4(d)为pH=9时BiVO4样品O1s2/3的高分辨率能图谱,其中不对称的O1s2/3特征峰,可以分解为两个结合能位于529.42eV和530.04eV的两个特征峰,与特征图谱对比,两个特征峰值分别归属为样品Bi—O键中的晶格氧(Olatt)和表面吸附氧(Oads),且表面吸附氧的存在有助于光催化活性的提高[17]。
通过计算BiVO4样品表面Bi与V摩尔比为1.14,说明制备的样品较纯净,这与XRD表征结果一致。 V4+与V5+摩尔比为0.91,Oads与Olatt摩尔比为0.39。V4+与V5+摩尔比和Oads与Olatt摩尔比标志着氧空位浓度的高低,其中氧空位的存在是光催化活性较高的理论依据之一。
2.5 光催化活性分析图5为光催化降解甲基橙机理图,当用能量等于或大于禁带宽度的光照射BiVO4时,其价带上的电子就会被激发,从价带越过禁带到达导带,从而在价带和导带上分别形成光生空穴和光生电子。光生空穴具有强氧化性,能将OH-氧化为OH,OH具有更强的氧化性,能够氧化催化剂表面的甲基橙;而光生电子具有强还原性,能将O2还原成O2-,从而参与氧化还原反应。
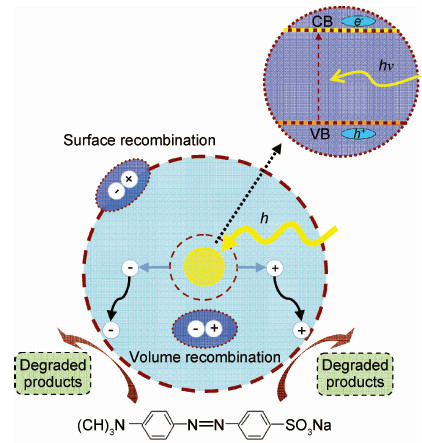 | 图5 光催化降解甲基橙机理图 Fig.5 Proposed degradation mechanism of methyl orange by BiVO4 under visible light irradiation | |
图6为不同pH值下制备的样品对甲基橙的降解率,通过对甲基橙的脱色率来评价所制得样品的光催化活性,由图6可知,当pH值为5,7,9,11和13时制得的样品在250W金属卤化物灯下光照50min后,对甲基橙的脱色率分别达到38.61%,63.23%,66.23%,38.63%,37.81%。综上所述:当pH值为9时所制得的催化剂效果最好,光照50min对甲基橙的脱色率达66.23%。这说明存在最佳制备pH值。分析活性提高的主要原因有:(1)不同pH值下,BiVO4结晶习性存在一定差异,这是由于不同pH值下BiVO4不同晶面的吸附H+和吸附OH-存在明显差异,使不同方向上的晶面生长速度各不相同,从而改变结晶习性[19]。(2)带隙能的降低,导致光吸收能力的增强,从而更有效地利用可见光,进而提高了光催化活性。这与UV-Vis表征时pH=9的样品具有较小的带隙能存在一定的关系。(3)pH值为9时制得的样品可能产生较多的氧空位,相关文献报道[17],氧空位的增加有助于光催化活性的提高。
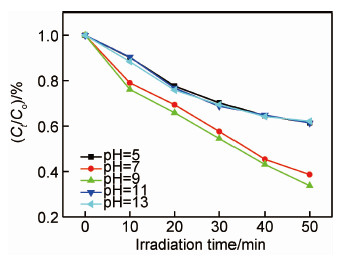 | 图6 不同pH值下制备的样品对甲基橙的降解率 Fig.6 Methyl orange degradation rate under visible light illumination at different pH values | |
为了进一步探讨样品的光催化活性,对样品的可见光降解反应进行了动力学方面的研究。首先,甲基橙的降解为一级反应,则其速率方程为:
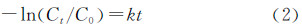
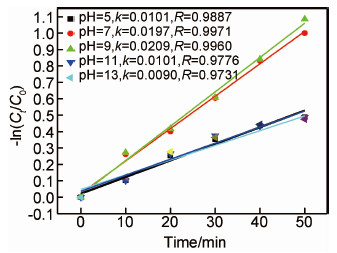 | 图7 催化剂的-ln(Ct/C0)与可见光照射时间t的关系 Fig.7 -ln(Ct/C0) as a function of t on the catalysts irradiated under visible light | |
(1)本实验成功制备了单斜相BiVO4光催化剂,并通过改变反应pH值制备出具有不同禁带宽度和不同形貌的BiVO4样品。当反应pH值为5时,产物大多为不规则的片状结构,禁带宽度为2.48eV。当pH值增至7和9时,产物片状结构大量减少,表现出明显的颗粒状结构,并且禁带宽度逐渐减小,分别为2.47eV和2.39eV。当反应 pH值增至11和13时,产物颗粒状结构团聚明显,并且禁带宽度有所增大,分别为2.45eV和2.47eV。
(2)pH=9时所制备的样品表现出最高的光催化活性,在250W金属卤化物灯下光照 50min,对甲基橙的脱色率达66.23 %,这与其较小的禁带宽度、较小的晶体粒径、大量的氧空位及表面吸附氧有着直接的关系。
| [1] | TAN G Q, ZHANG L L, REN H J, et al. Microwave hydrothermal synthesis of N-doped BiVO4 nanoplates with exposed (040) facets and enhanced visible-light photocatalytic properties[J].Ceramics International,2014,40 (7):9541-9547. |
| [2] | SHANG M, WANG W Z, ZHANG L, et al. 3D Bi2WO6/TiO2 hierarchical heterostructure: controllable synthesis and enhanced visible photocatalytic degradation performances[J]. Journal of Physical Chemistry C, 2009,113(33): 14727-14731. |
| [3] | LEE D K, CHO I, LEE S, et al.Effects of carbon content on the photocatalytic activity of C/BiVO4 composites under visible light irradiation[J].Materials Chemistry and Physics, 2010,119(1-2):106-111. |
| [4] | 李朋,赵昆渝,郭军,等.TiO2纳米孔到纳米管结构转变的因素及其机理研究[J].材料工程,2014,(1):58-63. LI Peng, ZHAO Kun-yu, GUO Jun, et al. Factors and mechanism for transition of TiO2 from nanopores to nanotubes[J]. Journal of Materials Engineering, 2014, (1):58-63. |
| [5] | CHENG L J, KANG Y, TONG F. Effect of preparation conditions on characteristics of hollow TiO2 fibers fabricated by chemical deposition and template method[J].Applied Surface Science,2012,263:223-229. |
| [6] | 顾建军, 刘鹏飞, 韩金荣, 等. Fe 掺杂量和退火氛围对TiO2薄膜晶体结构和磁性能的影响[J].材料工程,2014,(10):101-105. GU Jian-jun, LIU Peng-fei, HAN Jin-rong, et al. Influence of Fe-doping and annealing atmosphere on crystalline structure and magnetism of TiO2 thin films[J].Journal of Materials Engineering, 2014, (10):101-105. |
| [7] | LI Y K, DONG S Y, WANG Y F,et al. Reduced graphene oxide on a dumbbell-shaped BiVO4 photocatalyst for an augmented natural sunlight photocatalytic activity[J].Journal of Molecular Catalysis A:Chemical, 2014, 387:138-146. |
| [8] | ZHU Z F, ZHANG L, LI J Q, et al. Synthesis and photocatalytic behavior of BiVO4 with decahedral structure[J]. Ceramics International, 2013, 39(7): 7461-7465. |
| [9] | 王敏, 车寅生, 董占军, 等.B-Eu共掺杂BiVO4及对甲基橙的可见光光催化降解[J].材料热处理学报,2014,35(7):9-14. WANG Min, CHE Yin-sheng, DONG Zhan-jun, et al. Synthesis of B-Er co-doped BiVO4 photocatalyst and its photodegradation of methyl orange under visible-light irradiation[J]. Transactions of Materials and Heat Treatment, 2014, 35 (7): 9-14. |
| [10] | GAO X M, FU F, ZHANG L P, et al. The preparation of Ag-BiVO4 metal composite oxides and its application in efficient photocatalytic oxidative thiophene[J]. Physica B:Condensed Matter,2013, 419:80-85. |
| [11] | ZHANG X F, DU L L, WANG H, et al.Highly ordered mesoporous BiVO4: controllable ordering degree and super photocatalytic ability under visible light[J].Microporous and Mesoporous Materials,2013,173:175-180. |
| [12] | ZHU G Q, HOJAMBERDIEV M, QUE W X, et al.Hydrothermal synthesis and visible-light photocatalytic activity of porous peanut-like BiVO4 and BiVO4/Fe3O4 submicron structures[J].Ceramics International, 2013, 39(8):9163-9172. |
| [13] | ZHAO Z X, DAI H X, DENG J G, et al. Effect of sulfur doping on the photocatalytic performance of BiVO4 under visible light illumination[J]. Chinese Journal of Catalysis,2013,34(8):1617-1626. |
| [14] | LU Y, LUO Y S, KONG D Z, et al. Large-scale controllable synthesis of dumbbell-like BiVO4 photocatalysts with enhanced visible-light photocatalytic activity[J]. Journal of Solid State Chemistry,2012,186: 255-260. |
| [15] | ZHANG L L, LONG J X, PAN W W,et al. Efficient removal of methylene blue over composite-phase BiVO4 fabricated by hydrothermal control synthesis[J].Materials Chemistry and Physics,2012,136(2-3): 897-902. |
| [16] | OBREGON S, CABALLERO A, COLON G.Hydrothermal synthesis of BiVO4: structural and morphological influence on the photocatalytic activity[J]. Applied Catalysis B:Environmental, 2012,117-118: 59-66. |
| [17] | WANG M, CHE Y S, NIU C, et al. Effective visible light-active boron and europium co-doped BiVO4 synthesized by sol-gel method for photodegradation of methyl orange[J].Journal of Hazardous Materials, 2013,262:447-455. |
| [18] | WANG M, CHE Y S, NIU C, et al. Lanthanum and boron co-doped BiVO4 with enhanced visible light photocatalytic activity for degradation of methyl orange[J]. Journal of Rare Earths,2013,31(9):878-884. |
| [19] | KARUNAKARAN C, KALAIVANI S, VINAYAGAMOORTHY P, et al.Electrical, optical and visible light-photocatalytic properties of monoclinic BiVO4 nanoparticles synthesized hydrothermally at different pH[J].Materials Science in Semiconductor Processing,2014,21: 122-131. |
 2015, Vol. 43
2015, Vol. 43


