文章信息
- 张平, 莫尊理, 张春, 韩立娟, 李政. 2015.
- ZHANG Ping, MO Zun-li, ZHANG Chun, HAN Li-juan, LI Zheng. 2015.
- 磁响应性TiO2/石墨烯纳米复合材料的合成及光催化性能
- Preparation and Photocatalytic Properties of Magnetic Responsive TiO2/Graphene Nanocomposites
- 材料工程, 43(3): 72-77
- Journal of Materials Engineering, 43(3): 72-77.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2015.03.013
-
文章历史
- 收稿日期:2013-12-19
- 修订日期:2014-12-18
2. 甘肃省科学院 自然能源研究所, 兰州 730046
2. Natural Energy Institute of Gansu Academy of Sciences, Lanzhou 730046, China
TiO2因具有化学性质稳定、耐酸碱性好、无毒性、氧化能力强的优点,且来源丰富、成本较低、催化性能优异,被认为是当前最具推广潜力的一种光催化剂[1, 2, 3, 4]。为了进一步改善TiO2的光催化性能,人们已作了很多有益探索,其中之一就是将TiO2与碳基材料(如碳纳米管)进行复合,取得了较好的效果[5 ,6]。研究[7 ,8]表明TiO2与碳纳米管复合后,碳纳米管和TiO2间产生的协同效应能够促使TiO2产生的光生电子转移到碳纳米管上,不仅降低了光生电子-空穴对复合几率,还使该复合材料具有响应可见光的能力。
石墨烯是2004年发现的二维碳纳米材料[9],其电学性质比碳纳米管更为优异,将其用来代替碳纳米管修饰一些材料可取得更好的效果。张晓艳等[10]通过还原氧化石墨制备石墨烯,在此基础上采用溶胶-凝胶法制备出了TiO2/石墨烯复合材料,并研究了该材料的光催化分解水产氢活性。Zhang等[11]制备了P25-石墨烯复合材料,研究发现由于石墨烯的引入,该复合材料不仅能够很好地吸附有机染料,而且还拓展了可见光响应范围,能够有效分离光生电子和空穴。另外,还有大量关于利用石墨烯提高TiO2光催化性方面的研究工作[12, 13, 14, 15, 16, 17, 18, 19],但石墨烯和TiO2复合仍有其不足之处,如固液分离困难,无法实现循环利用。
解决TiO2固液分离实现循环利用,则可降低光催化剂成本,推动光催化技术在更多领域的应用。采用催化剂负载化,是一种解决光催化剂的分离和回收问题的有效途径。负载型光催化剂主要是通过物理或化学作用将TiO2负载于载体上。常见的固体载体有活性炭[20]、玻璃纤维[21]、沸石[22]等无机材料。本工作通过乳液插层水解法,利用具有层状结构的石墨烯作为模板[23],将磁性Fe3O4超声分散在无水乙醇中,加入钛酸丁酯继续分散为微乳液,该乳液插层于石墨烯的片层间,再加水引发钛酸丁酯水解,使Fe3O4和TiO2两种纳米粒子同时插层镶嵌于石墨烯层间,有效地简化了复合材料制备程序,缩短了制备时间,所制备磁响应性的TiO2/石墨烯纳米复合材料具有良好光催化性和磁性,通过磁性分离可实现固液分离。
1 实验 1.1 主要原料石墨粉(上海中秦化学试剂有限公司),FeCl3·6H2O(安阳市兴亚化学试剂有限公司),无水乙酸钠(天津市化学试剂一厂),钛酸丁酯(国药集团),无水乙醇(国药集团),亚甲基蓝(天津凯通化学试剂有限公司),药品均为分析纯,实验均使用去离子水。
1.2 磁性Fe3O4粒子的制备称取0.675g FeCl3·7H2O和1.8g无水乙酸钠在35mL乙二醇中搅拌30min,使其完全溶解。将混合液置于聚四氟乙烯高压反应釜中,在200℃下反应8h后得到黑色粉末,反复用二次水和乙醇超声清洗,洗去表面残留的乙二醇,得到均匀的Fe3O4纳米粒子。
1.3 石墨烯的制备采用Hummers法制备氧化石墨[24],将5g提纯石墨和3.75g硝酸钠加入1000mL烧杯中,加入60mL浓硫酸,将混合物置于冰水浴中,不断搅拌,随后再逐渐加入22.5g高锰酸钾,整个冰水浴冷却过程持续2h。冷却结束后,在常温下继续温和搅拌混合物5天,得到高黏稠液体。在搅拌的条件下加入到500mL质量分数5%的H2SO4中,搅拌2h后,再向溶液中加入15g质量分数30%的H2O2,继续搅拌2h。用二次去离子水洗涤过滤,然后加入到二次去离子水和无水乙醇的混合溶液中超声1h,静置24h后将沉淀去除,得到氧化石墨烯水溶液。取100mL氧化石墨烯水溶液,向其中加入1mL水合肼,然后在90℃下水浴回流24h,最后用二次去离子水洗涤过滤,在60℃下烘干,得到样品石墨烯。
1.4 磁响应TiO2/石墨烯纳米复合材料制备称取一定量的石墨烯,分散在10mL无水乙醇中超声6h形成A液。将一定量的Fe3O4加入30mL无水乙醇中超声1.5h,在超声过程中加入2mL钛酸丁酯。超声30min后,将A液加入其中,在温度在30℃下,将上述乳液在超声震荡30min形成B液。将一定量乙酸加水稀释至45mL形成C液。在50℃下将C液以1滴/3s的速率滴入B液,磁力搅拌,滴完后继续搅拌2.5h。冷却后用磁铁提取产物,分别用无水乙醇洗涤多次,干燥后得到产物。
1.5 测试与表征SEM分析采用JSM-6701F冷场发射扫描电镜,加速电压为30kV;TEM采用JEM2100型透射电子显微镜,在加速电压为50~200kV的情况下,观察材料的微观结构。XRD测试采用D/Max-2400型X射线衍射仪,CuKα射线,管电压为40kV,管电流为100mA,扫描范围为10~80°,步速为10(°)/min;磁测量在Model 6000 PPMS 磁强计上进行,测量4.2~295K温度范围内的零场磁化率χAC随温度的变化,所加驱动场为10A/m,频率为300Hz,在此温度范围内几个不同点测量等温磁化曲线,所加外场0~8×105A/m;采用XPA-7型光催化反应器对光催化材料进行催化性能测试;超声波采用KQ5200B型数控超声波清洗器,频率30~45Hz。
2 结果与讨论 2.1 SEM分析图1(a),(b)分别为石墨烯和磁响应TiO2/石墨烯纳米复合材料SEM照片,可以观察到清晰的石墨烯片层(图1(a)),磁性Fe3O4纳米粒子和TiO2纳米粒子均匀分散在石墨烯的片层结构上,且与石墨烯层有机体结合(图1(b))。乳液插层水解法使得磁性Fe3O4纳米粒子和TiO2纳米粒子同时插入石墨烯层间,形成稳定的体系,同时可以观察到膨胀之后的石墨烯呈现剥离现象。磁性Fe3O4粒子和TiO2粒子在石墨烯片层上均匀分布,而且粒径较小,由此可以认为复合材料的纳米粒子是在乳液中进行,乳液“微反应器”[25]尺寸小且均匀分布在石墨烯片层上,磁性Fe3O4粒子和TiO2粒子在反应过程中分散均匀,有效地限制了纳米粒子的团聚和生长。通过乳液插层水解法制备出的磁响应TiO2/石墨烯纳米复合材料,充分利用TiO2粒子的光催化性能和磁性粒子在外加磁场可提取的优势,结合石墨烯的层状结构,使得复合材料的理化性能得到很好的改善。材料具有良好的光催化性能同时兼具磁性,可通过外加磁场对光催化材料进行靶向定位、分离和重复使用。
 | 图1 石墨烯(a)和磁响应性TiO2/石墨烯复合材料(b)的SEM照片 Fig.1 SEM images of obtained samples (a)graphene;(b)magnetic responsible TiO2/graphene composite | |
图2为磁响应TiO2/石墨烯纳米复合材料的TEM照片,可以看出磁响应TiO2/石墨烯纳米复合材料的层状形态分布特征明显,片层结构清晰可见,磁性Fe3O4纳米粒子和TiO2纳米粒子均匀分散在石墨烯的片层结构上,以纳米尺寸负载石墨烯片层上,形成了层状结构的纳米复合材料。采用乳液插层水解法制备磁响应TiO2/石墨烯纳米复合材料时,逐滴加入乙酸水溶液控制酞酸丁酯水解,牵制了磁性Fe3O4纳米粒子和TiO2纳米粒子保持原来分散的状态,限制了纳米粒子的生长空间,使得磁性Fe3O4纳米粒子和TiO2纳米粒子在反应过程中均匀分散在石墨烯片层上,有效地解决了纳米粒子的团聚问题[26],与传统方法相比优势明显,是一种有效制备磁性光催化复合材料的方法。
 | 图2 磁响应性TiO2/石墨烯复合材料的TEM照片 Fig.2 TEM image of the magnetic responsible TiO2/graphene composite | |
图3中曲线a~d分别为石墨烯、Fe3O4、TiO2及磁响应TiO2/石墨烯纳米复合材料的XRD图。从图3曲线a中可以看出,2θ位于25.6°为石墨烯无定型状峰,图3曲线b中2θ分别位于30.3°,35.1°,42.8°,55.1°,62.9°处为Fe3O4的311,400,422,511,440晶面的特征衍射峰,图3曲线c中2θ位于25.3°,37.9°,48.0°,53.8°,55.1°和62.7°处出现的强峰是锐钛矿TiO2的101,004,200,105,211和204晶面的特征衍射峰。从图3曲线d磁响应TiO2/石墨烯纳米复合材料与各物质XRD图对比分析可以看出,复合材料中各物质的吸收峰都有所体现且比较明显,说明该复合材料中各物质为共存状态(图中方框为石墨烯的衍射峰)。采用Scherrer公式(D=Kλ/βcosθ)对Fe3O4和TiO2的晶粒尺寸进行了计算,其中D为估算的晶粒尺寸,K值取0.89,β为积分半高宽度,θ为衍射角,λ为X射线波长(0.15418nm)[27 ,28]。结果显示,Fe3O4纳米粒子约为45.5nm,TiO2纳米粒子约为18.8nm,磁性Fe3O4纳米粒子和TiO2纳米粒子镶嵌于石墨烯片层上并与石墨烯成功复合。
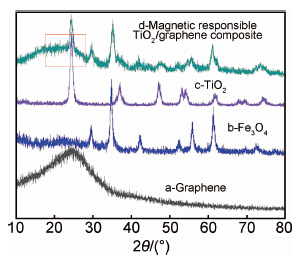 | 图3 试样的XRD图 Fig.3 XRD patterns of obtained samples | |
图4为磁响应TiO2/石墨烯纳米复合材料及纯Fe3O4粒子饱和VSM测试曲线。从图4中曲线a,b可知,纯Fe3O4粒子饱和磁化强度为60.02A·m2/kg,磁响应TiO2/石墨烯纳米复合材料的饱和磁化强度为20.13A·m2/kg。二者相比磁响应TiO2/石墨烯纳米复合材料饱和磁化强度有较大程度的减弱,是由于磁性Fe3O4粒子和TiO2同时负载于石墨烯片层形成磁响应TiO2/石墨烯纳米复合材料后,石墨烯和TiO2对磁性粒子起到包覆作用,使磁响应性降低[29]。即便如此,如图4中插图所示,复合材料在外加磁场的作用下仍能顺利提取。
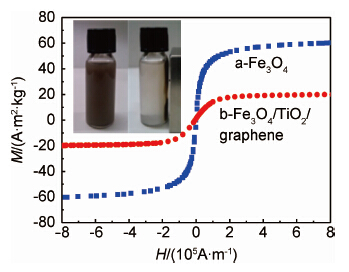 | 图4 复合材料的VSM测试分析图(插图为复合材料分散 在水溶液中(左)和外加磁铁吸引(右)的数码照片) Fig.4 VSM analysis of composite materials (insert is the photo of the composite materials dispersed in aqueous solution (left) and by applying a magnet outside the vessel (right)) | |
图4插图中,左图是复合材料均匀分散在水溶液中形成均匀的悬浊液的数码照片;右图是磁响应TiO2/石墨烯纳米复合材料在磁场作用磁分离后的数码照片。复合材料均匀分散的悬浊液在外加磁场作用下,复合材料定向移向磁铁,经过1min,全部移向磁铁,显示出优异的磁响应性。磁响应TiO2/石墨烯纳米复合材料在磁场作用下可实现固液分离,从溶液中顺利提取,实现磁分离进而重复使用。
2.5 光催化性能测试图5为磁响应TiO2/石墨烯纳米复合材料光催化性能测试曲线。分别将光催化剂加入浓度为20mg/L的亚甲基蓝溶液中,磁力搅拌和氧气(流量为0.6~1mL/min)曝气下,暗反应搅拌20min,启动氙灯(800W))并开始计时,每隔30min取样5mL,离心分离后,测定清液中亚甲基蓝的浓度,并根据反应后清液中亚甲基蓝的浓度和亚甲基蓝初始浓度,计算光催化剂对亚甲基蓝的降解率,并测试亚甲基蓝的光解作为空白。
 | 图5 纳米复合材料的光催化降解亚甲基蓝性能测试 Fig.5 Photocatalytic degradation of Methylene blue for nanocomposites | |
采用的计算公式如下:
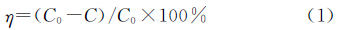
式中:η为亚甲基蓝的降解率;C0为光催化反应前亚甲基蓝的吸光度;C为光催化反应后亚甲基蓝的吸光度。
图5中曲线a,b,c分别是TiO2的含量为28%,31%,33%的配比下制备的磁响应TiO2/石墨烯纳米复合材料光催化降解亚甲基蓝的性能曲线,图5中曲线d和e分别为纯的TiO2光催化降解亚甲基蓝的性能曲线和亚甲基蓝光解曲线。由图5可知,暗反应吸附20min后,TiO2的含量为28%,31%,33%的配比下制备的磁响应TiO2/石墨烯纳米复合材料和纯TiO2的吸附去除率分别为38.78%,59.74%,28.69%,10.56%,光催化反应120min时,TiO2的含量为28%,31%,33%的配比下制备的磁响应TiO2/石墨烯纳米复合材料和纯TiO2对亚甲基蓝的光催化去除率分别为72.72%,92.19%,56.85%,39.9%,亚甲基蓝的自身光解仅为10%。由图5可知,磁响应TiO2/石墨烯复合材料均较纯TiO2对亚甲基蓝具有更高的吸附率,其中TiO2含量为31%的磁响应TiO2/石墨烯复合材料对亚甲基蓝的吸附率最高,达到59.74%,为TiO2吸附率的5倍多,光催化反应120min时,对亚甲基蓝的去除率达到92.19%。磁响应TiO2/石墨烯复合材料显示良好的光催化活性是由于石墨烯的片层结构使之具有较大的比表面积,使得复合材料对亚甲基蓝显示出良好的吸附性能,同时,石墨烯促进TiO2光催化产生的空穴和电子的分离,使得复合材料的光催化性能有较大的提高。
2.6 重复使用性图6显示了磁响应TiO2/石墨烯复合材料降解亚甲基蓝的重复使用性能。以磁响应TiO2/石墨烯纳米复合材料作为光催化剂,对初始浓度为20mg/L的亚甲基蓝液进行光催化降解,光催化降解180min后,测定其降解率。用磁铁回收磁响应TiO2/石墨烯纳米复合材料,重复使用,进行光催化剂的重复使用性实验。从图6可以看出,磁响应TiO2/石墨烯光催化剂重复使用7次后,光照3h,对亚甲基蓝的降解率仍大于90%,可见,所制备的磁响应TiO2/石墨烯纳米复合材料对亚甲基蓝的降解率无明显下降,显示出良好的重复使用性。
 | 图6 复合材料降解亚甲基蓝的重复使用性能 Fig.6 Effect of the reusability of composite material to degrade methylene blue | |
通过扫描电镜(SEM)、透射电镜(TEM)、X射线衍射(XRD)、震动样品磁强计(VSM)、光催化性能测试及重复性实验,显示已成功地制备了具有良好光催化活性、可反复使用的磁响应TiO2/石墨烯纳米复合材料。
3 结论(1)利用具有层状结构的石墨烯作为模板,将磁性Fe3O4和钛酸丁酯超声分散在无水乙醇中形成微乳液,并将该乳液插层于石墨烯的片层间形成稳定体系后再引发水解,使磁性Fe3O4粒子和TiO2粒子同时插入石墨烯层间,制得一种新型的磁响应TiO2/石墨烯纳米复合材料。
(2)该材料的制备过程可有效利用石墨烯片层结构,将Fe3O4粒子和TiO2粒子均匀的分散在层间,形成稳定的体系。
(3)复合材料具有良好的光催化活性,且可通过外加磁场进行靶向定位或磁分离可反复使用,重复使用7次后,光催化降解率仍大于90%,在光催化领域具有良好的应用前景。
| [1] | ASAHI R, MORIKAWA T, OHWAKI T, et al. Visible-light photocatalysis in nitrogen-doped titanium oxides[J]. Science, 2001, 293(5528): 269-271. |
| [2] | LIANG C Y, UCHYTIL P, PETRYCHKOVYCH R, et al. A comparison on gas separation between PES (polyethersulfone)/MMT (Na-montmorillonite) and PES/TiO2 mixed matrix membranes[J]. Separation and Purification Technology, 2012, 92(1): 57-63.. |
| [3] | ZHANG B, ZHANG J, CHEN F. Preparation and characterization of magnetic TiO2/ZnFe2O4 photocatalysts by a sol-gel method[J]. Research on Chemical Intermediates, 2008, 34(4): 375-380. |
| [4] | 霍莉, 丁克强, 常青云, 等. Fe3+ 掺杂对TiO2光催化氧化甲醇的影响[J]. 河北师范大学学报, 2005, 29(4): 372-375.HUO Li, DING Ke-qiang, CHANG Qing-yun, et al. Influence of Fe3+ doping on the photocatalytic activities of TiO2 for oxidation of methanol[J]. Journal of Hebei Normal University, 2005, 29(4): 372-375. |
| [5] | 胡开文. 碳纳米管负载TiO2光催化剂制备与活性研究[J]. 湖北工业大学学报, 2009, 24(4): 22-24.HU Kai-wen. Synthesis, characterization and photocatalytic property of carbon nanotube supported TiO2[J]. Journal of Hubei University of Technology, 2009, 24(4): 22-24. |
| [6] | 吴玉程, 刘晓璐, 叶敏, 等. 碳纳米管负载纳米TiO2复合材料的制备及其性能[J]. 物理化学学报, 2008, 24(1): 97-102.WU Yu-cheng, LIU Xiao-lu, YE Min, et al. Preparation and properties of carbon nanotube-TiO2 nanocomposites[J]. Acta Physico-Chimica Sinica, 2008, 24(1): 97-102. |
| [7] | YU H, QUAN X, CHEN S, et al. TiO2-multiwalled carbon nanotube heterojunction arrays and their charge separation capability[J]. The Journal of Physical Chemistry C, 2007, 111(35): 12987-12991. |
| [8] | WANG W, PHILIPPE S, PHILIPPE K, et al. Visible light photodegradation of phenol on MWNT-TiO2 composite catalysts prepared by a modified sol-gel method[J]. Journal of Molecular Catalysis A: Chemical, 2005, 235(1): 194-199. |
| [9] | NOVOSELOV K S, GEIM A K, MOROZOV S V, et al. Electric field effect in atomically thin carbon films[J]. Science, 2004, 306(5696): 666-669. |
| [10] | 张晓艳, 李浩鹏, 崔晓莉. TiO2/石墨烯复合材料的合成及光催化分解水产氢活性[J]. 无机化学学报, 2009, 25(11): 1903-1907. ZHANG Xiao-yan, LI Hao-peng, CUI Xiao-li. Preparation and photocatalytic activity for hydrogen evolution of TiO2/graphene sheets composite[J]. Chinese Journal of Inorganic Chemistry, 2009, 25(11): 1903-1907. |
| [11] | ZHANG H, LV X, LI Y, et al. P25-graphene composite as a high performance photocatalyst[J]. ACS Nano, 2009, 4(1): 380-386. |
| [12] | WU J C S, CHEN C H. A visible-light response vanadium-doped titania nanocatalyst by sol-gel method[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2004, 163(3): 509-515. |
| [13] | CHOI W, TERMIN A, HOFFMANN M R. The role of metal ion dopants in quantum-sized TiO2: correlation between photoreactivity and charge carrier recombination dynamics[J]. The Journal of Physical Chemistry, 1994, 98(51): 13669-13679. |
| [14] | LI L, LIU C, LIU Y. Study on activities of vanadium (IV/V) doped TiO2 (R) nanorods induced by UV and visible light[J]. Materials Chemistry and Physics, 2009, 113(2): 551-557. |
| [15] | CHANG S, LIU W. Surface doping is more beneficial than bulk doping to the photocatalytic activity of vanadium-doped TiO2[J]. Applied Catalysis B: Environmental, 2011, 101(3): 333-342. |
| [16] | NNHAR M S, HASEGAWA K, KAGAYA S. Photocatalytic degradation of phenol by visible light-responsive iron-doped TiO2 and spontaneous sedimentation of the TiO2 particles[J]. Chemosphere, 2006, 65(11): 1976-1982. |
| [17] | LAZAU C, SFIRLOAGA P, ORHA C, et al. Development of a novel fast-hydrothermal method for synthesis of Ag-doped TiO2 nanocrystals[J]. Materials Letters, 2011, 65(2): 337-339. |
| [18] | VENKATACHALAM N, PALANICHAMY M, MURUGESAN V. Sol-gel preparation and characterization of alkaline earth metal doped nano TiO2: Efficient photocatalytic degradation of 4-chlorophenol[J]. Journal of Molecular Catalysis A: Chemical, 2007, 273(1): 177-185. |
| [19] | YAMASHITA H, HARADA M, MISAKA J, et al. Photocatalytic degradation of organic compounds diluted in water using visible light-responsive metal ion-implanted TiO2 catalysts: Fe ion-implanted TiO2[J]. Catalysis Today, 2003, 84(3): 191-196. |
| [20] | YAP P S, LIM T T, LIM M, et al. Synthesis and characterization of nitrogen-doped TiO2/AC composite for the adsorption-photocatalytic degradation of aqueous bisphenol-A using solar light[J]. Catalysis Today, 2010, 151(1): 8-13. |
| [21] | YU H, LEE S C, YU J, et al. Photocatalytic activity of dispersed TiO2 particles deposited on glass fibers[J]. Journal of Molecular Catalysis A: Chemical, 2006, 246(1): 206-211. |
| [22] | MAHALAKSHMI M, PRIYA S V, ARABINDOO B, et al. Photocatalytic degradation of aqueous propoxur solution using TiO2 and Hβ zeolite-supported TiO2[J]. Journal of Hazardous Materials, 2009, 161(1): 336-343. |
| [23] | 甘永平, 秦怀鹏, 黄辉, 等. 金红石TiO2-石墨烯复合材料的制备及其光催化性能[J].物理化学学报, 2013, 29 (2): 403-410. GAN Yong-ping, QIN Huai-peng, HUANG Hui, et al. Preparation and photocatalytic activity of rutile TiO2-graphene composites[J]. Acta Physico-Chimica Sinica, 2013, 29 (2), 403-410. |
| [24] | HUMMERS J W S, OffEMAN R E. Preparation of graphitic oxide[J]. Journal of the American Chemical Society, 1958, 80(6): 1339. |
| [25] | 莫尊理, 张平, 陈红, 等. 乳液插层法制备 PMMA/Nd(OH)3/MMT 三相纳米复合材料及表征[J]. 功能材料, 2006, 37(9): 1473-1476. MO Zun-li, ZHANG Ping, CHEN Hong, et al. Synthesis of PMMA/Nd(OH)3/MMT nanocomposite by emulsion inserted method and its characterization[J]. J Funct Mater, 2006, 37(9): 1473-1476. |
| [26] | MO Z L, ZHANG P, ZUO D D, et al. Synthesis and characterization of polyaniline nanorods/Ce(OH)3- Pr2O3/montmorillonite composites through reverse micelle template[J]. Materials Research Bulletin, 2008, 43(7): 1664-1669. |
| [27] | AKPAN U G, HAMEED B H. The advancements in sol-gel method of doped-TiO2 photocatalysts[J]. Applied Catalysis A: General, 2010, 375(1): 1-11. |
| [28] | XU A W, GAO Y, LIU H Q. The preparation, characterization, and their photocatalytic activities of rare-earth-doped TiO2 nanoparticles[J]. Journal of Catalysis, 2002, 207(2): 151-157. |
| [29] | SHAH S I, LI W, HUANG C P, et al. Study of Nd3+, Pd2+, Pt4+, and Fe3+ dopant effect on photoreactivity of TiO2 nanoparticles[J]. Proceedings of the National Academy of Sciences of the United States of America, 2002, 99(2): 6482-6486. |
 2015,Vol. 43
2015,Vol. 43


