文章信息
- 杨泛明, 黎丽君, 肖浪, 廖敏, 张可意, 谭伟石, 贺国文
- YANG Fan-ming, LI Li-jun, XIAO Lang, LIAO Min, ZHANG Ke-yi, TAN Wei-shi, HE Guo-wen
- 聚醚P123和四乙烯五胺双功能化Fe-Zr的CO2吸附性能
- CO2 adsorption performance over Fe-Zr functionalized with both polyether P123 and tetraethylenepentamine
- 材料工程, 2021, 49(9): 158-166
- Journal of Materials Engineering, 2021, 49(9): 158-166.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2020.000651
-
文章历史
- 收稿日期: 2020-07-17
- 修订日期: 2020-10-30
2. 湖南城市学院 全固态储能材料与器件湖南省重点实验室, 湖南 益阳 413000
2. All-Solid-State Energy Storage Materials and Devices Key Laboratory of Hunan Province, Hunan City University, Yiyang 413000, Hunan, China
二氧化碳(CO2)是C1家族中重要的化工原料,但也是主要的温室气体,因此CO2捕集受到了广泛关注[1-4]。当前,CO2捕集技术主要有吸收法、吸附法。其中,CO2吸附技术因具有吸附量较大、吸附速率较快、再生容易、对设备腐蚀性较小等特点备受关注[5]。CO2吸附法中,新型高效吸附剂的研究与开发是其核心。目前,已经有多种有机胺固载的功能材料被应用于CO2吸附之中,如氧化物[6-7]、硅基分子筛[8-10]、碳材料[11-15]、金属-有机框架(MOFs)材料[16-18]、聚合物[19-20]等。然而,这些小吸附剂的N原子利用率较低。因此,研究者正在设计具有更高N原子利用率的新材料,从而进一步提高CO2吸附性能。
有机胺改性固体材料的CO2吸附性能与载体和有机胺的物理化学性质有关。近期,研究者设计了一种具有较强Lewis酸性的双金属材料Fe-Zr,并对其CO2吸附性能进行了考察[21]。改变金属盐种类和组成,可以快速调控Fe-Zr表面性质。与分子筛相似,通过改变金属离子种类可以调控双金属材料表面酸性,从而在双金属材料表面引入有机胺[22-23]。根据文献报道,在吸附体系中引入水分,可以提高CO2吸附性能[24]。然而,水分含量不易控制。为了进一步提高有机胺改性双金属材料的CO2吸附性能,可将水分更换为具有类似作用的—OH,使之参与CO2吸附过程,增大N原子利用率,提高CO2与氨基反应摩尔比[24]。因此,可以同时利用含—OH的物质和有机胺同时对双金属材料进行改性,提高CO2吸附性能。
本工作以聚醚P123为—OH供体对双金属材料Fe-Zr进行改性合成Fe-Zr(P),再利用四乙烯五胺对其进行改性制得TEPA(n)/Fe-Zr(P) (n表示TEPA的质量分数)。利用P123和TEPA对双金属材料进行改性具有以下优点:(1)聚醚P123可以提供—OH,并且可以存在于双金属材料孔道之内[24];(2)TEPA分子体积较小,更容易被引入至P123改性后的双金属材料孔道之内;(3)TEPA的N含量较高(37%),有利于增大吸附剂表面N含量,提高CO2吸附性能。本工作对吸附剂在不同条件下的吸附性能进行了考察,并对CO2吸附机理进行了深入分析。
1 实验材料与方法 1.1 实验试剂聚醚P123(MN≈5800,酷尔化学); 亚铁氰化钾·三水(AR,国药); 氯氧化锆·八水(AR,国药); 四乙烯五胺(AR, 阿拉丁); 无水乙醇(AR, 阿拉丁); 二氧化碳(5%,日臻气体); 氩气(99.99%,日臻气体)。
1.2 Fe-Zr(P)的合成采用水热合成法合成P123改性双金属材料Fe-Zr(P)[21],具体步骤如下:将2 g聚醚P123溶于65 g去离子水中,搅拌1 h,得到澄清溶液。在所得澄清溶液中加入2.1 g K4Fe(CN)6·3H2O,并将15 g ZrOCl2溶液(含2.684 g ZrOCl2)逐滴加入溶液中。搅拌3 h后,将所得产物转移到聚四氟乙烯内衬之中,并于100 ℃进行水热处理24 h。最后,将所得固体产物水洗至中性,并将其置于120 ℃干燥箱中保持24 h,即可得到P123改性的固体材料Fe-Zr(P)。
1.3 TEPA(n)Fe-Zr(P)的合成利用浸渍法合成TEPA改性吸附剂TEPA(n)Fe-Zr(P)[21, 24],步骤如下:将TEPA溶于10 g无水乙醇之中,搅拌10 min形成透明溶液;将0.5 g固体材料Fe-Zr(P)加入至澄清溶液之中,搅拌3 h;将所得糊状物置于120 ℃干燥箱中并保持24 h,得到产物TEPA(n)/Fe-Zr(P)。
1.4 材料表征采用X射线衍射(XRD)、X射线光电子能谱(XPS)、红外光谱(IR)对Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的结构进行分析。采用N2吸附-脱附技术分析Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的孔结构。采用透射电子显微镜(TEM)分析材料多孔性。采用热重分析技术分析Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的热稳定性。
1.5 CO2吸附利用穿透曲线分析Fe-Zr(P)和TETA(n)/Fe-Zr(P)的CO2吸附性能[21, 24-26],方法如下:将吸附剂置于流速为100 mL/min的高纯Ar中并升温至100 ℃,移除表面杂质;降温至所需温度,并进行CO2吸附,得到CO2吸附穿透曲线。对穿透曲线进行积分,即可得到CO2吸附量;将温度升高至100 ℃并将气体更换为高纯Ar (100 mL/min),实现吸附剂再生。N原子利用率(η)计算公式如式(1)所示。
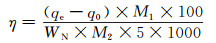
|
(1) |
式中:qe,q0分别为TETA(n)/Fe-Zr(P)和Fe-Zr(P)的饱和吸附量; M1,M2分别为TEPA和CO2的相对分子质量; WN为每克吸附剂中TEPA质量。
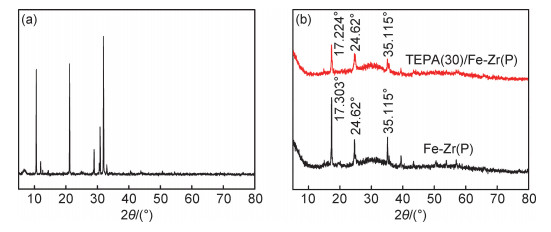
2 结果与分析 2.1 材料表征 2.1.1 X射线衍射(XRD)图 1为K4Fe(CN)6·3H2O,Fe-Zr(P)和TEPA(30)/Fe-Zr(P)的XRD图。由图 1可知,Fe-Zr(P)的衍射曲线中没有K4Fe(CN)6·3H2O特征衍射峰,并且在17.303°,24.62°和35.115°处出现新的衍射峰,说明原料发生化学反应,Fe-Zr(P)制备成功。利用TEPA对Fe-Zr(P)进行改性,衍射峰形状保持不变,Fe-Zr(P)的结构保持稳定。与Fe-Zr(P)相比较,TEPA(30)/Fe-Zr(P)的结晶度较低,因此衍射峰强度较低。根据文献报道[21],TEPA可能与载体Fe-Zr(P)表面发生反应,导致衍射角发生改变。因此,2θ为17.303 °的衍射峰移动至17.224°。
|
图 1 K4Fe(CN)6·3H2O(a),Fe-Zr(P)和TEPA(30)/Fe-Zr(P)(b)的XRD图 Fig. 1 XRD patterns of K4Fe(CN)6·3H2O(a), Fe-Zr(P) and TEPA(30)/Fe-Zr(P)(b) |
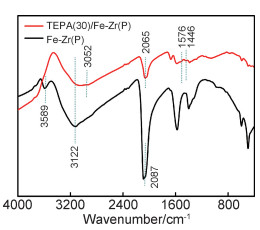
图 2为Fe-Zr(P)和TEPA(30)/Fe-Zr(P)的红外光谱图。与文献结果相似[21],波数为2087,3122 cm-1处分别出现—CN和H2O吸收峰。此外,Fe-Zr(P)中P123提供—OH,因此在3589 cm-1处可以检测到—OH吸收峰。利用TEPA对Fe-Zr(P)改性后,3589 cm-1处的吸收峰消失,并且在3052,1672,1576 cm-1和1446 cm-1处检测到新的吸收峰。其中:(1)3052 cm-1处的吸收峰归属于N—H伸缩振动[6-7, 21];(2)1576 cm-1和1446 cm-1处分别为—NH2和—CH2的吸收峰[6-7, 21, 23]。结合IR和XRD测试结果,推测P123被引入双金属材料孔道内,并且TEPA改性成功。
|
图 2 Fe-Zr(P)和TEPA(30)/Fe-Zr(P)的IR图 Fig. 2 IR spectra of Fe-Zr(P) and TEPA(30)/Fe-Zr(P) |
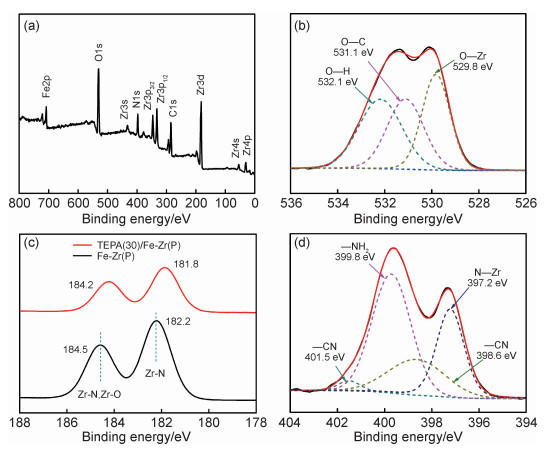
图 3为Fe-Zr(P)和TEPA(30)/Fe-Zr(P)的XPS测试结果。由XPS全谱图(图 3(a))可知,Fe-Zr(P)中可以检测到Fe, Zr, C, N,O元素。由Fe-Zr(P)中O1s分谱图(图 3(b))可知, Fe-Zr(P)中存在O—C键和O—H键, 说明P123被成功引入双金属材料中。与文献报道相似[21], Zr3d的XPS分谱图中检测到N—Zr键和Zr—O键的峰(图 3(c)),说明—CN与Zr发生化学反应,制得载体Fe-Zr(P)。利用TEPA改性后,电子结合能为184.5 eV和182.2 eV的分谱峰分别移动至184.2 eV,和181.8 eV(图 3(c))。根据文献报道[21],TEPA中N原子可以与载体表面Zr原子反应产生N—Zr键,从而将TEPA引入Fe—Zr(P)表面,因此在TEPA(30)/Fe—Zr(P)中可以检测到N—H键和N—Zr键的分谱峰(图 3(d))。由XRD,IR和XPS测试结果可以推测,P123和TEPA均被引入双金属材料中。
|
图 3 Fe-Zr(P)和TEPA(30)/Fe-Zr(P)的XPS图 (a)Fe-Zr(P)的全谱图;(b)Fe-Zr(P)中O1s的分峰图;(c)Fe-Zr(P)和TEPA(30)/Fe-Zr(P)中Zr3d对比图;(d)TEPA(30)/Fe-Zr(P)中N1s的分峰图 Fig. 3 XPS spectra of Fe-Zr(P) and TEPA(30)/Fe-Zr(P) (a)full spectra of Fe-Zr(P); (b)O1s spectra of Fe-Zr(P); (c)Zr3d spectra of Fe-Zr(P) and TEPA(30)/Fe-Zr(P); (d)N1s spectra of TEPA(30)/Fe-Zr(P) |
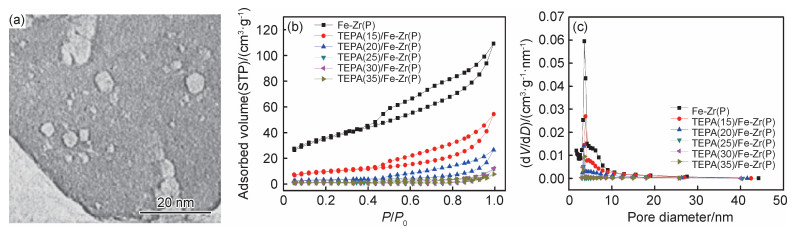
图 4和表 1为Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的N2吸附-脱附测试结果。由图 4和表 1可知:(1)Fe-Zr(P)的TEM图中有小孔存在(图 4(a)),说明Fe-Zr(P)为多孔材料; (2)Fe-Zr(P)表现出Ⅱ型吸附等温线,并且带有回滞环(图 4(b)),可以说明介孔的存在; (3)Fe-Zr(P)的孔径处于2~40 nm之间(图 4(c)),平均孔径为5.6 nm,孔体积为0.158 cm3/g,说明Fe-Zr(P)为介孔材料; (4)材料比表面积SBET、孔体积Vp和平均孔径dp随着TEPA质量分数的增加逐渐降低,这是由于Fe-Zr(P)的孔道逐渐被TEPA覆盖所致; (5)所有改性材料的孔径处于2~30 nm之间,并且平均孔径处于5~15 nm之间,因此载体和改性材料均为介孔材料。
|
图 4 Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的TEM图和N2吸附等温线以及孔径分布曲线 (a)Fe-Zr(P)的TEM图;(b)Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的N2吸附等温线;(c)Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的孔径分布曲线 Fig. 4 TEM image, N2 adsorption isotherms and pore size distribution curves of Fe-Zr(P) and TEPA(n)/Fe-Zr(P) (a)TEM image of Fe-Zr(P); (b)N2 adsorption isotherms of Fe-Zr(P) and TEPA(n)/Fe-Zr(P); (c)pore size distribution curves of Fe-Zr(P) and TEPA(n)/Fe-Zr(P) |
| Adsorbent | SBET/(m2·g-1) | Vtotal/(cm3·g-1) | dp/nm |
| Fe-Zr(P) | 123 | 0.158 | 13.8 |
| TEPA(15)/Fe-Zr(P) | 33 | 0.085 | 12.6 |
| TEPA(20)/Fe-Zr(P) | 11 | 0.041 | 8.4 |
| TEPA(25)/Fe-Zr(P) | 3 | 0.018 | 8.2 |
| TEPA(30)/Fe-Zr(P) | 2 | 0.010 | 5.5 |
| TEPA(35)/Fe-Zr(P) | 2 | 0.008 | 5.4 |
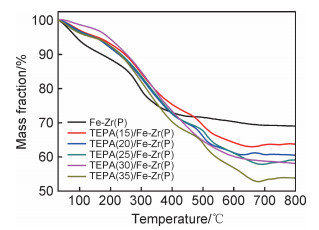
图 5为Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的热重分析曲线图。由图 5可知:(1)120 ℃前,Fe-Zr(P)表面出现质量损失,这是由于材料表面水分和其他杂质气体被移除的原因所致。(2)与文献报道相似[21, 24],温度升高至240 ℃时,Fe-Zr(P)中的P123被移除,并且双金属材料开始分解,因此出现明显失重。(3)与Fe-Zr(P)相比较,TEPA(n)/Fe-Zr(P)的热稳定性较差。温度高于182 ℃时,TEPA被移除,因此出现明显失重。(4)随着TEPA质量分数增加,失重率逐渐增大。TEPA质量分数为15%,20%,25%,30%,35%时,失重率分别为8.52%,11.2%,12.73%,16.18%,17.9%。
|
图 5 Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的热重分析曲线 Fig. 5 TGA curves of Fe-Zr(P) and TEPA(n)/Fe-Zr(P) |
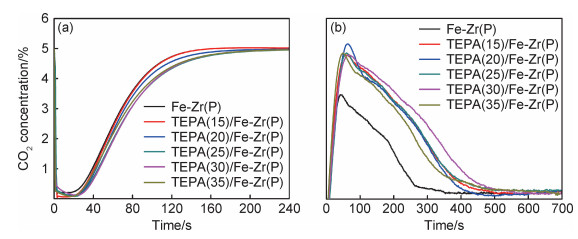
与文献报道方法一致[21, 24-26],本工作利用穿透曲线法对Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的CO2吸附性能进行测试。本工作中,首先对Fe-Zr(P)和TEPA(n)/Fe-Zr(P)在75 ℃,10 mL/min下的穿透曲线进行测试,所得结果如图 6所示。由图 6可知,240 s内,CO2浓度回到初始水平,说明240 s内CO2吸附可以达到饱和。由CO2程序升温脱附(CO2-TPD)测试曲线可知,实验时间内,脱附曲线回到基线位置,即CO2脱附完全。因此,本工作CO2吸附性能测试方法可行。
|
图 6 Fe-Zr(P),TEPA(n)/Fe-Zr(P)在75 ℃的CO2吸附穿透曲线(a)和CO2-TPD图(b) Fig. 6 CO2 adsorption breakthrough curves(a) and CO2-TPD graphs(b) over Fe-Zr(P) and TEPA(n)/Fe-Zr(P) at 75 ℃ |
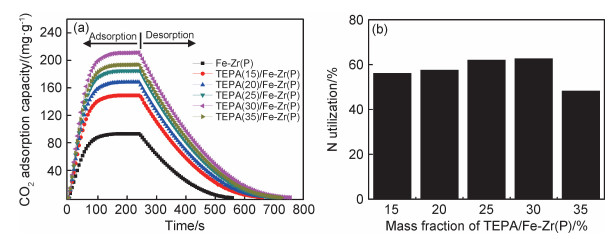
温度为75 ℃,气体流速为10 mL/min时,Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的CO2吸附性能随TETA/Fe-Zr(P)质量分数和吸附时间变化曲线如图 7所示。由图 7可知:(1)160 s之前,随着吸附时间延长,吸附量逐渐增大。160 s之后,吸附量保持稳定。根据N2吸附-脱附测试结果及文献报道结果[23, 27],TEPA(n)/Fe-Zr(P)为多孔材料,并且孔径均处于2~30 nm之间,足以容纳动力学直径为0.33 nm的CO2分子。通入CO2后,气体分子在孔道内部扩散并与碱性位点接触,发生化学吸附。随着时间延长,越来越多的碱性位点与CO2反应,吸附量增大。160 s之后,大部分可利用的碱性位点反应完毕,吸附量保持稳定;(2)与Fe-Zr(P)相比较,TEPA(n)/Fe-Zr(P)具有更大的吸附量,这是由于TEPA(n)/Fe-Zr(P)表面改性物质与CO2反应发生化学吸附所致。(3)CO2吸附量和N原子利用率均随着TEPA质量分数的增加先增大后减小。TEPA/Fe-Zr(P)质量分数小于30%时,吸附量达到最大值,为211.3 mg/g,此时N原子利用率为62.7%。根据表征结果和文献报道结果[21-24],本工作所制备的吸附剂中含有—OH,孔道尺寸较小。利用TEPA改性后,孔径更小。质量分数小于30%时,CO2可顺利进入孔道内部并与碱性位点发生反应。随着TEPA含量增加,吸附量和N原子利用率逐渐增大。质量分数超过30%时,TEPA过量。过量的TEPA覆盖于材料外表面,阻止部分CO2与孔道内的碱性位点接触,吸附量和N原子利用率逐渐降低。
|
图 7 Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的CO2吸附性能随吸附时间和TEPA质量分数变化结果 (a)吸附-脱附量随时间变化曲线; (b)N原子利用率 Fig. 7 CO2 adsorption performance of Fe-Zr(P) and TEPA(n)/Fe-Zr(P) as a function of adsorption time and TEPA mass fraction (a)adsorption and desorption capacity as a function of adsorption time; (b)N utilization |
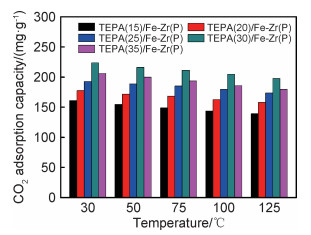
温度对有机胺改性多孔材料的CO2吸附性能有较大影响[21-24, 28]。气体流速为10 mL/min时,对TEPA(n)/Fe-Zr(P)在不同温度下的CO2吸附性能进行考察,结果如图 8所示。与传统吸附剂不同,TEPA(n)/Fe-Zr(P)的吸附量随温度变化逐渐降低,但变化幅度较小。根据图 7结果及文献报道结果[24],推测CO2在材料表面既发生物理吸附,又发生化学吸附。温度较低时,以物理吸附为主。温度较高时,以化学吸附为主。物理吸附过程放热,因此吸附量随着吸附温度升高而降低。随着温度升高,CO2更容易扩散至孔道内部并与氨基发生反应,化学吸附量逐渐增大。因此,随着温度升高,CO2吸附量变化幅度较小。
|
图 8 Fe-Zr(P)和TEPA(n)/Fe-Zr(P)的吸附量随吸附温度变化 Fig. 8 CO2 adsorption capacity of Fe-Zr(P) and TEPA(n)/Fe-Zr(P) as a function of adsorption temperature |
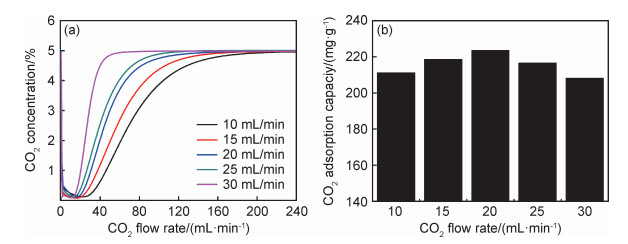
图 9为TEPA(30)/Fe-Zr(P)的CO2吸附性能随气体流速变化图。由图 9可知:(1)随着气体流速增大,CO2穿透时间逐渐减少。根据文献报道[21],气体流速增大,CO2与TEPA(30)/Fe-Zr(P)表面碱性位点接触时间降低,因此在较短的时间内即可在其表面发生穿透; (2)气体流速小于20 mL/min时,吸附量随流速增加而增大。气体流速大于20 mL/min时,吸附量逐渐减少。根据文献报道[21],气体流速增大时,更多的CO2分子进入TEPA(30)/Fe-Zr(P)的孔道之内并与碱性位点发生反应,化学吸附平衡向正反应方向移动,吸附量逐渐增大。气体流速超过20 mL/min时,CO2与碱性位点接触时间过短,吸附过程难以完成,因此吸附量逐渐减小。
|
图 9 TEPA(n)/Fe-Zr(P)的CO2吸附性能随气体流速变化图 (a)CO2吸附穿透曲线;(b)TEPA(30)/Fe-Zr(P)的CO2吸附量 Fig. 9 CO2 adsorption performance of TEPA(n)/Fe-Zr(P) at different gas flow rates (a)breakthrough curves of CO2 adsorption; (b)CO2 adsorption capacity of TEPA(30)/Fe-Zr(P) |
将本工作所制备吸附剂与其他有机胺改性材料的吸附性能进行对比,具体如表 2所示。由表 2可知,TEPA(30)/Fe-Zr(P)具有较大的吸附量,是一种具有较大潜力的CO2吸附剂。
| Adsorbent | Temperature/℃ | Gas flow rate/(mL·min-1) | CO2 uptake/(mg·g-1) | Reference |
| TEPA(30)/Fe-Zr(P) | 30 | 10 | 223.7 | Present study |
| TEPA(30)/Fe-Zr(P) | 75 | 10 | 211.3 | Present study |
| TiO2-TEPA | 30 | 71.7 | [7] | |
| WSC-500-1 | 0 | 265.7 | [12] | |
| T-GU-700-6 | 25 | 105.6 | [13] | |
| NHC-650-1 | 25 | 196.7 | [14] | |
| LC-500-1 | 25 | 154.0 | [15] | |
| HCPs-SC-SO3NH4 | 25 | 110.0 | [19] | |
| Fe-Zr-TETA-200 | 75 | 20 | 180.4 | [21] |
| PEI/Zr7-SBA-15 | 75 | 68.6 | [22] | |
| Zr-MCM-41-TETA-200 | 30 | 5 | 158.4 | [23] |
| Zr-SBA(P)-50 | 75 | 5 | 167.2 | [24] |
| DBU-3 | 25 | 20 | 150.9 | [25] |
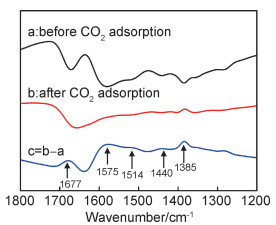
根据文献报道[29],可以对TEPA(30)/Fe-Zr(P)在CO2吸附前后的红外光谱进行分析,探究P123和TEPA在CO2吸附中的作用,揭示CO2吸附机制。图 10为TEPA(30)/Fe-Zr(P)吸附CO2前后的红外光谱图。由图 10可知,吸附CO2后,曲线c中1677,1575,1514,1440,1385 cm-1和1288 cm-1处出现吸收峰。根据文献报道[24, 29],波数为1677,1575 cm-1和1514 cm-1处分别为NH3+或C—NH,HCOO-,CO的吸收峰。波数为1440 cm-1和1386 cm-1处出现COO-的伸缩振动峰。然而,1302~1306 cm-1处不出现吸收峰,说明吸附过程不产生HCO3-[30]。由红外分析结果可以推测,CO2与TEPA(30)/Fe-Zr(P)接触时,可以与材料表面—OH和氨基发生反应,产生氨基钾酸氢盐,提高材料化学吸附性能。
|
图 10 TEPA(30)/Fe-Zr(P)吸附CO2前后的红外光谱图 Fig. 10 IR spectra of TEPA(30)/Fe-Zr(P) before and after CO2 adsorption |
CO2循环吸附性能优劣是衡量固体材料能否应用于实际情况之中的重要指标[6-7, 11-15, 21-24]。气体流速为10 mL/min时,分别对TEPA(30)/Fe-Zr(P)在30 ℃和75 ℃时的CO2吸附性能进行考察,测试结果如图 11所示。由图 11可知,循环20次,吸附性能均保持稳定,说明本工作所制备的吸附剂有望应用于CO2吸附之中。

|
图 11 TEPA(30)/Fe-Zr(P)分别在30 ℃和75 ℃下的CO2吸附性能 Fig. 11 CO2 adsorption performance of TEPA(30)/Fe-Zr(P) at 30 ℃ and 75 ℃ |
(1) 利用聚醚P123对介孔双金属材料进行改性制得含羟基的双金属材料Fe-Zr(P),并利用四乙烯五胺对其进行功能化,通过N-Zr配位合成富含氨基的吸附剂TEPA(n)/Fe-Zr(P)。
(2) TEPA(n)/Fe-Zr(P)的热分解温度可达182 ℃。
(3) 随着四乙烯五胺含量增大,CO2吸附量和N利用率先增大后减小。随着吸附温度升高,CO2吸附量逐渐减小,但变化幅度较小。随着气体流速增大,CO2吸附量先增大后减小。
(4) 吸附温度为75 ℃,气体流速为10 mL/min时,TEPA(30)/Fe-Zr(P)的吸附量可达211.3 mg/g,N原子利用率为62.7%。循环20次,吸附量保持稳定。
(5) CO2在聚醚P123和四乙烯五胺双功能化Fe-Zr表面既发生物理吸附,又发生化学吸附。除物理吸附外,TEPA(n)/Fe-Zr(P)中羟基和氨基均参与CO2吸附,产生氨基钾酸氢盐,提高CO2化学吸附量和N原子利用率。
| [1] |
LIAO P, CAI G, SHI J, et al. Post-modified porphyrin imine gels with improved chemical stability and efficient heterogeneous activity in CO2 transformation[J]. New Journal of Chemistry, 2019, 43: 10017-10024. DOI:10.1039/C9NJ00570F |
| [2] |
李文秀, 葛珂宁, 张兵, 等. 用于分离CH4/CO2疏水性SiO2膜的制备[J]. 材料工程, 2013(2): 78-82. LI W X, GE K N, ZHANG B, et al. Preparation of hydrophobic silica membranes for methane and carbon dioxide separation[J]. Journal of Materials Engineering, 2013(2): 78-82. DOI:10.3969/j.issn.1001-4381.2013.02.016 |
| [3] |
SINGH M, SENTHILKUMAR S, RAJPUT S, et al. Pore-functionalized and hydrolytically robust Cd(Ⅱ)-metal-organic framework for highly selective, multicyclic CO2 adsorption and fast-responsive luminescent[J]. Inorganic Chemistry, 2020, 59: 3012-3025. DOI:10.1021/acs.inorgchem.9b03368 |
| [4] |
GOMEZ-POZUELO G, SANA-PEREZ E S, ARENCIBIA A, et al. CO2 adsorption on amine-functionalized clays[J]. Microporous and Mesoporous Materials, 2019, 282: 38-47. DOI:10.1016/j.micromeso.2019.03.012 |
| [5] |
SANA-PEREZ E S, ARENCIBIA A, CALLEJA G, et al. Tuning the textural properties of HMS mesoporous silica functionalization towards CO2 adsorption[J]. Microporous and Mesoporous Materials, 2018, 260: 235-244. DOI:10.1016/j.micromeso.2017.10.038 |
| [6] |
JIANG G, HUANG Q, KENARSARI D K, et al. A new mesoporous amine-TiO2 based pre-combustion CO2 capture technology[J]. Applied Energy, 2015, 147: 214-223. DOI:10.1016/j.apenergy.2015.01.081 |
| [7] |
KAPICA-KOZAR J, PIROG E, KUSIAK-NEJMAN E, et al. Titanium dioxide modified with various amines used as sorbents of carbon dioxide[J]. New Journal of Chemistry, 2017, 41: 1549-1557. DOI:10.1039/C6NJ02808J |
| [8] |
MAFRA L, CENDAK T, SCHNEIDER S, et al. Amine functionalized porous silica for CO2/CH4 separation by adsorption: which amine and why[J]. Chemical Engineering Journal, 2018, 336: 612-621. DOI:10.1016/j.cej.2017.12.061 |
| [9] |
TAHERI F S, GHAEMI A, MALEKI A, et al. High CO2 adsorption on amine-functionalized improved mesoporous silica nanotube as an eco-friendly nanocomposite[J]. Energy and Fuels, 2019, 33(6): 5384-5397. DOI:10.1021/acs.energyfuels.9b00703 |
| [10] |
YAMADA H, CHOWDHURY F A, FUJIKI J, et al. Enhancement mechanism of the CO2 adsorption-desorption efficiency of silica-supported tetraethylenepentamine by chemical modification of amino groups[J]. ACS Sustainable Chemistry & Engineering, 2019, 7(10): 9574-9581. |
| [11] |
RAO L, LIU S, WANG L, et al. N-doped porous carbons from low-temperature and single-step sodium amide activation of carbonized water chestnut shell with excellent CO2 capture performance[J]. Chemical Engineering Journal, 2019, 359: 428-435. DOI:10.1016/j.cej.2018.11.065 |
| [12] |
RAO L, MA R, LIU S, et al. Nitrogen enriched porous carbons from d-glucose with excellent CO2 capture performance[J]. Chemical Engineering Journal, 2019, 362: 794-801. DOI:10.1016/j.cej.2019.01.093 |
| [13] |
AN L, LIU S, WANG L, et al. Novel nitrogen-doped porous carbons derived from graphene for effective CO2 capture[J]. Industrial & Engineering Chemistry Research, 2019, 58(8): 3349-3358. |
| [14] |
GUO L, YANG J, HU G, et al. Role of hydrogen peroxide preoxidizing on CO2 adsorption of nitrogen-doped carbons produced from coconut shell[J]. ACS Sustainable Chemistry & Engineering, 2016, 4(5): 2806-2813. |
| [15] |
LIU S, YANG P, WANG L, et al. Nitrogen-doped porous carbons from lotus leaf for CO2 capture and supercapacitor electrodes[J]. Energy and Fuels, 2019, 33(7): 6568-6576. DOI:10.1021/acs.energyfuels.9b00886 |
| [16] |
LIAO W M, ZHANG J H, WANG Z, et al. Semiconductive amine-functionalized Co(Ⅱ)-MOF for visible-light-driven hydrogen evolution and CO2 reduction[J]. Inorganic Chemistry, 2018, 57(18): 11436-11442. DOI:10.1021/acs.inorgchem.8b01265 |
| [17] |
XU L, XING C Y, KE D, et al. Amino-functionalized β-cyclodextrin to construct green metal-organic framework material for CO2 capture[J]. ACS Applied Materials & Interfaces, 2020, 12: 3032-3041. |
| [18] |
JIA M, FENG Y, QIU J, et al. Amine-functionalized MOFs@GO as filler in mixed matrix membrane for selective CO2 separation[J]. Separation and Purification Technology, 2019, 213: 63-69. DOI:10.1016/j.seppur.2018.12.029 |
| [19] |
ALAHMED A H, BRIGGS M E, COOPER A I, et al. Covalent and electrostatic incorporation of amines into hypercrosslinked polymers for increased CO2 selectivity[J]. Journal of Polymer Science-Polymer Chemistry, 2018, 56(22): 2513-2521. DOI:10.1002/pola.29228 |
| [20] |
YANG Y, CHUAH C Y, NIE L, et al. Enhancing the mechanical strength and CO2/CH4 separation performance of polymeric membranes by incorporating amine-appended porous polymers[J]. Journal of Membrane Science, 2019, 569: 149-156. DOI:10.1016/j.memsci.2018.10.018 |
| [21] |
YANG F M, LIU Y, CHEN L, et al. Synthesis of amine-modified solid Fe-Zr adsorbents for CO2 adsorption[J]. Journal of Chemical Technology and Biotechnology, 2016, 91(8): 2340-2348. DOI:10.1002/jctb.4827 |
| [22] |
KUWAHARA Y, KANG D Y, COPELAND J Y, et al. Enhancement of CO2 uptake by poly(ethyleneimine) using zirconosilicate supports[J]. Journal of the American Chemical Society, 2012, 134(26): 10757-10760. DOI:10.1021/ja303136e |
| [23] |
YANG F M, CHEN L, AU C T, et al. Preparation of triethylenetetramine-modified zirconosilicate molecular sieve for carbon dioxide adsorption[J]. Environmental Progress & Sustainable Energy, 2015, 34(6): 1814-1821. |
| [24] |
YANG F M, CHEN L, AU C T, et al. Triethylenetetramine-modified P123-occluded Zr-SBA-15 molecular sieve for CO2 adsorption[J]. Australian Journal of Chemistry, 2015, 68(9): 1427-1433. DOI:10.1071/CH14680 |
| [25] |
GRAY M L, CHAMPAGNE K J, FAUTH D, et al. Performance of immobilized tertiary amine solid sorbents for the capture of carbon dioxide[J]. International Journal of Greenhouse Gas Control, 2008, 2(1): 3-8. DOI:10.1016/S1750-5836(07)00088-6 |
| [26] |
OLEA A, SANZ-PEREZ E S, ARENCIBIA A, et al. Amino-functionalized pore-expanded SBA-15 for CO2 adsorption[J]. Adsorption, 2013, 19(2): 589-600. DOI:10.1007/s10450-013-9482-y |
| [27] |
MONAZAM E R, SHADLE L J, MILLER D C, et al. Equilibrium and kinetics analysis of carbon dioxide capture using immobilized amine on a mesoporous silica[J]. AIChE Journal, 2013, 59(3): 923-935. DOI:10.1002/aic.13870 |
| [28] |
ZHANG Z, MA X, WANG D, et al. Development of silica-gel-supported polyethylenimine sorbents for CO2 capture from flue gas[J]. AIChE Journal, 2012, 58(8): 2495-2502. DOI:10.1002/aic.12771 |
| [29] |
LIAO Y, CAO S W, YUAN Y, et al. Efficient CO2 capture and photoreduction by amine-functionalized TiO2[J]. Chemistry-A European Journal, 2014, 20(33): 10220-10222. DOI:10.1002/chem.201403321 |
| [30] |
TSENG C L, CHEN Y K, WANG S H, et al. 2-ethanolamine on TiO2 investigated by in situ infrared spectroscopy, adsorption, photochemistry and its interaction with CO2[J]. The Journal of Physical Chemistry C, 2010, 114(27): 11835-11843. DOI:10.1021/jp9117166 |
 2021, Vol. 49
2021, Vol. 49


