文章信息
- 张双红, 杨波, 翟伟, 李爽, 孔纲
- ZHANG Shuang-hong, YANG Bo, ZHAI Wei, LI Shuang, KONG Gang
- 甲基硅酸盐/硅酸盐复合膜的组成和性能研究
- Composition and properties of methyl silicate/silicate composite coatings
- 材料工程, 2021, 49(5): 163-170
- Journal of Materials Engineering, 2021, 49(5): 163-170.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000850
-
文章历史
- 收稿日期: 2019-09-17
- 修订日期: 2020-06-17
2. 华南理工大学 材料科学与工程学院, 广州 510640
2. School of Materials Science and Engineering, South China University of Technology, Guangzhou 510640, China
铬酸盐处理是一种传统的金属表面防腐技术,防腐性能好,价格便宜,操作简单,所以得到广泛应用。但是研究发现铬酸盐中的六价铬有致癌性,且对环境造成严重污染,因此逐渐被严禁使用[1-2],必须开发新型无铬处理技术来代替铬酸盐处理[3-4]。近年来,研究发现采用硅酸盐或其混合溶液对镀锌钢[5-6]、铝及铝合金[7-14]和镁合金[15]等进行表面处理,金属的防腐蚀性能得到有效提高。硅酸盐溶液对环境友好,原料来源广泛、成本低,长期防护过程中硅酸盐膜层表面即使局部发生腐蚀,还会重新生成保护膜,即具有自愈性[16-17],作为铬酸盐的替代物,硅酸盐具有良好的应用前景。前期研究发现[17-20],在金属锌表面生成的硅酸盐膜层是一种由二氧化硅及硅酸锌组成的致密的网络结构膜,具有较好的防腐蚀性能,但由于硅酸盐膜层为亲水性膜层,在潮湿的空气或含水环境中不稳定,影响其长效防护作用,因此提高硅酸盐膜的疏水性有利于提升膜层的防腐蚀效果。
甲基硅酸钠的分子结构与硅酸钠相似,也含有硅羟基(Si—OH),同时由于分子中含有甲基(Si—CH3),使得甲基硅酸盐表现出疏水性。Min等[21]在硅酸钾溶液中添加甲基硅酸钾进行改性,研究发现经甲基硅酸钾改性后的硅酸盐膜层表现出明显的疏水性,但耐腐蚀性并没有明显提高,分析认为添加甲基硅酸钾后,改变了原硅酸盐溶液中不同聚合程度硅酸盐负离子的比例,导致膜层的致密性变差,影响膜层耐腐蚀性的提升。本工作研究两步法制备甲基硅酸盐/硅酸盐复合膜,保证硅酸盐膜层的致密结构免受破坏,同时提升膜层的疏水性,并对甲基硅酸盐/硅酸盐复合膜的结构及性能进行表征分析,与单独的硅酸盐膜、甲基硅酸盐膜进行对比分析,还分析研究了甲基硅酸盐/硅酸盐复合膜的成膜机理。
1 实验材料与方法基体材料选择厚度为0.8 mm的Q235钢板,基材成分组成的质量分数为0.038 C,0.03 Si,0.21 Mn,0.012 P,0.01 S,0.01 Al,0.01 Cr和0.01 Ni等,余量为Fe。剪裁后试样的尺寸为50 mm×40 mm。基材试样要进行热镀锌处理,首先对基材进行除油、除锈,然后浸入到助镀剂(含有150 g/L氯化铵和150 g/L氯化锌的混合溶液)中约1 min,助镀后烘干以免镀锌时发生锌液爆炸飞溅。将助镀后的试样浸入到温度为450 ℃的熔融锌液中约1 min,然后缓慢提起,再立即放入冷水中冷却,获得的热镀锌试样的锌层厚度约为50 μm。
实验用二氧化硅(沉淀法制备微米级无定型二氧化硅粉体,广州化学试剂厂),氢氧化钠(NaOH,≥99.5%,广州化学试剂厂)和蒸馏水,配制二氧化硅浓度为50 g/L,模数(SiO2/Na2O)为3.5的硅酸钠溶液。为方便对比,将甲基硅酸钠(固含量≥30%(质量分数,下同),广州聚成兆业有机硅原料中心)溶液进行稀释,保证其溶液中二氧化硅浓度同样为50 g/L。表 1列出了单独硅酸盐膜、单独甲基硅酸盐膜及其复合膜的制备工艺(用SS和SMS分别标记单独硅酸盐膜和单独甲基硅酸盐膜;用S2S5和S2S60分别标记甲基硅酸盐后处理时间5 s和60 s获得的甲基硅酸盐/硅酸盐复合膜,未处理的热镀锌试样记为HDG)。
| Sample | Treatment procedure |
| SS | HDG was immersed in the silicate solution for 60 s, and then dried at a temperature of 110 ℃ for 30 min. |
| SMS | HDG was immersed in the methyl silicate coating for 60 s, and then dried at a temperature of 110 ℃ for 30 min. |
| S2S5 | HDG was immersed in the silicate solution for 60 s, dried by hot air; and then immersed in the methyl silicate solution for 5 s, dried at a temperature of 110 ℃ for 30 min. |
| S2S60 | HDG was immersed in the silicate solution for 60 s, dried by hot air; and then immersed in the methyl silicate solution for 60 s, dried at a temperature of 110 ℃ for 30 min. |
实验采用Zetasizer Nano-ZS90型纳米粒度仪、Vector 33型红外光谱仪观测并比较分析溶液的结构与组成。用Nove NanoSEM 430型扫描电子显微镜(SEM)观察膜层的表面形貌,用能谱分析仪(EDS)和Vector 33型红外光谱仪分析膜层的组成成分。膜层的疏水性用OCA40Micro型接触角测试仪来检测。中性盐雾实验结果参照国标(GB/T 6461-2002)评定,采用网格法来评价膜层的耐腐蚀能力,至少采取3个试样算平均值。
用CHI 604B型电化学工作站进行塔菲尔(Tafel)极化曲线和电化学阻抗谱(EIS)测量,采用三电极体系,参比电极为饱和甘汞电极(SCE),辅助电极为铂电极,试样片为工作电极(暴露面积1 cm2)。塔菲尔极化曲线测量步骤:在室温条件下,先将试样浸泡在5% NaCl的溶液中约20 min,开路电位稳定后测量,以1 mV/s的速度进行扫描,极化电位设置在开路电位的±0.2 V范围。用电化学工作站相关软件可以计算出腐蚀电流密度(Icorr)、极化电阻(Rp)、自然腐蚀电位(Ecorr)等参数值。电化学阻抗谱的测量步骤:同样将试样浸泡到室温条件下的5% NaCl溶液中约20 min直到获得稳定的开路电位,信号的幅值设置为10 mV,频率设置为0.01 Hz~100 kHz范围。用Zview软件对数据进行拟合分析。
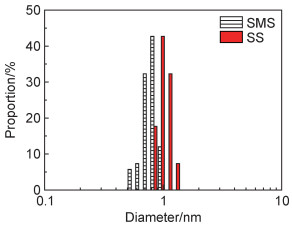
2 结果与分析 2.1 溶液分析硅酸盐溶液与常规无机盐不同,硅酸钠溶液中的硅酸盐负离子通过Si—O—Si连接,形成聚合程度不同的离子[20]。通过纳米粒度仪对溶液进行粒度分布测试,检测结果如图 1所示。甲基硅酸钠溶液(SMS)中粒子的平均粒径小于1 nm,硅酸钠溶液(SS)中粒子的平均粒径比甲基硅酸钠溶液中粒子的平均粒径要稍大一些,即离子的聚合程度相对较高。
|
图 1 硅酸钠溶液和甲基硅酸钠溶液中粒子的粒度分布 Fig. 1 Size distribution of particles in sodium silicate solution and sodium methyl silicate solution |
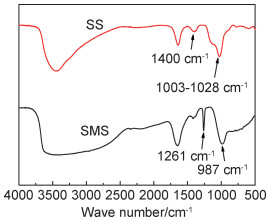
对硅酸钠溶液和甲基硅酸钠溶液进行红外光谱测试,并进行对比分析,结果如图 2所示。根据文献[20-21],甲基硅酸钠溶液在987 cm-1和1261 cm-1分别出现Si—OH和Si—CH3的吸收峰,与甲基硅酸钠的分子结构式相符。硅酸钠溶液的红外谱在1003~1028 cm-1的是Si—O—Si的吸收峰,峰的左侧有一个小平台,对应溶液中粒径较大的三维结构的硅氧聚合物离子[22-23],这与粒度分布结果相符。1400 cm-1为Na—OH的吸收峰[22]。硅酸钠溶液中的硅氧聚合物是由Si原子通过O原子互相连接,构成聚合程度和粒径不同的离子团[24-25]。
|
图 2 硅酸钠和甲基硅酸钠溶液的FT-IR谱 Fig. 2 FT-IR spectra of sodium silicate and sodium methyl silicate solution |
图 3为不同膜层表面微观形貌。单独硅酸盐膜表面有胞状颗粒,这可能是成膜过程中硅氧聚合物离子脱水缩合所形成的二氧化硅分子团,硅酸盐膜层呈凝胶状,表面几乎没有裂纹,如图 3(a)所示。而甲基硅酸盐膜表面粗燥不平,且布满裂纹,如图 3(b)所示。图 3(c)和(d)为硅酸盐膜试样再经甲基硅酸钠处理后的复合膜表面微观形貌,观察发现复合膜表面没有裂纹,膜层与基体结合良好,膜层致密且均匀。其中,当甲基硅酸钠处理时间较短(5 s)时,膜层表面分布些许颗粒,如图 3(c)所示;延长甲基硅酸钠处理时间(60 s),如图 3(d)所示,膜层表面的颗粒消失,复合膜表面更加均匀平整。这可能是由于甲基硅酸钠处理后,甲基硅酸盐膜逐渐覆盖原硅酸盐膜,且随处理时间延长,甲基硅酸盐膜层覆盖越完全。由图 3可见,甲基硅酸盐/硅酸盐复合膜层表面的微观形貌与锌层上单独甲基硅酸盐膜表面布满网状裂纹完全不同,这可能是由于硅酸盐膜表面比锌层表面有更多的羟基,促进甲基硅酸盐的成膜。对比分析不同膜层的EDS测试,数据结果列于表 2。从表 2可知,单独硅酸盐膜层表面含有更多的O和Si元素,而复合膜层与单独甲基硅酸盐膜则含有更多的C元素,这应该是来自甲基硅酸钠中的甲基,复合膜的EDS结果与甲基硅酸盐膜较为接近,可见复合膜外表层(EDS可检测范围)的主要成分是来自甲基硅酸钠的成膜,表明甲基硅酸钠在硅酸盐膜层表面成膜。

|
图 3 硅酸盐膜、甲基硅酸盐膜及其复合膜的SEM图 (a)SS;(b)SMS;(c)S2S5;(d)S2S60 Fig. 3 SEM images of silicate coating, methyl silicate coating and composite coatings (a)SS; (b)SMS; (c)S2S5;(d)S2S60 |
| Sample | Zn | O | Si | C |
| SS | 20.17 | 59.90 | 17.83 | 2.10 |
| SMS | 22.78 | 42.00 | 6.79 | 28.43 |
| S2S5 | 22.61 | 42.89 | 8.91 | 25.59 |
| S2S60 | 18.07 | 40.73 | 12.64 | 28.57 |
根据膜层的增质分析,无论是单独硅酸盐膜、甲基硅酸盐膜还是甲基硅酸盐/硅酸盐复合膜,增重基本维持在一个小范围内,约3.00 g/m2;参照各种硅酸盐和甲基硅酸盐的密度,以膜的组成物的密度为2.00 ~ 3.00 g/cm3计,可推算出膜厚均在1.00 ~ 1.50 μm之间。
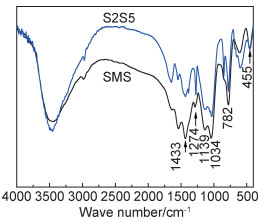
对单独甲基硅酸盐膜层和S2S5复合膜层的红外光谱进行对比分析,结果示于图 4。由图 4可见,结合文献[20-21]可知,甲基硅酸盐膜在1433 cm-1处有对应Si—CH3的C—H吸收峰,1274 cm-1处可能是对应着Si—CH3的Si—C吸收峰,而1139~1034, 782 cm-1和455 cm-1处分别是对应着膜层的Si—O—Si,Si—O—CH3和Si—O—Zn键的Si—O吸收峰;S2S5复合膜的吸收峰与单独甲基硅酸盐膜的非常相似,复合膜层也含有—OH, Si—CH3, Si—O—Si和Si—O—Zn等键。结果表明,硅酸盐膜试样经甲基硅酸钠溶液处理后,甲基硅酸盐膜在硅酸盐膜表面成膜,且基本覆盖完全。
|
图 4 复合膜S2S5和甲基硅酸盐膜层的FT-IR谱 Fig. 4 FT-IR spectra of S2S5 composite coating and methyl silicate coating |
对不同膜层进行疏水性测试,结果如图 5所示。由图可见,单独硅酸盐膜的接触角仅为6.8°,即其为亲水性膜层,而甲基硅酸盐膜的接触角高达104°,表现出明显的疏水性。硅酸盐膜试样经甲基硅酸钠溶液分别处理5 s和60 s后,获得的复合膜接触角分别为99.3°和103.8°,相比于单独硅酸盐膜,复合膜的接触角明显增大,表现为疏水性膜层。这是由于膜层表面的疏水性基团(Si—CH3)使得复合膜表现出疏水性,表明甲基硅酸盐在硅酸盐膜表面成膜。

|
图 5 硅酸盐膜、甲基硅酸盐膜及其复合膜的接触角 (a)SS;(b)SMS;(c)S2S5;(d)S2S60 Fig. 5 Contact angle of silicate coating, methyl silicate coating and composite coatings (a)SS; (b)SMS; (c)S2S5;(d)S2S60 |
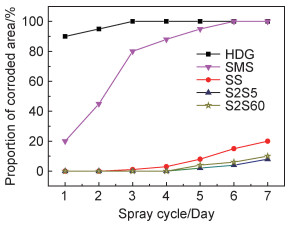
图 6是硅酸盐膜、甲基硅酸盐膜、两种复合膜及HDG试样的中性盐雾实验结果。结果显示,经过一个盐雾周期,HDG试样表面覆满了白锈,而单独甲基硅酸盐膜层表面的腐蚀面积仅为20%,这说明单独甲基硅酸盐膜层能够提高锌层的耐蚀性能。但从第二个周期开始,甲基硅酸盐膜层表面白锈迅速增多,其腐蚀面积达到了45%,这可能是由于单独甲基硅酸盐膜层较为疏松,表面布满裂纹,影响了膜层的耐腐蚀保护作用。经过三个周期盐雾腐蚀后,HDG表面100%被白锈覆盖,单独甲基硅酸盐膜层表面80%被白锈覆盖。经过七个周期盐雾腐蚀实验,HDG和甲基硅酸盐膜表面均完全腐蚀,而单独硅酸盐表面的腐蚀面积约为20%,甲基硅酸盐/硅酸盐复合膜表面的腐蚀面积仍不足10%,可见复合膜的耐盐雾腐蚀能力相对较好。S2S5和S2S60两种复合膜的耐盐雾性能较为接近,可见甲基硅酸钠溶液处理时间对复合膜层的耐盐雾性能影响不大。
|
图 6 硅酸盐膜、甲基硅酸盐膜、复合膜及HDG的中性盐雾实验结果 Fig. 6 NSS test results of silicate coating, methyl silicate coating, composite coatings and HDG |
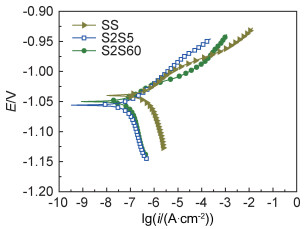
对单独硅酸盐试样和复合膜试样进行极化曲线测试,结果如图 7所示。由图可见,甲基硅酸盐/硅酸盐复合膜试样极化曲线的阴极分支向电流减小的方向移动明显,说明复合膜抑制腐蚀电流主要是抑制电化学腐蚀的阴极反应,即氧还原反应:O2+2H2O+4e-→4OH-。塔菲尔极化曲线相应的参数列于表 3。经甲基硅酸钠溶液处理后,复合膜的极化阻抗是单独硅酸盐膜极化阻抗(19.04 kΩ·cm2)的5~6倍,复合膜的腐蚀电流密度比单独硅酸盐膜的(0.14 μA·cm-2)降低了60%。无论在甲基硅酸钠溶液处理5 s还是60 s,获得的甲基硅酸盐/硅酸盐复合膜的耐蚀性均明显提高。
|
图 7 硅酸盐膜和复合膜的极化曲线 Fig. 7 Potentiodynamic polarization curves of single silicate coating and silicate composite coatings |
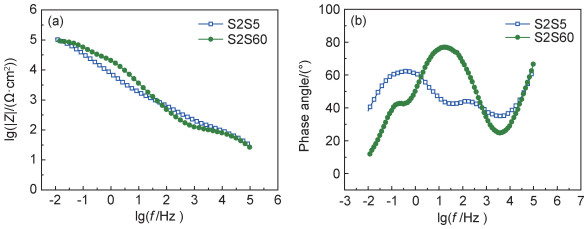
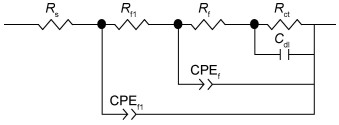
进一步分析两种甲基硅酸盐/硅酸盐复合膜的电化学性能,结果示于图 8。由图 8(a)可见,经甲基硅酸钠溶液处理不同时间获得的两种复合膜的低频阻抗较为接近,即膜层的耐蚀性相近,可见甲基硅酸钠溶液的处理时间对复合膜层的耐蚀性影响不大。由图 8(b)可见,两种甲基硅酸盐/硅酸盐复合膜均具有3个时间常数,根据复合膜试样的电化学阻抗谱,两种复合膜均可用同一种等效电路进行拟合,结果示于图 9,其中Rs表示溶液电阻,CPEf和CPEf1表示常相位角元件(与膜层电容相关),Rf和Rf1为膜层电阻,Rct为电荷转移电阻,Cdl为双电层电容(膜层/基体锌层界面)。甲基硅酸盐膜和硅酸盐膜的结构和特性是不一样的,两个膜层的导电率和介电常数也有区别,这分别影响到膜层电阻和膜层电容,因此进行等效电路分析时,将甲基硅酸盐/硅酸盐复合膜当作双层膜处理是合理的。等效电路中的Rf1对应外层甲基硅酸盐膜,Rf对应内层硅酸盐膜,具体等效电路拟合参数值列于表 4。
|
图 8 甲基硅酸盐/硅酸盐复合膜的EIS图 (a)Bode;(b)Nyquist Fig. 8 EIS plots of methyl silicate/silicate composite coatings (a)Bode; (b)Nyquist |
|
图 9 复合膜试样的等效电路图 Fig. 9 Equivalent circuit of composite coatings |
| Sample | Rf1/(Ω·cm2) | CPEf1 | Rf/(kΩ·cm2) | CPEf | Rct/(kΩ·cm2) | Cdl/(10-5 F·cm-2) | ||
| Y0/(10-6Ω-1·cm-2·S-n) | n | Y0/(10-6Ω-1·cm-2·S-n) | n | |||||
| S2S5 | 68.44 | 2.34 | 0.74 | 45.54 | 1.81 | 0.84 | 66.67 | 6.01 |
| S2S60 | 341.60 | 4.02 | 0.65 | 41.66 | 4.44 | 0.94 | 61.16 | 2.38 |
由表 4可知,甲基硅酸盐/硅酸盐复合膜的总阻抗值超过100 kΩ·cm2,是单独硅酸盐膜的约5倍[17]。表明硅酸盐膜试样经甲基硅酸钠处理后,获得的甲基硅酸盐/硅酸盐复合膜的耐蚀性得到有效提升。
2.5 甲基硅酸钠处理对膜层结构的影响甲基硅酸钠的成膜机理与硅酸盐膜相似,主要是脱水缩合形成网络结构膜[24]。但是甲基硅酸钠含有疏水性基团(Si—CH3),由于甲基在膜层中无法再进行链接,所以甲基硅酸盐膜与锌基体的黏结性相对较差,膜层中相对缺少Si—O—Si网络结构,导致锌层上的单独甲基硅酸盐膜表面粗燥不平且布满裂纹(图 3(b))。
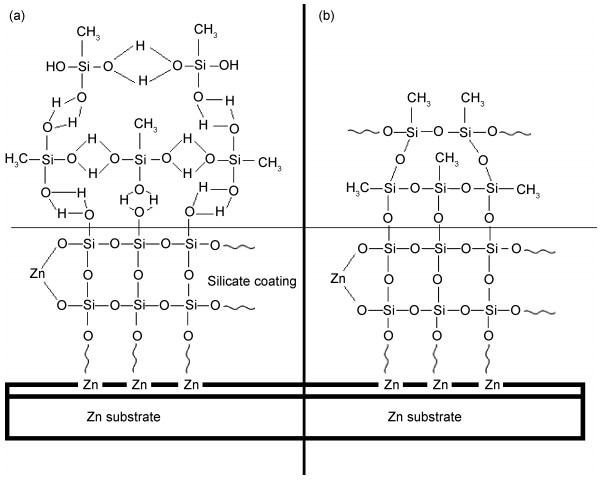
甲基硅酸钠在硅酸盐膜表面的成膜机理与在锌层上相似,但是硅酸盐膜外层主要是二氧化硅,与锌层表面的Zn—OH数量相比,硅酸盐膜层表面可提供更多的Si—OH与甲基硅酸钠的Si—OH进行化学反应生成Si—O—Si键链接的三维网络。因此,甲基硅酸盐膜与硅酸盐膜之间能更好的咬合,使得复合膜表面均匀平整,没有出现锌层上甲基硅酸盐膜表面开裂的情况(图 3(c)和(d))。图 10是甲基硅酸钠在硅酸盐膜层表面成膜的示意图。由图 10可见,硅酸盐膜表面较多的Si—OH键促进甲基硅酸钠在其表面形成疏水性的甲基硅酸盐膜。和单独硅酸盐膜相比,复合膜的内部结构致密不变,膜层疏水性增大。
|
图 10 甲基硅酸钠溶液在硅酸盐转化膜表面键合成膜机理示意图 (a)即时吸附后;(b) 固化后 Fig. 10 Adsorption mechanism schematic diagram of sodium methyl silicate on silicate coating surface (a)immediately after adsorption; (b)after curing |
(1) 采用两步法制备甲基硅酸盐/硅酸盐复合膜,单独硅酸盐膜为亲水性膜层,其接触角仅为6.8°,而甲基硅酸盐膜的接触角高达104°,硅酸盐膜试样经甲基硅酸钠溶液分别处理5 s和60 s后,获得的复合膜接触角分别为99.3°和103.8°,复合膜表现为疏水性膜层,且接触角与单独甲基硅酸盐膜相近。
(2) 根据EDS和FT-IR结果表明甲基硅酸盐/硅酸盐复合膜层的外层与单独甲基硅酸钠膜基本一致,但其微观形貌与单独甲基硅酸盐膜表面布满网状裂纹不同,复合膜层的表面均匀平整,没有裂纹。
(3) 甲基硅酸盐/硅酸盐复合膜的极化阻抗是单独硅酸盐膜极化阻抗(19.04 kΩ·cm2)的5~6倍,复合膜的总阻抗值超过100 kΩ·cm2,复合膜的腐蚀电流密度比单独硅酸盐膜的(0.14 μA·cm-2)降低了60%,相比于单独的硅酸盐膜、甲基硅酸盐膜,甲基硅酸盐/硅酸盐复合膜层的耐蚀性得到有效提高。
| [1] |
程琪, 许哲峰, 于晓华, 等. 硅烷-钼复合无铬钝化膜的耐蚀性及标准曲线构建[J]. 中国表面工程, 2017, 30(5): 60-66. CHENG Q, XU Z F, YU X H, et al. Corrosion resistance and standard curve of silane-molybdenum composite chromium-free passivation film[J]. China Surface Engineering, 2017, 30(5): 60-66. |
| [2] |
DESAI C, JAIN K, MADAMWAR D. Evaluation of in vitro Cr(Ⅵ) reduction potential in cytosolic extracts of three indigenous bacillus sp. isolated from Cr(Ⅵ) polluted industrial landfill[J]. Bioresource Technology, 2008, 99(14): 6059-6069. DOI:10.1016/j.biortech.2007.12.046 |
| [3] |
POMMIERS S, FRAYRET J, CASTETBON A, et al. Alternative conversion coatings to chromate for the protection of magnesium alloys[J]. Corrosion Science, 2014, 84(8): 135-146. |
| [4] |
ZULETA A A, CORREA E, VILLADA C, et al. Comparative study of different environmentally friendly (chromium-free) methods for surface modification of pure magnesium[J]. Surface & Coatings Technology, 2011, 205(23/24): 5254-5259. |
| [5] |
JAMALI F, DANAEE I, ZAAREI D. Effect of nano-silica on the corrosion behavior of silicate conversion coatings on hot-dip galvanized steel[J]. Materials and Corrosion, 2015, 66(5): 459-464. DOI:10.1002/maco.201407633 |
| [6] |
JIANG L, WOLPERS M, VOLOVITCH P, et al. An atomic emission spectroelectrochemical study of passive film formation and dissolution on galvanized steel treated with silicate conversion coatings[J]. Surface and Coatings Technology, 2012, 206(13): 3151-3157. DOI:10.1016/j.surfcoat.2012.01.016 |
| [7] |
BAHRI H, DANAEE I, RASHED G R, et al. Effect of silica ratio on the corrosion behavior of nano-silica potassium silicate coatings on aluminum alloy 2024[J]. Journal of Materials Engineering and Performance, 2015, 24(2): 839-847. DOI:10.1007/s11665-014-1325-9 |
| [8] |
KAZEMI M, DANAEE I, ZAAREI D. Deposition and corrosion behavior of silicate conversion coatings on aluminum alloy 2024[J]. Materialwissenschaft und Werkstofftechnik, 2014, 45(7): 574-581. DOI:10.1002/mawe.201400212 |
| [9] |
KAZEMI M, DANAEE I, ZAAREI D. The effect of pre-anodizing on corrosion behavior of silicate conversion coating on AA2024[J]. Materials Chemistry and Physics, 2014, 148(1/2): 223-229. |
| [10] |
BAHRI H, DANAEE I, RASHED G R. The effect of curing time and curing temperature on the corrosion behavior of nanosilica modified potassium silicate coatings on AA2024[J]. Surface and Coatings Technology, 2014, 254(10): 305-312. |
| [11] |
CANOSA G, ALFIERI P V, GIUDICE C A. Environmentally friendly, nano lithium silicate anticorrosive coatings[J]. Progress in Organic Coatings, 2012, 73(2/3): 178-185. |
| [12] |
GAO H, LI Q, CHEN F N, et al. Study of the corrosion inhibition effect of sodium silicate on AZ91D magnesium alloy[J]. Corrosion Science, 2011, 53(4): 1401-1407. DOI:10.1016/j.corsci.2011.01.008 |
| [13] |
GAGGIANO R, MORIAMÉ P, BIESEMANS M, et al. Mechanism of formation of silicate thin films on porous anodic alumina[J]. Surface and Coatings Technology, 2011, 205(21/22): 5210-5217. |
| [14] |
GAGGIANO R, MORIAMÉ P, BIESEMANS M, et al. Influence of SiO2/Na2O ratio and temperature on the mechanism of interaction of soluble sodium silicates with porous anodic alumina[J]. Surface and Coatings Technology, 2011, 206(6): 1269-1276. DOI:10.1016/j.surfcoat.2011.08.043 |
| [15] |
ZHANG R F, ZHANG S F, XIANG J H, et al. Influence of sodium silicate concentration on properties of micro arc oxidation coatings formed on AZ91HP magnesium alloys[J]. Surface and Coatings Technology, 2012, 206(24): 5072-5079. DOI:10.1016/j.surfcoat.2012.06.018 |
| [16] |
YUAN M R, LU J T, KONG G, et al. Self healing ability of silicate conversion coatings on hot dip galvanized steels[J]. Surface and Coatings Technology, 2011, 205(19): 4507-4513. DOI:10.1016/j.surfcoat.2011.03.088 |
| [17] |
袁美蓉, 卢锦堂, 孔纲, 等. 热镀锌层上硅酸盐膜的耐蚀性和自愈性[J]. 材料工程, 2012(6): 48-53. YUAN M R, LU J T, KONG G, et al. Corrosion resistance and self healing ability of silicate conversion coatings on hot dip galvanized Steels[J]. Journal of Materials Engineering, 2012(6): 48-53. DOI:10.3969/j.issn.1001-4381.2012.06.011 |
| [18] |
YUAN M R, LU J T, KONG G. Effect of SiO2: Na2O molar ratio of sodium silicate on the corrosion resistance of silicate conversion coatings[J]. Surface and Coatings Technology, 2010, 204(8): 1229-1235. DOI:10.1016/j.surfcoat.2009.10.024 |
| [19] |
YUAN M R, LU J T, KONG G, et al. Effect of silicate anion distribution in sodium silicate solution on silicate conversion coatings of hot-dip galvanized steels[J]. Surface and Coatings Technology, 2011, 205(19): 4466-4470. DOI:10.1016/j.surfcoat.2011.03.064 |
| [20] |
ZHANG S H, KONG G, SUN Z W, et al. Effect of formulation of silica-based solution on corrosion resistance of silicate coating on hot-dip galvanized steel[J]. Surface and Interface Analysis, 2016, 48(3): 132-138. DOI:10.1002/sia.5898 |
| [21] |
MIN J, PARK J H, SOHN H, et al. Synergistic effect of potassium metal siliconate on silicate conversion coating for corrosion protection of galvanized steel[J]. Journal of Industrial and Engineering Chemistry, 2012, 18(2): 655-660. DOI:10.1016/j.jiec.2011.11.057 |
| [22] |
陈和生, 孙振亚, 邵景昌. 八种不同来源二氧化硅的红外光谱特征研究[J]. 硅酸盐通报, 2011, 30(4): 934-937. CHEN H S, SUN Z Y, SHAO J C. Investigation on FT-IR spectroscopy for eight different sources of SiO2[J]. Bulletin of the Chinese Ceramic Society, 2011, 30(4): 934-937. |
| [23] |
PRENZEL T, MEHNER A, LUCCA D A, et al. Chemical and mechanical properties of silica hybrid films from NaOH catalyzed sols for micromachining with diamond cutting tools[J]. Thin Solid Films, 2013, 531(6): 208-216. |
| [24] |
NORDSTR M J, NILSSON E, JARVOL P, et al. Concentration- and pH-dependence of highly alkaline sodium silicate solutions[J]. Journal of Colloid and Interface Science, 2011, 356(1): 37-45. DOI:10.1016/j.jcis.2010.12.085 |
| [25] |
孔纲, 张双红, 孙子文, 等. 二氧化硅粉体粒度对硅酸盐转化膜制备的影响[J]. 材料研究学报, 2014, 28(6): 462-468. KONG G, ZHANG S H, SUN Z W, et al. Effect of size of silica powder on preparation of silicate conversion coatings on galvanized steel[J]. Chinese Journal of Materials Research, 2014, 28(6): 462-468. |
 2021, Vol. 49
2021, Vol. 49


